Khám phá tiềm năng của tế bào gốc đa năng trong y học tái tạo
Tế bào gốc đa năng là một lĩnh vực nghiên cứu đầy hứa hẹn, mang tiềm năng to lớn cho y học tái tạo và mô hình hóa bệnh tật. Những tế bào này, bao gồm các dòng tế bào bất tử tự nhiên như WI-38 Cells, cũng như tế bào gốc đa năng được cảm ứng (iPSCs) được tạo ra từ mô người trưởng thành, có khả năng đặc biệt là phân hóa thành bất kỳ loại tế bào nào trong cơ thể. Điều này khiến chúng trở thành công cụ vô giá để nghiên cứu sự phát triển của con người, cơ chế bệnh tật và các phương pháp điều trị tiềm năng.
Ở tuyến đầu của nghiên cứu tế bào gốc đa năng là các tế bào gốc đa năng được cảm ứng, có thể được tạo ra từ chính các tế bào của bệnh nhân, như tế bào sợi da hoặc tế bào máu. Bằng cách tái lập trình các tế bào trưởng thành này bằng các yếu tố cụ thể, các nhà nghiên cứu có thể tạo ra các tế bào iPSCs đặc hiệu cho bệnh nhân, giữ nguyên nền tảng di truyền của người hiến tặng.
Vai trò quan trọng của tế bào gốc nguyên thủy người trong nghiên cứu tế bào gốc đa năng
Tế bào nguyên thủy của người cũng đóng vai trò quan trọng trong nghiên cứu tế bào gốc đa năng, cung cấp cơ sở để so sánh và xác minh các tế bào được tạo ra từ tế bào gốc đa năng cảm ứng (iPSC). Ví dụ, Tế bào gốc tủy răng người (hDPSC) và Tế bào gốc nang răng người (hDFSC) là nguồn tài nguyên quý giá để nghiên cứu sự phát triển và tái tạo răng. Tương tự, tế bào HUVEC từ một người hiến tặng duy nhất được sử dụng rộng rãi trong nghiên cứu sinh học mạch máu và tạo mạch, và đóng vai trò là tiêu chuẩn để đánh giá các tế bào nội mô được tạo ra từ iPSC.
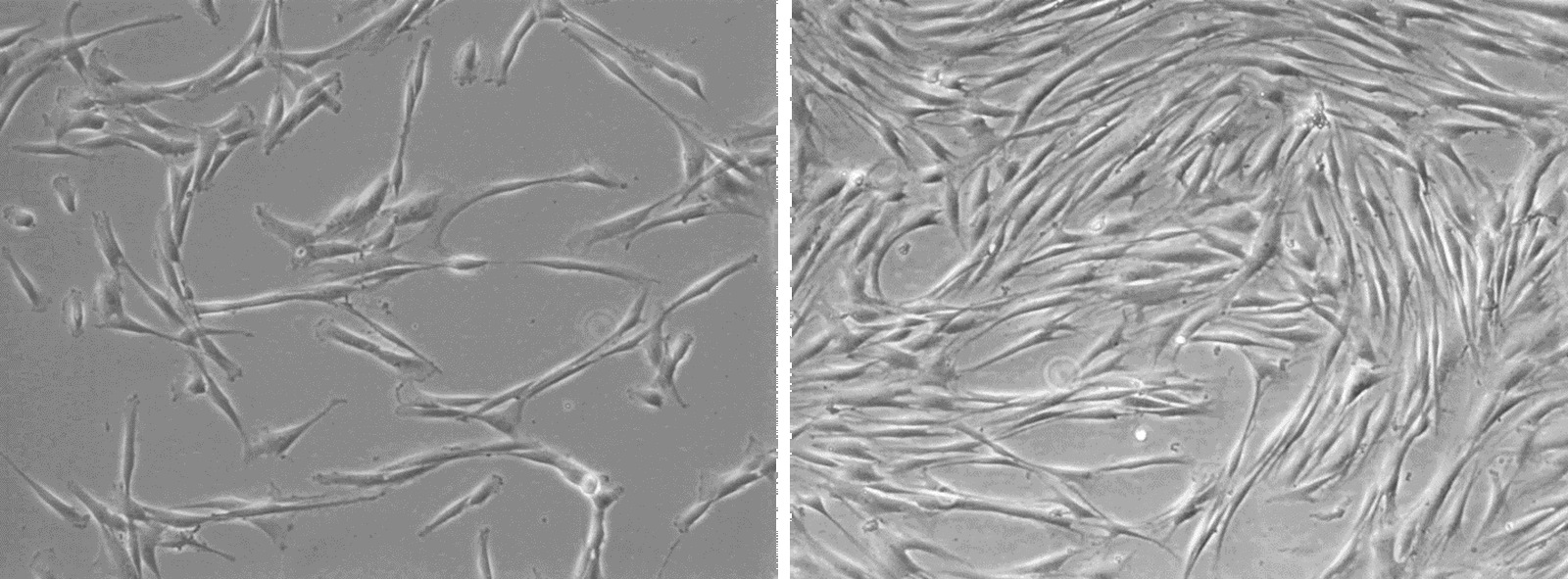
Một ví dụ khác là tế bào P-19, một loại ung thư phôi đa tiềm năng, ban đầu được thu được từ một khối u teratocarcinoma ở chuột C3H/He. Như hình bên trái cho thấy, dòng tế bào P19 có nguồn gốc từ chuột (Mus musculus).
Mục lục về tế bào gốc trung mô người
Tế bào gốc đa năng là nền tảng của nghiên cứu y học tái tạo và sinh học phát triển. Những tế bào này, bao gồm tế bào gốc phôi (ESCs) và tế bào gốc đa năng được cảm ứng (iPSCs), có khả năng đặc biệt là phân hóa thành bất kỳ loại tế bào nào trong cơ thể. Tính chất độc đáo này khiến chúng trở thành công cụ vô giá trong việc nghiên cứu sự phát triển của con người, mô phỏng bệnh tật, sàng lọc thuốc và các liệu pháp dựa trên tế bào tiềm năng. Đặc biệt, iPSCs đã cách mạng hóa lĩnh vực này bằng cách cho phép tạo ra tế bào gốc đặc hiệu cho bệnh nhân từ mô người trưởng thành, mở ra những khả năng hứa hẹn cho y học cá nhân hóa. Các nhà nghiên cứu hiện có thể tạo ra iPSCs từ bệnh nhân mắc các bệnh khác nhau, phân hóa chúng thành các loại tế bào liên quan và nghiên cứu các cơ chế cơ bản của các tình trạng này trong môi trường thí nghiệm. Hơn nữa, khả năng tạo ra liệu pháp tế bào tự thân từ iPSCs của bệnh nhân mang lại tiềm năng to lớn cho y học tái tạo, vì các tế bào này có thể được sử dụng để thay thế các mô bị tổn thương hoặc bệnh lý mà không có nguy cơ bị thải loại miễn dịch. Khi lĩnh vực nghiên cứu tế bào gốc đa năng tiếp tục phát triển, ngày càng rõ ràng rằng các tế bào này sẽ đóng vai trò quan trọng trong việc định hình tương lai của y học và nâng cao hiểu biết của chúng ta về sinh học con người.
| Sản phẩm | Mô tả | Số hiệu |
|---|---|---|
| Tế bào gốc trung mô người - Mô mỡ | Tế bào gốc trung mô được tách chiết từ mô mỡ người | 300645 |
| Tế bào gốc trung mô người - Màng ối | Tế bào gốc trung mô được phân lập từ màng ối người | 300644 |
| Tế bào gốc trung mô người - Tủy xương (HMSC-BM) | Tế bào gốc trung mô được tách chiết từ tủy xương người | 300665 |
| Tế bào gốc trung mô người - Lông nhau thai | Tế bào gốc trung mô được phân lập từ nhung mao màng đệm người | 300646 |
| Tế bào gốc trung mô người - Niêm mạc tử cung | Tế bào gốc trung mô được tách chiết từ mô nội mạc tử cung người | 300647 |
| Tế bào gốc trung mô người - Dây rốn - Động mạch | Tế bào gốc trung mô được phân lập từ động mạch dây rốn người | 300648 |
| Tế bào gốc trung mô người - Chất nhầy Wharton (HMSC-WJ) | Tế bào gốc trung mô được tách chiết từ chất nhầy Wharton của dây rốn người | 300685 |
Tiềm năng và thách thức của tế bào gốc đa năng cảm ứng (iPSCs) trong mô hình hóa bệnh tật và điều trị
Tế bào iPSC được phân lập từ bệnh nhân mang lại cơ hội chưa từng có để mô phỏng các bệnh lý ở người trong môi trường thí nghiệm. Bằng cách phân hóa các tế bào này thành các loại tế bào liên quan đến bệnh lý, các nhà nghiên cứu có thể nghiên cứu các cơ chế phân tử cơ bản của các bệnh lý khác nhau và sàng lọc các ứng cử viên thuốc tiềm năng. Ví dụ, các tế bào cơ tim được phân lập từ tế bào iPSC của bệnh nhân mắc các rối loạn tim mạch di truyền đã được sử dụng để tái tạo các biểu hiện bệnh lý và kiểm tra hiệu quả của các hợp chất điều trị [198]. Tương tự, các tế bào thần kinh được phân hóa từ iPSCs của bệnh nhân mắc các rối loạn thần kinh như Alzheimer và Parkinson đã cung cấp những hiểu biết quý giá về tiến triển bệnh và phản ứng với thuốc [199].
Tuy nhiên, một số thách thức cần được giải quyết trước khi iPSC có thể được sử dụng rộng rãi cho mô hình hóa bệnh tật và điều trị. Những thách thức này bao gồm:
- Sự biến đổi về hiệu suất tái lập trình và chất lượng của iPSC
- Sự biến đổi di truyền và biểu sinh trong quá trình tái lập trình
- Hiện tượng chưa trưởng thành hoặc có đặc điểm giống phôi của các tế bào được phân lập từ iPSC
- Thiếu các quy trình tiêu chuẩn hóa cho quá trình biệt hóa và trưởng thành
- Những lo ngại về an toàn liên quan đến khả năng gây ung thư và phản ứng miễn dịch
Nghiên cứu nhằm giải quyết các vấn đề này bằng cách phát triển các phương pháp tái lập trình hiệu quả và tiêu chuẩn hóa hơn, hoàn thiện các quy trình phân hóa và áp dụng các biện pháp kiểm soát chất lượng nghiêm ngặt. Sự tiến bộ trong công nghệ chỉnh sửa gen như CRISPR/Cas9 cũng cho phép sửa chữa các đột biến gây bệnh trong iPSCs được phân lập từ bệnh nhân, mở đường cho các liệu pháp thay thế tế bào tự thân [200].
Tương lai của iPSC trong y học tái tạo
Sự ra đời của công nghệ iPSC đã mở ra những khả năng hứa hẹn cho y học tái tạo. Khác với tế bào gốc phôi, iPSC có thể được tạo ra từ chính tế bào của bệnh nhân, do đó tránh được các vấn đề đạo đức và nguy cơ thải ghép miễn dịch. Nhiều nghiên cứu tiền lâm sàng đã chứng minh tiềm năng của các tế bào được tạo ra từ iPSC trong điều trị các bệnh lý khác nhau, chẳng hạn như:
- Bệnh Parkinson: Cấy ghép tế bào thần kinh dopaminergic được tạo ra từ iPSCs trong các mô hình động vật [201]
- Chấn thương tủy sống: Sự tích hợp của các tế bào tiền thân thần kinh được tạo ra từ iPSC giúp phục hồi chức năng [202]
- Bệnh thoái hóa điểm vàng: Thay thế biểu mô sắc tố võng mạc bị tổn thương bằng các tế bào được tạo ra từ iPSC [203]
- Suy tim: Tiêm tế bào cơ tim được tạo ra từ iPSC để cải thiện chức năng tim [204]
Khi lĩnh vực này phát triển, dự kiến sẽ có thêm nhiều thử nghiệm lâm sàng sử dụng tế bào được phân lập từ iPSC. Tuy nhiên, việc chuyển đổi các kết quả tiền lâm sàng đầy hứa hẹn này thành các liệu pháp an toàn và hiệu quả sẽ đòi hỏi phải vượt qua nhiều thách thức, như đảm bảo độ tinh khiết và ổn định của tế bào được phân lập từ iPSC, phát triển quy trình sản xuất có quy mô lớn và thiết lập các hướng dẫn quy định phù hợp.
Tóm lại, iPSC là một công cụ mạnh mẽ cho mô hình hóa bệnh tật, phát hiện thuốc và y học tái tạo. Mặc dù vẫn còn nhiều thách thức, tốc độ nghiên cứu và tiến bộ công nghệ nhanh chóng trong lĩnh vực này hứa hẹn sẽ cách mạng hóa việc điều trị nhiều bệnh tật ở người. Sự hợp tác liên ngành giữa các nhà khoa học, bác sĩ lâm sàng và các cơ quan quản lý sẽ là yếu tố quan trọng để khai thác hết tiềm năng của iPSC trong việc cải thiện sức khỏe con người.
Điểm chính
- iPSCs được tạo ra từ các tế bào soma bằng cách giới thiệu các gen liên quan đến khả năng đa tiềm năng
- iPSCs có các đặc tính tương tự như tế bào gốc phôi nhưng tránh được các vấn đề đạo đức
- IPSCs được tạo ra từ bệnh nhân cho phép mô phỏng bệnh tật và sàng lọc thuốc theo cách cá nhân hóa
- các tế bào được tạo ra từ iPSCs đã cho thấy kết quả đầy hứa hẹn trong các nghiên cứu tiền lâm sàng đối với nhiều bệnh tật
- Các thách thức trong nghiên cứu iPSC bao gồm tính biến đổi, sự không ổn định di truyền và các vấn đề an toàn
- Các tiến bộ trong công nghệ tái lập trình, biệt hóa và chỉnh sửa gen đang thúc đẩy sự phát triển của lĩnh vực này
- Việc chuyển giao lâm sàng các liệu pháp dựa trên iPSC sẽ đòi hỏi phải vượt qua các rào cản kỹ thuật và quy định
- Hợp tác liên ngành là yếu tố quan trọng để khai thác hết tiềm năng của iPSC trong y học tái tạo

MỘT ĐỐI TÁC ĐÁNG TIN CẬY: CYTION
Ứng dụng tiềm năng và hướng phát triển tương lai của tế bào gốc đa năng
Lĩnh vực nghiên cứu tế bào gốc đa năng hứa hẹn mang lại những đột phá trong y học tái tạo và nâng cao hiểu biết của chúng ta về sự phát triển của con người và các bệnh lý. Cả tế bào gốc phôi người (hESCs) và tế bào gốc đa năng được cảm ứng (hiPSCs) đều có khả năng phi thường trong việc phân hóa thành bất kỳ loại tế bào nào trong cơ thể, khiến chúng trở thành công cụ vô giá trong việc nghiên cứu cơ chế bệnh lý, sàng lọc thuốc và các liệu pháp dựa trên tế bào tiềm năng.
một trong những ứng dụng thú vị nhất của tế bào gốc đa năng là việc sử dụng chúng trong y học tái tạo. Các nghiên cứu tiền lâm sàng đã chứng minh tiềm năng điều trị của các tế bào được phân hóa từ hESC và hiPSC trong các mô hình bệnh lý như chấn thương tủy sống, mù lòa và rối loạn tim mạch. Hiện nay, một số thử nghiệm lâm sàng sử dụng sản phẩm từ hESC đang được tiến hành, nhắm vào các bệnh lý như chấn thương tủy sống, thoái hóa điểm vàng và đái tháo đường type 1 (Bảng 1). Ngoài ra, Nhật Bản đã phê duyệt nghiên cứu lâm sàng đầu tiên trên thế giới sử dụng tế bào biểu mô sắc tố võng mạc được phân lập từ hiPSC để điều trị thoái hóa điểm vàng.
Tuy nhiên, trước khi tiềm năng đầy đủ của tế bào gốc đa năng có thể được hiện thực hóa trong thực hành lâm sàng, một số thách thức cần được giải quyết:
- Phát triển các phương pháp tái lập trình hiệu quả và an toàn mà không sử dụng véc-tơ virus và gen gây ung thư
- Thiết lập các biện pháp kiểm soát chất lượng nghiêm ngặt để đảm bảo an toàn và chức năng của các sản phẩm được phát triển từ tế bào gốc phôi người (hESC) và tế bào gốc đa năng cảm ứng (hiPSC)
- Tối ưu hóa các quy trình biệt hóa để thu được các quần thể tế bào tinh khiết và chức năng
- Thực hiện các nghiên cứu tiền lâm sàng toàn diện trên các mô hình động vật phù hợp để đánh giá hiệu quả và an toàn của các liệu pháp dựa trên tế bào gốc đa năng
- Vượt qua khung pháp lý để được phê duyệt cho các thử nghiệm lâm sàng và thương mại hóa cuối cùng
Một ứng dụng đầy hứa hẹn khác của tế bào gốc đa năng, đặc biệt là hiPSC, là trong mô hình bệnh và phát hiện thuốc. Tế bào hiPSC được phân lập từ bệnh nhân có thể tái tạo các khía cạnh khác nhau của bệnh lý khi được phân hóa thành các loại tế bào liên quan, cung cấp một nền tảng mạnh mẽ để nghiên cứu cơ chế bệnh và xác định các mục tiêu điều trị mới. Ngoài ra, tế bào hiPSC từ cả người hiến tặng khỏe mạnh và bệnh nhân cung cấp một hệ thống sinh lý học phù hợp hơn để đánh giá hiệu quả và độc tính của thuốc so với các dòng tế bào người bất tử truyền thống.
Tóm lại, mặc dù đã có những tiến bộ đáng kể trong lĩnh vực nghiên cứu tế bào gốc đa năng, vẫn cần thêm các nghiên cứu để hiểu rõ hơn về sinh học của tính đa năng và quá trình biệt hóa, cũng như để vượt qua các thách thức liên quan đến ứng dụng điều trị. Các nỗ lực tiếp tục để cải thiện công nghệ tái lập trình, thiết lập các quy trình biệt hóa đáng tin cậy và đảm bảo an toàn và hiệu quả của các sản phẩm được tạo ra từ hESC và hiPSC sẽ mở đường cho việc ứng dụng lâm sàng của các công cụ mạnh mẽ này trong y học tái tạo và phát hiện thuốc.
Bằng cách khai thác tiềm năng to lớn của tế bào gốc đa năng, chúng ta có thể hướng tới việc phát triển các liệu pháp sáng tạo cho nhiều loại bệnh tật ở người và cuối cùng cải thiện kết quả điều trị cho bệnh nhân.