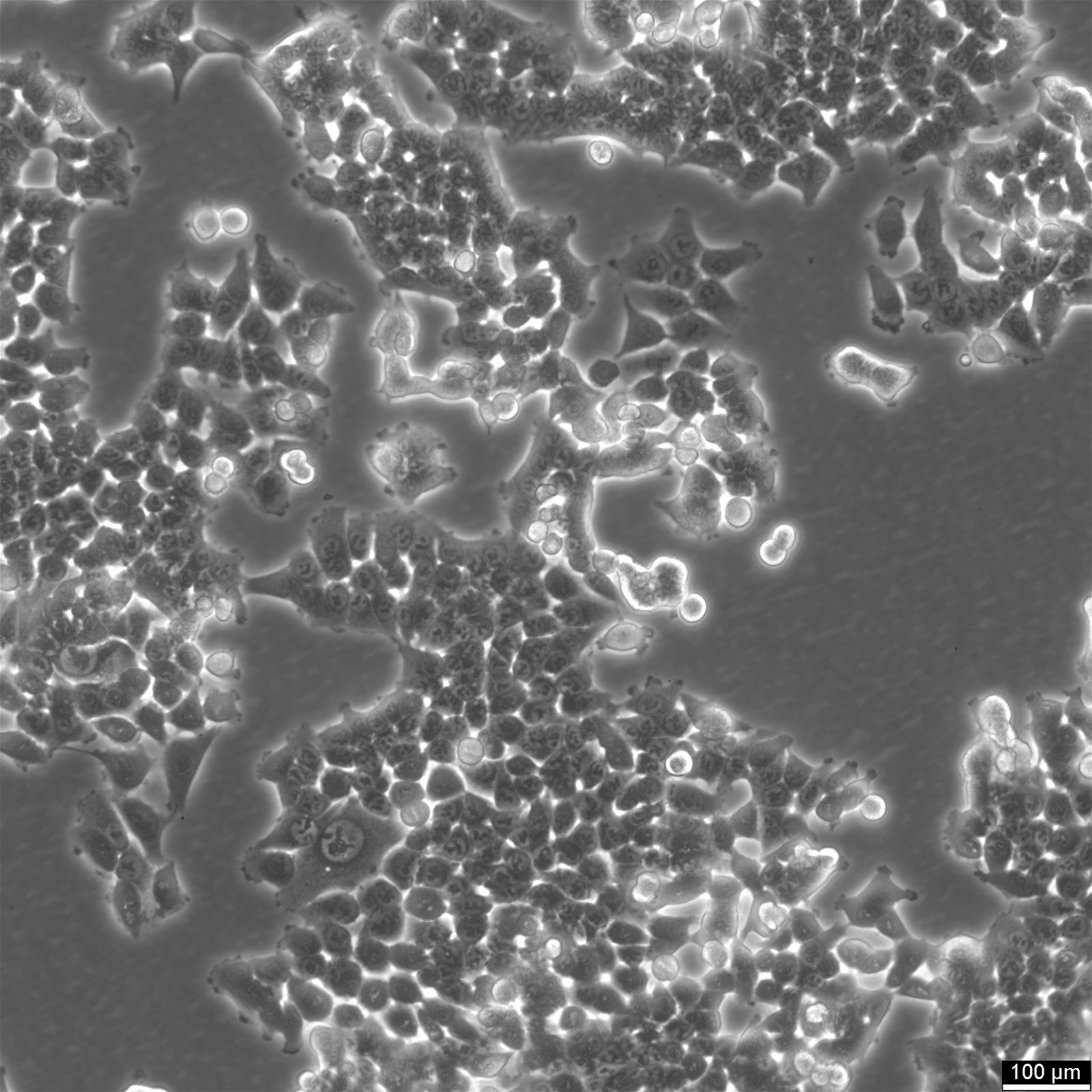
Dòng tế bào HCT116: Một trụ cột trong nghiên cứu ung thư đại trực tràng
Dòng tế bào HCT116 đóng vai trò là nền tảng quan trọng trong việc nghiên cứu ung thư đại trực tràng, cung cấp những hiểu biết quý giá về cơ chế bệnh lý của bệnh và các hướng điều trị tiềm năng. Được biết đến với tính ứng dụng cao trong nghiên cứu ung thư và đánh giá dược lý, HCT116 hỗ trợ các nghiên cứu then chốt về hành vi khối u và hiệu quả của thuốc.
Nguồn gốc và đặc điểm cơ bản của tế bào HCT116
Hiểu rõ nguồn gốc và đặc điểm cơ bản của tế bào HCT116, bao gồm các đặc điểm hình thái, cấu trúc gen và kích thước tế bào, là điều cần thiết cho các nhà nghiên cứu khi tiến hành các nghiên cứu sử dụng dòng tế bào này.
Nguồn gốc và cảnh quan di truyền: Tế bào HCT116 được lấy từ ruột kết của một nam giới da trắng 48 tuổi được chẩn đoán mắc ung thư đại trực tràng, nổi bật với đột biến ở codon 13 (G13D) của gen KRAS, thuộc con đường tín hiệu RAS/RAF/MEK/ERK. Đột biến này đóng vai trò quan trọng trong quá trình biến đổi ung thư của các tế bào này, nhấn mạnh tầm quan trọng của chúng trong nghiên cứu ung thư.
Hình thái và đặc điểm tăng trưởng: Các tế bào HCT116 có hình thái tương tự biểu mô, thường phát triển trong môi trường nuôi cấy lớp đơn nhưng cũng có thể tạo thành các khối cầu có đường kính 150-400 µm. Khả năng thích ứng trong các mô hình tăng trưởng này nhấn mạnh tính linh hoạt của chúng trong các thiết lập thí nghiệm khác nhau.
Hình thái nhiễm sắc thể: Thành phần nhiễm sắc thể của tế bào HCT116 gần như lưỡng bội, với khoảng 70% quần thể tế bào mang 45 nhiễm sắc thể. Đáng chú ý, có sự khuếch đại tái diễn trên cánh dài của các nhiễm sắc thể 8, 10, 16 và 17, trong khi nhiễm sắc thể Y vắng mặt, góp phần tạo nên dấu ấn di truyền độc đáo của chúng.
Phân tích so sánh: Dòng tế bào HCT116 so với HT29
Khi so sánh HCT116 với HT29, một dòng tế bào ung thư đại tràng người khác, những khác biệt rõ rệt về tiềm năng ung thư và khả năng biệt hóa của chúng được thể hiện:
Tiềm năng ung thư và khả năng biệt hóa: Tế bào HCT116 được đặc trưng bởi tiềm năng ung thư cao và khả năng biệt hóa hạn chế, khiến chúng trở thành mô hình để nghiên cứu các biểu hiện ung thư ác tính. Ngược lại, tế bào HT29 có khả năng biệt hóa thành các dòng tế bào tương tự tế bào ruột và sản xuất mucin, cung cấp một mô hình đối lập mô phỏng các khía cạnh đa dạng của sinh học ung thư đại trực tràng.
Sự hiểu biết so sánh về các dòng tế bào HCT116 và HT29 làm phong phú thêm bộ công cụ sẵn có cho các nhà nghiên cứu, cho phép tiến hành các nghiên cứu chi tiết hơn về bản chất đa dạng của ung thư đại trực tràng.
Xử lý tế bào HCT116
|
Thời gian nhân đôi: |
Thời gian nhân đôi của tế bào ung thư HCT116 dao động từ 25 đến 35 giờ. |
|
Dính bám hoặc treo lơ lửng: |
Dòng tế bào ung thư đại tràng HCT116 là tế bào bám dính, phát triển thành lớp đơn. |
|
Mật độ gieo tế bào: |
Mật độ gieo tế bào khuyến nghị cho nuôi cấy tế bào HCT116 là 2 x10⁴tế bào/cm². Đối với việc nuôi cấy lại, tế bào nên được tách ra bằng dung dịch Accutase sau khi rửa bằng 1x PBS. Sau khi ly tâm, khối tế bào được tái phân tán trong môi trường nuôi cấy tươi và chuyển sang bình mới. |
|
Dung dịch nuôi cấy: |
Môi trường McCoys 5a, bổ sung 3,0 g/L L-glucose, 1,5 mM L-glutamine, 3,0 g/LNaHCO₃ và 10% huyết thanh bò non, là tối ưu cho việc nuôi cấy tế bào HCT116. Nên thay đổi môi trường 1 đến 2 lần mỗi tuần. |
|
Điều kiện nuôi cấy (Nhiệt độ,CO2): |
Việc nuôi cấy được thực hiện trong tủ ấm có độ ẩm ở 37°C với môi trườngCO₂ 5%. |
|
Bảo quản: |
Tế bào HCT116 có thể được bảo quản ở nhiệt độ dưới -150°C trong pha hơi hoặc pha lỏng của nitơ lỏng. |
|
Quy trình đông lạnh và môi trường: |
Sử dụng môi trường CM-1 hoặc CM-ACF cho việc bảo quản đông lạnh. Phương pháp đông lạnh có kiểm soát tốc độ được khuyến nghị, cho phép giảm nhiệt độ dần dần 1°C mỗi phút, giúp duy trì khả năng sống của tế bào. |
|
Quy trình rã đông: |
Rã đông tế bào HCT116 trong bể nước 37°C. Sau khi thêm môi trường nuôi cấy, ly tâm để loại bỏ cặn môi trường đông lạnh. Hòa tan lại khối tế bào trong môi trường tươi và nuôi cấy trong bình mới. |
|
Mức độ an toàn sinh học: |
Cấp độ 1 |
Ưu điểm của dòng tế bào HCT116
Phần này đi sâu vào dòng tế bào HCT116, nhấn mạnh vai trò quan trọng của nó trong nghiên cứu ung thư, đặc biệt là trong việc nghiên cứu ung thư đại trực tràng, và thảo luận về những ưu điểm nội tại của nó.
Dòng tế bào HCT116 nổi bật trong nghiên cứu ung thư nhờ một số ưu điểm chính:
Mô hình ung thư đại trực tràng: Nó được công nhận rộng rãi là mô hình in vitro cho ung thư đại trực tràng, loại ung thư phổ biến thứ ba trên thế giới. Khả năng mô phỏng ung thư đại trực tràng ở người của nó khiến nó trở nên vô giá trong việc hiểu về sinh học ung thư và thử nghiệm các chiến lược điều trị.
Đồng nhất: Đáng chú ý, khoảng 70% tế bào HCT116 có hồ sơ di truyền nhất quán, tạo ra một quần thể tương đối đồng nhất. Sự đồng nhất này rất quan trọng cho các nghiên cứu tập trung vào biểu hiện gen, các con đường tín hiệu tế bào và đánh giá hiệu quả của các liệu pháp thuốc, vì nó đảm bảo tính nhất quán và độ tin cậy trong kết quả thí nghiệm.
Hiệu quả chuyển gen: Một trong những đặc điểm nổi bật của tế bào HCT116 là khả năng tiếp nhận chuyển gen cao, đặc biệt với các vectơ virus. Đặc điểm này đặc biệt hữu ích trong nghiên cứu liệu pháp gen, cho phép đưa vật liệu di truyền vào tế bào với hiệu quả và độ chính xác cao, từ đó hỗ trợ các thao tác di truyền phức tạp và nghiên cứu chức năng.
Nâng cao các phát hiện của bạn với dòng tế bào HCT116 đã được xác thực của chúng tôi
Ứng dụng nghiên cứu của dòng tế bào HCT116
Dòng tế bào HCT116 có nhiều ứng dụng đa dạng trong nghiên cứu ung thư. Một số ứng dụng nổi bật bao gồm:
Sinh học ung thư
Dòng tế bào ung thư đại tràng HCT116 được sử dụng để nghiên cứu sự tiến triển và phát triển của ung thư đại tràng. Ngoài ra, nó giúp làm sáng tỏ các cơ chế và con đường tín hiệu liên quan đến sự phát triển, di chuyển và xâm lấn của tế bào ung thư. Một nghiên cứu đã sử dụng tế bào HCT116 để nghiên cứu các gen liên quan đến sự phát triển kháng thuốc. Các nhà nghiên cứu đã tăng biểu hiện gen MDR1 trong tế bào ung thư đại tràng và quan sát biểu hiện của các isoform NOX (NADPH oxidase) và Nrf2. Nghiên cứu cho thấy sự tăng biểu hiện của NOX2 và Nrf2 gây ra kháng thuốc trong tế bào ung thư; do đó, các gen này có thể được nhắm mục tiêu để vượt qua sự phát triển kháng thuốc trong điều trị ung thư [1]. Tương tự, một nghiên cứu được thực hiện vào năm 2021 báo cáo rằng con đường tín hiệu NF-κB tham gia vào việc điều chỉnh sự phát triển và di chuyển của ung thư đại tràng. Do đó, nó có thể được nhắm mục tiêu để phát triển các liệu pháp mới và hiệu quả chống lại ung thư đại tràng [2].
Trong lĩnh vực ung thư học, việc hiểu rõ các quá trình phức tạp của chu kỳ tế bào, sự phát triển và tăng trưởng, cũng như quá trình apoptosis là cơ bản. Các chức năng sinh học này đóng vai trò quan trọng trong nghiên cứu các dòng tế bào người, đặc biệt là những dòng tế bào được phân lập từ các tế bào ung thư như tế bào ung thư đại tràng người và mô hình ung thư tụy. Các dòng tế bào HCT116 và SW620, ví dụ, đóng vai trò quan trọng trong việc khám phá các cơ chế cơ bản của ung thư đại tràng và ung thư tụy, tương ứng. Thông qua các kỹ thuật như phân tích dòng chảy và thử nghiệm tạo khối u, các nhà nghiên cứu có thể làm sáng tỏ các mẫu biểu hiện gen và hành vi của các tế bào độc lập trong khối u, từ đó hiểu rõ hơn cách ung thư tương tác trong ma trận ngoại bào.
Vai trò của apoptosis trong tiến triển ung thư
Apoptosis, hay chết tế bào có chương trình, đóng vai trò quan trọng trong việc duy trì cân bằng tế bào và là lĩnh vực nghiên cứu chính trong ung thư học. Sự phân biệt giữa apoptosis không liên quan và apoptosis được kích hoạt cụ thể trong bối cảnh ung thư, như cái chết của tế bào ung thư đại tràng, là rất quan trọng. Quá trình này không chỉ liên quan đến việc loại bỏ tế bào mà còn bao gồm sự tương tác phức tạp của các tín hiệu có thể ảnh hưởng đến sự phát triển khối u và di căn. Bằng cách nghiên cứu apoptosis và cái chết của tế bào kết hợp với các yếu tố ức chế di căn và hoạt động ức chế khối u, các nhà khoa học có thể hiểu rõ hơn về các con đường điều chỉnh sự tiến triển của ung thư và tiềm năng di căn.
Di căn và các dấu hiệu phân tử trong ung thư
Di căn vẫn là một trong những khía cạnh đáng sợ nhất của ung thư, với di căn qua đường máu là một mối quan tâm lớn trong việc lan rộng của các tế bào ác tính. Việc nghiên cứu di căn bao gồm việc tìm hiểu khả năng di chuyển và xâm lấn của tế bào ung thư, hay còn gọi là vận động tế bào, và cách các tế bào tương tác với môi trường xung quanh, bao gồm ma trận ngoại bào. Các dấu hiệu phân tử như biểu hiện CD133 và thụ thể yếu tố tăng trưởng biểu bì là yếu tố quan trọng trong việc xác định và hiểu hành vi của các tế bào ung thư đại tràng dương tính và các loại ung thư khác. Con đường SIRT6, ví dụ, đã trở thành một lĩnh vực nghiên cứu quan trọng do vai trò tiềm năng của nó trong việc điều chỉnh sự phát triển khối u và ung thư đại tràng di căn.
Độc học/phát triển thuốc
Dòng tế bào HCT116 được sử dụng làm mô hình sàng lọc cho các loại thuốc chống ung thư mới. Nhiều nghiên cứu đã được tiến hành để đánh giá hiệu quả và độc tính của các loại thuốc chống ung thư, bao gồm các sản phẩm tự nhiên và các hạt nano tổng hợp hóa học. Do đó, nghiên cứu đã đánh giá độc tính tế bào của các hạt nano bạc tổng hợp từ chiết xuất của thuốc thảo dược Caesalpinia pulcherrima trên tế bào HCT116 [3]. Trong một nghiên cứu, các nhà nghiên cứu đã sử dụng dòng tế bào ung thư HCT116 để đánh giá tiềm năng chống ung thư của chiết xuất nước trà ca cao. Họ phát hiện ra rằng chiết xuất trà ca cao làm giảm sự phát triển của ung thư đại tràng và gây chết tế bào [4]. Một nghiên cứu khác sử dụng tế bào ung thư HCT116 và phát hiện ra rằng chiết xuất từkhoai mỡ, Dioscorea bulbifera, có hoạt tính gây chết tế bào trong các tế bào ung thư đại tràng thông qua việc kích hoạt chuỗi tín hiệu JNK và ức chế gen ERK1/2 [5].
Tác động của metformin đối với tế bào ung thư, đặc biệt trong bối cảnh ung thư đại tràng và tụy, minh họa cách hiểu rõ các chức năng sinh học của tế bào ung thư có thể dẫn đến các chiến lược điều trị tiềm năng. Nghiên cứu về khả năng sinh tồn clonogenic, tức khả năng hình thành các dòng tế bào, của tế bào ung thư sau khi điều trị bằng các tác nhân như metformin hoặc nhắm vào các con đường cụ thể như thụ thể yếu tố tăng trưởng biểu bì có thể cung cấp những hiểu biết quý giá về các phương pháp điều trị ung thư hiệu quả. Ngoài ra, việc sử dụng các dòng tế bào HCT116 và quần thể tế bào HCT116 trong các nghiên cứu này cho phép hiểu rõ hơn về cách tế bào ung thư phản ứng với các can thiệp điều trị khác nhau, mở đường cho các phương pháp điều trị ung thư cá nhân hóa hơn.
Tế bào HCT116: Các công bố nghiên cứu
Phần này sẽ giới thiệu một số công bố nghiên cứu quan trọng và được trích dẫn nhiều nhất gần đây sử dụng dòng tế bào HCT116.
Nghiên cứu này được công bố trên tạp chí Journal of Photochemistry and Photobiology B: Biology (2017). Các nhà nghiên cứu đã sử dụng dòng tế bào ung thư đại tràng HCT116 và dòng tế bào ung thư phổi A549 để đánh giá tác dụng độc tế bào của các hạt nano oxit thiếc được tổng hợp từ hạt tiêu đen.
Nghiên cứu này trên Tạp chí Cancer Letters (2018) đề xuất rằng lncRNA SNHG15 thúc đẩy sự di chuyển của tế bào ung thư đại tràng trong các dòng tế bào ung thư đại tràng, bao gồm HCT116.
Sự biểu hiện quá mức của RNA không mã hóa dài TUG1 thúc đẩy sự tiến triển của ung thư đại tràng
Bài báo này được công bố trên tạp chí Medical Science Monitor vào năm 2016. Nghiên cứu cho thấy RNA không mã hóa oncogenic TUG1 thúc đẩy sự phát triển và di chuyển của tế bào ung thư đại tràng HCT116.
Nghiên cứu trên tạp chí Biochemical Pharmacology (2018) đề xuất rằng sự phát triển kháng thuốc làm tăng mức độ của các enzym sản xuất H2S trong tế bào ung thư đại tràng HCT116.
Bài báo nghiên cứu trên tạp chí International Journal of Environmental Health Research (2023) đề xuất rằng chiết xuất Inula viscosa L. có tác dụng chống ung thư trên tế bào ung thư đại tràng HCT116 thông qua điều chỉnh microRNA.
Tài nguyên cho tế bào HCT116
Dưới đây là một số tài nguyên về dòng tế bào HCT116.
- Tiêm gen vào HCT116: Video này là hướng dẫn từng bước để tiêm gen vào tế bào ung thư HCT116.
- Nuôi cấy dòng tế bào HCT116: Video này trình bày quy trình nuôi cấy lại dòng tế bào ung thư đại tràng HCT116.
- Tái nuôi cấy dòng tế bào HCT116: Trang web này chứa nhiều thông tin hữu ích về môi trường nuôi cấy HCT116. Ngoài ra, nó cung cấp các quy trình đông lạnh, rã đông và tái nuôi cấy tế bào.
Câu hỏi thường gặp về tế bào HCT116
Tài liệu tham khảo
- Waghela, B.N., F.U. Vaidya, và C. Pathak: Sự tăng biểu hiện của NOX-2 và Nrf-2 thúc đẩy sự kháng thuốc 5-fluorouracil trong tế bào ung thư đại tràng người (HCT-116). Biochemistry (Moscow), 2021, 86, tr. 262-274.
- Yang, M., et al., Astragalin ức chế sự tăng sinh và di chuyển của tế bào ung thư đại tràng HCT116 ở người bằng cách điều chỉnh con đường tín hiệu NF-κB. Frontiers in Pharmacology, 2021, 12: tr. 639256.
- Deepika, S., C.I. Selvaraj, và S.M. Roopan, Đánh giá hoạt tính sinh học của Caesalpinia pulcherrima L. Swartz và độc tính của các hạt nano bạc tổng hợp trên dòng tế bào HCT116. Khoa học Vật liệu và Kỹ thuật, C, 2020, 106, tr. 110279.
- Gao, X., et al., Trà ca cao (Camellia ptilophylla) gây ra apoptosis phụ thuộc vào ty thể trong tế bào HCT116 thông qua việc sinh ra ROS và con đường tín hiệu PI3K/Akt. Nghiên cứu Thực phẩm Quốc tế, 2020, 129, tr. 108854.
- Hidayat, A.F.A., et al., Dioscorea bulbifera gây ra quá trình apoptosis thông qua ức chế con đường tín hiệu ERK 1/2 và kích hoạt con đường tín hiệu JNK trong tế bào ung thư đại tràng người HCT116. Biomedicine & Pharmacotherapy, 2018. 104: tr. 806-816.