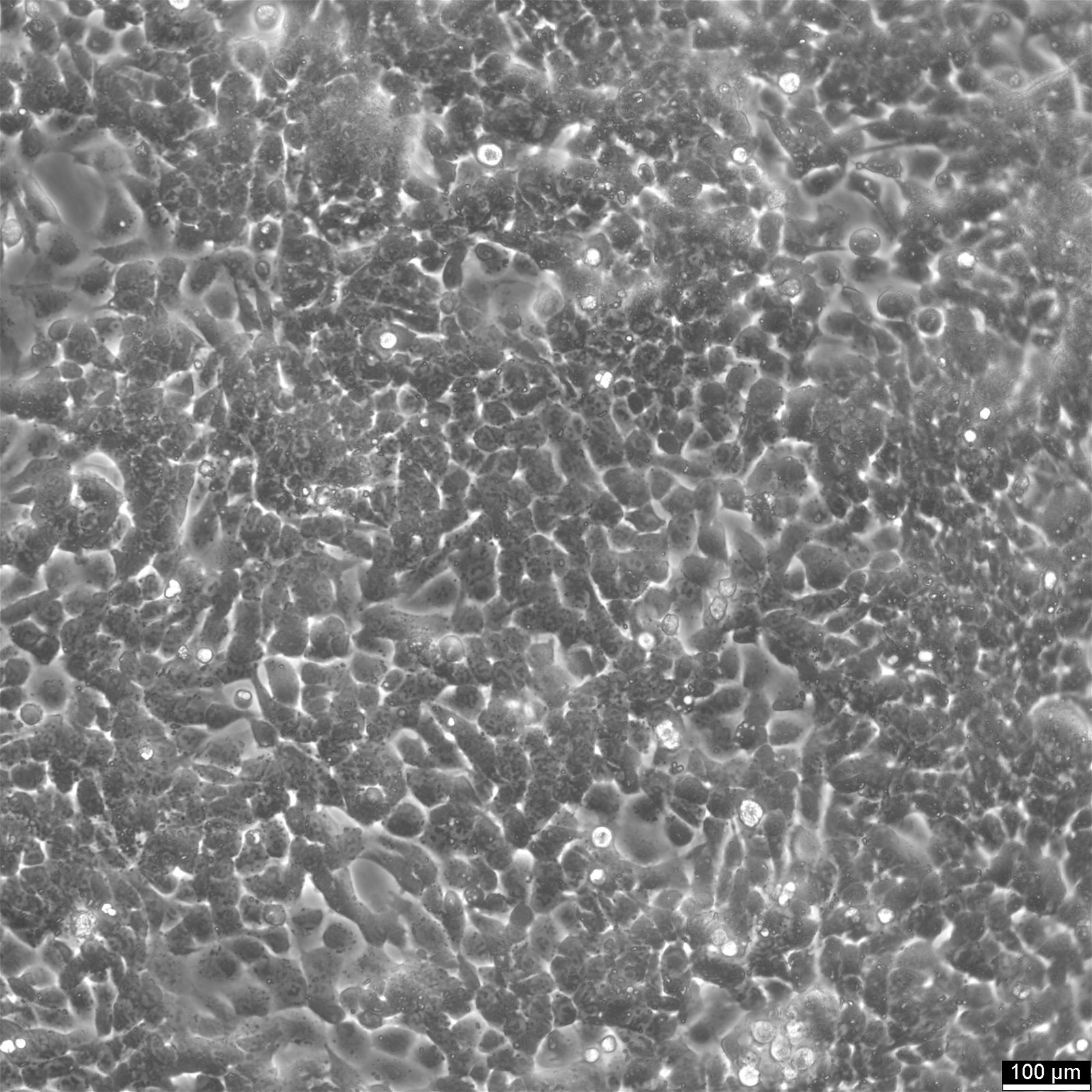
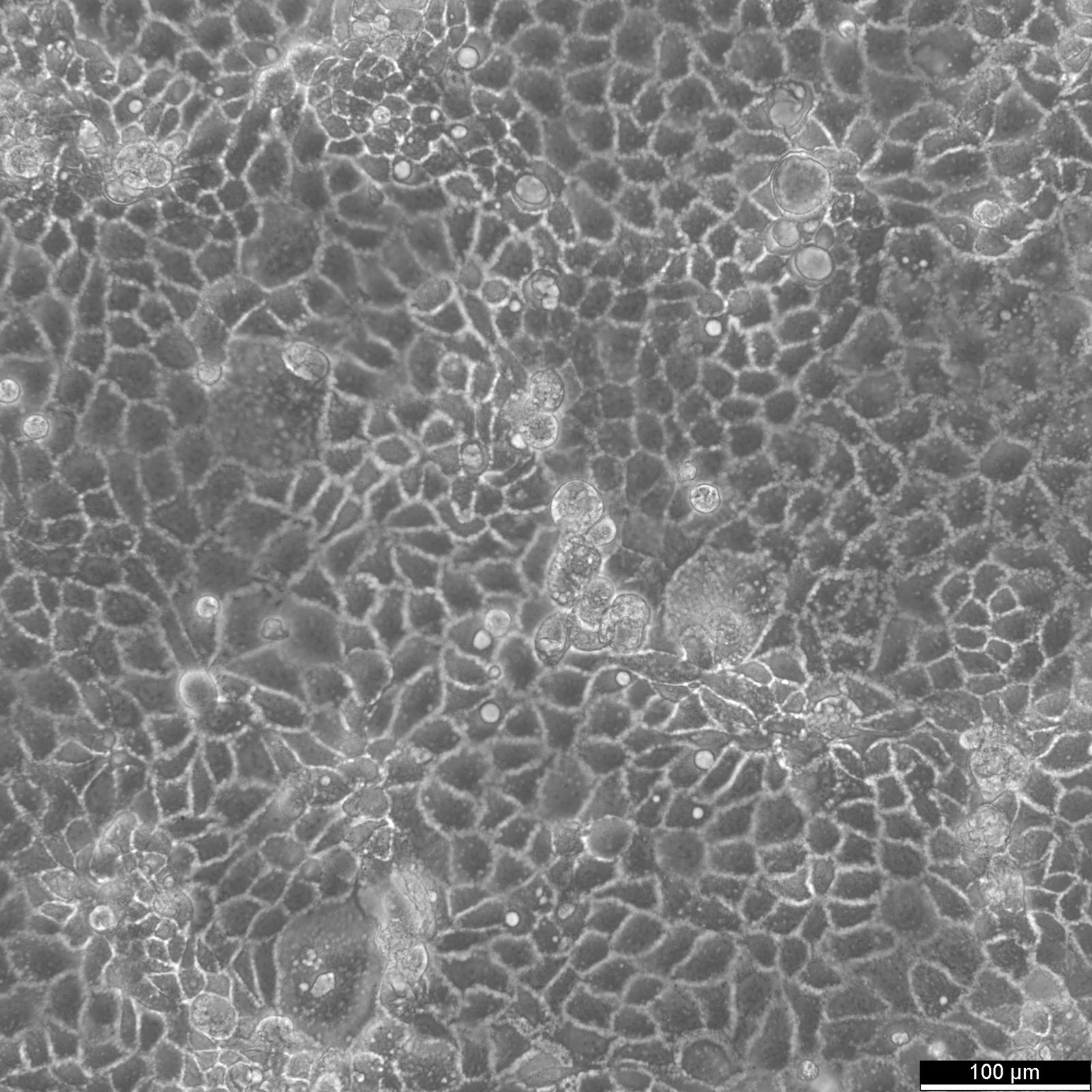
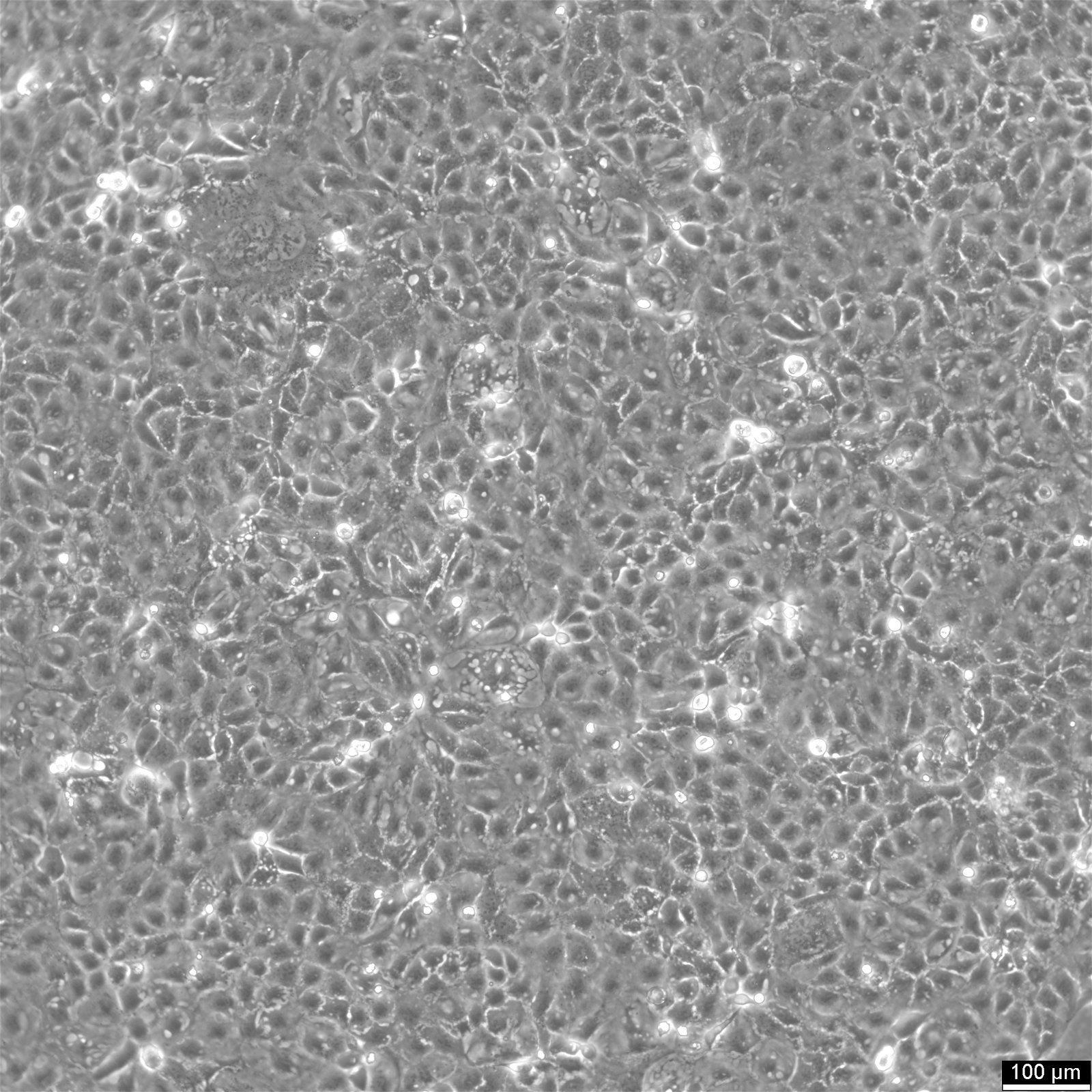
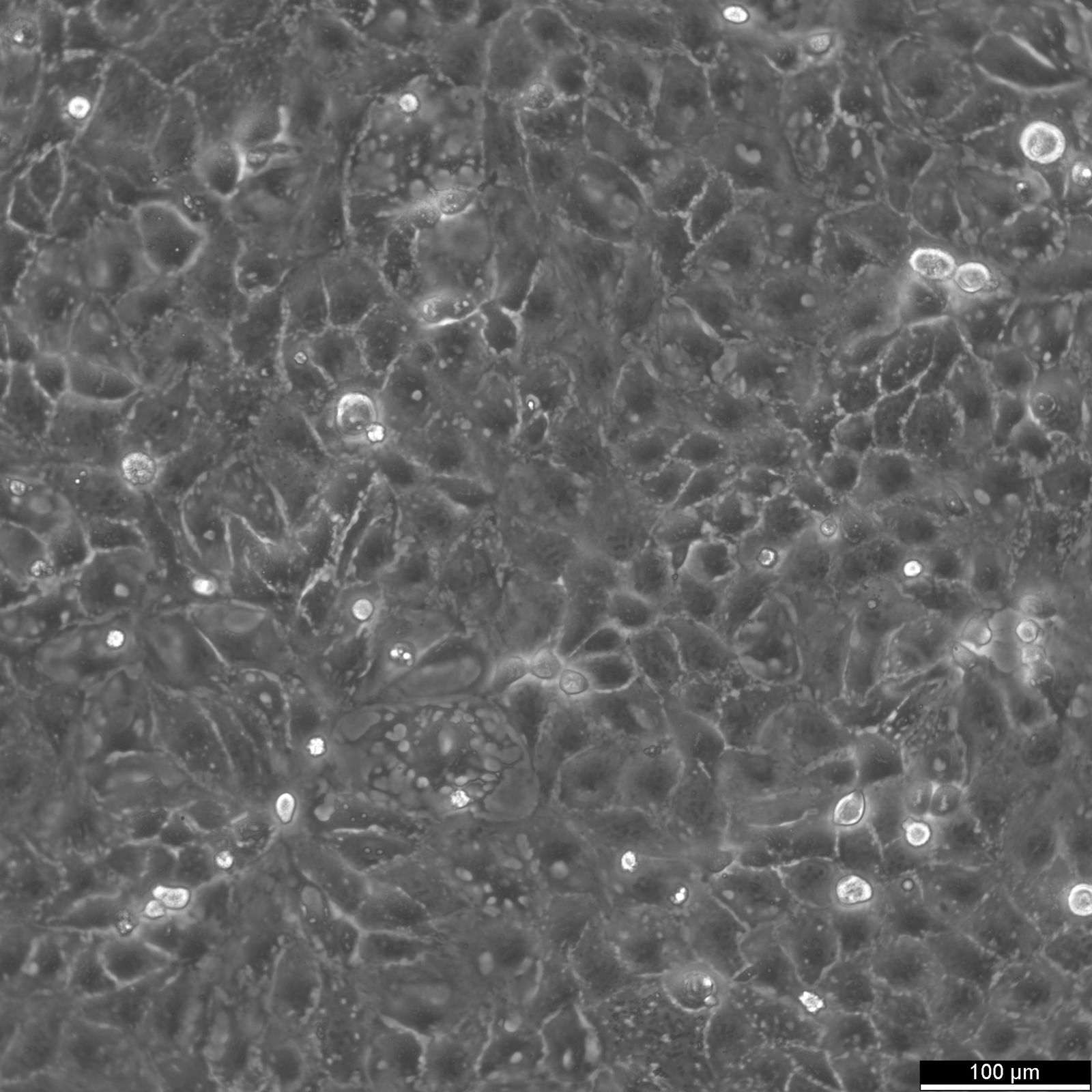
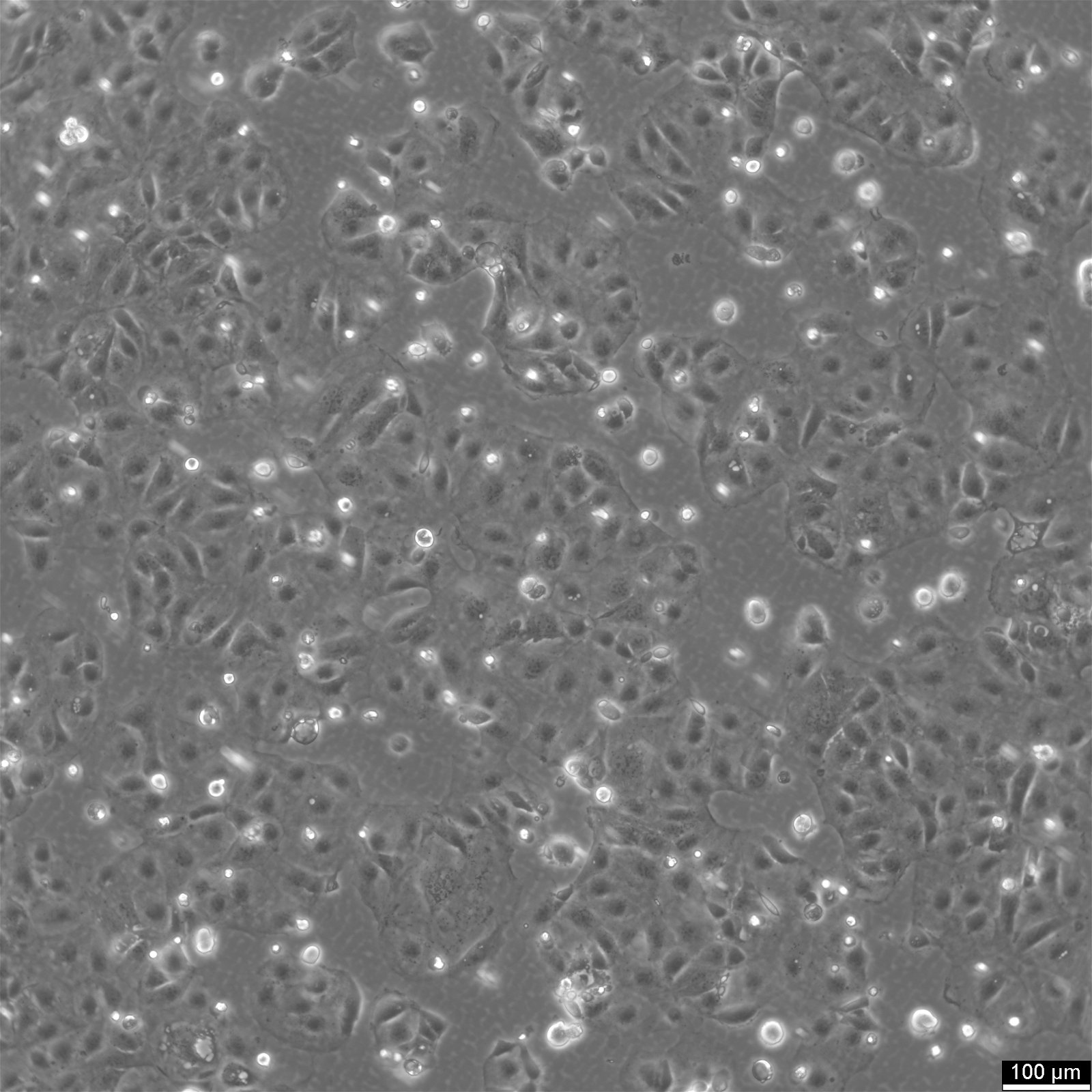
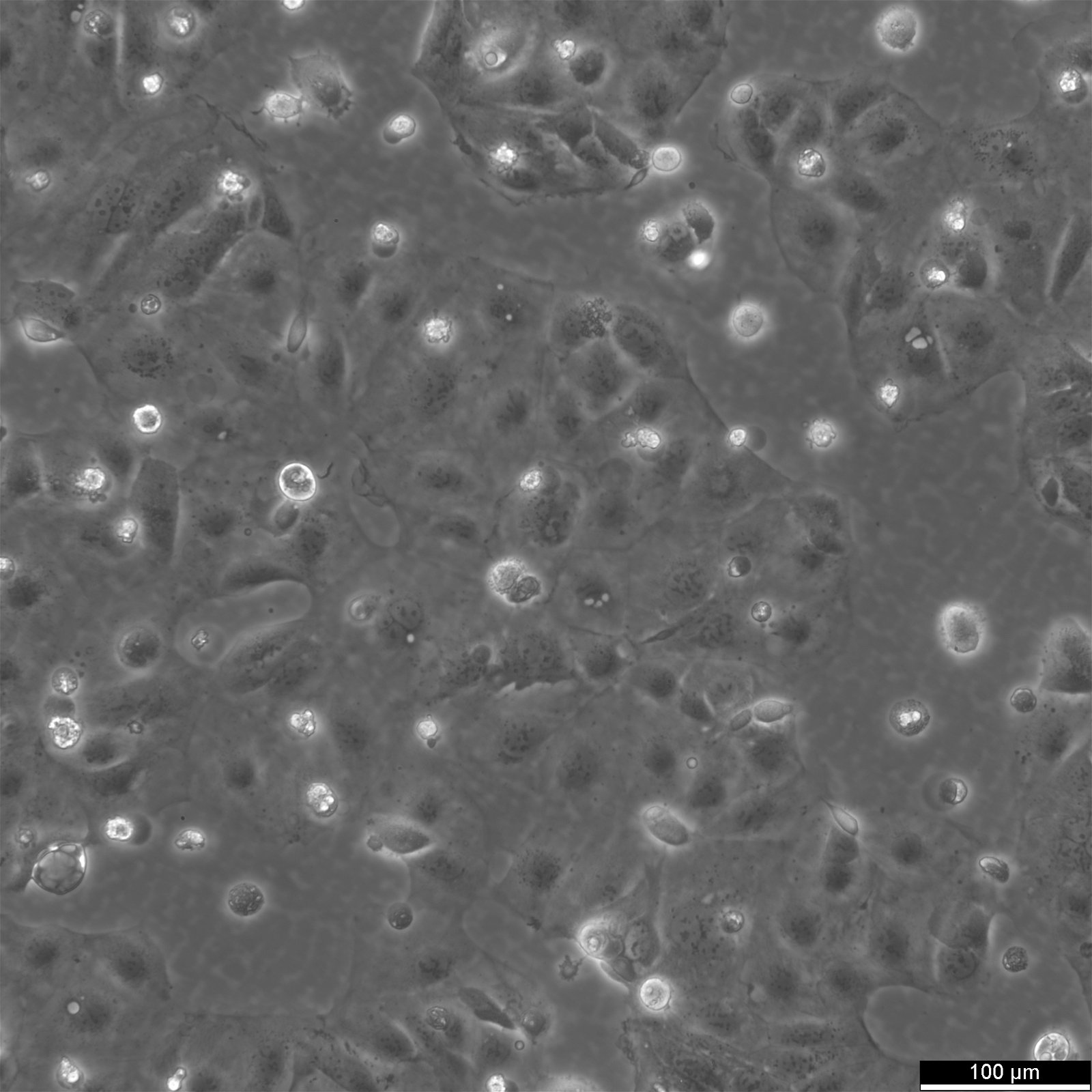
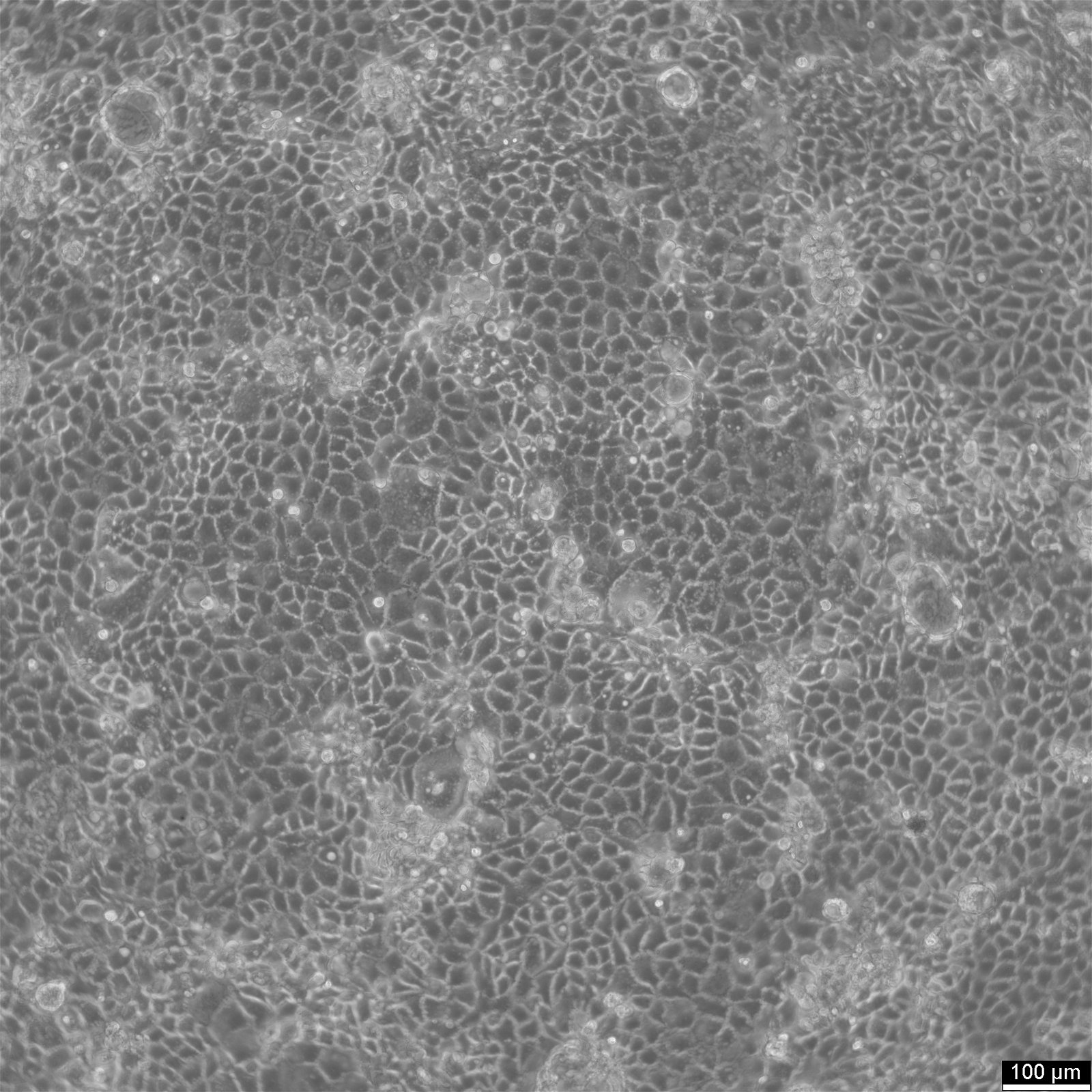
Caco-2-celler






















430,00 €*
Produktene sendes frosset på tørris i kryorør. Hvert kryorør inneholder vanligvis 3 × 10 6 celler for vedheftende linjer eller 5 × 106 celler for suspensjonslinjer (se batch-CoA for detaljer).
Introduksjon til Caco-2-celler
| Beskrivelse | Caco-2-celler er en avansert in vitro-modell for den humane tarmbarrieren, først og fremst fordi de kan differensieres til et cellelag som ligner på enterocyttene i tynntarmen. Ved dyrking av Caco2-cellelinjen på vevskulturfilterinnlegg med polykarbonatfiltre gjennomgår Caco-2-celler spontan differensiering. Differensieringen av Caco2-celler resulterer i uttrykk av spesialiserte celletyper, komplett med mikrovilli, enzymer og transportører, noe som er en parallell til de komplekse funksjonene og mekanismene som finnes i en in vivo-situasjon. I forbindelse med modeller for studier av tarmabsorpsjon er Caco-2-celler, som stammer fra en human kolorektal adenokarsinom-pasient, viktige på grunn av deres evne til å utvikle høye TEER-verdier, noe som tyder på intakte tight junctions og epitelbarrierefunksjon. Disse egenskapene er avgjørende for analyser som kolesterolutstrømmingsanalysen og undersøkelser av celletransport, inkludert bevegelse av lipidnanopartikler og påvisning av proteininteraksjoner. Caco-2-celler er avgjørende for studier av tarmabsorpsjon, ettersom de gir en pålitelig in vitro-tilnærming av tarmepitelet. Disse cellene etterligner tarmens enterocytter og gjør det enklere å analysere oral legemiddelabsorpsjon ved å simulere tarmbarrieren. Forskere bruker Caco-2-celler til å forutsi hvordan stoffer passerer tarmslimhinnen, noe som er avgjørende for den farmakokinetiske profileringen av orale legemidler. Caco-2-celler er også et viktig verktøy for å undersøke opptak, homeostase og transport av kolesterol i tarmen, noe som er avgjørende for å forstå lipidmetabolismen og tilknyttede sykdommer. Caco-2-celler er fortsatt en hjørnestein i forskning på tykktarmskarsinom og toksikologi, ikke bare på grunn av sin relevans for gastrointestinale studier på mennesker, men også fordi de gir detaljert innsikt i galleveiene, metabolismen av xenobiotika i tykktarmen, kreft og toksikologisk forskning. |
|---|---|
| Organisme | Menneskelig |
| Vev | Colon |
| Sykdom | Adenokarsinom |
| Bruksområder | Modell av mage-tarmkanalen, måling av transepitelial/endotelial elektrisk motstand (TEER). Caco-2-celler utvikler høye TEER-verdier på opptil 2000 cm2 (målt med CLS ved hjelp av CellZscope, nanoAnalytics, Münster, Tyskland). |
| Synonymer | CaCo-2, CACO-2, Caco 2, CACO 2, CACO2, CaCo2, CaCO2, Caco2, Caco-II |
Detaljer
| Alder | 72 år |
|---|---|
| Kjønn | Mann |
| Etnisitet | Kaukasisk |
| Morfologi | Epitel-lignende |
| Vekstegenskaper | Vedhengende |
Dokumentasjon
| Sitat | CaCo-2 (Cytion katalognummer 300137) |
|---|---|
| Biosikkerhetsnivå | 1 |
| NCBI_TaxID | 9606 |
| CellosaurusAccession | CVCL_0025 |
Genetisk sammensetning av Caco-2-cellelinjen
| Uttrykte reseptorer | Varmestabilt enterotoksin (Sta, E. coli), epidermal vekstfaktor (EGF), retinsyrebindende protein I og retinolbindende protein II, keratinpositiv. |
|---|---|
| Antigenuttrykk | Blodtype O, Rh+, HLA klasse II negativ |
| Isoenzymer | Me-2, 1, PGM3, 1, PGM1, 1, ES-D, 1, AK-1, 1, GLO-1, 1, G6PD, B. |
| Tumorfremkallende | Ja, i nakne mus. Danner moderat godt differensierte adenokarsinomer som er forenlige med primærkolon (grad II) |
| Virusresistens | Humant immunsviktvirus (HIV, LAV) |
| Ploidistatus | (P14), hypertetraploid |
| MSI-status | Stabil (MSS) |
Håndtering
| Kulturmedium | EMEM (MEM Eagle), m: 2 mM L-Glutamin, m: 2,2 g/L NaHCO3, m: EBSS (Cytion artikkelnummer 820100a) |
|---|---|
| Kosttilskudd | Suppler mediet med 10 % FBS og 1 % NEAA |
| Dissosiasjonsreagens | Accutase |
| Doblingstid | 60 til 70 timer |
| Subkulturer | Fjern det gamle mediet fra de adherente cellene, og vask dem med PBS uten kalsium og magnesium. Bruk 3-5 ml PBS for T25-kolber og 5-10 ml for T75-kolber. Dekk deretter cellene helt med Accutase, med 1-2 ml for T25-kolber og 2,5 ml for T75-kolber. La cellene inkubere i romtemperatur i 8-10 minutter for å løsne dem. Etter inkubasjon blandes cellene forsiktig med 10 ml medium for å resuspendere dem, og sentrifuger deretter ved 300xg i 3 minutter. Kast supernatanten, resuspender cellene i nytt medium, og overfør dem til nye kolber som allerede inneholder nytt medium. |
| Delingsforhold | Et forhold på 1:2 til 1:3 anbefales |
| Såtetthet | 1 x 104 celler/cm2 vil resultere i et 90 % konfluent monolag i løpet av omtrent 4 dager. |
| Gjenoppretting etter tining | Etter tining, plasser cellene på 5 x 104 celler/cm2 og la cellene komme seg etter fryseprosessen og feste seg i minst 24 timer. |
| Frys medium | Som kryopreserveringsmedium bruker vi komplett vekstmedium (inkludert FBS) + 10 % DMSO for tilstrekkelig levedyktighet etter opptining, eller CM-1 (Cytion-katalognummer 800100), som inneholder optimaliserte osmobeskyttende midler og metabolske stabilisatorer for å øke utvinningen og redusere kryoindusert stress. |
| Opptining og dyrking av celler |
|
| Inkubasjonsatmosfære | 37 °C, 5 %CO2, befuktet atmosfære. |
| Flaskebelegg | Ingen |
| Fryseprosedyre | Kryopreserverte cellelinjer sendes på tørris i validert, isolert emballasje med tilstrekkelig kjølemiddel til å opprettholde en temperatur på ca. -78 °C under hele transporten. Ved mottak skal beholderen inspiseres umiddelbart, og hetteglassene skal straks overføres til egnet lagringsplass. |
| Leveringsbetingelser | Kryopreserverte cellelinjer sendes på tørris i validert, isolert emballasje med tilstrekkelig kjølemiddel til å opprettholde en temperatur på ca. -78 °C under hele transporten. Ved mottak skal beholderen inspiseres umiddelbart, og hetteglassene skal straks overføres til egnet lagringsplass. |
| Lagringsforhold | For langtidsoppbevaring plasseres hetteglassene i flytende nitrogen i dampfase ved ca. -150 til -196 °C. Lagring ved -80 °C er kun akseptabelt som et kort mellomtrinn før overføring til flytende nitrogen. |
Kvalitetskontroll
| Sterilitet | Mykoplasma-kontaminering utelukkes ved hjelp av både PCR-baserte analyser og luminescensbaserte metoder for påvisning av mykoplasma. For å sikre at det ikke finnes bakterie-, sopp- eller gjærkontaminering, blir cellekulturene inspisert visuelt hver dag. |
|---|---|
| STR-profil |
Amelogenin: x,x
CSF1PO: 11
D13S317: 11, 13, 14
D16S539: 12, 13
D5S818: 12, 13
D7S820: 11, 12
TH01: 6
TPOX: 9, 11
vWA: 16, 18
D3S1358: 14, 17
D21S11: 30, 32
D18S51: 12
D8S1179: 12, 14
FGA: 19
D1S1656: 15, 16
D2S1338: 17, 25
D12S391: 17, 23
D19S433: 15
|
| HLA-alleler |
A*: '02:01:01
B*: '15:01:01
C*: '04:01:01
DRB1*: '04:04:01
DQA1*: '03:01:01
DQB1*: '03:02:01
DPB1*: '04:01:01
E: '01:03:02
|
Analysesertifikat (CoA)
| Partienummer | Sertifikattype | Dato | Katalognummer |
|---|---|---|---|
| 300137-220424 | Analysesertifikat | 23. May. 2025 | 300137 |
| 300137-170625 | Analysesertifikat | 18. Aug. 2025 | 300137 |
Avtale om materialoverføring
Hvis du har tenkt å bruke Cytion-cellelinjer utelukkende til intern forskning på ett enkelt forskningssted, må du fylle ut og signere vår materialoverføringsavtale (MTA) og sende den sammen med bestillingen din.
For alle kommersielle anvendelser – inkludert, men ikke begrenset til, betaling for tjenester, kvalitetskontrolltesting, produktutgivelse, diagnostisk bruk eller regulatoriske studier – vennligst fyll ut skjemaet for tiltenkt bruk, slik at vi kan utarbeide en avtale som er tilpasset prosjektet ditt.
Merk: MTA gjelder kun for visse cellelinjer. Hvis denne merknaden og MTA-dokumentet vises på en produktside, gjelder avtalen. For cellelinjer som ikke dekkes av MTA, vil det ikke vises noen henvisning til avtalen. MTA er ikke gyldig for kunder i Amerika, Kina eller Taiwan. Kontakt vårt amerikanske selskap for å motta den aktuelle avtalen.
-
Nødvendige produkter
Nødvendige produkter
Frysemedium CM-1 - 50 mlVarianter av kryopreserveringsmedier: 50 mlCytions frysemedium CM-1 er et toppmoderne kryopreserveringsmedium som er utviklet for å sikre det høyeste nivået av cellelevedyktighet og funksjonalitet etter opptining. Dette allsidige mediet er egnet for et bredt spekter av celletyper, inkludert både humane og animalske celler, noe som gjør det til et viktig verktøy for ulike forskningsapplikasjoner. Freeze Medium CM-1 er formulert med en nøye balansert kombinasjon av kryobeskyttende midler og essensielle næringsstoffer, og minimerer dannelsen av iskrystaller og cellestress under fryseprosessen, slik at cellenes integritet bevares.
De viktigste egenskapene til Freeze Medium CM-1 inkluderer
Bred kompatibilitet: Effektivt for et bredt spekter av celletyper, inkludert primærceller, stamceller og etablerte cellelinjer.
Høy levedyktighet: Optimalisert for å maksimere cellegjenvinning og levedyktighet etter opptining, noe som sikrer pålitelige eksperimentelle resultater.
Klar til bruk: Praktisk tilberedt og sterilisert for umiddelbar bruk, noe som reduserer forberedelsestiden og risikoen for kontaminering.
Forbedret stabilitet: Opprettholder konsistent ytelse under standard kryopreserveringsforhold, noe som sikrer reproduserbare resultater.
Lang holdbarhet: CM-1 er et serumholdig kryopreserveringsmedium som er klart til bruk, og som kan oppbevares i kjøleskapet i opptil ett år.
Bruk av CM-1 til nedfrysing av celler
Følg disse trinnene for å bruke CM-1 til nedfrysing av både adherente celler og suspensjonsceller
For adherente celler, vask og dissosier dem fra kultursubstratet. For suspensjonsceller går du direkte til neste trinn.
Tell cellene for å sikre at de har riktig konsentrasjon.
Sentrifuger cellene for å pelleter dem, og resuspender dem deretter i CM-1-frysemedium.
Overfør de resuspenderte cellene til kryovialer.
Bruk en langsom nedfrysingsmetode før du overfører cellene til langtidslagring
Metode
Beskrivelse
Trinn
❄️
Manuell frysing
En trinnvis metode som innebærer gradvis reduksjon av temperaturen for å sikre cellenes levedyktighet
1️⃣ Plasser celler i frysemedium i en fryser på 4 °C i 40 minutter.
2️⃣ Overfør til en fryser på -80 °C i 24 timer.
3️⃣ Oppbevar cellene i flytende nitrogen for langtidsoppbevaring
❄️
Bruk av Mr. Frosty
Et praktisk apparat som gjør det mulig å kontrollere frysehastigheten uten elektrisk strøm
1️⃣ Klargjør celler i kryovialer med frysemedium.
2️⃣ Plasser kryovialene i Mr. Frosty-beholderen.
3️⃣ Oppbevares ved -80 °C i 24 timer før de overføres til flytende nitrogen
❄️
Fryser med kontrollert hastighet
En høypresisjonsfryser fra Thermo Fisher eller andre produsenter som er utviklet for kontrollert temperaturreduksjon
1️⃣ Programmer enheten til å senke temperaturen gradvis.
2️⃣ Plasser de forberedte cellene i fryseren.
3️⃣ Etter frysesyklusen overføres cellene til flytende nitrogen
Oppbevar kryovialene ved temperaturer under -130 °C eller i flytende nitrogen for langtidsoppbevaring.
Ingredienser
Inneholder FBS, DMSO, glukose, salter
Bufferkapasitet: pH = 7,2 til 7,6
Cytions frysemedium CM-1 er en pålitelig løsning for kryopreservering som sikrer høy cellelevedyktighet og funksjonalitet etter opptining for et bredt spekter av forskningsapplikasjoner.59,00 €*EMEM (MEM Eagle), m: 2 mM L-Glutamin, m: 2,2 g/L NaHCO3, m: EBSSEagle’s Minimum Essential Medium (EMEM) er et av de mest brukte basismediene for dyrking av et bredt spekter av pattedyrceller, særlig vedheftende cellelinjer. Denne klassiske formuleringen, som opprinnelig ble utviklet av Harry Eagle, inneholder de essensielle aminosyrene, vitaminene og de uorganiske saltene som kreves for å støtte veksten av både primærceller og etablerte cellelinjer under standard dyrkingsforhold.
Denne bruksklare, sterilt filtrerte flytende formuleringen er tilsatt Earle’s Balanced Salt Solution (EBSS), 2 mM L-glutamin, D-glukose (1,0 g/l) og 2,2 g/l natriumbikarbonat (NaHCO3), noe som gjør den egnet for bruk i en CO2-kontrollert inkubatoratmosfære (typisk 5 % CO2). Det inkluderte fenolrød fungerer som en pH-indikator, noe som muliggjør praktisk visuell overvåking av mediumtilstanden under cellekulturen.
Viktige egenskaper
Klassisk Eagles MEM-formulering med Earles balanserte saltløsning (EBSS)
2 mM L-glutamin inkludert – klar til umiddelbar bruk
2,2 g/L natriumbikarbonat – bufret for inkubasjon med 5 % CO2
Med D-glukose (1,0 g/l) som primær karbonkilde
Med fenolrødt som pH-indikator
Uten HEPES og uten natriumpyruvat
Sterilfiltrert flytende medium, klar til bruk
pH 7,0 – 7,6
Typiske anvendelser
EMEM støtter dyrking av et bredt utvalg av pattedyrcellelinjer, inkludert HeLa, HEK 293, Vero, MRC-5, L-929, BHK-21 og mange primærceller. Vanlige bruksområder inkluderer:
Rutinemessig vedlikehold og utvidelse av vedheftende cellelinjer
Arbeidsflyter for virusformering og vaksineproduksjon
Cytotoksisitet og bioassay-anvendelser
Studier av transfeksjon og proteinekspresjon
Grunnleggende forskning innen cellebiologi og molekylærbiologi
For optimal cellevekst tilsettes EMEM vanligvis 5–10 % føtal bovint serum (FBS) og, avhengig av cellelinjen, ikke-essensielle aminosyrer (NEAA) og antibiotika som penicillin/streptomycin.
Håndtering og oppbevaring
Oppbevar den uåpnede flasken ved +2 °C til +8 °C, beskyttet mot lys. Etter åpning skal produktet brukes under aseptiske forhold. L-glutamin i løsning er utsatt for gradvis nedbrytning – vi anbefaler å bruke mediet innen 4 uker etter åpning for best ytelse, eller å tilsette fersk L-glutamin før bruk hvis det oppbevares i lengre perioder. La mediet varme seg opp til 37 °C før det tilsettes cellene.
Kvalitet
Produsert i henhold til strenge kvalitetsstandarder. Hver batch testes for sterilitet, pH, osmolalitet og endotoksinnivåer for å sikre jevn ytelse i cellekulturapplikasjoner.
Produktspesifikasjoner
Spesifikasjon
Detalj
ProdukttypeMEM
ProduktkategoriCellekulturmedier
FormatVæske
SteriltJa
Størrelse500 ml
L-glutaminMed L-glutamin (2 mM)
GlukoseMed glukose (1,0 g/l)
NatriumbikarbonatMed NaHCO3 (2,2 g/L)
HEPESUten HEPES
Natrium-pyruvatUten natriumpyruvat
FenolrødMed fenolrødt
SaltløsningEarle’s Balanced Salt Solution (EBSS)
pH7,0 – 7,6
EndotoksininnholdIkke spesifisert
Oppbevaring+2 °C til +8 °C
Formulering (sammensetning per liter)
Komponent
Konsentrasjon (mg/L)
Uorganiske salter
Kalsiumklorid · 2H2O265,00
Magnesiumsulfat97,72
Kaliumklorid400,00
Natriumklorid6 800,00
Natriumdihydrogenfosfat, vannfritt122,00
Natriumbikarbonat (NaHCO3)2 200,00
Aminosyrer
L-arginin · HCl126,00
L-cystin · 2HCl31,30
L-glutamin292,00
L-histidin · HCl · H2O42,00
L-isoleucin52,00
L-leucin52,00
L-lysin · HCl72,50
L-metionin15,00
L-fenylalanin32,00
L-treonin48,00
L-tryptofan10,00
L-tyrosin · 2Na · 2H2O51,90
L-valin46,00
Vitaminer
D-kalsiumpantotenat1,00
Kolin klorid1,00
Folsyre1,00
myo-inositol2,00
Nikotinamid1,00
Pyridoksal · HCl1,00
Riboflavin0,10
Tiamin · HCl1,00
Andre komponenter
D(+)-glukose1 000,00
Fenolrødt10,0025,00 €*Accutase-løsning for løsning av celler – 100 mlVarianter: 100 mlAccutase celleavløsningsløsning med EDTA og fenolrød – 100 ml
Accutase er en bruksklar, sterilt filtrert celleavløsningsløsning utviklet som et skånsomt alternativ til trypsin/EDTA for å løsne vedheftende pattedyrceller fra standard plastutstyr for vevskultur og overflater med vedheftbelegg. Den kombinerer proteolytisk og kollagenolytisk enzymaktivitet i en balansert saltløsning for å gi effektiv, men kontrollert løsning, samtidig som proteiner på celleoverflaten bevares og høy levedyktighet etter passering samt rask gjenfesting støttes.
Accutase-formuleringen er basert på Dulbeccos fosfatbufferte saltvann (DPBS) med EDTA og fenolrødt som en visuell pH-indikator. Enzymerne er av ikke-pattedyr
- og ikke-bakteriell opprinnelse, noe som gjør Accutase spesielt godt egnet til stamcelleforskning, vaksinearbeidsflyter og alle anvendelser der forurensninger av animalsk eller mikrobiell opprinnelse må minimeres. Løsningen hemmer seg selv ved 37 °C, så det kreves ikke noe nøytraliserende reagens eller serumholdig medium etter løsrivelse – cellene kan overføres direkte til ferskt medium.
Viktige egenskaper
Klar til bruk 1x sterilt filtrert væske – ingen fortynning eller rekonstituering nødvendig
Kombinert proteolytisk og kollagenolytisk enzymaktivitet for skånsom dissosiasjon
Hver batch er standardisert til en definert dissosiasjonsaktivitet for konsistens fra parti til parti
Enzymer av ikke-pattedyr
- og ikke-bakteriell opprinnelse
Selvhemmer ved 37 °C – ingen nøytraliserende løsning nødvendig
Formulert i Dulbeccos PBS med EDTA
Fenolrødt inkludert som visuell pH-indikator
pH 6,8–7,8
Typiske anvendelser
Accutase dissocierer skånsomt et bredt spekter av vedheftende og følsomme celletyper, inkludert humane embryonale stamceller (hESCs), humane induserte pluripotente stamceller (iPSCs), nevrale stamceller, primære nevroner og rutinemessig dyrkede vedheftende cellelinjer som HeLa, HEK 293, CHO, MDCK, Vero, NIH/3T3, BHK-21 og A549. Typiske bruksområder inkluderer:
Rutinemessig subkultur og passering av vedheftende pattedyrceller
Skånsom enkeltcelle-dissociasjon av hESC, iPSC og andre følsomme linjer
Prøveforberedelse for strømningscytometri og FACS-analyse
Analyse av celleoverflatemarkører der epitopintegritet er viktig
Assayer for cellemigrasjon, proliferasjon og apoptose
Hvileassays ved serumdeprivasjon og onkogen-transfeksjonsstudier
Migrasjonstester av tumorceller og nevralkamceller
Oppskalering av produksjonen i bioreaktor-arbeidsflyter
For rutinearbeid, påfør ca. 10 ml Accutase per 75 cm2 kulturoverflate og inkuber i 5–10 minutter ved romtemperatur. Den optimale inkubasjonstiden bør bestemmes for hver cellelinje og bør ikke overstige en time. Før tilsetning, skyll cellelaget med en Ca2+/Mg2+-fri saltløsning, for eksempel DPBS uten kalsium og magnesium, for å fjerne rester av serum og toverdige kationer.
Håndtering og oppbevaring
Oppbevar den uåpnede flasken frosset ved -15 °C eller lavere. Tine enten ved romtemperatur eller over natten ved +2 °C til +8 °C. Ikke tine Accutase i et 37 °C vannbad, da høye temperaturer reduserer enzymaktiviteten. Etter tining kan løsningen oppbevares i opptil 2 måneder ved +2 °C til +8 °C; ikke oppbevar ved romtemperatur. Ikke forvarm reagensen til 37 °C før bruk – tilsett den direkte til vasket celler ved romtemperatur. For lang holdbarhet anbefales det å dele opp i engangsdoser for å unngå gjentatte tinesykluser. Arbeid alltid under aseptiske forhold.
Kvalitet
Produsert under strenge kvalitetsstandarder. Hver batch av Accutase er sterilt filtrert og testet for sterilitet, pH, utseende og dissosiasjonsaktivitet for å sikre konsistent, reproduserbar ytelse fra batch til batch.
Produktspesifikasjoner
Spesifikasjon
Detalj
ProdukttypeReagens for celleavløsning/dissosiasjon
FormatSterilfiltrert væske, klar til bruk
Volum100 ml
Arbeidskonsentrasjon1x (klar til bruk)
EnzymaktivitetKombinert proteolytisk og kollagenolytisk
Enzymets opprinnelseIkke-pattedyr og ikke-bakteriell
BuffersystemDulbeccos PBS med EDTA
pH-indikatorFenolrød
pH-område6,8 – 7,8
UtseendeKlar, lysrød til oransje løsning
Oppbevaringstemperatur-15 °C eller lavere
Stabilitet etter tiningOpptil 2 måneder ved +2 °C til +8 °C
Anbefalt bruksvolum~10 ml per 75 cm² kulturoverflate
Typisk inkubasjonstid5–10 minutter ved romtemperatur
FraktbetingelserFrosset på tørris
Tilsiktet brukKun til forskningsbruk og videre produksjon
Formulering (sammensetning per liter)
Komponent
Konsentrasjon (mg/L)
Uorganiske salter
Natriumklorid (NaCl)8000,00
Dinatriumhydrogenfosfat (Na2HPO4)1150,00
Kaliumklorid (KCl)200,00
Kaliumdihydrogenfosfat (KH2PO4)200,00
Andre komponenter
EDTA · 4Na (tetranatrium-EDTA)220,00
Fenolrød3,00
Proprietær enzymblanding (proteolytisk og kollagenolytisk aktivitet)1x
Accutase er et registrert varemerke tilhørende Innovative Cell Technologies, Inc.75,00 €*Antibiotisk/antimykotisk løsning (100x)Produktoversikt
Volum: 100 ml Oppbevaring: ≤-15 °C Sterilitet: Sterilfiltrert
Antibiotic/Antimycotic Solution (100x) er et sterilt, bruksklart konsentrat som er utviklet for å redusere risikoen for mikrobiell kontaminering i cellekulturer og relaterte laboratorieapplikasjoner. Denne 100x-løsningen inneholder en veletablert kombinasjon av penicillin, streptomycin og amfotericin B, som gir bredspektret antimikrobiell aktivitet mot grampositive og gramnegative bakterier, gjærsopp og filamentøse sopper. Formuleringen er egnet for bruk i eukaryote cellekulturer, bakteriemedier og andre systemer som er følsomme for kontaminering, og støtter rene og konsekvente laboratorieoperasjoner.
Anvendelse og fordeler Denne løsningen er optimalisert for rutinemessige forskningsprotokoller og brukes i stor utstrekning for å opprettholde aseptiske forhold i arbeidsflyter for cellekulturer. Den gir pålitelig ytelse i kontamineringssensitive miljøer, og hjelper forskere med å redusere risikoen for mikrobiell overvekst uten at det går på bekostning av cellenes helse eller eksperimentell reproduserbarhet. Den sterilfiltrerte formuleringen eliminerer behovet for ytterligere solubiliseringstrinn, noe som bidrar til strømlinjeformet tilberedning av medier og reduserer variabiliteten i daglige laboratorieprosedyrer.
Bruk og kompatibilitet For å oppnå standard arbeidskonsentrasjoner fortynner du løsningen 1:100 i ditt komplette dyrkingsmedium. Produktet er kompatibelt med et bredt spekter av pattedyrcellelinjer og basalmedier. Med konsekvent lagertilgjengelighet kan forskere dra nytte av pålitelig forsyningskontinuitet og forenklet logistikkplanlegging. Løsningen skal oppbevares ved ≤ -15 °C og beskyttes mot gjentatte fryse-tine-sykluser for å opprettholde stabiliteten. Kun til forskningsbruk. Ikke til bruk i diagnostiske eller terapeutiske prosedyrer. Ikke til bruk på mennesker eller dyr.45,00 €*PBSFosfatbufret saltvannsløsning (PBS)
Fosfatbufret saltvann (PBS) er en mye brukt bufferløsning i biologisk og kjemisk forskning. Den spiller en avgjørende rolle når det gjelder å opprettholde pH-balansen og osmolariteten under ulike eksperimentelle prosedyrer, inkludert vevsprosessering og cellekultur. Vår PBS-løsning er omhyggelig formulert med ingredienser av høy renhet for å sikre stabilitet og pålitelighet i hvert eneste eksperiment. Osmolariteten og ionekonsentrasjonene i PBS-løsningen vår etterligner i stor grad de som finnes i menneskekroppen, noe som gjør den isotonisk og ugiftig for de fleste celler.
Sammensetningen av vår PBS-løsning
Vår PBS-løsning er en pH-justert blanding av ultrarene fosfatbuffere og saltvannsløsninger. Ved en 1X arbeidskonsentrasjon inneholder den
8000 mg/L natriumklorid (NaCl)
200 mg/L kaliumklorid (KCl)
1150 mg/L vannfritt dibasisk natriumfosfat (Na2HPO4)
200 mg/L Vannfritt kaliumfosfat monobasisk (KH2PO4)
Denne sammensetningen sikrer en optimal pH
- og ionebalanse, og er egnet for et bredt spekter av biologiske anvendelser.
Bruksområder for vår PBS-løsning
Vår PBS-løsning er ideell for ulike bruksområder innen biologisk forskning. De isotone og giftfrie egenskapene gjør den egnet til fortynning av substanser og skylling av cellebeholdere. PBS-løsninger som inneholder EDTA, er effektive for å løsne celler som sitter fast og klumper seg sammen. PBS bør imidlertid ikke tilsettes toverdige metaller som sink, da dette kan føre til utfelling. I slike tilfeller anbefales Good's buffere. I tillegg er vår PBS-løsning et akseptabelt alternativ til viralt transportmedium for transport og lagring av RNA-virus, inkludert SARS-CoV-2.
Kvalitetskontroll
Sterilfiltrert
Oppbevaring og holdbarhet
Oppbevares ved +2 °C til +25 °C, beskyttet mot lys.
Etter åpning, oppbevares ved 2 °C til 25 °C og brukes innen 24 måneder.
Transportforhold
Omgivelsestemperatur
Vedlikehold
Oppbevares i kjøleskap ved +2 °C til +8 °C i mørke. Unngå frysing og hyppig oppvarming til +37 °C, da det reduserer produktkvaliteten.
Ikke varm opp mediet til mer enn 37 °C eller bruk ukontrollerte varmekilder som mikrobølgeovner.
Hvis bare en del av mediet skal brukes, ta ut den nødvendige mengden og varm den opp til romtemperatur før bruk.
Sammensetning
Kategori
Komponenter
Konsentrasjon (mg/L)
Salter
Kaliumklorid
200
Kaliumfosfat, vannfritt, monobasisk
200
Natriumklorid
8000
Natriumfosfat, vannfritt, dibasisk
115020,00 €* -
Relaterte produkter
Relaterte produkter