Menneskelige cellelinjer, verifisert helt ned til den minste markøren
Hver eneste humane cellelinje vi sender ut, har gjennomgått STR-identitetsprofilering, et kontamineringspanel med flere tester og en tredjepartsrevisjon – før den forlater laboratoriet vårt.
Menneskelige celler
Velkommen til Cytion, din fremste destinasjon for autentiserte og forurensningsfrie humane cellelinjer. Vår omfattende cellebank er kuratert for å støtte biomedisinsk forskning med pålitelighet og presisjon. Hver modell gjennomgår strenge tester for å sikre genetisk identitet, renhet og ytelse, noe som muliggjør reproduserbare resultater på tvers av et bredt spekter av applikasjoner.
Celler for banebrytende forskning
Utforsk et bredt utvalg av autentiserte, validerte og mykoplasmafrie humane cellelinjer som er egnet for sykdomsmodellering, legemiddelutvikling, proteinproduksjon, hybridomgenerering og virusformering. Hver batch produseres under kontrollerte forhold og verifiseres gjennom flere trinns kvalitetskontroll for å sikre pålitelighet fra tining til eksperiment.

| Organisme | Menneskelig |
|---|---|
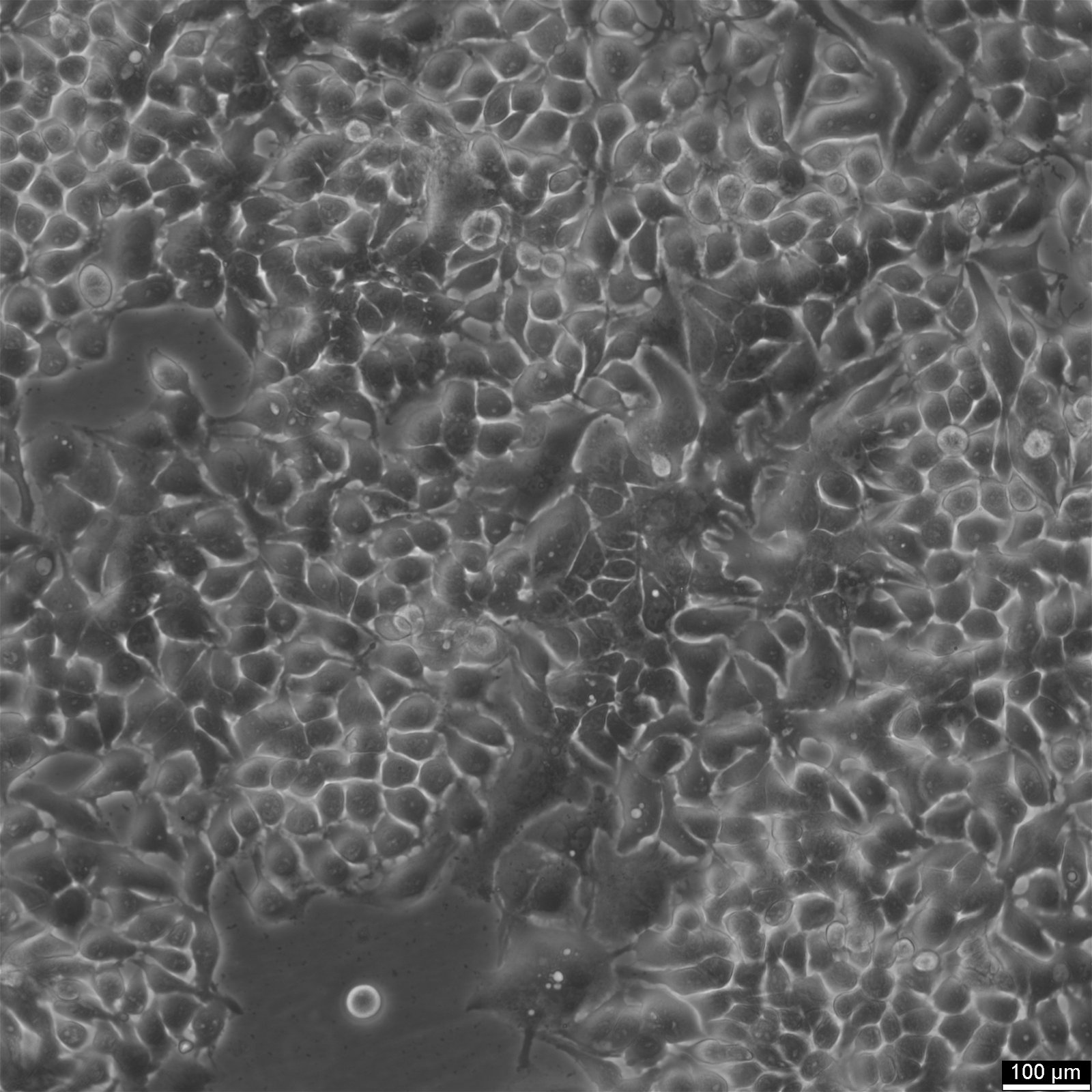
| Vev | Bukspyttkjertelen |
| Sykdom | Adenokarsinom i bukspyttkjertelen |
| Organisme | Menneskelig |
|---|---|
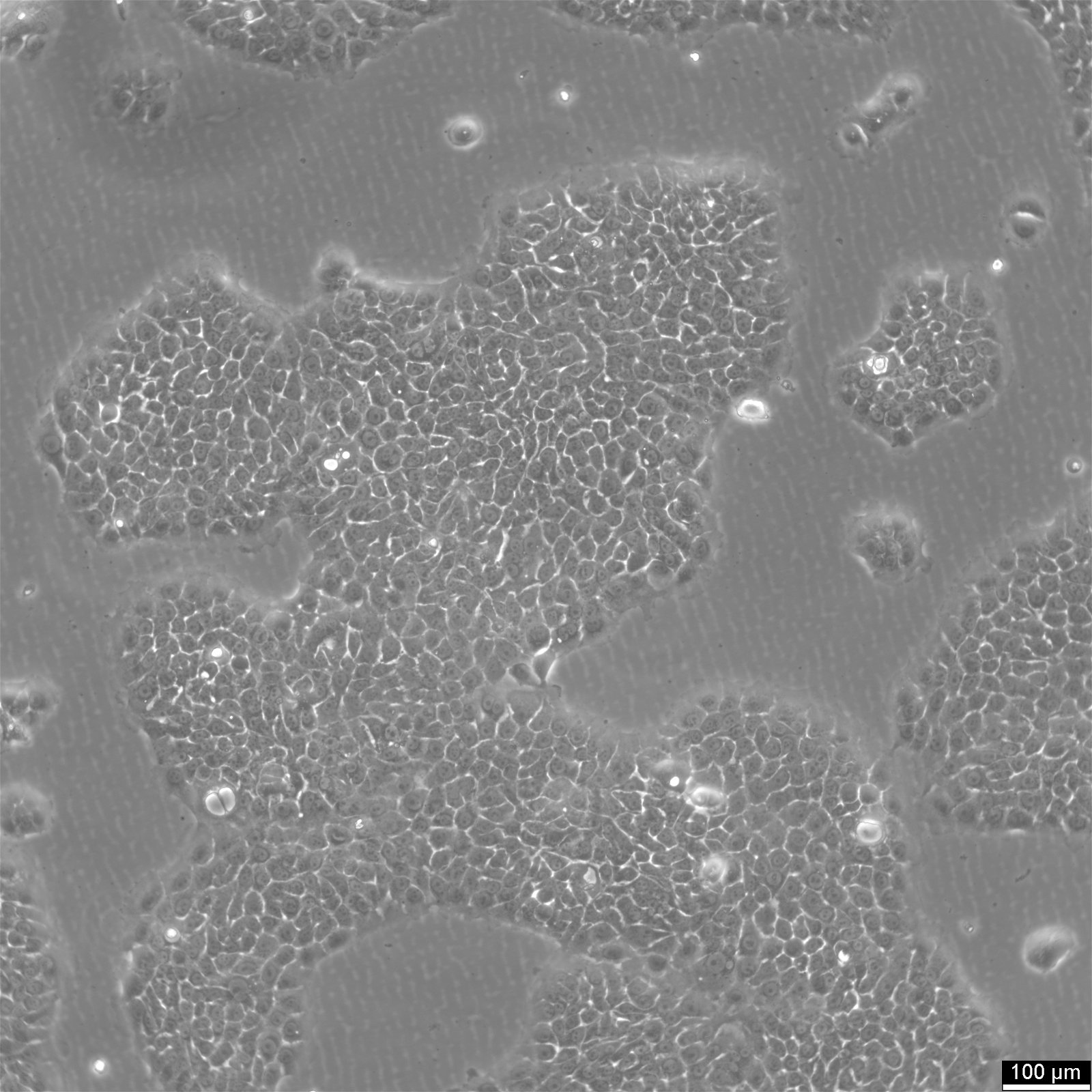
| Vev | Tykktarm, Dukes' type C |
| Sykdom | Kolorektalt adenokarsinom |
| Organisme | Menneskelig |
|---|---|
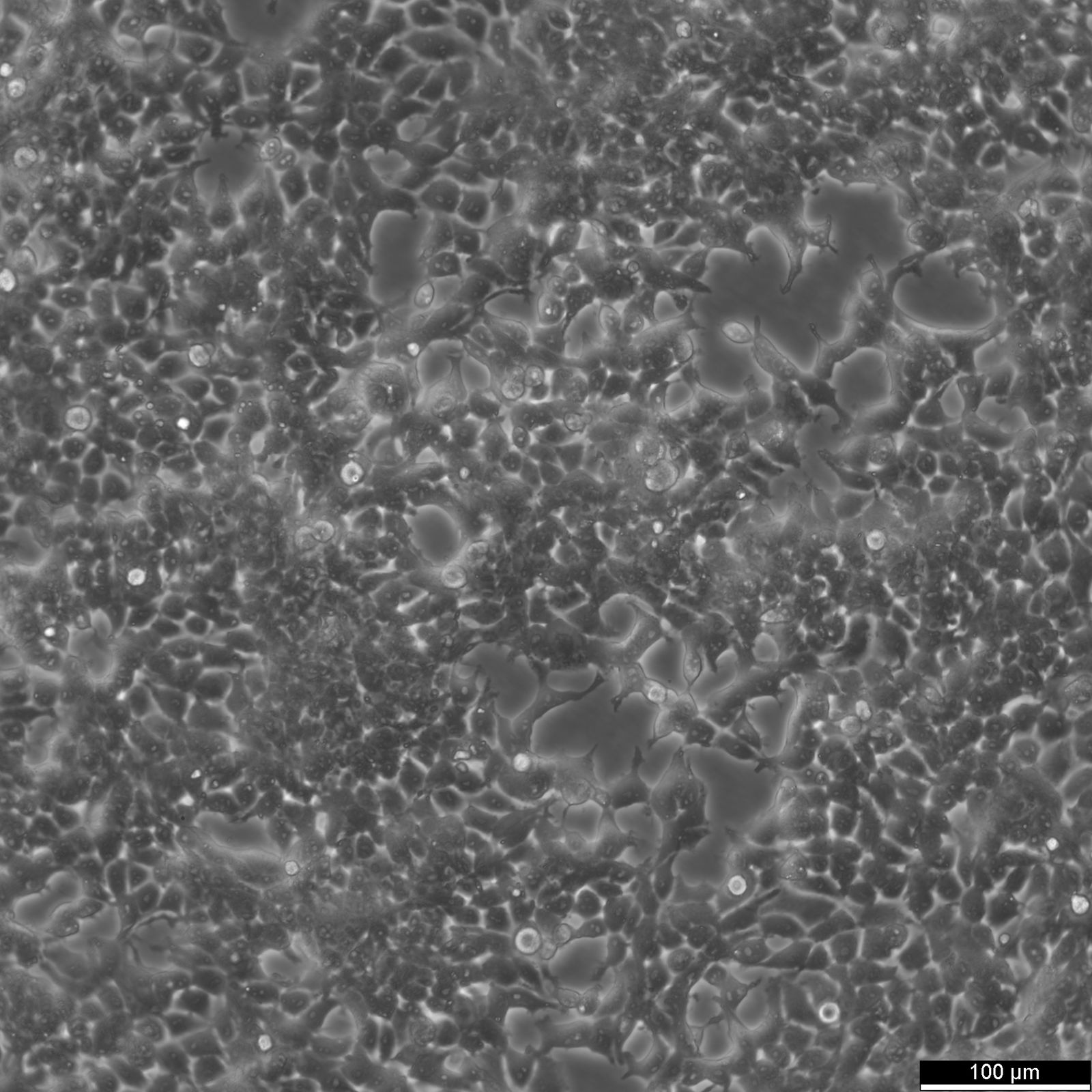
| Vev | Hjerne, høyre frontale parieto-occipitale cortex |
| Sykdom | Glioblastom |
| Organisme | Menneskelig |
|---|---|
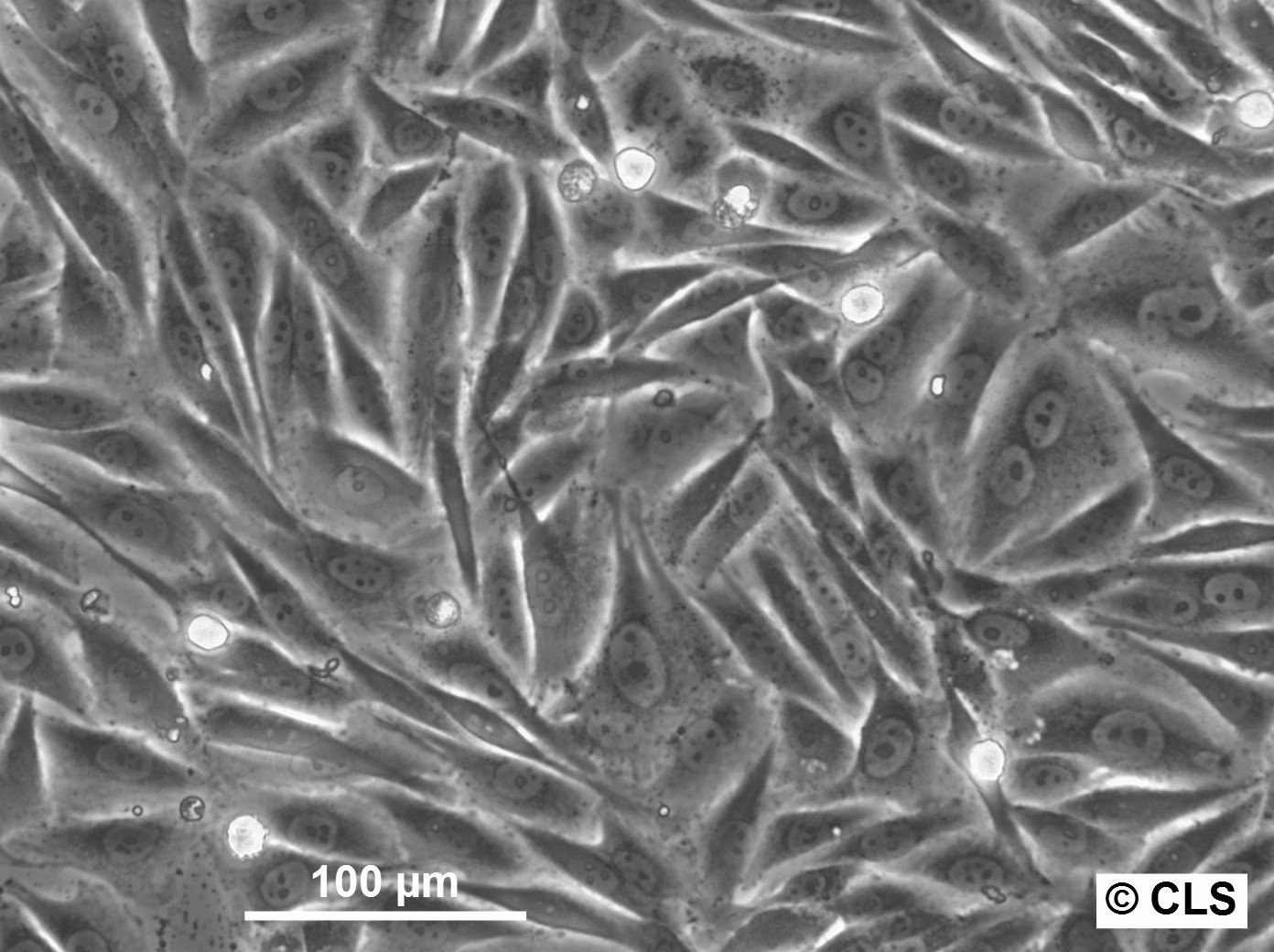
| Vev | Eggstokk |
| Sykdom | Lavgradig serøst ovariekarsinom |