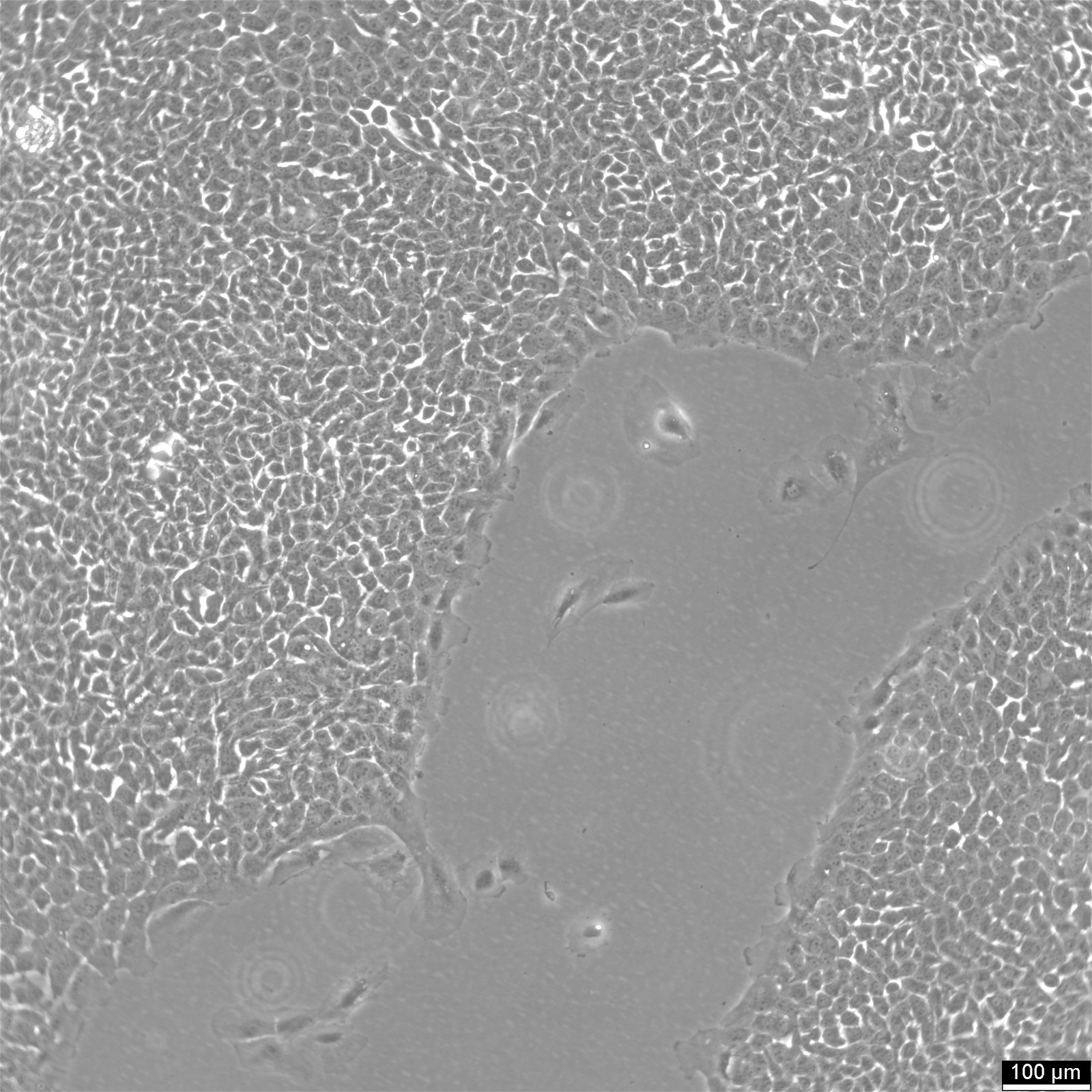
MCF10A šūnu līnija: Krūts vēža bioloģijas atklāšana netumorizējošos kontekstos
MCF10A šūnu līnija ir galvenais krūts vēža pētījumu rīks, kas ir imortizēts, bet ne-tumorigēns cilvēka krūts epitēlija šūnu modelis. Šī šūnu līnija tiek plaši izmantota, lai pētītu normālas krūts šūnu funkcijas, transformācijas procesus un krūts bioloģijas pamatmehānismus, tostarp šūnu uzvedību, signalizācijas ceļus un gēnu ekspresijas modeļus. Turklāt MCF10A šūnas kalpo kā būtisks resurss krūts audzēju attīstības izpētei, to progresēšanas izpratnei un potenciālo terapeitisko stratēģiju novērtēšanai.
MCF10A šūnu izcelsme un vispārīgās īpašības
Izpētot MCF10A šūnu līniju, pētnieki par prioritāti izvirza izpratni par tās izcelsmi un atšķirīgajām iezīmēm, kas izgaismo tās pielietojumu un lietderību pētniecībā. MCF10A šūnu līnija, kas iegūta no 36 gadus vecas baltādainas sievietes piena dziedzera ar fibrocistisku krūts slimību 1984. gadā, ir pazīstama ar savu netumorizējošo profilu, padarot to par paraugu normālu cilvēka krūts audu pētījumiem in vitro.
MCF10A šūnu līnijas galvenās īpašības ir šādas:
- Epitēlija morfoloģija: MCF10A šūnas parasti aug monoslāņos, bet konfluentās kultūrās tās var veidot kupolveidīgas struktūras, kas izceļ to dinamiskos augšanas modeļus.
- Šūnu lielums: MCF10A šūnu izmērs svārstās no 14,5 μm līdz 26,2 μm, kas ļauj izmantot dažādas eksperimentālās iekārtas.
- Kariotips: MCF10A šūnām ir kariotips ar 47 hromosomām, kas sniedz ieskatu krūts epitēlija šūnu ģenētiskajos un hromosomu pētījumos.
MCF10AT1: Pirms ļaundabīgs atvasinājums
MCF10AT1 šūnu līnija, kas radīta, transfektējot MCF10A šūnas ar HRAS gēnu, ir pirms ļaundabīga stadija, kas, ievadot imūnkompromitētām pelēm, spēj veidot duktālas struktūras un bojājumus, kas līdzīgi netipiskai duktālai hiperplāzijai (ADH) un Ductal Carcinoma in Situ (DCIS). Šī transformācija uzsver šūnu līnijas lietderību krūts vēža agrīnās stadijas attīstības modelēšanā un pāreju no labdabīgas uz ļaundabīgu stāvokli izpētē.
MCF10A šūnas: Informācija par šūnu kultūru
MCF10A, plaši izmantota šūnu līnija krūts vēža pētījumos, prasa precīzu apstrādi un uzturēšanu, lai nodrošinātu tās dzīvotspēju un lietderību eksperimentālos apstākļos. Šajā rokasgrāmatā izklāstīti būtiski apsvērumi efektīvai MCF10A šūnu kultivēšanai, norādot to dubultošanās laiku, vēlamo barotni, izsējas blīvumu un adherences īpašības.
MCF10A šūnu kultivēšanas galvenie punkti
Populācijas dubultošanās laiks: MCF10A šūnu līnija parasti dubultojas aptuveni 20 stundas, kas liecina par tās spēcīgo augšanas ātrumu optimālos apstākļos.
Adherences īpašības: Šīm šūnām piemīt adherentas augšanas īpašības, tāpēc tām nepieciešams ciets substrāts, lai pieķertos un vairotos.
Subkultivēšanas prakse: Subkulturēšanai ieteicams izmantot dalījuma attiecību 1:2 līdz 1:4. Protokolā ietilpst šūnu mazgāšana ar PBS, atdalīšana ar Accutase un pēc centrifugēšanas un atkārtotas suspensijas svaigā barotnē to pārvietošana uz jaunu kolbu. Ieteicams divas līdz trīs reizes nedēļā atsvaidzināt barotni, lai nodrošinātu veselīgu augšanu.
Augšanas barotne: MCF10A šūnas labi attīstās MEGM - specializētā barotnē, kas jāpapildina ar 100 ng/ml holēras toksīna, lai optimizētu šūnu augšanu un darbību.
Optimāli augšanas apstākļi: Lai precīzi atkārtotu fizioloģiskos apstākļus, kultūras jāuztur mitrinātā inkubatorā 37 °C temperatūrā ar 5 % CO2 atmosfērā.
Uzglabāšanas vadlīnijas: Ilgstošai uzglabāšanai šūnas jāuzglabā šķidrā slāpekļa tvaika fāzē vai temperatūrā, kas zemāka par -150 °C, īpaši zemas temperatūras saldētavā.
Sasaldēšanas un atkausēšanas procedūras: MCF10A šūnām ieteicamā sasaldēšanas vide ir CM-1 vai CM-ACF. Lai samazinātu termisko šoku, izmantojiet lēnas sasaldēšanas metodi. Atkausēšana jāveic uzmanīgi 37 °C ūdens vannā, līdz paliek neliels ledus gabaliņš. Pēc tam šūnas jāsajauc ar svaigu barotni, jānocentrifugē un šūnu granulas resuspendē jaunā barotnē, pirms pārnes uz barotni.
Bioloģiskās drošības apsvērumi: MCF10A šūnu kultūras var droši apstrādāt 1. bioloģiskās drošības līmeņa laboratorijās, nodrošinot vienkāršu uzturēšanu un atbilstību drošības standartiem.
Šo vadlīniju ievērošana veicinās veiksmīgu MCF10A šūnu kultivēšanu, ļaujot tām arī turpmāk sniegt ieguldījumu krūts vēža izpētes attīstībā.
MCF10A šūnu līnijas priekšrocības un ierobežojumi
MCF10A šūnu līnijas izpēte sniedz niansētu izpratni gan par tās labvēlīgajām īpašībām, gan raksturīgajiem ierobežojumiem, kas ir būtiski, lai to efektīvi izmantotu krūts vēža pētījumos.
Priekšrocības
Netumorizējoša daba: MCF10A šūnu raksturīga iezīme ir to netumorigēnisks raksturs, kas ļauj pētniekiem pētīt normālu krūts šūnu uzvedību un bioloģiju bez sarežģījumiem, ko rada audzēju veidošanās imūndeficētām pelēm.
3D struktūras veidošanās: MCF10A šūnām piemīt unikāla spēja veidot trīsdimensiju acināru struktūras, kas atgādina normālu krūts epitēliju, ja tās kultivē īpašā barotnē, piemēram, kolagēnā. Šī spēja ir noderīga, lai pētītu krūts šūnu organizāciju un uzvedību 3D kontekstā, sniedzot ieskatu, kas tuvāks in vivo apstākļiem.
Ierobežojumi
- Fenotipiskais plastiskums: MCF10A šūnas, neraugoties uz to priekšrocībām, ir mainīga fenotipa un uzvedības ziņā dažādos kultūras apstākļos, kas var ietekmēt eksperimentu rezultātu konsekvenci un reproducējamību.
MCF10A šūnu līnijas izmantošana pētniecībā
MCF10A šūnu līnija ir stūrakmens daudzpusīgās pētniecības paradigmās, jo īpaši krūts šūnu bioloģijas un onkoloģijas jomā. Šeit mēs izklāstām tās daudzveidīgos lietojumus:
Normāla krūts dziedzera epiteļa funkcija
MCF10A šūnas ir noderīgas in vitro, lai noskaidrotu normālu krūts epitēlija šūnu funkciju nianses, kas ietver šūnu adhēziju, ko nodrošina tādi proteīni kā E-kadherīns, morfogenētiskos procesus un sarežģītas signalizācijas kaskādes. Lai gan tas ir nenovērtējams, tomēr salīdzinājums ar ļaundabīgām līdzīgām šūnām, piemēram, MCF7 šūnām, dažkārt uzsver šūnu līnijas nespēju pilnībā atdarināt in vivo novēroto ar vēzi saistīto vidi.
Farmakoloģiskā profilēšana
MCF10A šūnas kā izcils modelis tiek izmantots farmakoloģiskajā profilēšanā, lai noteiktu topošo pretkrūts vēža savienojumu citotoksicitāti un terapeitisko potenciālu. Piemēram, šīs šūnas ir bijušas izšķirošas, nosakot augu izcelsmes bioaktīvo sastāvdaļu, piemēram, Senna alata, efektivitāti, tādējādi pamatojot to ieguldījumu jaunās terapeitiskās stratēģijās.
Kanceroģenēzes pētījumi
Neskatoties uz to, ka MCF10A šūnas nav tumorogēnas, tās ir pielāgojams paraugs krūts audzēju ģenēzes izpētei. Izmantojot tās kopā ar tumorigēnām šūnu līnijām vai modificētas ar gēnu inženierijas palīdzību, tās atvieglo krūts vēža molekulārās ģenēzes un progresēšanas izpēti. Kā piemēru var minēt pētījumus, kuros MCF10A šūnās tiek manipulēts ar gēniem, tostarp PHLDA1, lai izpētītu to ietekmi uz šūnu migrāciju un invaziju, tādējādi atklājot jaunus potenciālos intervences mērķus.
Trīsdimensiju kultūru modeļi
MCF10A šūnas labi attīstās trīsdimensiju (3D) kultūru sistēmās, piemēram, jauktā Matrigel vidē, kas imitē in vivo apstākļus, veicinot mūsu izpratni par šūnu uzvedības telpisko un mehānisko kontekstu. Šī 3D pieeja ir noderīga, lai noteiktu ceļus, kas regulē krūts šūnu diferenciāciju un agrīno jaunveidojumu morfoloģisko attīstību.
Metastatiskā potenciāla novērtējums
Pētījumos par metastāžu veidošanās mehānismiem izmanto MCF10A šūnas, lai simulētu epitēlija pāreju uz mezenhīmu, kas ir galvenais notikums metastāžu izplatībā. Pētnieki novēro šīs pārejas dažādos šūnu modeļos, izmantojot tādus marķierus kā E-kadherīns, lai gūtu ieskatu par šūnu dinamiku krūts karcinomas progresēšanas laikā.
Mammosfēras veidošanās un progenitoru šūnu pētījumi
MCF10A šūnu spēja veidot mammosfēras, ja tās kultivē neadherentos apstākļos, padara tās par nenovērtējamu resursu, lai pētītu krūts priekšdziedzera šūnas un to lomu krūts vēža bioloģijā, sākot no ierosmes līdz invazīvu īpašību iegūšanai.
MCF10A šūnu ievērojamā daudzpusība un uzticamība cilvēka krūts epitēlijam nostiprina to statusu kā neaizstājamu līdzekli nepārtrauktajos centienos atklāt krūts vēža sarežģītību, uzsverot to nemainīgo vērtību progresīvos pētījumos.
Izmantojiet mūsu MCF10A šūnas, lai atraisītu savu pētījumu potenciālu
MCF10A šūnas: Pētniecības publikācijas
Šeit ir norādīti daži no ievērojamākajiem un biežāk citētajiem pētījumiem, kuros izmantota MCF10A šūnu līnija, sniedzot būtisku ieguldījumu krūts vēža izpētes jomā.
TGF-β signalizācijas ceļa ieskats: International Journal of Oncology (2004) publicētajā pētījumā tika pētīts TGF-β signalizācijas ceļš MCF10A šūnās, atklājot, ka ārstēšana ar TGF-β var izraisīt migrācijas un invazīvo fenotipu, uzsverot šūnu reakcijas uz TGF-β sarežģītību.
Indeņu maisiņu ekstrakta pētījums: Toxin Reviews (2023 ) publicētajā pētījumā tika pētīta Vespa orientalis hornetis raga indes maisiņa ekstrakta ietekme uz MCF10A šūnām, pārbaudot tā citotoksiskās, nekrotiskās, apoptotiskās un autofagiskās īpašības, tādējādi paverot jaunas iespējas, lai izprastu šūnu reakciju uz dabīgajiem toksīniem.
Leptīna loma šūnu invāzijā: Pētījumā Cells (2019) ierosināts, ka leptīns, labi zināms adipokīns, veicina ar EMT saistīto transkripcijas faktoru ekspresiju un pastiprina invaziju MCF10A šūnās, izmantojot ceļu, kas atkarīgs no Src un FAK, tādējādi uzsverot sarežģīto mijiedarbību starp adipokīniem un vēža šūnu uzvedību.
Koneksīna 32 tumorigēnās īpašības: Šajā pētījumā, kas publicēts žurnālā Biochimica et Biophysica Acta (BBA) - Molecular Cell Research (2020), tika izvirzīta hipotēze, ka proteīns koneksīns-32 var piešķirt MCF10A šūnām pro-tumorigēnas īpašības, kas liecina par potenciālu koneksīna-32 lomu krūts vēža attīstības agrīnā stadijā.
Pseudevernia furfuracea ekstrakta ietekme: rakstā žurnālā Biomolecules (2021 ) tika novērtēta Pseudevernia furfuracea (L.) Zopf ekstrakta un tā metabolīta fizodiskās skābes ietekme uz audzēja mikrovides modulāciju MCF10A šūnās, sniedzot ieskatu par dabisko savienojumu potenciālo terapeitisko pielietojumu audzēja un tromba mijiedarbības modulēšanā.
Šīs publikācijas uzsver MCF10A šūnu līnijas daudzpusību un pielietojamību krūts vēža bioloģijas izpratnes veicināšanā, sākot no šūnu signalizācijas ceļu izpētes līdz dabisko un sintētisko savienojumu potenciālās terapeitiskās iedarbības novērtēšanai.
MCF10A šūnu līnijas resursi: Protokoli, videomateriāli un citi resursi
Tālāk ir sniegti daži tiešsaistes resursi par MCF10A šūnām.
- MCF10A transfekcija: Šī saite sniedz detalizētu protokolu par plazmīdu DNS transfekciju MCF10A šūnās.
- Šūnu kultūru protokoli: Šajā videoklipā ir izskaidrots pamatprotokols adherento šūnu pasāžas, sasaldēšanas un atkausēšanas veikšanai.
MCF10A šūnu kultūras protokols ir norādīts šeit.
- MCF10A šūnu kultūras protokols: Šajā dokumentā ir soli pa solim izklāstīts MCF10A šūnu pasāžas protokols.
- MCF10A šūnu subkultivēšana: Šī saite palīdzēs jums uzzināt MCF10A krūts epitēlija šūnu subkulturēšanas protokolu.
- MCF10A šūnu līnija: Šī tīmekļa vietne palīdzēs apgūt visus MCF10A šūnu kultūras pamatprotokolus, tostarp proliferējošo un kriokonservēto kultūru subkultivēšanas un apstrādes protokolus.
MCF10A šūnu izpēte: Visaptverošs biežāk uzdoto jautājumu apkopojums par to lomu krūts vēža pētniecībā un šūnu bioloģijā
Atsauces
- Qu, Y., et al., MCF10A kā uzticama normālu cilvēka krūts dziedzera epitēlija šūnu modeļa novērtējums. PLoS One, 2015. 10(7): p. e0131285.
- Marella, N.V., et al., Cytogenetic and cDNA microarray expression analysis of MCF10 human breast cancer progression cell lines (MCF10 cilvēka krūts vēža progresējošo šūnu līniju citogenētiskā un cDNA mikrotīkla ekspresijas analīze). Cancer Res, 2009. 69(14): p. 5946-53.
- So, J.Y., et al., Differential Expression of Key Signaling Proteins in MCF10 Cell Lines, a Human Breast Cancer Progression Model. Mol Cell Pharmacol, 2012. 4(1): p. 31-40.
- Goh, J.J.H., et al., Transcriptomics indicate nuclear division and cell adhesion not recapitulated in MCF7 and MCF10A compared to luminal A breast tumours. Sci Rep, 2022. 12(1): p. 20902.
- Modarresi Chahardehi, A., et al., Low cytotoxicity, and antiproliferative activity on cancer cells, of the plant Senna alata (Fabaceae). Revista de Biología Tropical, 2021. 69.
- Bonatto, N., et al., PHLDA1 (pleckstrin homology-like domain, family A, member 1) knockdown promotes migration and invasion of MCF10A breast epithelial cells. Cell Adh Migr, 2018. 12(1): p. 37-46.