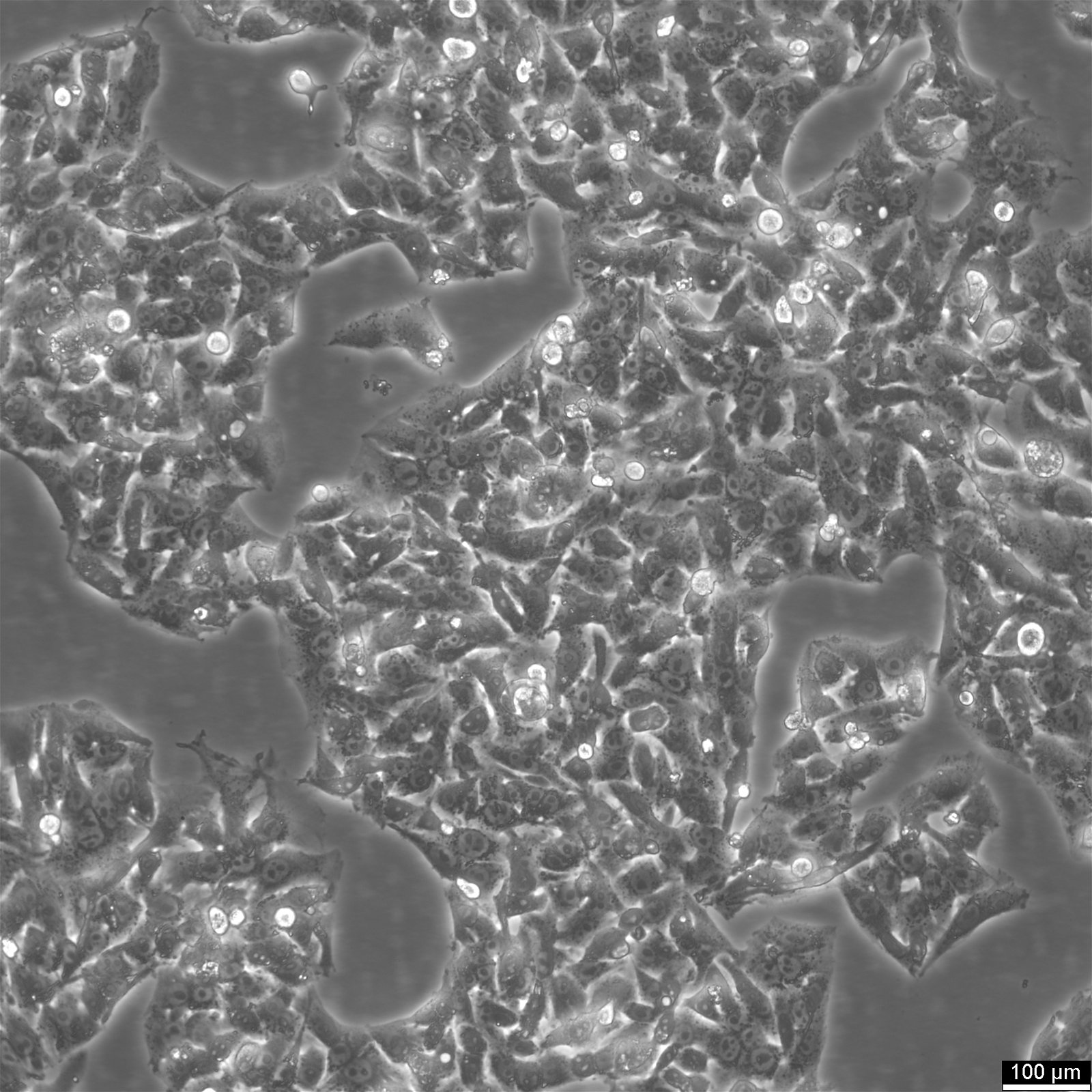
HepG2 šūnas - aknu vēža pētniecības resurss
Hep-G2 ir cilvēka aknu vēža šūnu līnija, kas iegūta no 15 gadus veca baltādaina vīrieša ar hepatocelulāro karcinomu aknu audiem. Šīs šūnas bieži izmanto zāļu metabolisma un hepatotoksicitātes pētījumos. Lai gan HepG2 šūnām ir augsts proliferācijas rādītājs un epitēlijam līdzīgs izskats, tās nav tumorogēnas un veic dažādas diferencētas aknu funkcijas. Pētnieki 1975. gadā ieguva HepG2 šūnas no hepatocelulārās karcinomas, tādējādi kļūstot par pirmo aknu šūnu līniju, kurai piemīt hepatocītu kritiskās īpašības. Atšķirībā no iepriekš izveidotās SK-Hep1 šūnu līnijas, kurai trūkst būtisku aknu šūnu marķieru, HepG2 šūnas spēj izdalīt dažādus plazmas proteīnus un ir vērtīgs modelis cilvēka hepatocītu šūnu virsmas domēnu iekššūnu dinamikas izpētei. Šīm šūnām piemīt epitēlijam līdzīga morfoloģija, to hromosomu skaits ir 55, un tās var stimulēt ar cilvēka augšanas hormonu.
HepG2 raksturojums
Primāriem hepatocītiem raksturīga kubiska forma, un parasti tie satur divus kodolus. Turpretī HepG2 šūnām ir epitēlijveida morfoloģija ar vienu kodolu un hromosomu skaitu no 48 līdz 54 šūnās. Lai gan HepG2 šūnas var veidot līdz 25 % no kopējā šūnu proteīna, to izmērs ir lielāks nekā normāliem hepatocītiem, un tās veido aptuveni 10 % no visa šūnas proteīna. Šūnu olbaltumvielas ir kritiski svarīgi elementi šūnā, kas izpilda gēnos noteiktās funkcijas.
Audzēju šūnās, tostarp šūnās ar nenormālu hromosomu skaitu, bieži vien ir palielināts kodolu skaits - līdz pat septiņiem kodoliem vienā šūnā. HepG2 šūnas, pateicoties to augstajai diferenciācijas pakāpei in vitro, ir ideāls modelis, lai pētītu žults kanālu, sinusoidālo membrānu proteīnu un lipīdu iekššūnu apriti un dinamiku cilvēka hepatocītos.
HepG2 šūnas vidējais diametrs ir aptuveni 10-20 µm, kas ir mazāks par hepatocītu ar 15 µm diametru, bet līdzīgs hepatoblastomas (HB) audzēja šūnām, kuru diametrs ir 10-20 µm.
HepG2 ģenētika
Hep-G2 šūnu līnijā ir vairākas translokācijas, tostarp starp 1. un 21. hromosomas īsajiem posmiem, 2., 16. un 17. hromosomas trisomijas un 20. hromosomas tetrasomija. Novērots arī 4q3 hromosomas reģiona zudums, kas saistīts ar hepatoblastomā (HB) bieži novēroto translokāciju t(1;4) un citām hromosomu anomālijām, piemēram, 2. un 20. hromosomas trisomiju. Hromosomu skaits HepG2 šūnās svārstās no 50 līdz 60, kas norāda uz hiperdiploīdu kariotipu, bet dažos gadījumos hromosomu skaits pārsniedz 100 un tiem raksturīga tetraploīda palielināšanās. HepG2 šūnas satur aptuveni 7,5 pg DNS, kas ir par 15 % vairāk nekā vidējā somatiskā šūnā. Salīdzinājumam, primārajiem hepatocītiem ir kubiska šūnu forma, un parasti tie satur divus kodolus [1].
HepG2 šūnu mutāciju profils
HepG2 šūnu līnijā ir TERT promotora reģiona mutācija C228T, kas sastopama arī hepatocelulārajā karcinomā (HCC) un hepatoblastomā (HB). Šī mutācija veicina imortalizāciju, aizsargājot vēža šūnu telomerus. Turklāt HepG2 šūnām ir savvaļas tipa TP53, kas ir ļoti svarīgs gēns cilvēka vēža apkarošanai, jo tam ir nozīme šūnu cikla apstādināšanā, apoptozē un novecošanās procesā. Šī gēna mutācijas var veicināt šūnu proliferāciju.
HepG2 šūnas piedalās vairākos ceļos, tostarp šūnu augšanas disregulācijā, izdzīvošanas ceļos, piemēram, augļa un embrionālā HB, un Wnt/β-katenīna ceļā. Turklāt šai šūnu līnijai ir raksturīga CTNNB1 gēna trešā eksona delecija, kas ir identiska epitēlija tipa HB [2,3].
Pārskats par HepG2 hepatocelulārās karcinomas šūnām aknu pētniecībā
HepG2 šūnas, kas iegūtas no cilvēka hepatomas, ir kļuvušas par nenovērtējamu līdzekli aknu funkciju un slimību, tostarp hepatocelulārās karcinomas, izpētei. Šīs aknu šūnu līnijas sniedz ieskatu par cilvēka hepatocītu šūnu reakcijām dažādos eksperimentālos apstākļos. Luciferāzes reportieru plazmīdu izmantošana HepG2 šūnās ir īpaši efektīva gēnu ekspresijas un šūnu transfekciju izsekošanā, kas ir būtiski metabolisma pētījumos, piemēram, pētot etanola ietekmi uz aknu šūnām
Vīrusu infekciju un aknu slimību pētījumi, izmantojot HepG2 šūnas
Tādas imortizētas aknu audzēju šūnu līnijas kā HepG2 un Huh7 ir ļoti svarīgas vīrusu infekciju pētījumos, demonstrējot pilnīgu D hepatīta (HDV) šūnu cikla replikāciju un B hepatīta (HBV) ekspresiju [5,6]. Vienlaikus HepaRG šūnu līnijām ir būtiska nozīme HBV iekļūšanas mehānismu noskaidrošanā [7]. HepG2 šūnas tiek izmantotas arī dažādu cilvēka aknu slimību izpētei, sākot no ģenētiskām slimībām, piemēram, progresējošas ģimenes intrahepatiskās holestāzes (PFIC) un Dubina-Džonsona sindroma, līdz vides un uztura pētījumiem, kas saistīti ar citotoksiskiem un genotoksiskiem aģentiem, kā arī zāļu mērķēšanas un hepatokarcinogēnozes pētījumiem [8,9]. Tās tiek izmantotas arī pētījumos ar bioloģiskām mākslīgajām aknu ierīcēm
HepG2 šūnu mijiedarbība ar biomateriāliem audu inženierijā
HepG2 šūnu mijiedarbība ar dažādiem biomateriāliem ir būtiska audu inženierijā. Tādi paņēmieni kā koloidālās zondes metode palīdz izprast šo mijiedarbību, izmērot šūnu adhēzijas īpašības, kas ir ļoti svarīgas, lai noteiktu šūnu dzīvotspēju skeletonu un precīzu aknu audu modeļu izstrādē
Šūnu uzvedība un inovācijas uz HepG2 balstītos modeļos
Šūnu uzvedības izpēte uz HepG2 balstītos modeļos ir ļoti svarīga aknu slimību pētniecībā. Trīsdimensiju sferoīdu šūnu kultūru attīstība ir ļāvusi izveidot HepG2 šūnu sferoīdus, piedāvājot fizioloģiski atbilstošāku modeli, kas precīzi atspoguļo normālus hepatocītus. Šie trīsdimensiju modeļi ar paaugstinātu metabolisma aktivitāti liecina par HepG2 šūnu potenciālu kalpot par hepatoblastomas modeli un ir nozīmīgi vēža ārstēšanas pētījumos, jo īpaši aknu audzēju simulēšanā un jaunu terapeitisko pieeju testēšanā [10-12]
HepG2 salīdzinājums un raksturojums ar citām audzēju šūnu līnijām
HepG2 ir viena no visplašāk izmantotajām aknu audzēju šūnu līnijām, kas izvēlēta plaša pielietojuma dēļ zinātniskajos pētījumos starp aptuveni 40 pieejamām aknu audzēju šūnu līnijām [13]. Neskatoties uz to, ka, salīdzinot ar normāliem hepatocītiem, HepG2 šūnu līnija ir vāji vai vispār neizmanto dažus citohroma P450 enzīmus, HepG2 metabolisma profils ir veicinājis centienus modificēt šo šūnu līniju, lai uzlabotu zāļu metabolisma pētījumus [13]. Salīdzinot ar tādām audzēju šūnu līnijām kā MCF7, PC3, 143B un HEK293, HepG2 šūnām ir unikāli aminoskābju satura profili, kas būtiski ietekmē olbaltumvielu sintēzi un sekrēciju, uzsverot to unikālos metabolisma ceļus [14]
Aknu slimību izpēte ar HepG2
HepG2 šūnu subkultivēšana
Tālāk ir aprakstīti pieci soļi, kā no šūnu kultūru kolbām ar Accutase palīdzību noņemt adhēzētās šūnas:
- Noņemiet barotni no šūnu kultūru kolbas un izskalojiet pielipušās šūnas, izmantojot PBS bez kalcija un magnija. Izmantojiet 3-5 ml PBS T25 kolbām un 5-10 ml T75 kolbām.
- Pievienojiet Accutase šūnu kultūru kolbām, izmantojot 1-2 ml uz T25 kolbu un 2,5 ml uz T75 kolbu. Pārliecinieties, ka Accutase pārklāj visu šūnu slāni.
- Kolbu inkubējiet istabas temperatūrā 8-10 minūtes.
- Uzmanīgi resuspendējiet šūnas ar barotni, izmantojot 10 ml svaigas barotnes.
- Centrifugēt resuspendētās šūnas 5 minūtes ar 300xg, atkārtoti suspendēt tās svaigā barotnē un iepildīt jaunās kolbās ar svaigu barotni.
HepG2 šūnu nākotnes perspektīvas
HepG2 šūnu līnijas potenciāla pilnīgas atraisīšanas meklējumi turpinās, gūstot revolucionārus panākumus citohromu ekspresijas palielināšanā. Pētnieki pēta arī trīsdimensiju sferoīdu šūnu kultūru iespējas, kas piedāvā fizioloģiski atbilstošāku sistēmu. Metabolisma aktivitāte, tostarp citohromu aktivitāte, 3D sferoidālajos HepG2 modeļos ir ievērojami augstāka nekā 2D šūnās, tādējādi tuvinot mūs modeļa izveidei, kas atspoguļo normālus hepatocītus. Turklāt dinamisko procesu izpēte, kas ir šūnu virsmas proteīnu nepareizas izplatības pamatā, var pavērt ceļu labākai izpratnei par aknu slimībām
HepG2 šūnas: Izpratne par to lomu un atšķirībām biomedicīniskajos pētījumos - bieži uzdotie jautājumi
Atsauces
- Vyas, R.C., Darroudi, F., Natarajan, A.T. Radiācijas izraisīta hromosomu bojāšanās un atkārtota savienošana cilvēka limfocītu hromosomās interfāzē un metafāzē, Mutat Res, 1991; 249(1):29-35.
- Woodfield, S.E., Shi, Y., Patel, R.H., Chen, Z., Shah, A.P., Srivastava, R.K., Whitlock, R.S., Ibarra, A.M., Larson, S.R., Sarabia, S.F., et al. MDM4 inhibīcija: Jaunā terapeitiskā stratēģija P53 reaktivēšanai hepatoblastomas gadījumā. Sci. Rep. 2021, 11, 2967.
- Hussain, S.P., Schwank, J., Staib, F., Wang, X.W., Harris, C.C. TP53 Mutations and hepatocellular Carcinoma: Insights into the Etiology and Pathogenesis of Liver Cancer. Oncogene 2004.
- Schicht, G., Seidemann, L., Haensel, R., Seehofer, D., Damm, G. Critical Investigation of the Usability of Hepatoma Cell Lines HepG2 and Huh7 as Models for the Metabolic Representation of Resectable Hepatocellular Carcinoma. Cancers 2022, 14(17), 4227.
- Verrier, E.R., Colpitts, C.C., Schuster, C., Zeisel, M.B., Baumert, T.F. Cell Culture Models for the Investigation of Hepatitis B and D Virus Infection. Virusi 2016, 8, 261.
- Verrier, E.R., Colpitts, C.C., Bach, C., Heydmann, L., Weiss, A., Renaud, M., Durand, S.C., Habersetzer, F., Durantel, D., AbouJaoudé, G., et al. A Targeted Functional RNA Interference screen Uncovers Glypican 5 as an Entry Factor for Hepatitis B and D Virus. Hepatology 2016, 63, 35-48.
- Gripon, P., Rumin, S., Urban, S., Le Seyec, J., Glaise, D., Cannie, I., Guyomard, C., Lucas, J., Trepo, C., Guguen-Guillouzo, C. Infection of a Human Hepatoma Cell Line by Hepatitis B Virus. Proc. Natl. Acad. Sci. USA 2002, 99, 15655-15660.
- Mersch-Sundermann, V., Knasmüller, S., Wu, X.J., Darroudi, F., Kassie, F. No cilvēka iegūtas aknu šūnu līnijas izmantošana citoprotektoru, antigenotoksisku un kogenotoksisku vielu noteikšanai. Toksikoloģija. 2004; 198(1-3): 329-340.
- Fanelli, A. HepG2 (aknu hepatocelulārā karcinoma): šūnu kultūra. HepG2. Skatīts 2017. gada 3. decembrī.
- Xuan, J., Chen, S., Ning, B., Tolleson, W.H., Guo, L. Development of HepG2-Derived Cells Expressing Cytochrome P450s for Assessing Metabolism-Associated Drug-Induced Liver Toxicity. Physiol. Behav. 2017, 176, 139-148.
- Ooka, M., Lynch, C., Xia, M. Application of in Vitro Metabolism Activation in High-Throughput Screening. Int. J. Mol. Sci. 2020, 21, 8182.
- Huang, L., Coughtrie, M.W.H., Hsu, H. Down-Regulation of Dehydroepiandrosterone Sulfotransferase Gene in Human Hepatocellular Carcinoma. Mol. Cell. Endocrinol.
- Zhu, Z., Hao, X., Yan, M., et al. Cancer stem/progenitor cells are highly enriched in CD133 + CD44 + population in hepatocellular carcinoma. Int J Cancer. 2010; 126:2067-2078.
- Arbus, C., Benyamina, A., Llorca, P.-M., Baylé, F., Bromet, N., Massiere, F., Garay, R.P., Hameg, A. Ciamemazīna metabolismā iesaistīto cilvēka citohroma P450 fermentu raksturojums. Eur J Pharm Sci. 2007 Dec;32(4-5):357-66.