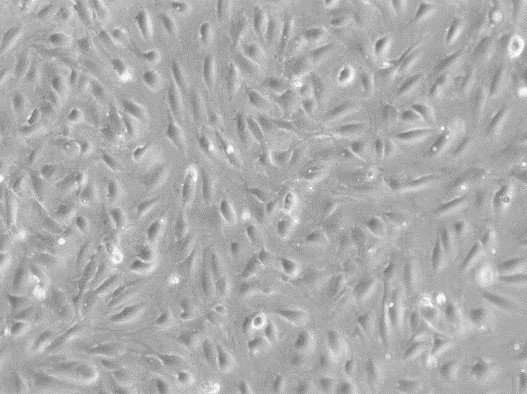
Cilvēka nabassaites vēnas endotēlija šūnas (HUVEC)
HUVEC ir primārās endotēlija šūnas, kas ir svarīgs instruments biomedicīnas pētījumos. Tās palīdz pētniekiem pētīt angiogenezi, asinsvadu bioloģiju un tādas slimības kā ateroskleroze un vēzis. HUVEC izmanto, lai pētītu endotēlija šūnu uzvedību, šūnu signalizācijas mehānismus un zāļu testēšanu, sniedzot vērtīgu ieskatu par iespējamām sirds un asinsvadu slimību un vēža ārstēšanas metodēm. Tās kalpo arī kā modeļa sistēma asinsvadu bioloģijas pētījumiem.
Šajā rakstā iekļauta visa pamatinformācija, kas nepieciešama pirms darba ar HUVEC šūnām. Tajā tiks aplūkoti šādi jautājumi:
- HUVEC šūnu izcelsme un vispārīgās īpašības
- Informācija par HUVEC šūnu līnijas kultivēšanu
- HUVEC šūnu līnija: Priekšrocības un ierobežojumi
- HUVEC šūnu pielietojums pētniecībā
- Publikācijas ar HUVEC šūnām
- Resursi par HUVEC šūnu līniju: Protokoli, videomateriāli un citi resursi
1. HUVEC šūnu izcelsme un vispārīgas īpašībass
Zināšanas par šūnu līnijas izcelsmi un vispārējām īpašībām ir izšķirošas, lai noteiktu tās piemērotību jūsu pētījumam. Šī sadaļa palīdzēs jums uzzināt šo būtisko informāciju par HUVEC endotēlija šūnām: Kādiem nolūkiem izmanto HUVEC šūnas? Kāda ir HUVEC šūnu pilnā forma? Kādas ir HUVEC atšķirīgās īpašības? Kāda ir HUVEC morfoloģija? Kāds ir HUVEC diametrs? Kāds ir Huvec šūnu izmērs?
- HUVEC šūnas iegūst no cilvēka nabassaites vēnas endotēlija.
- HUVEC morfoloģija ir endotēlijam līdzīga. Tās parasti ir daudzstūra formas, un to centrā ir apaļš kodols.
- HUVEC šūnu diametrs ir 17 μm.
- Šīs endotēlija šūnas ir diploīdas. To modālais hromosomu skaits ir 46.
HUVEC TERT2
HUVEC TERT2 ir imortalizēta šūnu līnija, kas iegūta no primārajām cilvēka nabas vēnas endotēlija šūnām (HUVEC). Tā tika izveidota, ieviešot cilvēka telomerāzes reversās transkriptāzes (TERT) gēnu HUVEC šūnu genomā. Šī modifikācija palīdzēja pagarināt to dzīves ilgumu kultūrā, ļaujot veikt ilgākus eksperimentus bez ierobežojumiem, kas saistīti ar primārajām HUVECs.
Kāda ir atšķirība starp HUVEC un HMEC-1?
HUVEC un HMEC-1 endotēlija šūnu līniju struktūra un sarežģītība ir salīdzināma. Tomēr HMEC-1 šūnām ir viendabīgāka populācija nekā HUVEC šūnu lieluma un granulometriskuma ziņā. Tas var samazināt eksperimentālo datu atšķirības.
2.informācija par HUVEC šūnu līnijas kultivēšanu
Šī raksta sadaļa ir veltīta tam, lai sniegtu jums svarīgas zināšanas par HUVEC šūnu kultūru. Tas ievērojami atvieglos darbu ar tām. Šeit jūs atradīsiet atbildes uz šādiem bieži uzdotiem jautājumiem: Kāds ir HUVEC šūnu dubultošanās laiks? Kāds ir HUVEC izsējas blīvums? Cik daudz eja ir HUVEC? Kas ir HUVEC šūnu barotne? Kā kultivēt HUVEC?
Galvenie punkti HUVEC šūnu kultivēšanai
|
Dubultošanās laiks: |
HUVEC šūnu dubultošanās laiks ir aptuveni 23,5 stundas. Tomēr tas var atšķirties atkarībā no šūnu kultivēšanas apstākļiem un pasāžu skaita. |
|
Adhēzijas vai suspensijas veidā: |
HUVEC ir adherentu šūnu līnija. Šūnas aug un veido monoslāņus. |
|
Sadalījuma attiecība: |
HUVEC subkultivācijas attiecība ir no 1:2 līdz 1:4. Šūnas mazgā ar 1x fosfātu buferšķīduma fizioloģisko šķīdumu un pievieno disociācijas šķīdumu (Accutase) 8 līdz 10 minūtes istabas temperatūrā. Pēc tam pievieno barotni un atdalītās šūnas centrifugē. Supernatantu izvada, un šūnu granulas rūpīgi resuspendē. Šūnas iepilda jaunā audzēšanas kolbā. |
|
Augšanas barotne: |
HUVEC šūnu kultivēšanai izmanto endotēlija šūnu augšanas barotni. Barotni nomaina ik pēc 2-3 dienām. HUVEC var izmantot līdz 8-10 cikliem. |
|
Augšanas apstākļi: |
Cilvēka endotēlija šūnu līniju (HUVEC) uztur mitrinātā inkubatorā ar 5 % CO2 37 °C temperatūrā. |
|
Uzglabāšana: |
HUVEC šūnas parasti uzglabā zem -150 °C temperatūrā īpaši zemas temperatūras saldētavā vai šķidrā slāpekļa tvaika fāzē. Tas aizsargā šūnu dzīvotspēju ilgāku laiku. |
|
Saldēšanas process un vide: |
HUVEC šūnu saglabāšanai ieteicams izmantot CM-1 vai CM-ACF sasaldēšanas barotni. Parasti ieteicams lēns sasaldēšanas process, jo tas ļauj samazināt temperatūru tikai par 1 °C minūtē, novēršot šūnu šoku un saglabājot dzīvotspēju. |
|
Atkausēšanas process: |
Lai atkausētu sasaldētās šūnas, ievietojiet tās iepriekš uzsildītā ūdens vannā 37 °C temperatūrā uz 40 līdz 60 sekundēm, līdz paliek tikai neliels ledus gabaliņš. Pēc tam pievieno šūnām svaigu barotni un centrifugē. Šis solis ir nepieciešams, lai no šūnām noņemtu sasaldēšanas barotnes atliekas. Resuspendēt šūnu granulas un pārvietot šūnas jaunā kolbā ar barotni. |
|
Bioloģiskās drošības līmenis: |
Lai pareizi apstrādātu HUVEC šūnu kultūras, nepieciešama 1. bioloģiskās drošības līmeņa laboratorija. |
3. Priekšrocības un ierobežojumi
Tāpat kā citām cilvēka šūnu līnijām, arī HUVEC šūnām ir savas priekšrocības un ierobežojumi. Šajā sadaļā mēs aplūkosim dažus nozīmīgus aspektus, kas būtiski ietekmē to izmantošanu pētniecībā.
Priekšrocības
HUVEC šūnu galvenās priekšrocības ir šādas:
-
Endotēlija šūnu modelis
Ļoti piemēroti modeļi angioģenēzes, asinsvadu bioloģijas un slimību, kas saistītas ar endotēlija funkciju, izpētei.
-
Viegli kultivējamas
Salīdzinoši viegli izolējamas no cilvēka nabassaites. Nav sarežģītu prasību attiecībā uz šūnu kultivēšanu, un tās ir viegli uzturējamas pētniecības laboratorijās.
Ierobežojumi
Ar HUVEC endotēlija šūnu līniju saistītie ierobežojumi ir šādi:
-
Ierobežots dzīves ilgums
HUVEC ir ierobežots dzīves ilgums, parasti tas ir 8 līdz 10 pasāžas, kas ir ierobežojums ilgtermiņa eksperimentiem. Palielinoties pasāžu skaitam, tās var novecot.
4. HUVEC šūnu pielietojums pētniecībā
HUVEC šūnām ir ievērojams potenciāls dažādiem lietojumiem biomedicīnas jomā. Turpmāk mēs uzsvērsim dažus svarīgus HUVEC šūnu izmantošanas veidus pētniecībā.
- Sirds un asinsvadu slimību pētījumi: HUVEC šūnu līnija ir vērtīgs endotēlija šūnu modelis, tādējādi sniedzot ieskatu mehānismos, kas ir sirds un asinsvadu slimību, piemēram, aterosklerozes, trombozes un hipertensijas, pamatā. Pētnieki izmanto šīs šūnas, lai pētītu mehānismus, kas ir endotēlija disfunkcijas, oksidatīvā stresa un iekaisuma pamatā. Piemēram, 2020. gadā veiktajā pētījumā tika izmantotas HUVECs un izpētīts, ka garajai nekodējošajai RNS TTTY15 ir izšķiroša nozīme hipoksijas izraisītā asinsvadu endotēlija šūnu bojājuma uzlabošanā, vēršoties pret miRNA-186-5p asi [1].
- Vēža pētījumi: HUVEC ir ideāli piemērotas asinsvadu bioloģijas pētījumiem. Tāpēc tās izmanto audzēju angioģenēzes un endotēlija šūnu mijiedarbības izpētei. Tas palīdz pētniekiem izprast, kā audzēji iegūst lieko asins apgādi un vairojas. Piemēram, Hui Wang un kolēģi atklāja, ka mutes dobuma plakanšūnu karcinomas (OSCC) šūnu izdalītās eksosomas paaugstina miRNA-210-3p līmeni un samazina epfrīna A3 ekspresiju HUVEC šūnās un veicina caurulīšu veidošanos, regulējot PI3K/AKT kaskādi, kā apstiprināja HUVEC caurulīšu veidošanās tests [2].
- Zāļu testēšana: HUVEC endotēlija šūnas plaši izmanto zāļu testēšanai. Pētnieki, izmantojot HUVEC, var novērtēt zāļu efektivitāti, toksicitāti un dabisko savienojumu, nanodaļiņu un citu terapeitisko līdzekļu iespējamo blakusiedarbību in vitro. Piemēram, pētījumā tika novērtēta Rheum ribes ekstrakta sintezētu sudraba nanodaļiņu toksicitāte, izmantojot HUVEC šūnas [3].
5. Publikācijas ar HUVEC šūnām
Šajā raksta sadaļā uzskaitītas dažas bieži citētas un interesantas pētnieciskas publikācijas, kurās izmantotas HUVEC šūnas.
Šis pētījums publicēts žurnālā Comparative Biochemistry and Physiology Part C: Toxicology & Pharmacology (2019). Tajā norādīts, ka neiromediators gamma-aminosviestskābe (GABA) inhibēH2O2izraisītu oksidatīvo stresu HUVEC šūnās; tādējādi tā varētu būt efektīvs farmakoloģisks līdzeklis pret oksidatīvo bojājumu izraisītām sirds un asinsvadu slimībām.
Šajā pētījumā, kas publicēts Biochemical and Biophysical Research Communications (2020), tika pētīts, kā estrogēns regulē signāla pārnesēju - glikoproteīnu130 (gp130) HUVEC šūnās.
Substrāta cietība regulē A549 šūnu un HUVEC šūnu migrāciju un angiogēzes potenciālu
Šajā pētnieciskajā rakstā žurnālā Journal of Cellular Physiology (2017) tika pētīta mainīga substrāta stīvuma ietekme uz endotēlija šūnu (A549 un HUVECs) migrāciju un angiogenezi. Lai novērtētu šo ietekmi, tika veikti HUVEC migrācijas un HUVEC angiogenezes testi.
Vara oksīda nanodaļiņu lizosomālā nogulsnēšanās izraisa HUVEC šūnu nāvi
Šajā pētījumā, kas publicēts žurnālā Biomaterials (2018), pētīti iespējamie mehānismi, kas izraisa vara oksīda nanodaļiņu toksicitāti asinsvadu endotēlija šūnās.
Šajā pētījumā, kas publicēts žurnālā Medicine (2020), ierosināts, ka dabiskais savienojums kvercetīns nomāc TNF-alfa izraisītu HUVEC apoptozi un iekaisumu, regulējot AP-1 un NF-kB signalizācijas ceļus.
6. HUVEC šūnu līnijas resursi: Protokoli, videoklipi un citi resursi
Tālāk ir sniegti daži tiešsaistes resursi par HUVEC šūnām.
- HUVEC transfekcija: Šī tīmekļa vietnes saite sniegs visaptverošas zināšanas par HUVEC transfekciju. Piemēram, tā ietver informāciju par transfekcijas reaģentiem un in vitro HUVEC transfekcijas protokolu.
Šajā saitē ir sniegts HUVEC šūnu kultūras protokols.
- HUVEC šūnu kultūras: Šis dokuments palīdzēs apgūt HUVEC šūnu kultūru subkultivēšanas un kriokonservēto kultūru apstrādes protokolus.
Atsauces
- Zheng, J., et al., LncRNA TTTY15 regulē hipoksijas izraisītu asinsvadu endotēlija šūnu bojājumu, mērķējot miR-186-5p sirds un asinsvadu slimību gadījumā. European Review for Medical & Pharmacological Sciences, 2020. 24(6).
- Wang, H., et al., OSCC exosomas regulē miR-210-3p, kas vērsta uz EFNA3, lai veicinātu mutes vēža angiogenezi caur PI3K/AKT ceļu. BioMed research international, 2020. 2020.
- Unal, İ. and S. Egri, Biosynthesis of silver nanoparticles using the aqueous extract of Rheum ribes, characterization and the evaluation of its toxicity on HUVECs and Artemia salina. Inorganic and Nano-Metal Chemistry, 2022: p. 1-14.