Дослідження потенціалу плюрипотентних стовбурових клітин у регенеративній медицині
Плюрипотентні стовбурові клітини - це захоплююча область досліджень, що має величезний потенціал для регенеративної медицини та моделювання захворювань. Ці клітини, до яких відносяться спонтанно імморталізовані клітинні лінії, такі як клітини WI-38, а також індуковані плюрипотентні стовбурові клітини (iPSC), отримані з тканин дорослої людини, мають унікальну здатність диференціюватися в будь-який тип клітин в організмі. Це робить їх безцінними інструментами для вивчення розвитку людини, механізмів розвитку захворювань і потенційних методів лікування.
В авангарді досліджень плюрипотентних стовбурових клітин знаходяться індуковані плюрипотентні стовбурові клітини, які можуть бути створені з власних клітин пацієнта, таких як фібробласти шкіри або клітини крові. Перепрограмуючи ці дорослі клітини за допомогою специфічних факторів, дослідники можуть створювати індивідуальні для пацієнта ІПСК, які зберігають генетичний фон донора.
Важливість первинних клітин людини в дослідженнях плюрипотентних стовбурових клітин
Первинні клітини людини також мають вирішальне значення в дослідженнях плюрипотентних стовбурових клітин, забезпечуючи основу для порівняння та валідації клітин, отриманих з iPSC. Наприклад, стовбурові клітини зубної пульпи людини (hDPSC ) і стовбурові клітини зубного фолікула людини (hDFSC ) є цінними ресурсами для вивчення розвитку і регенерації зубів. Аналогічно, HUVEC, клітини одного донора, широко використовуються в дослідженнях судинної біології та ангіогенезу і слугують еталоном для оцінки ендотеліальних клітин, отриманих з iPSC.
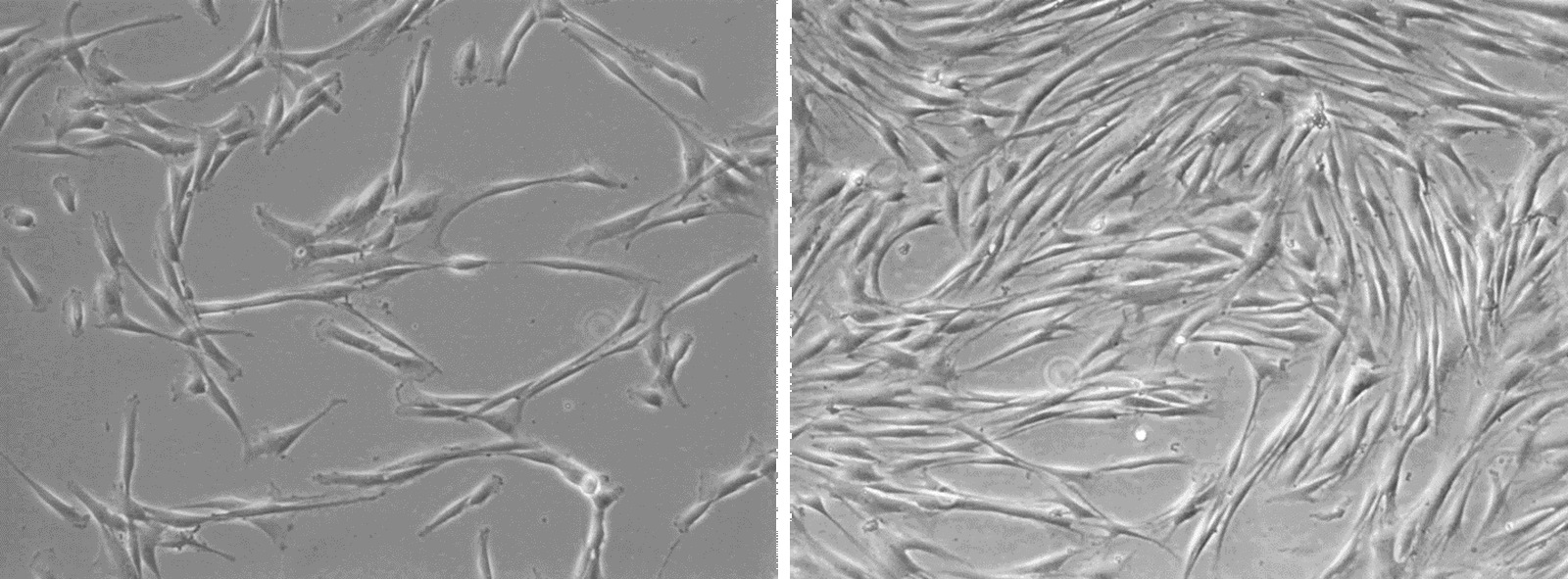
Інший приклад - клітина P-19, тип плюрипотентної ембріональної карциноми, спочатку була отримана з тератокарциноми миші штаму C3H/He. Лінія клітин P19, зображена зліва, походить від миші (Mus musculus).
Каталог мезенхімальних стовбурових клітин людини
Плюрипотентні стовбурові клітини є наріжним каменем регенеративної медицини та досліджень біології розвитку. Ці клітини, які включають ембріональні стовбурові клітини (ЕСК) та індуковані плюрипотентні стовбурові клітини (ІПСК), мають чудову здатність диференціюватися в будь-який тип клітин в організмі. Ця унікальна властивість робить їх безцінними інструментами для вивчення розвитку людини, моделювання захворювань, скринінгу лікарських препаратів і потенційної клітинної терапії. iPSC, зокрема, зробили революцію в цій галузі, дозволивши створювати специфічні для пацієнта стовбурові клітини з тканин дорослої людини, що відкриває захоплюючі можливості для персоналізованої медицини. Тепер дослідники можуть отримувати iPSC від пацієнтів з різними захворюваннями, диференціювати їх у відповідні типи клітин і вивчати механізми, що лежать в основі цих станів, в пробірці. Більше того, можливість створення аутологічної клітинної терапії з отриманих від пацієнта iPSC має величезні перспективи для регенеративної медицини, оскільки ці клітини потенційно можуть бути використані для заміщення пошкоджених або хворих тканин без ризику імунного відторгнення. Оскільки дослідження плюрипотентних стовбурових клітин продовжують розвиватися, стає все більш очевидним, що ці клітини відіграватимуть ключову роль у формуванні майбутнього медицини та поглибленні нашого розуміння біології людини.
| Продукт | Опис | Кішка. Немає. |
|---|---|---|
| Мезенхімальні стовбурові клітини людини - жирова тканина | Мезенхімальні стовбурові клітини, виділені з жирової тканини людини | 300645 |
| Мезенхімальні стовбурові клітини людини - амніон | Мезенхімальні стовбурові клітини, отримані з амніотичної мембрани людини | 300644 |
| Мезенхімальні стовбурові клітини людини - кістковий мозок (МСК-КМ) | Мезенхімальні стовбурові клітини, виділені з кісткового мозку людини | 300665 |
| Мезенхімальні стовбурові клітини людини - ворсинки хоріона | Мезенхімальні стовбурові клітини, отримані з ворсинок хоріона людини | 300646 |
| Мезенхімальні стовбурові клітини людини - ендометрій | Мезенхімальні стовбурові клітини, виділені з тканини ендометрію людини | 300647 |
| Мезенхімальні стовбурові клітини людини - пуповина - артерія | Мезенхімальні стовбурові клітини, отримані з артерії пуповини людини | 300648 |
| Мезенхімальні стовбурові клітини людини - желе Уортона (HMSC-WJ) | Мезенхімальні стовбурові клітини, виділені з Уортонового желе пуповини людини | 300685 |
Потенціал та виклики iPSC у моделюванні та терапії захворювань
Пацієнтські iPSC пропонують безпрецедентну можливість моделювати захворювання людини в пробірці. Диференціюючи ці клітини у відповідні типи клітин, дослідники можуть вивчати молекулярні механізми, що лежать в основі різних патологій, і проводити скринінг потенційних кандидатів у ліки. Наприклад, кардіоміоцити, отримані з iPSC від пацієнтів з генетичними захворюваннями серця, були використані для відтворення фенотипів захворювань і перевірки ефективності терапевтичних сполук [198]. Аналогічно, нейрони, отримані з iPSC у пацієнтів з неврологічними розладами, такими як хвороба Альцгеймера та хвороба Паркінсона, надали цінну інформацію про прогресування захворювання та реакцію на лікування [199].
Однак, перш ніж iPSC можна буде широко використовувати для моделювання та терапії захворювань, необхідно вирішити кілька проблем. До них відносяться
- Варіабельність ефективності перепрограмування та якості iPSC
- Генетичні та епігенетичні аберації під час репрограмування
- Незрілий або ембріональний фенотип клітин, отриманих з iPSC
- Відсутність стандартизованих протоколів диференціації та дозрівання
- Занепокоєння щодо безпеки, пов'язані з пухлиногенністю та імуногенністю
Дослідження спрямовані на вирішення цих проблем шляхом розробки більш ефективних і стандартизованих методів перепрограмування, вдосконалення протоколів диференціювання та впровадження суворих заходів контролю якості. Досягнення в технологіях редагування генів, таких як CRISPR/Cas9, також дозволяють виправляти хвороботворні мутації в отриманих від пацієнта iPSC, прокладаючи шлях до аутологічної клітинної замісної терапії [200].
Майбутнє iPSC в регенеративній медицині
Поява технології iPSC відкрила захоплюючі можливості для регенеративної медицини. На відміну від ембріональних стовбурових клітин, iPSC можуть бути отримані з власних клітин пацієнта, що дозволяє уникнути етичних проблем і ризику імунного відторгнення. Кілька доклінічних досліджень продемонстрували потенціал клітин, отриманих з iPSC, у лікуванні різних захворювань, таких як
- Хвороба Паркінсона: Трансплантація дофамінергічних нейронів, отриманих з iPSC, у тваринних моделях [201]
- Травма спинного мозку: Приживлення нейральних клітин-попередників, отриманих з iPSC, що сприяють функціональному відновленню [202]
- Макулодистрофія: Заміна пошкодженого пігментного епітелію сітківки клітинами, отриманими з iPSC [203]
- Серцева недостатність: Ін'єкція кардіоміоцитів, отриманих з iPSC, для поліпшення серцевої функції [204]
Очікується, що з розвитком галузі з'явиться більше клінічних досліджень із застосуванням клітин, отриманих з iPSC. Однак для того, щоб перетворити ці багатообіцяючі доклінічні результати в безпечні та ефективні методи лікування, необхідно подолати ряд перешкод, таких як забезпечення чистоти і стабільності клітин, отриманих з iPSC, розробка масштабованих виробничих процесів і створення відповідних регуляторних норм і правил.
Отже, iPSC є потужним інструментом для моделювання захворювань, розробки ліків та регенеративної медицини. Незважаючи на те, що проблеми залишаються, швидкий темп досліджень і технологічний прогрес у цій галузі відкривають широкі перспективи для революційних змін у лікуванні різних захворювань людини. Подальша міждисциплінарна співпраця між науковцями, клініцистами та регуляторними органами матиме вирішальне значення для реалізації повного потенціалу iPSC у покращенні здоров'я людини.
Ключові моменти
- iPSC отримують із соматичних клітин шляхом введення генів, пов'язаних з плюрипотентністю
- iPSC мають схожі властивості з ембріональними стовбуровими клітинами, але уникають етичних проблем
- IPSC, отримані від пацієнта, дозволяють моделювати захворювання та проводити персоналізований скринінг лікарських засобів
- клітини, отримані з iPSC, показали багатообіцяючі результати в доклінічних дослідженнях різних захворювань
- Виклики в дослідженнях iPSC включають варіабельність, генетичну нестабільність та проблеми безпеки
- Досягнення в технологіях перепрограмування, диференціації та редагування генів рухають цю галузь вперед
- Клінічне впровадження терапії на основі iPSC вимагатиме подолання технічних та регуляторних перешкод
- Міждисциплінарна співпраця має вирішальне значення для реалізації повного потенціалу iPSC в регенеративній медицині

ПАРТНЕР, ЯКОМУ МОЖНА ДОВІРЯТИ: ЦИТАТА
Потенційне застосування та майбутні напрямки розвитку плюрипотентних стовбурових клітин
Дослідження плюрипотентних стовбурових клітин мають величезні перспективи для революції в регенеративній медицині та поглиблення нашого розуміння людського розвитку і хвороб. Як ембріональні стовбурові клітини людини (hESC), так і індуковані плюрипотентні стовбурові клітини (hiPSC) мають чудову здатність диференціюватися в будь-який тип клітин в організмі, що робить їх безцінними інструментами для вивчення механізмів захворювань, скринінгу ліків і потенційних методів клітинної терапії.
одним з найцікавіших застосувань плюрипотентних стовбурових клітин є їх використання в регенеративній медицині. Доклінічні дослідження продемонстрували терапевтичний потенціал hESC- та hiPSC-похідних клітин у різних моделях захворювань, таких як травма спинного мозку, сліпота та серцеві розлади. Наразі триває кілька клінічних досліджень із застосуванням продуктів, отриманих з hESC, спрямованих на лікування таких захворювань, як травма спинного мозку, макулодистрофія та діабет 1-го типу (табл. 1). Крім того, Японія схвалила перше в світі клінічне дослідження з використанням отриманих з hiPSC пігментних епітеліальних клітин сітківки для лікування макулодистрофії.
Однак, перш ніж повний потенціал плюрипотентних стовбурових клітин буде реалізований у клінічній практиці, необхідно вирішити кілька проблем:
- Розробка ефективних і безпечних методів перепрограмування без використання вірусних векторів і онкогенів
- Впровадження суворих заходів контролю якості для забезпечення безпеки та функціональності продуктів, отриманих з hESC- та hiPSC-похідних
- Оптимізація протоколів диференціювання для отримання чистих і функціональних клітинних популяцій
- Проведення ретельних доклінічних досліджень на відповідних моделях тварин для оцінки ефективності та безпеки терапії на основі плюрипотентних стовбурових клітин
- Орієнтуватися в регуляторному ландшафті для отримання дозволу на клінічні випробування та подальшу комерціалізацію
Ще одне перспективне застосування плюрипотентних стовбурових клітин, зокрема hiPSC, - це моделювання захворювань та розробка ліків. Пацієнтські hiPSC можуть відтворювати різні аспекти патології при диференціюванні у відповідні типи клітин, забезпечуючи потужну платформу для вивчення механізмів захворювання та виявлення нових терапевтичних мішеней. Крім того, hiPSC, отримані як від здорових донорів, так і від пацієнтів, пропонують більш фізіологічно релевантну систему для оцінки ефективності та токсичності лікарських засобів порівняно з традиційними імморталізованими клітинними лініями людини.
На закінчення, незважаючи на значний прогрес, досягнутий в області дослідження плюрипотентних стовбурових клітин, необхідні подальші дослідження для повного розуміння біології плюрипотентності і диференціювання, а також для подолання проблем, пов'язаних з терапевтичним застосуванням. Постійні зусилля, спрямовані на вдосконалення технологій перепрограмування, створення надійних протоколів диференціювання та забезпечення безпеки й ефективності продуктів, отриманих з hESC та hiPSC, прокладуть шлях до клінічного застосування цих потужних інструментів у регенеративній медицині та розробці ліків.
Використовуючи величезний потенціал плюрипотентних стовбурових клітин, ми можемо працювати над розробкою інноваційних методів лікування широкого спектру захворювань людини і, в кінцевому рахунку, покращувати результати лікування пацієнтів.