Об'єм: 100 мл
Зберігання: ≤ –15°C
Стерильність: стерильно фільтрований
Стабільний розчин глутаміну (L-аланіл-L-глутамін, 200 мМ) — це високостабільна дипептидна форма L-глутаміну, розроблена як пряма заміна традиційного L-глутаміну в середовищах для культивування клітин. L-глутамін — це незамінна амінокислота і основне джерело енергії для культивованих клітин, що відіграє важливу роль у рості клітин, метаболізмі та синтезі білків.
Застосування та переваги
У стандартних рідких середовищах L-глутамін відносно швидко розкладається при температурі 37 °C, що призводить до утворення токсичних побічних продуктів, таких як іони амонію, які можуть негативно впливати на життєздатність клітин і результати експериментів. Стабільний глутамін долає це обмеження, забезпечуючи нерозкладну дипептидну форму, яка залишається незмінною в умовах культивування.
Клітини ферментативно розщеплюють дипептидний зв'язок, щоб вивільнити L-глутамін за потреби, забезпечуючи постійне свіже постачання та запобігаючи накопиченню шкідливих відходів. Це робить розчин особливо вигідним для довготривалих клітинних культур та систем росту з високою щільністю.
Склад і застосування
Розчин L-аланіл-L-глутаміну готується у воді, придатній для культивування клітин, у концентрації 200 мМ і проходить стерильну фільтрацію для застосування в умовах, чутливих до забруднення. Його можна розбавляти безпосередньо в повноцінному середовищі відповідно до експериментальних вимог. Зберігати при температурі ≤ –15 °C і уникати повторних циклів заморожування-розморожування для збереження стабільності продукту.
Тільки для дослідницьких цілей. Не призначений для використання в діагностичних або терапевтичних процедурах. Не призначений для використання на людях або тваринах.
Об'єм: 100 мл
Зберігання: від +2 °C до +8 °C
Стерильність: стерильно фільтрований
Буферний розчин HEPES (1 М), також відомий як N-2-гідроксиетилпіперазин-N-2-етанолсульфонова кислота, є цвітеріонним органічним буферним агентом, який широко використовується в середовищах для культивування клітин. Він призначений для підтримки стабільних умов pH у фізіологічному діапазоні від 6,7 до 8,6, забезпечуючи оптимальну функцію клітин під час застосування in vitro.
Застосування та переваги
HEPES забезпечує надійну буферну здатність у системах культивування клітин, особливо коли клітини обробляються поза інкубатором CO₂. Додавання 10–25 мМ HEPES до культивувальних середовищ забезпечує підвищену стабільність pH під час тривалих періодів маніпуляцій, що допомагає підтримувати стабільні умови експерименту.
Цей буфер є непроникним для мембран, мінімально впливає на біохімічні реакції та демонструє високу хімічну та ферментативну стабільність. Ці властивості роблять його придатним для широкого спектру застосувань у клітинних культурах та біохімії.
Склад та застосування
Розчин постачається у вигляді 1 М концентрату, приготованого у воді, придатній для культивування клітин, і проходить стерильну фільтрацію для використання в середовищах, чутливих до забруднення. Його можна розбавляти до бажаної робочої концентрації залежно від вимог застосування. Зберігати при температурі від +2 °C до +8 °C і обробляти в асептичних умовах для збереження цілісності продукту.
Тільки для дослідницьких цілей. Не призначений для використання в діагностичних або терапевтичних процедурах. Не призначений для використання на людях або тваринах.
Об'єм: 50 мл
Зберігання: від +2 °C до +8 °C
Стерильність: стерильно фільтрований
Розчин D-(+)-глюкози (розчин декстрози) — це стерильний, готовий до вживання препарат, що містить природний цукор D-(+)-глюкозу, який є основним компонентом клітинного метаболізму. Глюкоза бере участь у важливих біологічних процесах, таких як вироблення енергії, глікозилювання та утворення гліканів, які сприяють формуванню клітинної структури та функціонуванню клітин.
Застосування та переваги
Цей розчин глюкози широко використовується як добавка в середовищах для культивування клітин та в численних застосуваннях клітинної та молекулярної біології. Як основне джерело вуглецю та енергії, глюкоза підтримує ріст, проліферацію та метаболічну активність клітин. Її участь у біосинтетичних шляхах також робить її критично важливою для підтримання нормальної клітинної фізіології та експериментальної послідовності.
Склад та застосування
Розчин постачається з високою концентрацією глюкози 250 г/л, що дозволяє гнучко розбавляти його в культуральних середовищах відповідно до експериментальних вимог. Він стерильно фільтрований, щоб забезпечити придатність для застосувань, чутливих до забруднення. Зберігати при температурі від +2 °C до +8 °C і обробляти в асептичних умовах для збереження якості та стабільності продукту.
Тільки для дослідницьких цілей. Не призначений для використання в діагностичних або терапевтичних процедурах. Не призначений для використання на людях або тваринах.
Об'єм: 10 мл
Зберігання: від +2 °C до +8 °C
Стерильність: стерильнофільтрований
Розчин інсуліну-трансферину-селену (ITS) (100x) — це хімічно визначена добавка, призначена для широкого спектра застосувань у клітинних культурах. Найчастіше її використовують як добавку до базових середовищ для клітинних культур для підтримки росту клітин в умовах зниженого вмісту сироватки або без сироватки.
Застосування та переваги
Наша добавка ITS забезпечує необхідні компоненти, потрібні для оптимальної роботи безсироваткових середовищ. Додаючи ITS до звичайних поживних середовищ, можна значно зменшити потребу у фетальній сироватці бика (FBS) для рутинного утримання багатьох клітинних ліній. Це допомагає мінімізувати варіабельність, пов’язану з використанням сироватки, зберігаючи при цьому стабільний ріст і життєздатність клітин.
Інсулін підтримує клітинне поглинання та метаболізм ключових поживних речовин, трансферин сприяє транспорту заліза, а селен сприяє антиоксидантній захисті та ферментативній активності. Разом ці компоненти сприяють збалансованому клітинному метаболізму та покращеній відтворюваності в визначених системах культивування.
Склад та застосування
Інсулін-трансферин-селен (ITS) постачається у вигляді 100-кратно концентрованого розчину в збалансованому сольовому розчині Ерла (EBSS) без фенолового червоного. Для стандартних застосувань розведіть у співвідношенні 1:100 у відповідному базовому середовищі, щоб досягти рекомендованої робочої концентрації. Зберігайте при температурі від +2 °C до +8 °C та поводьтеся з продуктом в асептичних умовах, щоб зберегти його стабільність та стерильність.
Тільки для дослідницьких цілей. Не призначений для використання в діагностичних або терапевтичних процедурах. Не призначений для використання у людей або тварин.
Об'єм: 5 мл
Зберігання: від +2 °C до +8 °C
Стерильність: стерильнофільтрований
Розчин рекомбінантного людського інсуліну — це хімічно визначений добавка, яка зазвичай використовується для культивування клітинних ліній ссавців, зокрема клітин яєчників китайського хом'яка (CHO). Цей розчин для культивування клітин містить рекомбінантний людський інсулін, експресований у Saccharomyces cerevisiae, що забезпечує високу чистоту та стабільні результати в дослідницьких цілях.
Застосування та переваги
Інсулін зазвичай додають до безсироваткових та хімічно визначених середовищ для стимулювання росту та продуктивності клітин. Як ключовий регуляторний гормон, інсулін підтримує клітинне поглинання, використання та накопичення глюкози, амінокислот і жирних кислот. Він також пригнічує розпад глікогену, білків і ліпідів, тим самим сприяючи покращенню життєздатності клітин та метаболічної стабільності в системах культивування. Хімічно визначений склад забезпечує відтворюваність та мінімізує варіабельність у чутливих робочих процесах культивування клітин.
Біологічні властивості та застосування
Інсулін — це дволанцюговий поліпептидний гормон, що природним чином виробляється β-клітинами острівців підшлункової залози. Його молекулярна маса становить приблизно 5800 Да. Ланцюги α та β з'єднані двома міжланцюговими дисульфідними зв'язками, а ланцюг α містить один внутрішньоланцюговий дисульфідний зв'язок. Для застосування в клітинних культурах розчин слід обробляти в асептичних умовах і зберігати при температурі від +2 °C до +8 °C для збереження стабільності та ефективності.
Тільки для дослідницьких цілей. Не призначений для використання в діагностичних або терапевтичних процедурах. Не призначений для використання у людей або тварин.
Об'єм: 100 мл
Зберігання: від +2 °C до +8 °C
Стерильність: стерильно фільтрований
Розчин пірувату натрію (100 мМ) — це стерильний, готовий до використання додаток, призначений для забезпечення додаткового, легкодоступного джерела енергії для середовищ культивування клітин. Піруват натрію відіграє ключову роль у клітинному енергетичному обміні та підтримує ріст метаболічно активних і швидко проліферуючих клітин, таких як пухлинні клітини. Додавання цього додатка може підвищити життєздатність клітин і допомогти підтримувати метаболічну стабільність у культуральних системах.
Застосування та переваги
Цей розчин широко використовується в рутинному культивуванні клітин для збагачення середовищ піруватом і сприяння оптимальним умовам росту. Він підтримує вироблення АТФ, може допомогти зменшити окислювальний стрес і сприяє поліпшенню метаболічної активності культивованих клітин. Вироблений у воді, придатній для культивування клітин, і стерильно фільтрований, продукт забезпечує стабільну якість і відтворюваність у дослідницьких робочих процесах.
Використання та сумісність
Рекомендована кінцева концентрація для більшості застосувань клітинної культури становить 1 мМ пірувату натрію, що досягається розведенням 100 мМ запасного розчину 1:100 у повноцінному культуральному середовищі. Розчин сумісний з широким спектром базових середовищ та ліній клітин ссавців. Зберігати при температурі від +2 °C до +8 °C та захищати від забруднення для збереження стабільності продукту.
Тільки для дослідницьких цілей. Не призначений для використання в діагностичних або терапевтичних процедурах. Не призначений для використання на людях або тваринах.
Об'єм: 100 мл Зберігання: ≤-15°C Стерильність: Стерильно відфільтрований
Розчин антибіотика/антимікотика (100х )
- це стерильний, готовий до використання концентрат, призначений для зменшення ризику мікробного забруднення в культурі клітин та інших лабораторних дослідженнях. Цей 100-кратний розчин містить добре відому комбінацію пеніциліну, стрептоміцину та амфотерицину В, що забезпечує антимікробну активність широкого спектру дії проти грампозитивних і грамнегативних бактерій, дріжджів та нитчастих грибів. Препарат підходить для використання в культурах еукаріотичних клітин, бактеріальних середовищах та інших чутливих до забруднення системах, підтримуючи чистоту та послідовність лабораторних операцій.
Застосування та переваги Оптимізоване для рутинних дослідницьких протоколів, це рішення широко використовується для підтримання асептичних умов у робочих процесах з клітинними культурами. Воно забезпечує надійну роботу в чутливих до забруднення середовищах, допомагаючи дослідникам зменшити ризик надмірного росту мікроорганізмів без шкоди для здоров'я клітин і відтворюваності експериментів. Стерильно відфільтрований склад усуває необхідність у додаткових етапах розчинення, сприяючи спрощеній підготовці середовищ і зменшуючи варіабельність щоденних лабораторних процедур.
Використання та сумісність Для досягнення стандартних робочих концентрацій розведіть розчин у співвідношенні 1:100 у вашому поживному середовищі. Продукт сумісний з широким спектром клітинних ліній ссавців і базальних середовищ. Завдяки постійній наявності на складі, дослідники отримують вигоду від надійного безперервного постачання та спрощеного планування логістики. Розчин слід зберігати при ≤ -15 °C і захищати від повторних циклів заморожування-розморожування для збереження стабільності. Тільки для дослідницьких цілей. Не для використання в діагностичних або терапевтичних процедурах. Не застосовувати для лікування людей або тварин.
Об'єм: 100 мл Зберігання: від +2°C до +8°C Стерильність: Стерильно відфільтрований
Замінніамінокислоти MEM (100x )
- це стерильна добавка, призначена для посилення росту та життєздатності клітин у системах культивування клітин ссавців. Формула відповідає 100-кратному концентрату замінних амінокислот, що містяться в стандартному мінімальному живильному середовищі (МЖС), що дозволяє безпосередньо додавати їх у базальні середовища з мінімальною підготовкою.
Застосування та переваги Ця добавка забезпечує додатковий пул амінокислот для клітин, що швидко проліферують, або для клітинних ліній, які втратили здатність синтезувати замінні амінокислоти de novo. Полегшуючи метаболічне навантаження біосинтезу, вона сприяє покращенню кінетики росту, подовженню життєздатності та більшій експериментальній стабільності
- особливо в чутливих до поживних речовин культурах або культурах з високою щільністю.
Склад і застосування Розчин містить гліцин, L-аланін, L-аспарагін, L-аспарагінову кислоту, L-глутамінову кислоту, L-пролін та L-серин. Сумісний з MEM та більшістю інших стандартних середовищ. Для використання розведіть 1:100 у кінцевому поживному середовищі. Цей продукт стерильно відфільтрований і готовий до використання без додаткових операцій. Тільки для дослідницьких цілей. Не для використання в діагностичних або терапевтичних процедурах. Не для використання на людях або тваринах.
Accutase — це готовий до використання, стерильнофільтрований розчин для відокремлення клітин, розроблений як м'яка альтернатива трипсину/EDTA для дисоціації адгезивних клітин ссавців зі стандартного пластикового посуду для культивування тканин та поверхонь з адгезивним покриттям. Він поєднує протеолітичну та колагенолітичну активність ферментів у збалансованому сольовому розчині для забезпечення ефективної, але контрольованої дисоціації, зберігаючи білки на поверхні клітин та підтримуючи високу життєздатність після пасажування та швидке повторне прикріплення.
Формула Accutase базується на фосфатно-буферному розчині Дюльбекко (DPBS) з ЕДТА та феноловим червоним як візуальним індикатором рН. Ферменти мають нессавцеве та небактеріальне походження, що робить Accutase особливо придатним для досліджень стовбурових клітин, робочих процесів з вакцинами та будь-яких застосувань, де необхідно мінімізувати забруднення, похідні від тварин або мікроорганізмів. Розчин самоінгібується при 37 °C, тому після відокремлення не потрібні нейтралізуючі реагенти або середовища, що містять сироватку — клітини можна переносити безпосередньо у свіже середовище.
Основні характеристики
Готова до використання 1x стерильнофільтрована рідина – розведення або відновлення не потрібні
Комбінована протеолітична та колагенолітична активність ферментів для м'якого роз'єднання
Кожна партія стандартизована до визначеної активності дисоціації для забезпечення стабільності між партіями
Ферменти не походять від ссавців та бактерій
Автоінгібується при 37 °C – не потребує нейтралізуючого розчину
Створено на основі PBS Дульбекко з EDTA
Феноловий червоний включений як візуальний індикатор pH
pH 6,8–7,8
Типові застосування
Accutase м'яко дисоціює широкий спектр адгезивних та чутливих типів клітин, включаючи ембріональні стовбурові клітини людини (hESCs), індуковані плюрипотентні стовбурові клітини людини (iPSCs), нейральні стовбурові клітини, первинні нейрони та стандартні культивовані адгезивні лінії, такі як HeLa, HEK 293, CHO, MDCK, Vero, NIH/3T3, BHK-21 та A549. Типові випадки використання включають:
Рутинне субкультурування та пасажування адгезивних клітин ссавців
Делікатне роз'єднання окремих клітин hESCs, iPSCs та інших чутливих ліній
Підготовка зразків для проточної цитометрії та аналізу FACS
Аналіз маркерів клітинної поверхні, де важлива цілісність епітопу
Аналізи міграції, проліферації та апоптозу клітин
Аналізи стану спокою шляхом депривації сироватки та дослідження трансфекції онкогенів
Аналізи міграції пухлинних клітин та клітин нервового гребеня
Збільшення масштабів виробництва в робочих процесах біореакторів
Для рутинної роботи нанесіть приблизно 10 мл Accutase на 75 см2 поверхні культури та інкубуйте протягом 5–10 хвилин при кімнатній температурі. Оптимальний час інкубації слід визначати для кожної клітинної лінії окремо, і він не повинен перевищувати одну годину. Перед додаванням промийте клітинний шар розчином солі без Ca2+/Mg2+, таким як DPBS без кальцію та магнію, щоб видалити залишки сироватки та двовалентні катіони.
Поводження та зберігання
Зберігайте нерозкриту пляшку в замороженому стані при температурі -15 °C або нижче. Розморожуйте при кімнатній температурі або протягом ночі при температурі від +2 °C до +8 °C. Не розморожуйте Accutase у водяній бані при 37 °C, оскільки підвищені температури знижують активність ферменту. Після розморожування розчин можна зберігати до 2 місяців при температурі від +2 °C до +8 °C; не зберігайте при кімнатній температурі. Не розігрівайте реагент до 37 °C перед застосуванням – додавайте його безпосередньо до промитих клітин при кімнатній температурі. Для тривалого зберігання рекомендується розливати реагент у одноразові аліквоти, щоб уникнути багаторазових циклів розморожування. Завжди працюйте в асептичних умовах.
Якість
Виробляється відповідно до суворих стандартів якості. Кожна партія Accutase проходить стерильну фільтрацію та тестується на стерильність, рН, зовнішній вигляд та дисоціаційну активність, щоб забезпечити стабільну та відтворювану ефективність від партії до партії.
Технічні характеристики
Характеристики
Деталі
Тип продуктуРеагент для відокремлення/дисоціації клітин
ФорматСтерильнофільтрована рідина, готова до використання
Об'єм100 мл
Робоча концентрація1x (готова до використання)
Активність ферментуКомбінована протеолітична та колагенолітична
Походження ферментуНессавцевий та небактеріальний
Буферна системаPBS Дюльбекко з ЕДТА
Індикатор pHФеноловий червоний
Діапазон pH6,8 – 7,8
Зовнішній виглядПрозорий розчин від блідо-червоного до оранжевого кольору
Температура зберігання-15 °C або нижче
Стабільність після розморожуванняДо 2 місяців при температурі від +2 °C до +8 °C
Рекомендований об’єм для використання~10 мл на 75 см² поверхні культури
Типовий час інкубації5 – 10 хвилин при кімнатній температурі
Умови транспортуванняЗаморожено на сухому льоді
ПризначенняТільки для наукових досліджень та подальшого виробництва
Формула (склад на літр)
Компонент
Концентрація (мг/л)
Неорганічні солі
Хлорид натрію (NaCl)8000,00
Гідрофосфат натрію (Na2HPO4)1150,00
Хлорид калію (KCl)200,00
Дігідрофосфат калію (KH2PO4)200,00
Інші компоненти
EDTA · 4Na (тетранатрій EDTA)220,00
Феноловий червоний3,00
Запатентована суміш ферментів (протеолітична та колагенолітична активність)1x
Accutase є зареєстрованою торговою маркою компанії Innovative Cell Technologies, Inc.
Ця готова до використання, стерильнофільтрована рідка суміш доповнена збалансованим сольовим розчином Ерла (EBSS), 2 мМ L-глутаміном, D-глюкозою (1,0 г/л) та 2,2 г/л бікарбонату натрію (NaHCO3), що робить її придатною для використання в атмосфері інкубатора з контрольованим вмістом CO2 (зазвичай 5 % CO2). Включений до складу феноловий червоний діє як індикатор рН, що дозволяє зручно візуально контролювати стан середовища під час культивування клітин.
Основні характеристики
Класичний склад MEM за Ейглом із збалансованим сольовим розчином Ерла (EBSS)
Містить 2 мМ L-глутаміну – готовий до негайного використання
2,2 г/л бікарбонату натрію — буфер для інкубації при 5 % CO2
З D-глюкозою (1,0 г/л) як основним джерелом вуглецю
З феноловим червоним як індикатором рН
Без HEPES та пірувату натрію
Стерильнофільтроване рідке середовище, готове до використання
pH 7,0 – 7,6
Типові застосування
EMEM підтримує культивування широкого спектру клітинних ліній ссавців, включаючи HeLa, HEK 293, Vero, MRC-5, L-929, BHK-21 та багатьох первинних клітин. Типові застосування включають:
Рутинне утримання та розмноження адгезивних клітинних ліній
Розмноження вірусів та виробництво вакцин
Дослідження цитотоксичності та біоаналізи
Дослідження трансфекції та експресії білків
Фундаментальні дослідження в галузі клітинної та молекулярної біології
Для оптимального росту клітин EMEM зазвичай доповнюють 5–10 % ембріональною сироваткою бика (FBS) та, залежно від клітинної лінії, неесенціальними амінокислотами (NEAA) та антибіотиками, такими як пеніцилін/стрептоміцин.
Поводження та зберігання
Зберігайте нерозкриту пляшку при температурі від +2 °C до +8 °C, захищаючи від світла. Після відкриття використовуйте в асептичних умовах. L-глутамін у розчині піддається поступовому розпаду — для досягнення найкращих результатів ми рекомендуємо використовувати середовище протягом 4 тижнів після відкриття або, у разі тривалого зберігання, додавати свіжий L-глутамін перед використанням. Перед додаванням до клітин дайте середовищу нагрітися до 37 °C.
Якість
Виробляється відповідно до суворих стандартів якості. Кожна партія проходить тестування на стерильність, рН, осмоляльність та рівень ендотоксинів для забезпечення стабільної ефективності при використанні в культурах клітин.
Технічні характеристики
Характеристики
Деталі
Тип продуктуMEM
Категорія продуктуСередовища для культивування клітин
ФорматРідкий
СтерильнийТак
Розмір500 мл
L-глутамінЗ L-глутаміном (2 мМ)
ГлюкозаЗ глюкозою (1,0 г/л)
Бікарбонат натріюЗ NaHCO3 (2,2 г/л)
HEPESБез HEPES
Піруват натріюБез пірувату натрію
Феноловий червонийЗ феноловим червоним
Сольовий розчинЗбалансований сольовий розчин Ерла (EBSS)
pH7,0 – 7,6
Вміст ендотоксинівНе вказано
ЗберіганняВід +2 °C до +8 °C
Формула (склад на літр)
Компонент
Концентрація (мг/л)
Неорганічні солі
Хлорид кальцію · 2H2O265,00
Сульфат магнію97,72
Хлорид калію400,00
Хлорид натрію6 800,00
Дігідрофосфат натрію, безводний122,00
Бікарбонат натрію (NaHCO3)2 200,00
Амінокислоти
L-аргінін · HCl126,00
L-цистин · 2HCl31,30
L-Глутамін292,00
L-гістидин · HCl · H2O42,00
L-ізолейцин52,00
L-лейцин52,00
L-лізин · HCl72,50
L-метіонін15,00
L-фенілаланін32,00
L-треонін48,00
L-триптофан10,00
L-тирозин · 2Na · 2H2O51,90
L-валін46,00
Вітаміни
D-кальцій пантотенат1,00
Хлорид холіну1,00
Фолієва кислота1,00
міо-інозитол2,00
Нікотинамід1,00
Піридоксаль · HCl1,00
Рибофлавін0,10
Тіамін · HCl1,00
Інші компоненти
D(+)-глюкоза1 000,00
Феноловий червоний10,00
- це сучасне середовище для кріоконсервування, розроблене для забезпечення найвищого рівня життєздатності та функціональності клітин після розморожування. Це універсальне середовище підходить для широкого спектру типів клітин, включаючи клітини людини і тварин, що робить його незамінним інструментом для різноманітних наукових досліджень. Створене на основі ретельно збалансованої комбінації кріопротекторів та основних поживних речовин, середовище Freeze Medium CM-1 мінімізує утворення кристалів льоду та клітинний стрес під час процесу заморожування, зберігаючи таким чином клітинну цілісність.
Основні характеристики середовища Freeze Medium CM-1 включають
Широка сумісність: Ефективний для широкого спектру типів клітин, включаючи первинні клітини, стовбурові клітини та сформовані клітинні лінії.
Висока життєздатність: Оптимізовано для максимального відновлення та життєздатності клітин після розморожування, що забезпечує надійні результати експериментів.
Готовність до використання: Зручно готуються і стерилізуються для негайного застосування, скорочуючи час підготовки і ризик забруднення.
Підвищена стабільність: Підтримує стабільні характеристики за стандартних умов кріоконсервування, забезпечуючи відтворюваність результатів.
Тривалий термін зберігання: CM-1
- це готовий до використання сироватковий розчин для кріоконсервування, який можна зберігати в холодильнику до одного року.
Використання CM-1 для заморожування клітин
Щоб використовувати CM-1 для заморожування як адгезійних, так і суспензійних клітин, виконайте такі дії
Для адгезивних клітин промийте і відокремте їх від культурального субстрату. Для суспендованих клітин перейдіть до наступного кроку.
Підрахуйте клітини, щоб переконатися, що вони мають належну концентрацію.
Відцентрифугуйте клітини, щоб осадити їх, а потім ресуспендуйте в заморожувальному середовищі CM-1.
Перенесіть ресуспендовані клітини в кріопробірки.
Використовуйте метод повільного заморожування перед перенесенням клітин на довгострокове зберігання
Метод
Опис
Етапи
❄️
Ручне заморожування
Поетапний метод, що передбачає поступове зниження температури для забезпечення життєздатності клітин
1️⃣ Помістіть клітини в середовище для заморожування в морозильну камеру при 4°C на 40 хвилин.
2️⃣ Перенесіть в морозильну камеру при -80°C на 24 години.
3️⃣ Зберігайте клітини в рідкому азоті для тривалого збереження
❄️
Використання містера Фрості
Зручний пристрій, який дозволяє контролювати швидкість заморожування без використання електроенергії
1️⃣ Підготуйте клітини в кріопробірках із заморожувальним середовищем.
2️⃣ Помістіть кріовіали в контейнер Mr. Frosty.
3️⃣ Зберігайте при -80°C протягом 24 годин перед перенесенням у рідкий азот
❄️
Морозильник з контрольованою температурою
Високоточний морозильник Thermo Fisher або інших виробників, призначений для контрольованого зниження температури
1️⃣ Запрограмуйте пристрій на поступове зниження температури.
2️⃣ Помістіть підготовлені клітини в морозильну камеру.
3️⃣ Після циклу заморожування перенесіть клітини в рідкий азот
Зберігайте кріовіали при температурі нижче -130°C або в рідкому азоті для тривалого збереження.
Склад
Містить FBS, ДМСО, глюкозу, солі
Буферна ємність: pH = 7,2-7,6
Середовище CM-1 від Cytion пропонує надійне рішення для кріоконсервування, що забезпечує високу життєздатність клітин та їх функціональність після розморожування для широкого спектру дослідницьких завдань.
Середовище Ham's F-12K (Kaighn's) ретельно розроблене для оптимізації умов культивування клітин. Воно має збагачений склад, що забезпечує підвищений рівень основних компонентів, таких як амінокислоти та піруват натрію, а також додаткові елементи, включаючи путресцин, тимідин, гіпоксантин та цинк. Ці добавки дозволяють дослідникам доповнювати середовище мінімальною кількістю сироватки або визначеними компонентами для конкретних типів клітин, що сприяє створенню точних експериментальних умов.
Зокрема, середовище Ham's F-12K (Kaighn's) не містить білків або факторів росту. Отже, часто необхідним є додавання факторів росту та фетальної сироватки великої рогатої худоби (FBS), що дозволяє дослідникам адаптувати середовище до вимог конкретних клітинних ліній. Для досягнення оптимальної продуктивності концентрація FBS повинна бути ретельно оптимізована для кожної клітинної лінії, забезпечуючи оптимальний ріст і функціональність.
Для підтримання фізіологічного рівня рН у середовищі Ham's F-12K (Kaighn's) використовується буферна система бікарбонату натрію (2,5 г/л), що вимагає контрольованого 5-10% CO2 середовища під час культивування. Це гарантує, що рН середовища залишається в ідеальному діапазоні для росту та життєздатності клітин
Контроль якості
pH = 7,2 +/
- 0,02 при 20-25°C.
Кожна партія була перевірена на стерильність і відсутність мікоплазми та бактерій.
Зберігання
Зберігати в холодильнику при температурі від +2°C до +8°C у темряві. Заморожування, а також нагрівання до +37°C мінімізує якість продукту.
Не нагрівайте середовище до температури понад 37°C і не використовуйте неконтрольовані джерела тепла (наприклад, мікрохвильові печі).
Якщо потрібно використати лише частину засобу, витягніть цю кількість з пляшки і підігрійте її при кімнатній температурі.
Термін придатності будь-якого середовища, окрім основного, становить 8 тижнів з дати виготовлення.
Склад
Компоненти
мг/л
Неорганічні солі
Хлорид кальцію x 2H2O
135,24
Купрум(ІІ) сульфат x 5H2O
0,00
Заліза (II) сульфат x 7H2O
0,83
Магнію хлорид x 6H2O
105,72
Магній сульфат x 7H2O
394,49
Калій хлористий
283,29
Калій дигідрофосфат
58,52
Натрій хлористий
7597,20
натрію дигідрофосфатбезводний
115,02
Цинк сульфат x 7H2O
0,14
Інші компоненти
D(+)-глюкоза безводна
1260,00
Гіпоксантин
4,08
DL-α-ліпоєва кислота
0,21
Феноловий червоний
3,00
Путресцин x 2HCl
0,32
Піруват натрію
220,00
NaHCO3
2500,00
Тимідин
0,73
Амінокислоти
L-аланін
17,82
L-аргінін x HCl
421,40
L-аспарагін x H2O
30,02
L-аспарагінова кислота
26,62
L-цистеїн x HCl x H2O
70,24
L-глютамин
292,20
L-глутамінова кислота
29,42
Гліцин
15,01
L-гістидин x HCl x H2O
41,92
L-ізолейцин
7,87
L-лейцин
26,24
L-лізин x HCl
73,04
L-метіонін
8,95
L-фенілаланін
9,91
L-пролін
69,06
L-серин
21,02
L-треонін
23,82
L-триптофан
4,08
L-тирозин
10,87
L-валін
23,42
Вітаміни
D(+)-біотин
0,07
D-Кальцію пантотенат
0,48
Холіну хлорид
13,96
Фолієва кислота
1,32
міо-інозитол
18,02
Нікотинамід
0,04
Піридоксин x HCl
0,06
Рибофлавін
0,04
Тіамін x HCl
0,34
Вітамін В12
1,36
Фосфатно-буферний розчин (PBS)
- це буферний розчин, який широко використовується в біологічних і хімічних дослідженнях. Він відіграє важливу роль у підтримці балансу рН та осмолярності під час різних експериментальних процедур, включаючи обробку тканин та культивування клітин. Наш буферний розчин PBS ретельно розроблений з використанням високочистих інгредієнтів для забезпечення стабільності та надійності в кожному експерименті. Осмолярність та концентрація іонів нашого PBS наближені до людського організму, що робить його ізотонічним та нетоксичним для більшості клітин.
Склад нашого розчину PBS
Наш розчин PBS
- це відрегульована за рівнем рН суміш фосфатних буферів надвисокої чистоти та фізіологічних розчинів. У 1-кратній робочій концентрації він містить
8000 мг/л хлориду натрію (NaCl)
200 мг/л хлориду калію (KCl)
1150 мг/л фосфат натрію двоосновний безводний (Na2HPO4)
200 мг/л фосфат калію одноосновний безводний (KH2PO4)
Цей склад забезпечує оптимальний рН та іонний баланс, що підходить для широкого спектру біологічних застосувань.
Застосування нашого розчину PBS
Наш розчин PBS ідеально підходить для різних застосувань у біологічних дослідженнях. Його ізотонічні та нетоксичні властивості роблять його придатним для розведення речовин і промивання клітинних контейнерів. Розчини PBS, що містять ЕДТА, ефективні для видалення прикріплених і злиплих клітин. Однак не слід додавати до PBS двовалентні метали, такі як цинк, оскільки це може призвести до випадання осаду. У таких випадках рекомендується використовувати буфери Good's. Крім того, наш розчин PBS є прийнятною альтернативою вірусному транспортному середовищу для транспортування та зберігання РНК-вірусів, включаючи SARS-CoV-2.
Контроль якості
Стерильно відфільтрований
Зберігання та термін придатності
Зберігати при температурі від +2°C до +25°C, в захищеному від світла місці.
Після відкриття зберігати при температурі від 2°C до 25°C і використати протягом 24 місяців.
Умови транспортування
Температура навколишнього середовища
Обслуговування
Зберігати в холодильнику при температурі від +2°C до +8°C у темряві. Уникайте заморожування та частого нагрівання до +37°C, оскільки це знижує якість продукту.
Не нагрівайте середовище вище 37°C і не використовуйте неконтрольовані джерела тепла, такі як мікрохвильові печі.
Якщо потрібно використати лише частину засобу, відберіть необхідну кількість і підігрійте його до кімнатної температури перед застосуванням.
Склад
Категорія
Компоненти
Концентрація (мг/л)
Солі
Калій хлористий
200
Калій фосфат одноосновний безводний
200
Натрій хлористий
8000
Натрій фосфат двоосновний безводний
1150
- це універсальне середовище для культивування клітин, яке широко використовується в біологічних дослідженнях для культивування різних клітин ссавців. Розроблене Джорджем Е. Муром, Робертом Е. Гернером та Х. Еддісоном Франкліном у 1966 році у відомому онкологічному центрі Розуелл-Парк, це середовище отримало свою назву завдяки тому, що його було створено в Меморіальному інституті Розуелл-Парк (RPMI).
Спочатку розроблене для підтримки росту лейкемічних клітин людини як у суспензійних, так і в моношарових культурах, середовище RPMI 1640 еволюціонувало завдяки модифікаціям дослідників і комерційних постачальників і стало придатним для широкого спектру клітин ссавців. Воно винятково сумісне з такими клітинними лініями, як HeLa, Jurkat, MCF-7, PC12, PBMC, астроцитами та карциномами.
Середовище RPMI 1640 відрізняється від інших середовищ для культивування клітин завдяки своєму унікальному складу. Воно містить значну кількість фосфатів, амінокислот та вітамінів. Зокрема, до його складу входять біотин, вітамін В12 і ПАБК, які відсутні в мінімально необхідному середовищі Eagle або модифікованому середовищі Dulbecco. Крім того, середовище RPMI 1640 містить значно підвищену концентрацію вітамінів інозитолу та холіну. Однак воно не містить білків, ліпідів або факторів росту. Тому для забезпечення оптимальних умов для росту клітин зазвичай необхідне додавання 10% фетальної сироватки великої рогатої худоби (FBS).
Буферна система середовища RPMI 1640 заснована на бікарбонаті натрію і потребує 5-10% CO2 для підтримання фізіологічного рівня рН. Включення відновника глутатіону ще більше відрізняє це середовище від інших.
Контроль якості
Стерильно відфільтроване
Зберігання та термін придатності
Зберігати при температурі від +2°C до +8°C, в захищеному від світла місці.
Після відкриття зберігати при 4°C і використати протягом 6-8 тижнів.
Умови транспортування
Температура навколишнього середовища
Обслуговування
Зберігати в холодильнику при температурі від +2°C до +8°C у темряві. Уникайте заморожування та частого нагрівання до +37°C, оскільки це знижує якість продукту.
Не нагрівайте середовище вище 37°C і не використовуйте неконтрольовані джерела тепла, такі як мікрохвильові печі.
Якщо потрібно використати лише частину засобу, відберіть необхідну кількість і підігрійте його до кімнатної температури перед застосуванням.
Склад
Категорія
Компоненти
Концентрація (мг/л)
Амінокислоти
Гліцин
10.00
L-аланіл-L-глутамін
434.40
L-аргінін
200.00
L-аспарагін H2O
56.82
L-аспарагінова кислота
20.00
L-цистин 2HCl
65.20
L-глутамінова кислота
20.00
L-гістидин HCl H2O
20.27
L-гідрокси-L-пролін
20.00
L-ізолейцин
50.00
L-лейцин
50.00
L-лізин HCl
40.00
L-метіонін
15.00
L-фенілаланін
15.00
L-пролін
20.00
L-серин
30.00
L-треонін
20.00
L-триптофан
5.00
L-тирозин 2Na 2H2O
28.83
L-валін
20.00
Вітаміни
p-Амінобензойна кислота
1.00
D-біотин
0.20
Холіну хлорид
3.00
D-Кальцію пантотенат
0.25
Фолієва кислота
1.00
міо-інозитол
35.00
Нікотинамід
1.00
Піридоксин HCl
1.00
Рибофлавін
0.20
Тіамін HCl
1.00
Вітамін B12
0.005
Неорганічні солі
Ca(NO3)2 4H2O
100.00
KCl
400.00
MgSO4 7H2O
100.00
NaCl
6000.00
NaHCO3
2000.00
Na2HPO4
800.00
Інші компоненти
D-глюкоза
2000.00
L-глутатіон відновлений
1.00
Фенол червоний натрієва сіль
5.30
Ця унікальна формула поєднує модифіковане середовище Дульбекко (DMEM) та Ham's F-12 (поживна суміш Ham's F-12) у точному співвідношенні 1:1. Додавання L-глутаміну ще більше покращує її склад.
DMEM, похідна від мінімального есенціального середовища Ігл (EMEM), має підвищену концентрацію амінокислот та вітамінів порівняно зі своїм попередником. Натомість Ham's F-12 базується на середовищі Ham's F-10, забезпечуючи доповнюючий набір необхідних компонентів.
Для забезпечення оптимального росту клітин зазвичай DMEM:Ham's F12 доповнюють FBS у типовій концентрації 5–10%. Це додавання є необхідним, оскільки у середовищі відсутні гормони росту, ліпіди та білки, що мають вирішальне значення для розвитку клітин.
DMEM:Ham's F12 містить буферну систему для регулювання рН і часто доповнюється феноловим червоним, індикатором рН. Культивовані клітини в DMEM:Ham's F12 або будь-якому середовищі, що використовує бікарбонатну буферну систему, потребують контрольованого середовища з вмістом CO2 5–10% для підтримання відповідного рівня рН.
Контроль якості
Стерильно фільтрований
Зберігання та термін придатності
Зберігати при температурі від +2 °C до +8 °C, захищаючи від світла.
Після відкриття зберігати при температурі 4 °C і використати протягом 6–8 тижнів.
Умови транспортування
Температура навколишнього середовища
Зберігання
Зберігати в холодильнику при температурі від +2 °C до +8 °C у темному місці. Уникати заморожування та частого нагрівання до +37 °C, оскільки це знижує якість продукту.
Не нагрівайте середовище вище 37°C та не використовуйте неконтрольовані джерела тепла, такі як мікрохвильові печі.
Якщо планується використання лише частини середовища, відберіть необхідну кількість та нагрійте її до кімнатної температури перед використанням.
Склад
Категорія
Компоненти
Концентрація (мг/л)
Амінокислоти
Гліцин
18,75
L-аланін
4,45
L-аргінін HCl
147,50
L-аспарагін H₂O
7,50
L-аспарагінова кислота
6,65
L-цистеїн HCl H₂O
17,56
L-цистин 2 HCl
31,29
L-глутамінова кислота
7,35
L-глутамін
365,00
L-гістидин HCl H₂O
31,48
L-ізолейцин
54,47
L-лейцин
59,05
L-лізин HCl
91,25
L-метіонін
17,24
L-фенілаланін
35,48
L-пролін
17,25
L-серин
26,25
L-треонін
53,45
L-триптофан
9,02
L-тирозин 2 Na 2 H2O
55,79
L-валін
52,85
Вітаміни
D-біотин
0,0035
Хлорид холіну
8,98
D-пантотенат кальцію
2,24
Фолієва кислота
2,66
міо-інозитол
12,60
Нікотинамід
2,02
Піридоксин HCl
0,031
Піридоксаль HCl
2,00
Рибофлавін
0,219
Тіамін HCl
2,17
Вітамін В12
0,68
Неорганічні солі
CaCl₂·2H₂O
154,50
CuSO4 5 H2O
0,0013
Fe(NO3)3 9 H2O
0,05
FeSO4 7 H2O
0,417
KCl
311,80
MgCl2 6 H2O
61,20
MgSO4 7 H2O
100,00
NaCl
6996,00
NaHCO3
1200,00
Na₂HPO₄
71,02
NaH2PO4 2 H2O
70,87
ZnSO4 7 H2O
0,432
Інші компоненти
D-глюкоза
3151,00
Гіпоксантин
2,40
ГЕПЕС
3574,50
Лінолева кислота
0,042
Ліпоєва кислота
0,105
Феноловий червоний натрієвий
8,63
Путресцин 2 HCl
0,081
Піруват натрію
55,00
Тімідин
0,365
- 0,02 при 20-25 °C. Кожна партія була перевірена на стерильність та відсутність мікоплазм і бактерій. Зберігання Зберігати в холодильнику при температурі від +2 °C до +8 °C в темному місці. Заморожування та нагрівання до +37 °C погіршують якість продукту. Не нагрівайте середовище до температури вище 37°C і не використовуйте неконтрольовані джерела тепла (наприклад, мікрохвильові печі). Якщо потрібно використовувати лише частину середовища, вилийте цю кількість з пляшки і нагрійте її до кімнатної температури. Термін придатності будь-якого середовища, крім базового, становить 6–8 тижнів з дати відкриття. Склад Компоненти мг/л Неорганічні соліХлорид кальцію x 2H2O132,00 Сульфат магнію97,67 Хлорид калію400 Хлорид натрію6 460 Донатрій гідрофосфат (безводний)504,00 Інші компонентиD(+)-Глюкоза (безводна)3 000 Глутатіон (відновлений)0 М'ясний пептон600 Фенол червоний натрієва сіль11 АмінокислотиL-аланін13 L-аргінін x HCl42,14 L-аспарагін x H2O45,03 L-аспарагінова кислота19,97 L-цистеїн x HCl x H2O31,75 L-глутамін (стабільний)219,15 L-глутамінова кислота22 Гліцин7,5 L-гістидин x HCl x H2O20,96 L-гідроксипролін19,67 L-ізолейцин39,3 L-лейцин39,36 L-лізин x HCl36,54 L-метіонін14,92 L-фенілаланін16,52 L-пролін17,27 L-серин26,28 L-треонін17,87 L-триптофан3,06 L-тирозин динатрієва сіль26,10 L-валін17,57 Вітамінип-Амінобензойна кислота1,0 Аскорбінова кислота0,56 D(+)-Біотин0 D-кальцій пантотенат0,20 Холоїдний хлорид5 Фолієва кислота10 Міо-інозитол36 Нікотинамід0 Нікотинова кислота0 Піридоксаль HCl0,5 Піридоксин HCl0,5 Рибофлавін0 Тіамін HCl0 Вітамін B122,0
- це універсальне і широко використовуване середовище для культивування клітин, спеціально розроблене для вирощування первинних експлантів. Це комплексне середовище поєднує в собі основні вітаміни, амінокислоти та інші фактори, щоб забезпечити повністю визначене джерело поживних речовин для різних типів клітин. Воно особливо підходить для нетрансформованих клітин, що робить його безцінним інструментом для біологічних досліджень.
Середовище 199 має широкий спектр застосування в польових умовах. Він може ефективно підтримувати кумулюсно-ооцитарний комплекс (COC) і сприяти дозріванню ооцитів in vitro. Крім того, він використовується для промивання аспіраційних ліній під час збору яйцеклітин у корів німецької голштинської породи. Крім того, середовище 199 слугує чудовим середовищем для культивування клітин серцевого ендотелію, отриманих від щурів. Ці застосування демонструють універсальність і пристосованість середовища 199 до різних експериментальних потреб.
Історія
Розробка середовища 199 у 1950-х роках ознаменувала значний прогрес у створенні середовищ для культивування тканин. До його появи багато поживних середовищ ґрунтувалися на продуктах тваринного походження та екстрактах тканин. Однак Морган і його колеги зробили революцію в цій галузі, розробивши повністю визначене джерело поживних речовин для клітинних культур. Експериментуючи з різними комбінаціями вітамінів, амінокислот та інших факторів, вони виявили виняткові властивості середовища 199, що стимулюють ріст.
Контроль якості
pH = 7,2 +/
- 0,02 при 20-25°C.
Кожна партія була перевірена на стерильність і відсутність мікоплазми та бактерій.
Зберігання
Зберігати в холодильнику при температурі від +2°C до +8°C у темряві. Заморожування та нагрівання до +37°С мінімізує якість продукту.
Не нагрівайте середовище до температури понад 37°С і не використовуйте неконтрольовані джерела тепла (наприклад, мікрохвильові печі).
Якщо потрібно використати лише частину засобу, витягніть цю кількість з пляшки і підігрійте її при кімнатній температурі.
Термін придатності будь-якого середовища, окрім базового, становить 8 тижнів з дати виготовлення.
Склад
Компоненти
мг/л
Неорганічні солі
Хлорид кальцію x 2H2O
264,92
Заліза (ІІІ) нітрат x 9H2O
0,72
Сульфат магнію
97,67
Калій хлористий
400,00
Ацетат натрію x 3H2O
82,95
Натрію хлорид
6,800.00
Натрій дигідрофосфат x H2O
140,00
Інші компоненти
Аденін сульфат
10,00
АМФ
0,20
АТФ
1,00
Холестерин
0,20
2'-Дезоксирибоза
0,50
D(+)-Глюкоза безводна
1,000.00
Глутатіон (червоний)
0,05
Гуанін x HCl
0,30
Гіпоксантин
0,30
Феноловий червоний
10,00
D-рибоза
0,50
Тимін
0,30
Твін 80
4,90
Урацил
0,30
Ксантин
0,30
NaHCO3
2,200.00
Амінокислоти
L-аланін
25,00
L-аргінін x HCl
70,00
L-аспарагінова кислота
30,00
L-цистеїн x HCl x H2O
0,10
L-цистин
20,00
L-глютамин стабільний
149,00
L-глутамінова кислота
67,00
Гліцин
50,00
L-гістидин x HCl x H2O
21,88
L-гідроксипролін
10,00
L-ізолейцин
20,00
L-лейцин
60,00
L-лізин x HCl
70,00
L-метіонін
15,00
L-фенілаланін
25,00
L-пролін
40,00
L-серин
25,00
L-треонін
30,00
L-триптофан
10,00
L-тирозин
40,00
L-валін
25,00
Вітаміни
4-Амінобензойна кислота
0,05
Аскорбінова кислота
0,05
D(+)-біотин
0,01
Кальциферол
0,10
D-Кальцію пантотенат
0,01
Холіну хлорид
0,50
Фолієва кислота
0,01
міо-інозитол
0,05
Менадіон
0,01
Нікотинова кислота
0.025
Нікотинамід
0.025
Піридоксаль x HCl
0.025
Піридоксол x HCl
0.025
Рибофлавін
0,01
DL-α-токоферолу фосфат натрієва сіль
0,01
Тіамін x HCl
0,01
Вітамін А ацетат
0,14
- це складне і збагачене живильне середовище для культури клітин. IMDM є модифікацією DMEM, що містить селен і має додаткові амінокислоти, вітаміни та неорганічні солі порівняно з DMEM. У ньому не вистачає заліза, тому його потрібно доповнювати фетальною сироваткою великої рогатої худоби (FBS). IMDM використовує буферну систему бікарбонату натрію і потребує 5-10% CO2 для підтримання фізіологічного рівня pH.
IMDM добре підходить для культур клітин високої щільності, що швидко проліферують, включаючи Jurkat, COS-7 і клітини макрофагів. Різні модифікації IMDM, доступні для різних застосувань клітинних культур, можна знайти за допомогою інструменту вибору середовища. Рідкі середовища забезпечують необхідні поживні речовини для всіх видів клітинних культур. Кожне з наших високоякісних середовищ для культивування клітин виготовляється відповідно до початково опублікованої формули або модифікацій, необхідних для забезпечення стабільних характеристик і стабільності середовища.
IMDM проти DMEM
IMDM містить нітрат калію замість нітрату заліза, а також HEPES і піруват натрію. Додаткові компоненти в IMDM роблять його більш придатним для спеціалізованих типів клітин і конкретних застосувань, ніж DMEM.
IMDM проти RPMI
IMDM і RPMI мають різні склади, які можуть бути важливими для стимуляції ПМА/іономіцином. Однією з суттєвих відмінностей є концентрація Ca2+. У той час як RPMI містить 0,42 мМ Ca2+, IMDM містить 1,49 мМ.
Контроль якості
pH = 7,2 +/
- 0,02 при 20-25°C.
Кожна партія була перевірена на стерильність і відсутність мікоплазми та бактерій.
Зберігання
Зберігати в холодильнику при температурі від +2°C до +8°C у темряві. Заморожування та нагрівання до +37°С мінімізує якість продукту.
Не нагрівайте середовище до температури понад 37°С і не використовуйте неконтрольовані джерела тепла (наприклад, мікрохвильові печі).
Якщо потрібно використати лише частину засобу, витягніть цю кількість з пляшки і підігрійте її при кімнатній температурі.
Термін придатності будь-якого середовища, окрім основного, становить 8 тижнів з дати виготовлення.
Склад
Компоненти
мг/л
Неорганічні солі
Хлорид кальцію x 2 H2O
219,00
Калій хлористий
330,00
Нітрат калію
0.076
Магній сульфат безводний
97,73
Натрій хлористий
4,505.00
Натрій дигідрофосфат безводний
109,00
Натрій селеніт
0,02
Інші компоненти
D(+)-глюкоза безводна
4,500.00
HEPES
5,958.00
Піруват натрію
110,00
Феноловий червоний
15,00
Амінокислоти
L-аланін
25,00
L-аргінін x HCl
84,00
L-аспарагін x H2O
25,00
L-аспарагінова кислота
30,00
L-цистин x 2HCl
91,24
L-глютамин
584,00
L-глутамінова кислота
75,00
Гліцин
30,00
L-гістидин x HCl x H2O
42,00
L-ізолейцин
104,80
L-лейцин
104,80
L-лізин x HCl
146,20
L-метіонін
30,00
L-фенілаланін
66,00
L-пролін
40,00
L-серин
42,00
L-треонін
95,20
L-триптофан
16,00
L-тирозин x 2Na
104,20
L-валін
93,60
Вітаміни
D(+)-біотин
0.013
D-Кальцію пантотенат
4,00
Холіну хлорид
4,00
Фолієва кислота
4,00
міо-інозитол
7,20
Поживні середовища для культивування клітин: Огляд
У галузі медико-біологічних наук однією з найважливіших методологій є культура клітин. Вилучення клітин, тканин або органів у тварин або рослин і подальша імплантація цих клітин, тканин або органів у штучне середовище, сприятливе для їхнього виживання та/або росту, - це те, що мається на увазі під словосполученням "культура клітин" Фундаментальними умовами для оптимального розвитку клітин є контрольована температура, субстрат для прикріплення клітин, відповідне живильне середовище та інкубатор, який підтримує оптимальний рівень рН та осмоляльність. Клітини повинні мати ці умови для того, щоб повністю розкрити свій потенціал.
Вибір адекватного живильного середовища для культивування in vitro є найважливішим і водночас життєво важливим етапом у процесі культивування клітин. Поживне середовище, також відоме як культуральне середовище, - це рідина або гель, створений для стимулювання розвитку організмів у мікроскопічному, клітинному або рослинному масштабі. Середовище, що використовується для культивування клітин, часто містить достатню кількість енергії та речовин, які контролюють клітинний цикл. Основними компонентами живильного середовища є амінокислоти, вітаміни, неорганічні солі, глюкоза і сироватка. Сироватку додають до середовища, оскільки вона є джерелом факторів росту, гормонів і факторів прикріплення. Крім забезпечення поживними речовинами, середовище також сприяє підтримці рівня рН та осмоляльності.
Типи середовищ, що використовуються в культурі клітин
Клітини людини і тварин можна вирощувати як у штучному або синтетичному середовищі, так і в повністю природному середовищі, доповненому природними елементами. Нижче ми надамо вам огляд різних доступних на сьогодні типів середовищ.
Природні середовища
У природних середовищах можна знайти лише біологічні рідини, які існують у своєму природному стані. Природні середовища дуже зручні та прості для культивування широкого спектру типів клітин тварин. Недостатнє розуміння точних компонентів, що входять до складу природних середовищ, є основним фактором, що зумовлює низьку повторюваність результатів, отриманих з використанням природних середовищ.
Штучні середовища
Приготування штучних або синтетичних середовищ передбачає додавання поживних речовин (як органічних, так і неорганічних), сироваткових білків, вуглеводів, кофакторів, вітамінів і солей, а також газових фаз O2 і CO2 [1].
Різні типи штучних поживних середовищ були розроблені для виконання однієї або декількох з наступних функцій: 1) Негайне виживання (збалансований розчин солі з точним рН і осмотичним тиском). 2) Тривале виживання (збалансований сольовий розчин, доповнений різними складами органічних хімічних речовин та/або сироваткою). 3) Невизначений розвиток. 4) Спеціалізовані функції.
Існує чотири різні класифікації штучних поживних середовищ:
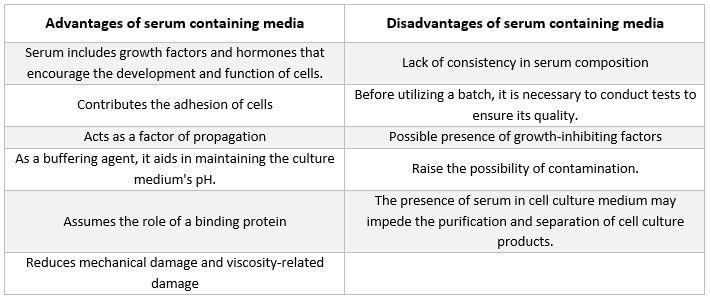
Поживні середовища, що містять сироватку
Найпоширенішою добавкою, яку можна знайти в середовищах для вирощування тваринних клітин, є фетальна сироватка великої рогатої худоби. Її додають до живильного середовища як недорогу добавку для досягнення найкращих умов росту. Крім того, що сироватка діє як транспортер або хелатор для нестабільних або нерозчинних у воді поживних речовин, гормонів і факторів росту, інгібіторів протеаз та інших речовин, вона також зв'язує і нейтралізує шкідливі молекули.
Безсироваткове середовище
Присутність сироватки в середовищі має ряд недоліків і може призвести до серйозних помилок в інтерпретації результатів імунологічних досліджень [2, 3]. Було створено безліч різних безсироваткових середовищ [4, 5]. Ці середовища, як правило, спеціально розроблені для підтримки культури одного типу клітин, наприклад, Knockout Serum Replacement і Knockout DMEM від Thermo Fisher Scientific, а також середовище mTESR від Stem Cell Technologies [6] для стовбурових клітин [7].
Крім того, ці середовища містять певну кількість очищених факторів росту, ліпопротеїнів та інших білків, які зазвичай містяться в сироватці крові [8]. Ці середовища часто називають "визначеними культуральними середовищами", оскільки компоненти, що входять до їх складу, добре вивчені.
Хімічно визначені середовища
До складу цих середовищ входять надчисті неорганічні та органічні компоненти, які не зазнали жодного забруднення. Вони також можуть включати чисті білкові добавки, такі як фактори росту.
генетична модифікація бактерій або дріжджів разом із додаванням певних жирних кислот, вітамінів, холестерину та амінокислот призводить до виробництва їхніх складових частин [9].
Безбілкові середовища
Безбілкові середовища - це середовища, які взагалі не містять білка, а натомість містять лише небілкові елементи. Порівняно з середовищами з додаванням сироватки, використання середовищ без білка сприяє більшій проліферації клітин та експресії білка, а також полегшує очищення будь-якого продукту, що утворюється в подальшому процесі [10-12]. Білок не входить до складу таких середовищ, як MEM і RPMI-1640. Однак, за необхідності, білкова добавка може бути додана.
Поживне середовище та його основні компоненти
Комерційні живильні середовища можна придбати у вигляді порошку або рідини, і вони часто містять різноманітні поживні речовини, такі як амінокислоти, глюкоза, солі, вітаміни та інші харчові добавки.
Потреби в цих компонентах відрізняються для кожної клітинної лінії, і ці відмінності зумовлюють велику кількість різних рецептур середовищ. Кожен компонент відповідає за певну функцію, яка буде описана в наступних параграфах:
Буферні системи
Для підтримання оптимальних умов росту необхідно контролювати рН, що часто здійснюється за допомогою однієї з двох буферних систем:
Природна буферна система
Співвідношення CO2/H2CO3 в атмосфері дорівнює співвідношенню в середовищі, створюючи природний буферний механізм. Для того, щоб зберегти природний буферний механізм, культури повинні утримуватися в повітряному середовищі з 5-10% CO2, що часто досягається за допомогою CO2-інкубатора. Однією з найкращих переваг використання природного буферу є його дешевизна та безпечність.
HEPES
Хімічна буферизація з використанням цвіттер-іонів HEPES має більшу буферну здатність в діапазоні рН 7,2-7,4 і не потребує регульованого газового середовища. Для певних типів клітин більша доза HEPES може бути шкідливою. Середовища, що містять HEPES, також набагато чутливіші до фототоксичної дії флуоресцентного світла [13].
Феноловий червоний
Індикатор рН феноловий червоний часто входить до складу комерційних поживних середовищ, що дозволяє здійснювати безперервний моніторинг рН. Метаболіти, що виробляються цими клітинами, розширюючи клітини, викликають зміну рН і, відповідно, зміну кольору середовища. Феноловий червоний має подвійний вплив на колір середовища, роблячи його жовтим при кислому рН і фіолетовим при лужному рН. рН 7,4, оптимальне значення для культури клітин, призводить до того, що середовище виглядає флуоресцентно-червоним.
Але феноловий червоний має кілька недоліків: По-перше, феноловий червоний здатний імітувати дію ряду стероїдних гормонів, в першу чергу естрогенів [14]. Тому при дослідженні чутливих до естрогенів клітин, таких як тканина молочної залози, рекомендується використовувати середовище, вільне від фенолового червоного. Натрієво-калієвий баланс порушується через присутність фенолового червоного в деяких безсироваткових середовищах. Додавання сироватки або гормону гіпофіза великої рогатої худоби до середовища може протидіяти цьому ефекту [15]. По-третє, присутність фенолового червоного перешкоджає виявленню в проточних цитометричних експериментах.
Неорганічні солі
Середовища, що містять неорганічні солі, такі як іони натрію, калію та кальцію, допомагають підтримувати осмотичну рівновагу і регулювати мембранний потенціал.
Амінокислоти
Оскільки амінокислоти є фундаментальними компонентами білка, вони є невід'ємним компонентом кожного середовища для росту клітин, яке коли-небудь було створено. Оскільки клітини не здатні виробляти певні амінокислоти самостійно, важливо, щоб живильне середовище містило незамінні амінокислоти. Вони необхідні для проліферації клітин, і концентрація, в якій вони присутні, визначає максимальну щільність клітин, якої можна досягти. Зокрема, L-глутамін, незамінна амінокислота, є особливо важливою.
L-глутамін функціонує як вторинне джерело енергії для метаболізму і постачає азот для виробництва NAD, NADPH і нуклеотидів. Через те, що L-глутамін є нестабільною амінокислотою, яка з часом переходить у форму, яку клітини не в змозі використовувати, він повинен надходити в середовище.
Крім того, в середовище можна додавати замінні амінокислоти, щоб поповнити ті, які були витрачені в процесі росту. Ріст клітин прискорюється, а їхня життєздатність підвищується, коли до поживного середовища додають замінні амінокислоти.
Вуглеводи
Вуглеводи у вигляді цукрів є основним джерелом енергії. Багато поживних середовищ містять мальтозу і фруктозу на додаток до більш поширених цукрів глюкози і галактози.
Білки та пептиди
Альбумін, трансферин і фібронектин є найбільш часто використовуваними білками і пептидами. Вони особливо важливі в середовищах, які не містять сироватки. Альбумін, трансферин, апротинін, фетуїн і фібронектин - це деякі з білків, які можна знайти в сироватці, яка є багатим джерелом білка.
Альбумін - це основний білок, що міститься в крові, і його функція полягає у зв'язуванні та транспортуванні різних речовин, включаючи воду, солі, вільні жирні кислоти, гормони та вітаміни, між різними органами та клітинами. Здатність альбуміну зв'язуватися з хімічними речовинами робить його ефективним кандидатом для видалення шкідливих сполук із середовища, в якому культивуються клітини.
Апротинін є захисним агентом у системах клітинних культур, оскільки він стабільний при нейтральному і кислому рН, а також стійкий до високих температур і руйнування, яке може бути спричинене протеолітичними ферментами. Він здатний інгібувати ряд серинових протеаз, зокрема трипсин.
Фетуїн - це глікопротеїн, який може бути виявлений у більшій кількості в сироватці крові плода та новонароджених тварин порівняно з сироваткою крові дорослих. Крім того, він діє як інгібітор серинової протеази. Білок фібронектин є важливим компонентом у процесі клітинної адгезії. Трансферин - білок, який транспортує залізо і відповідає за доставку заліза до мембран клітин.
Жирні кислоти та ліпіди
Відіграють вирішальну роль у безсироватковому середовищі, коли сироватка відсутня.
Вітаміни
Численні вітаміни необхідні для розвитку та проліферації клітин. Вітаміни не можуть вироблятися клітинами в достатній кількості, тому вони необхідні в культурі тканин як харчові добавки.
У культурі клітин сироватка є основним джерелом вітамінів, однак середовища також обробляють різними вітамінами, щоб зробити їх придатними для певного типу клітин. Найчастіше для стимуляції росту використовують вітаміни групи В.
Мікроелементи
Такі хімічні елементи, як мідь, цинк, селен і проміжні продукти трикарбонових кислот, відомі як мікроелементи. Мікроелементи часто додають до середовищ, які не містять сироватки, щоб замінити ті, які зазвичай присутні в сироватці. Ці елементи є важливими хімічними компонентами, необхідними для здорового розвитку клітин. Багато біохімічних реакцій залежать від певних мікроелементів, наприклад, активність ферментів.
Добавки до середовища
Повне живильне середовище, запропоноване для певних клітинних ліній, потребує додаткових компонентів, які відсутні у базовому середовищі та сироватці. Ці харчові добавки підтримують ріст клітин і відповідну метаболічну функцію.
Хоча гормони, фактори росту і сигнальні молекули необхідні для належної проліферації певних клітинних ліній, завжди слід дотримуватися наступних запобіжних заходів: Оскільки додавання добавок може змінити осмоляльність всього живильного середовища, що може пригнічувати розвиток клітин, завжди рекомендується перевіряти осмоляльність після додавання добавок. Для більшості клітинних ліній оптимальна осмоляльність знаходиться в діапазоні від 260 до 320 мОсм/кг.
Антибіотики
Антибіотики часто застосовують для пригнічення розвитку бактеріальних і грибкових забруднювачів [16], хоча вони не є необхідними для росту клітин. Оскільки антибіотики можуть приховувати забруднення мікоплазмою та резистентними бактеріями, їх рутинне використання для культури клітин не рекомендується [17, 18].
Крім того, антибіотики можуть порушувати метаболізм гіперчутливих клітин. Часто використовують комбінації пеніцилін-стрептоміцин, вироблені компаніями MilliporeSigma та Life Technologies. Плазмоцин був використаний у культурі клітинних ліній гліоми TS603, TS516 і BT260 [19], і було показано, що він ефективний у видаленні мікоплазмового забруднення [20].
Сироватка
Альбуміни, фактори росту та інгібітори росту присутні в сироватці крові. Сироватка є одним з найважливіших компонентів середовища для культивування клітин, оскільки вона містить амінокислоти, білки, вітаміни (особливо жиророзчинні вітаміни, такі як A, D, E і K), вуглеводи, ліпіди, гормони, фактори росту, мінерали та мікроелементи.
Сироватка з ембріональних і телячих джерел великої рогатої худоби часто використовується для сприяння розвитку культивованих клітин. Фетальна сироватка є багатим джерелом факторів росту і підходить для клонування клітин та розвитку чутливих клітин. Через знижену здатність стимулювати ріст телячу сироватку використовують в експериментах з контактним інгібуванням. Звичайні живильні середовища часто містять від 2% до 10% сироватки. Додавання сироватки до живильного середовища слугує наступним цілям [21]:
-
Сироватка забезпечує клітини необхідними поживними речовинами (як у розчиненому вигляді, так і у зв'язаному з білками стані).
-
Деякі фактори росту і гормони, що беруть участь у стимуляції росту і спеціалізованої клітинної активності, включені в сироватку.
-
Вона містить багато зв'язуючих білків, таких як альбумін і трансферин, які транспортують інші хімічні речовини в клітину. Наприклад, альбумін доставляє в клітини жири, вітаміни, гормони тощо.
-
Він також забезпечує білки, такі як фібронектин, які збільшують адгезію клітин до субстрату. Крім того, він виробляє елементи, які допомагають клітинам розростатися перед поділом.
-
Він містить інгібітори протеази, які запобігають протеолізу в клітинах.
-
Він також містить мінерали, такі як Na+, K+, Zn2+ та Fe2+.
-
Підвищує в'язкість середовища, захищаючи клітини від механічних пошкоджень під час перемішування суспензійної культури.
-
Також є буфером.
Список використаних джерел
[1] Morgan J, Morton H, Parker R. Живлення тваринних клітин у культурі тканин; початкові дослідження на синтетичному середовищі. Proc Soc Exp Biol Med. 1950;73:1-8
[2] Kerbel R, Blakeslee D. Швидка адсорбція компонента сироватки ембріонального теляти клітинами ссавців у культурі. Потенційне джерело артефактів у дослідженнях антисироваток до клітинно-специфічних антигенів. Імунологія. 1976;31:881-91
[3] Sula K, Draber P, Nouza K. Додавання сироватки до середовища для приготування клітинних суспензій як можливе джерело артефактів у клітинно-опосередкованих реакціях, що вивчаються за допомогою тесту підколінних лімфатичних вузлів. J Immunogenet. 1980;7:483-9
[4] Mariani E, Mariani A, Monaco M, Lalli E, Vitale M, Facchini A. Комерційні безсироваткові середовища: ріст гібридом та вироблення моноклональних антитіл. J Immunol Methods. 1991;145:175-83
[5] Барнс Д., Сато Г. Методи вирощування культивованих клітин у безсироватковому середовищі. Anal Biochem. 1980;102:255-70
[6] Yu H, Lu S, Gasior K, Singh D, Vazquez Sanchez S, Tapia Oта ін. HSP70 супроводжує без РНК TDP-43 в анізотропні внутрішньоядерні рідкі сферичні оболонки. Science. 2021;371:
[7] Meharena H, Marco A, Dileep V, Lockshin E, Akatsu G, Mullahoo Jта ін. Старіння, викликане синдромом Дауна, порушує ядерну архітектуру нейронних попередників. Клітинні стовбурові клітини. 2022;29:116-130.e7
[8] Iscove N, Melchers F. Повна заміна сироватки альбуміном, трансферином та соєвим ліпідом у культурах ліпополісахарид-реактивних В-лімфоцитів. J Exp Med. 1978;147:923-33
[9] Stoll T, Muhlethaler K, von Stockar U, Marison I. Систематичне вдосконалення хімічно визначеного безбілкового середовища для росту гібридом та виробництва моноклональних антитіл. J Biotechnol. 1996;45:111-23
[10] Дарфлер Ф. Безбілкове середовище для росту гібридом та інших клітин імунної системи. In Vitro Cell Dev Biol. 1990;26:769-78
[11] Barnes D, Sato G. Безсироваткові культури клітин: об'єднуючий підхід. Cell. 1980;22:649-55
[12] Hamilton W, Ham R. Клональний ріст клітинних ліній китайського хом'яка в безбілкових середовищах. In Vitro. 1977;13:537-47
[13] Zigler J, Lepe Zuniga J, Vistica B, Gery I. Аналіз цитотоксичних ефектів опроміненого світлом середовища, що містить HEPES. In Vitro Cell Dev Biol. 1985;21:282-7
[14] Berthois Y, Katzenellenbogen J, Katzenellenbogen B. Феноловий червоний у культуральних середовищах тканин є слабким естрогеном: наслідки для вивчення естроген-чутливих клітин у культурі. Proc Natl Acad Sci U.S.A. 1986;83:2496-500
[15] Карміол С. Розробка безсироваткових середовищ. In: Master JRW, редактор. Культура клітин тварин, 3-тє видання. Оксфорд: Видавництво Оксфордського університету; 2000.
[16] Перлман Д. Використання антибіотиків у поживних середовищах для культивування клітин. Methods Enzymol. 1979;58:110-6
[17] МакГерріті Г. Поширення та контроль мікоплазмової інфекції клітинних культур. In Vitro. 1976;12:643-8
[18] Мастерс Дж, Стейсі Г. Зміна середовища та пасажування клітинних ліній. Nat Protoc. 2007;2:2276-84
[19] Чакраборти А., Лаукка Т., Милликоскі М., Рінгель А., Букер М., Толсторуков М.та ін. Гістондеметилаза KDM6A безпосередньо відчуває кисень для контролю хроматину та долі клітин. Science. 2019;363:1217-1222
[20] Molla Kazemiha V, Azari S, Amanzadeh A, Bonakdar S, Shojaei Moghadam M, Habibi Anbouhi M та ін. Ефективність Плазмоцину™ на різних клітинних лініях ссавців, інфікованих молікутами, порівняно з загальновживаними антибіотиками в культурі клітин: локальний досвід. Цитотехнологія. 2011;63:609-20
[21] Краг Хансен У. Молекулярні аспекти зв'язування лігандів з сироватковим альбуміном. Pharmacol Rev. 1981;33:17-53