Bunková línia HCT116: Pilier vo výskume kolorektálneho karcinómu
Bunková línia HCT116 slúži ako základný kameň pri výskume kolorektálneho karcinómu a ponúka neoceniteľné poznatky o patogenéze tohto ochorenia a potenciálnych terapeutických možnostiach. HCT116 je známa svojou užitočnosťou vo výskume rakoviny a farmakologickom hodnotení, čo uľahčuje kľúčové štúdie správania sa nádoru a účinnosti liekov.
Pôvod a základné charakteristiky buniek HCT116
Pochopenie pôvodu a základných vlastností buniek HCT116, ako sú ich morfologické znaky, genetická výbava a bunkové rozmery, je pre výskumníkov, ktorí sa púšťajú do štúdií využívajúcich túto bunkovú líniu, nevyhnutné.
Pôvod a genetické prostredie: Bunky HCT116 pochádzajú z hrubého čreva 48-ročného muža bielej rasy s diagnózou kolorektálneho karcinómu a vyznačujú sa mutáciou v kodóne 13 (G13D) génu KRAS, ktorý je súčasťou signálnej dráhy RAS/RAF/MEK/ERK. Táto konkrétna mutácia je kľúčová pri onkogénnej transformácii týchto buniek, čo zdôrazňuje ich význam vo výskume rakoviny.
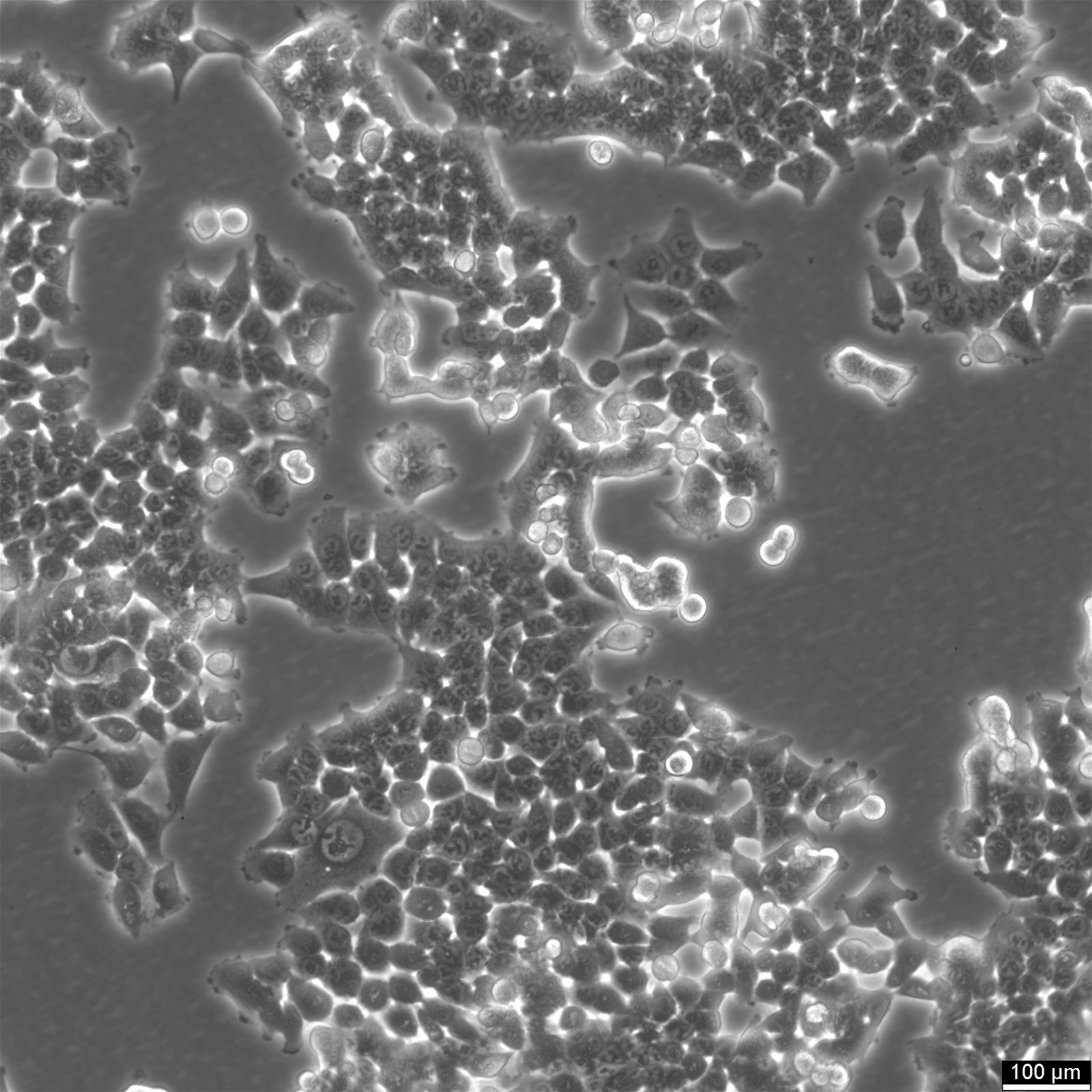
Morfológia a rastové charakteristiky: Bunky HCT116, ktoré majú morfológiu podobnú epitelu, zvyčajne rastú v jednovrstvových kultúrach, ale môžu vytvárať aj sféroidy s priemerom 150 - 400 µm. Táto prispôsobivosť rastových modelov zdôrazňuje ich všestrannosť v rôznych experimentálnych zostavách.
Chromozomálny profil: Chromozómové zloženie buniek HCT116 je takmer diploidné, pričom približne 70 % bunkovej populácie obsahuje 45 chromozómov. Pozoruhodné je, že v dlhých ramenách chromozómov 8, 10, 16 a 17 sa opakovane vyskytuje amplifikácia, zatiaľ čo chromozóm Y chýba, čo prispieva k ich jedinečnému genomickému podpisu.
Porovnávacia analýza: bunkové línie HCT116 vs. HT29
Pri porovnaní HCT116 s HT29, ďalšou bunkovou líniou ľudského kolorektálneho karcinómu, sa objavujú výrazné rozdiely v ich onkogénnom potenciáli a diferenciačných schopnostiach:
Onkogénna agresivita a diferenciácia: Bunky HCT116 sa vyznačujú vysokou onkogénnou agresivitou a obmedzeným diferenciačným potenciálom, čo z nich robí model na štúdium agresívnych nádorových fenotypov. Naproti tomu bunky HT29 vykazujú schopnosť diferencovať sa do línií podobných enterocytom a produkujúcich mucín, čím poskytujú kontrastný model, ktorý napodobňuje rôzne aspekty biológie kolorektálneho karcinómu.
Toto porovnávacie chápanie bunkových línií HCT116 a HT29 obohacuje súbor nástrojov, ktoré majú výskumníci k dispozícii, a umožňuje diferencovanejšie skúmanie mnohostrannej povahy kolorektálneho karcinómu.
Manipulácia s bunkami HCT116
|
Čas zdvojnásobenia: |
Čas zdvojenia rakovinových buniek HCT116 sa pohybuje od 25 do 35 hodín. |
|
Adherentné alebo v suspenzii: |
Bunková línia rakoviny hrubého čreva HCT116 je adherentná, bunky rastú v monovrstvách. |
|
Hustota výsevu: |
Pre bunkovú kultúru HCT116 sa odporúča hustota výsevu 2 x104 buniek/cm2. Na subkultiváciu by sa bunky mali oddeliť pomocou roztoku Accutase po premytí 1x PBS. Po odstredení sa bunkový pelet resuspenduje v čerstvom rastovom médiu a prenesie sa do novej banky. |
|
Rastové médium: |
Na kultiváciu buniek HCT116 je optimálne médium McCoys 5a doplnené 3,0 g/l L-glukózy, 1,5 mM L-glutamínu, 3,0 g/l NaHCO3 a 10 % fetálneho hovädzieho séra. Odporúča sa obnovovať médium 1 až 2 razy týždenne. |
|
Rastové podmienky (teplota,CO2): |
Kultivácia prebieha vo zvlhčenom inkubátore pri teplote 37 °C s atmosférou 5 %CO2. |
|
Skladovanie: |
Bunky HCT116 sa môžu skladovať pri teplote nižšej ako -150 °C v parnej alebo kvapalnej fáze tekutého dusíka. |
|
Proces zmrazovania a médium: |
Na kryokonzerváciu použite médium CM-1 alebo CM-ACF. Odporúča sa metóda mrazenia s riadenou rýchlosťou, ktorá umožňuje postupné znižovanie teploty o 1 °C za minútu, čo pomáha udržať životaschopnosť buniek. |
|
Proces rozmrazovania: |
Bunky HCT116 rozmrazujte vo vodnom kúpeli pri teplote 37 °C. Po pridaní rastového média odstreďte, aby ste odstránili zvyšky zmrazovacieho média. Resuspendujte bunkový pelet v čerstvom médiu a kultivujte v nových bankách. |
|
Úroveň biologickej bezpečnosti: |
Úroveň bezpečnosti: 1 |
Výhody bunkovej línie HCT116
Táto časť sa zaoberá bunkovou líniou HCT116, pričom zdôrazňuje jej kľúčovú úlohu vo výskume rakoviny, najmä v štúdiu kolorektálneho karcinómu, a rozoberá jej prirodzené výhody.
Bunková línia HCT116 vyniká vo výskume rakoviny vďaka niekoľkým kľúčovým výhodám:
Model kolorektálnej rakoviny: Slúži ako všeobecne uznávaný in vitro model kolorektálneho karcinómu, ktorý je celosvetovo tretím najčastejším nádorovým ochorením. Vďaka jej významu pre napodobňovanie ľudského kolorektálneho karcinómu je neoceniteľná pre pochopenie biológie rakoviny a testovanie terapeutických stratégií.
Homogenita: Pozoruhodné je, že približne 70 % buniek HCT116 vykazuje konzistentné genetické profily, čo predstavuje relatívne homogénnu populáciu. Táto homogenita je kľúčová pre štúdie zamerané na expresiu génov, bunkové signálne dráhy a hodnotenie účinnosti liečby liekmi, pretože zabezpečuje konzistenciu a spoľahlivosť experimentálnych výsledkov.
Účinnosť transfekcie: Jednou z charakteristických vlastností buniek HCT116 je ich vysoká schopnosť transfekcie, najmä pomocou vírusových vektorov. Táto vlastnosť je obzvlášť výhodná pri výskume génovej terapie, pretože umožňuje efektívne a presné zavedenie genetického materiálu, čím uľahčuje pokročilé genetické manipulácie a funkčné štúdie.
Pokračujte vo svojich objavoch s našou overenou bunkovou líniou HCT116
Výskumné využitie bunkovej línie HCT116
Bunková línia HCT116 má širokú škálu aplikácií vo výskume rakoviny. Niektoré významné aplikácie sú:
Biológia rakoviny
Bunková línia rakoviny hrubého čreva HCT116 sa používa na štúdium progresie a vývoja rakoviny hrubého čreva. Okrem toho pomáha objasniť základné mechanizmy a signálne dráhy, ktoré sa podieľajú na proliferácii, migrácii a invázii rakoviny. V štúdii sa bunky HCT116 použili na štúdium génov, ktoré sa podieľajú na vývoji rezistencie na lieky. Výskumníci nadmerne exprimovali gén MDR1 v bunkách rakoviny hrubého čreva a pozorovali expresiu izoforiem NOX (oxid NADPH) a Nrf2. Štúdia odhalila, že zvýšená regulácia NOX2 a Nrf2 spôsobuje chemorezistenciu rakovinových buniek; tieto gény teda môžu byť cielené na prekonanie rozvoja rezistencie počas liečby rakoviny [1]. Podobne výskum uskutočnený v roku 2021 uvádza, že signálna dráha NF-κB sa podieľa na regulácii proliferácie a migrácie rakoviny hrubého čreva. Možno ju teda zacieliť na vývoj nových a účinných terapeutík proti kolorektálnemu karcinómu [2].
V oblasti onkológie je pochopenie zložitých procesov bunkového cyklu, proliferácie a rastu a apoptózy zásadné. Tieto biologické funkcie sú kľúčové pri štúdiu ľudských bunkových línií, najmä tých, ktoré pochádzajú z malígnych buniek, ako sú bunky ľudského karcinómu hrubého čreva a modely karcinómu pankreasu. Napríklad bunkové línie HCT116 a SW620 sú dôležité pri skúmaní mechanizmov, ktoré sú základom rakoviny hrubého čreva a pankreasu. Prostredníctvom techník, ako je prietoková cytometria a klonogénne testy, môžu výskumníci objasniť profily génovej expresie a správanie nezávislých buniek v nádoroch, čo vrhá svetlo na to, ako rakovina komunikuje v extracelulárnej matrici.
Úloha apoptózy pri progresii rakoviny
Apoptóza alebo programovaná bunková smrť zohráva kľúčovú úlohu pri udržiavaní bunkovej homeostázy a je kľúčovou oblasťou štúdia vo výskume rakoviny. Zásadný význam má rozlišovanie medzi nepríbuznou apoptózou a apoptózou špecificky vyvolanou v kontexte rakoviny, napríklad bunkovou smrťou pri rakovine hrubého čreva. Tento proces nie je len o eliminácii buniek, ale zahŕňa komplexnú súhru signálov, ktoré môžu ovplyvniť rast nádoru a metastázovanie. Skúmaním apoptózy a bunkovej smrti v spojení so supresormi metastáz a aktivitou nádorových supresorov môžu vedci získať prehľad o cestách, ktoré regulujú progresiu rakoviny a metastatický potenciál.
Metastázy a molekulárne markery v rakovine
Metastázovanie zostáva jedným z najproblematickejších aspektov rakoviny, pričom hematogénne metastázy predstavujú významný problém pri šírení malígnych buniek. Skúmanie metastáz zahŕňa štúdium pohybových a invazívnych schopností rakovinových buniek alebo bunkovej lokomócie a spôsobu interakcie buniek s ich okolím vrátane extracelulárnej matrice. Molekulárne markery, ako je expresia CD133 a receptor epidermálneho rastového faktora, sú rozhodujúce pri identifikácii a pochopení správania pozitívnych buniek karcinómu hrubého čreva a iných typov rakoviny. Napríklad dráha SIRT6 sa stala oblasťou záujmu vzhľadom na jej potenciálnu úlohu pri modulácii rastu nádoru a metastázovania rakoviny hrubého čreva.
Toxikológia/vývoj liekov
Bunková línia HCT116 sa používa ako model na skríning nových liekov proti rakovine. Vykonalo sa niekoľko štúdií na posúdenie účinnosti a toxicity protinádorových liekov vrátane prírodných produktov a chemicky syntetizovaných nanočastíc. V rámci výskumu sa tak hodnotila cytotoxicita syntetizovaných nanočastíc striebra z výťažkov rastlinnej drogy Caesalpinia pulcherrima v bunkách HCT116 [3]. V štúdii vedci použili rakovinovú bunkovú líniu HCT116 na hodnotenie protinádorového potenciálu vodného extraktu kakaového čaju. Zistili, že extrakt z kakaového čaju znižuje proliferáciu rakoviny hrubého čreva a indukuje bunkovú smrť [4]. V ďalšej štúdii použili rakovinové bunky HCT116 a zistili, že extrakty zozemiaka vzdušného , Dioscorea bulbifera, vykazujú proapoptotickú aktivitu v bunkách kolorektálneho karcinómu prostredníctvom aktivácie signálnej kaskády JNK a potlačenia génu ERK1/2 [5].
Účinky metformínu na rakovinové bunky, najmä v kontexte rakoviny hrubého čreva a pankreasu, sú príkladom toho, ako môže pochopenie biologických funkcií rakovinových buniek viesť k potenciálnym terapeutickým stratégiám. Výskum klonogénneho prežívania alebo schopnosti vytvárať klony rakovinových buniek pri liečbe látkami, ako je metformín, alebo pri cielení na špecifické dráhy, ako je receptor epidermálneho rastového faktora, môže poskytnúť cenné poznatky o účinnej liečbe rakoviny. Okrem toho použitie klonov HCT116 a populácií buniek HCT116 v týchto štúdiách umožňuje lepšie pochopiť, ako rakovinové bunky reagujú na rôzne terapeutické zásahy, čo otvára cestu k personalizovanejším prístupom k liečbe rakoviny.
Bunky HCT116: Výskumné publikácie
V tejto časti sa preberá niekoľko významných a najcitovanejších nedávnych publikácií, v ktorých sa uvádza bunková línia HCT116.
Táto štúdia bola uverejnená v časopise Journal of Photochemistry and Photobiology B: Biology (2017). Výskumníci použili bunkové línie rakoviny hrubého čreva HCT116 a rakoviny pľúc A549 na vyhodnotenie cytotoxických účinkov syntetizovaných nanočastíc oxidu cíničitého zo semien piper nigrum.
Tento výskum v časopise Cancer Letters (2018) navrhuje, že lncRNA SNHG15 podporuje migráciu buniek rakoviny hrubého čreva v bunkových líniách rakoviny hrubého čreva vrátane HCT116.
Nadmerná expresia dlhej nekódujúcej RNA TUG1 podporuje progresiu rakoviny hrubého čreva
Tento článok bol uverejnený v časopise Medical Science Monitor v roku 2016. V štúdii sa zistilo, že onkogénna LncRNA TUG1 podporuje proliferáciu a migráciu buniek rakoviny hrubého čreva HCT116.
Tento výskum v časopise Biochemical Pharmacology (2018) navrhuje, že rozvoj liekovej rezistencie zvyšuje hladiny enzýmov produkujúcich H2S v bunkách rakoviny hrubého čreva HCT116.
V tejto výskumnej práci v časopise International Journal of Environmental Health Research (2023) sa navrhuje, aby extrakt z Inula viscosa L. pôsobil protinádorovo na bunky kolorektálneho karcinómu HCT116 prostredníctvom regulácie mikroRNA.
Zdroje pre bunky HCT116
Nižšie je uvedených niekoľko zdrojov o bunkách HCT116.
- Transfekcia HCT116: V tomto videu je krok za krokom uvedený návod na transfekciu rakovinových buniek HCT116.
- Kultivácia bunkovej línie HCT116: Toto video ukazuje protokol subkultivácie bunkovej línie rakoviny hrubého čreva HCT116.
- Subkultivácia bunkovej línie HCT116: Táto webová stránka obsahuje množstvo užitočných informácií o kultivačnom médiu HCT116. Okrem toho poskytuje postupy zmrazovania, rozmrazovania a subkultivácie buniek.
Často kladené otázky o bunkách HCT116
odkazy
- Waghela, B.N., F.U. Vaidya a C. Pathak: Upregulácia NOX-2 a Nrf-2 podporuje rezistenciu na 5-fluóruracil v bunkách ľudského karcinómu hrubého čreva (HCT-116). Biochémia (Moskva), 2021, 86, s. 262-274.
- Yang, M., a i., Astragalín inhibuje proliferáciu a migráciu ľudských buniek rakoviny hrubého čreva HCT116 reguláciou signálnej dráhy NF-κB. Frontiers in Pharmacology, 2021, 12: s. 639256.
- Deepika, S., C.I. Selvaraj, and S.M. Roopan, Screening bioactivities of Caesalpinia pulcherrima L. swartz and cytotoxicity of extract synthesized silver nanoparticles on HCT116 cell line (Skríning bioaktivity Caesalpinia pulcherrima L. swartz a cytotoxicity extraktu syntetizovaných strieborných nanočastíc na bunkovej línii HCT116 ). Materials Science and Engineering, C, 2020, 106, s. 110279.
- Gao, X., a i., Kakaový čaj (Camellia ptilophylla) indukuje mitochondriálne závislú apoptózu v bunkách HCT116 prostredníctvom tvorby ROS a signálnej dráhy PI3K/Akt. Food Research International, 2020, 129, s. 108854.
- Hidayat, A.F.A., et al., Dioscorea bulbifera indukovala apoptózu prostredníctvom inhibície ERK 1/2 a aktivácie JNK signálnych dráh v bunkách ľudského kolorektálneho karcinómu HCT116. Biomedicine & Pharmacotherapy, 2018. 104: p. 806-816.