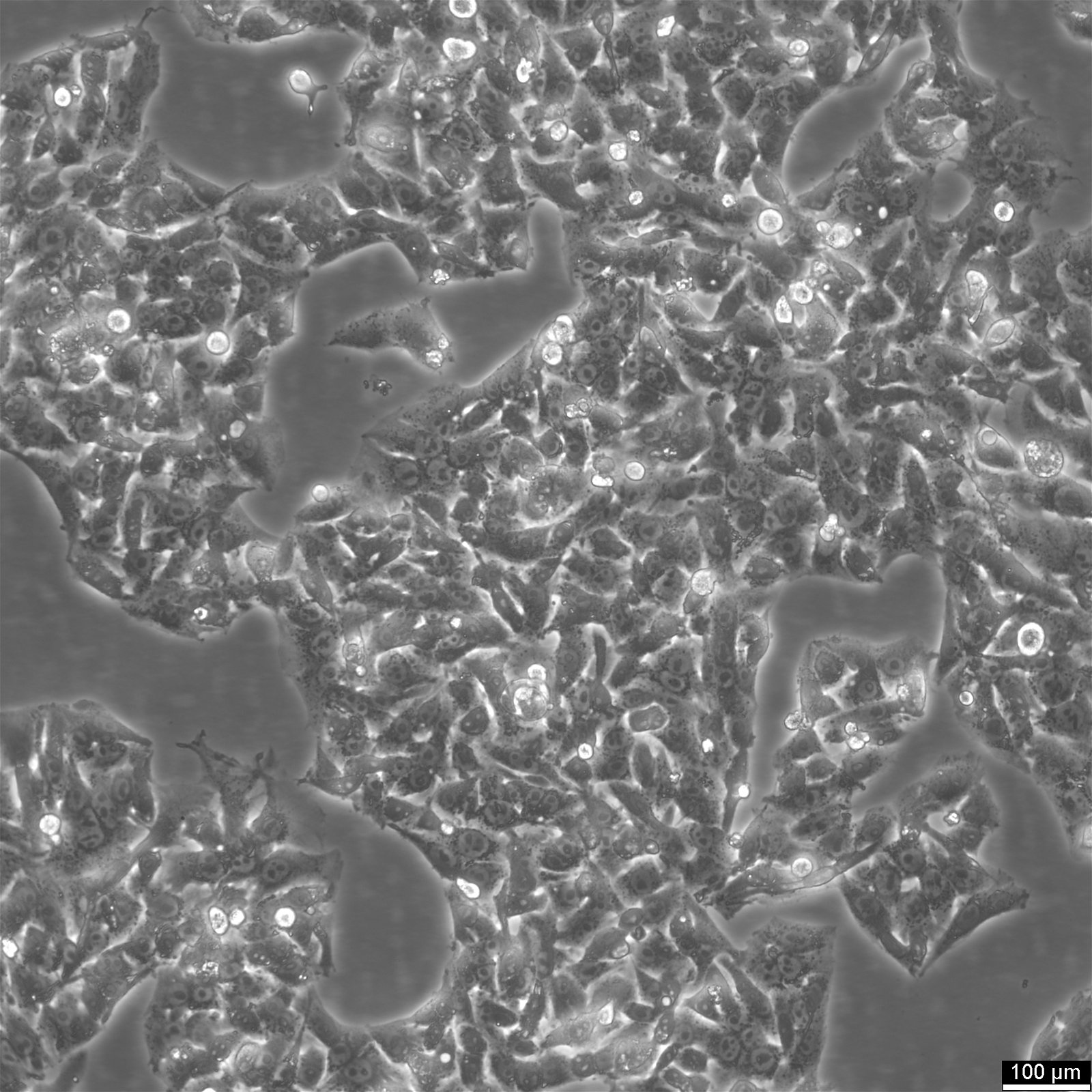
Bunky HepG2 - zdroj pre výskum rakoviny pečene
Hep-G2 je ľudská bunková línia rakoviny pečene pochádzajúca z tkaniva pečene 15-ročného muža kaukazskej rasy s hepatocelulárnym karcinómom. Tieto bunky sa často využívajú v štúdiách metabolizmu liečiv a hepatotoxicity. Hoci bunky HepG2 majú vysokú mieru proliferácie a vzhľad podobný epitelu, nie sú nádorové a vykonávajú rôzne diferencované funkcie pečene. V roku 1975 vedci odvodili bunky HepG2 z hepatocelulárneho karcinómu, čím sa stali prvou hepatálnou bunkovou líniou, ktorá vykazovala kritické vlastnosti hepatocytov. Na rozdiel od predtým vytvorenej bunkovej línie SK-Hep1, ktorej chýbajú základné markery pečeňových buniek, bunky HepG2 môžu vylučovať rôzne plazmatické proteíny a poskytujú cenný model na štúdium vnútrobunkovej dynamiky domén bunkového povrchu v ľudských hepatocytoch. Tieto bunky vykazujú morfológiu podobnú epitelu, majú modálny počet chromozómov 55 a možno ich stimulovať ľudským rastovým hormónom
Charakteristika HepG2
Typický tvar primárnych hepatocytov je kubický a zvyčajne obsahuje dve jadrá. Naproti tomu bunky HepG2 majú epitelovú morfológiu s jedným jadrom a počtom chromozómov v rozmedzí od 48 do 54 na bunku. Hoci bunky HepG2 môžu tvoriť až 25 % celkového bunkového proteínu, ich veľkosť je väčšia ako veľkosť normálnych hepatocytov a tvoria približne 10 % kompletného proteínu v bunke. Bunkové bielkoviny sú rozhodujúcimi aktérmi v bunke, ktorí vykonávajú funkcie určené génmi.
Nádorové bunky vrátane buniek s abnormálnym počtom chromozómov často vykazujú zvýšený počet jadier, až sedem na bunku. Vzhľadom na vysoký stupeň diferenciácie in vitro predstavujú bunky HepG2 ideálny model na štúdium vnútrobunkového obchodovania a dynamiky žlčových kanálikov, sinusoidálnych membránových proteínov a lipidov v ľudských hepatocytoch.
Priemerný priemer bunky HepG2 je približne 10 - 20 µm, čo je menší priemer ako u hepatocytov s priemerom 15 µm, ale podobný ako u nádorových buniek s hepatoblastómom (HB), ktoré majú priemer 10 - 20 µm.
Genetika HepG2
Bunková línia Hep-G2 vykazuje niekoľko translokácií vrátane translokácií medzi krátkymi ramenami chromozómov 1 a 21, trizómií chromozómov 2, 16 a 17 a tetrasómií chromozómu 20. Pozoruje sa aj strata oblasti chromozómu 4q3 spojená s translokáciou t(1;4), ktorá sa často vyskytuje pri hepatoblastóme (HB), a ďalšie chromozómové abnormality, ako sú trizómie 2 a 20. Počet chromozómov v bunkách HepG2 sa pohybuje od 50 do 60, čo naznačuje hyperdiploidný karyotyp, zatiaľ čo niektoré prípady vykazujú viac ako 100 chromozómov a vyznačujú sa tetraploidným rozšírením. Bunky HepG2 obsahujú približne 7,5 pg DNA, čo je o 15 % viac ako priemerná somatická bunka. Na porovnanie, primárne hepatocyty majú kubický tvar bunky a zvyčajne obsahujú dve jadrá [1].
Mutačný profil buniek HepG2
Bunková línia HepG2 nesie mutáciu C228T v promótorovej oblasti TERT, ktorá sa vyskytuje aj v hepatocelulárnom karcinóme (HCC) a hepatoblastóme (HB). Táto mutácia prispieva k nesmrteľnosti tým, že chráni teloméry v rakovinových bunkách. Bunky HepG2 navyše vykazujú divoký typ TP53, ktorý je kritickým génom pre potlačenie ľudskej rakoviny, pretože zohráva úlohu pri zastavení bunkového cyklu, apoptóze a starnutí. Mutácie v tomto géne môžu podporovať proliferáciu buniek.
Bunky HepG2 sa zúčastňujú na viacerých dráhach vrátane dysregulácie bunkového rastu, dráh prežitia, ako je fetálna a embryonálna HB, a dráhy Wnt/β-katenín. Okrem toho má táto bunková línia charakteristickú deléciu tretieho exónu génu CTNNB1, ktorá je identická s deléciou pozorovanou u epitelového typu HB [2,3].
Prehľad buniek hepatocelulárneho karcinómu HepG2 vo výskume pečene
Bunky HepG2 pochádzajúce z ľudského hepatómu sa stali neoceniteľným nástrojom na výskum funkcií pečene a ochorení vrátane hepatocelulárneho karcinómu. Tieto bunkové línie pečeňových buniek umožňujú nahliadnuť do bunkových reakcií ľudských hepatocytov za rôznych experimentálnych podmienok. Použitie luciferázových reportérových plazmidov v bunkách HepG2 bolo obzvlášť účinné pri sledovaní expresie génov a bunkových transfekcií, ktoré sú zásadné v metabolickom výskume, napríklad pri štúdiu účinkov etanolu na pečeňové bunky
Štúdie vírusových infekcií a ochorení pečene s použitím buniek HepG2
Imortalizované nádorové bunkové línie pečene, ako sú HepG2 a Huh7, majú zásadný význam pri štúdiu vírusových infekcií, pretože preukazujú úplnú replikáciu bunkového cyklu hepatitídy D (HDV) a expresiu hepatitídy B (HBV) [5,6]. Zároveň bunkové línie HepaRG zohrávajú rozhodujúcu úlohu pri objasňovaní mechanizmov vstupu HBV [7]. Bunky HepG2 sa využívajú aj na skúmanie rôznych ochorení ľudskej pečene, od genetických stavov, ako je progresívna familiárna intrahepatálna cholestáza (PFIC) a Dubinov-Johnsonov syndróm, až po environmentálne a diétne štúdie súvisiace s cytotoxickými a genotoxickými látkami, ako aj pri výskume zameranom na lieky a hepatokarcinogenézu [8,9]. Ich použitie sa rozširuje na skúšky s bio-umelými pečeňovými zariadeniami
Interakcie buniek HepG2 s biomateriálmi v tkanivovom inžinierstve
Interakcia buniek HepG2 s rôznymi biomateriálmi je kľúčová v tkanivovom inžinierstve. Techniky, ako je technika koloidnej sondy, pomáhajú pochopiť tieto interakcie meraním adhéznych vlastností buniek, ktoré sú nevyhnutné na určenie životaschopnosti buniek pri vývoji skeletov a presných modelov pečeňového tkaniva
Správanie buniek a inovácie v modeloch založených na HepG2
Štúdium správania buniek v modeloch založených na HepG2 má zásadný význam pre výskum ochorení pečene. Pokroky v trojrozmerných sféroidných bunkových kultúrach viedli k vytvoreniu sféroidov buniek HepG2, ktoré ponúkajú fyziologicky relevantnejší model, ktorý presne odráža normálne hepatocyty. Tieto trojrozmerné modely so zvýšenou metabolickou aktivitou naznačujú potenciál buniek HepG2 slúžiť ako model hepatoblastómu a majú význam vo výskume liečby rakoviny, najmä pri simulácii nádorov pečene a testovaní nových terapeutických prístupov [10-12]
Porovnanie a vlastnosti HepG2 medzi inými nádorovými bunkovými líniami
HepG2 je jednou z najpoužívanejších nádorových bunkových línií pečene, ktorá bola vybraná pre svoje široké využitie vo vedeckom výskume spomedzi približne 40 dostupných nádorových bunkových línií pečene [13]. Napriek slabej alebo chýbajúcej expresii určitých enzýmov cytochrómu P450 v porovnaní s normálnymi hepatocytmi, metabolický profil HepG2 podnietil snahy o modifikáciu bunkovej línie na lepšie štúdie metabolizmu liečiv [13]. V porovnaní s nádorovými bunkovými líniami, ako sú MCF7, PC3, 143B a HEK293, bunky HepG2 vykazujú jedinečné profily obsahu aminokyselín, ktoré významne ovplyvňujú syntézu a sekréciu proteínov, čo poukazuje na ich jedinečné metabolické dráhy [14]
Výskum ochorení pečene pomocou HepG2
Subkultivácia buniek HepG2
Tu je uvedených päť krokov na odstránenie adherovaných buniek z baniek s bunkovou kultúrou pomocou Accutase:
- Odstráňte médium z banky na kultiváciu buniek a opláchnite adherované bunky pomocou PBS bez vápnika a horčíka. Použite 3 - 5 ml PBS pre banky T25 a 5 - 10 ml pre banky T75.
- Do banky s bunkovou kultúrou pridajte akutázu s použitím 1 - 2 ml na banku T25 a 2,5 ml na banku T75. Uistite sa, že Accutase pokrýva celú bunkovú vrstvu.
- Inkubujte banku pri izbovej teplote 8-10 minút.
- Opatrne resuspendujte bunky s médiom, pričom použite 10 ml čerstvého média.
- Resuspendované bunky odstreďujte 5 minút pri 300xg, znovu ich rozpusťte v čerstvom médiu a dávkujte ich do nových baniek s čerstvým médiom.
Budúce vyhliadky pre bunky HepG2
Snaha o odhalenie plného potenciálu bunkovej línie HepG2 pokračuje vďaka prelomovému pokroku v oblasti zvyšovania expresie cytochrómov. Výskumníci tiež skúmajú možnosť trojrozmerných sféroidných bunkových kultúr, ktoré ponúkajú fyziologicky relevantnejší systém. Metabolická aktivita vrátane cytochrómov je v 3D sféroidných modeloch HepG2 pozoruhodne vyššia ako v 2D bunkách, čo nás približuje k vytvoreniu modelu, ktorý odráža normálne hepatocyty. Okrem toho skúmanie dynamických procesov, ktoré sú základom nesprávnej distribúcie povrchových proteínov buniek, môže otvoriť cestu k lepšiemu pochopeniu ochorení pečene
Bunky HepG2: Pochopenie ich úlohy a odlišností v biomedicínskom výskume - často kladené otázky
Odkazy
- Vyas, R.C., Darroudi, F., Natarajan, A.T. Radiáciou indukované chromozómové zlomy a opätovné spojenie v interfázovo-metafázových chromozómoch ľudských lymfocytov, Mutat Res, 1991; 249(1):29-35.
- Woodfield, S.E., Shi, Y., Patel, R.H., Chen, Z., Shah, A.P., Srivastava, R.K., Whitlock, R.S., Ibarra, A.M., Larson, S.R., Sarabia, S.F., et al. MDM4 Inhibition: A Novel Therapeutic Strategy to Reactivate P53 in Hepatoblastoma. Sci. Rep. 2021, 11, 2967.
- Hussain, S.P., Schwank, J., Staib, F., Wang, X.W., Harris, C.C. TP53 Mutations and hepatocellular Carcinoma: Insights into the Etiology and Pathogenesis of Liver Cancer. Oncogene 2004.
- Schicht, G., Seidemann, L., Haensel, R., Seehofer, D., Damm, G. Critical Investigation of the Usability of Hepatoma Cell Lines HepG2 and Huh7 as Models for the Metabolic Representation of Resectable Hepatocellular Carcinoma (Kritické skúmanie použiteľnosti hepatómových bunkových línií HepG2 a Huh7 ako modelov na metabolické zobrazenie resekabilného hepatocelulárneho karcinómu). Cancers 2022, 14(17), 4227.
- Verrier, E.R., Colpitts, C.C., Schuster, C., Zeisel, M.B., Baumert, T.F. Cell Culture Models for the Investigation of Hepatitis B and D Virus Infection. Viruses 2016, 8, 261.
- Verrier, E.R., Colpitts, C.C., Bach, C., Heydmann, L., Weiss, A., Renaud, M., Durand, S.C., Habersetzer, F., Durantel, D., AbouJaoudé, G., et al. A Targeted Functional RNA Interference screen Uncovers Glypican 5 as an Entry Factor for Hepatitis B and D Viruses. Hepatology 2016, 63, 35-48.
- Gripon, P., Rumin, S., Urban, S., Le Seyec, J., Glaise, D., Cannie, I., Guyomard, C., Lucas, J., Trepo, C., Guguen-Guillouzo, C. Infection of a Human Hepatoma Cell Line by Hepatitis B Virus. Proc. Natl. Acad. Sci. USA 2002, 99, 15655-15660.
- Mersch-Sundermann, V., Knasmüller, S., Wu, X.J., Darroudi, F., Kassie, F. Use of a human-derived liver cell line for the detection of cytoprotective, antigenotoxic and cogenotoxic agents. Toxikológia. 2004; 198(1-3): 329-340.
- Fanelli, A. HepG2 (hepatocelulárny karcinóm pečene): bunkové kultúry. HepG2. Získané 3. decembra 2017.
- Xuan, J., Chen, S., Ning, B., Tolleson, W.H., Guo, L. Development of HepG2-Derived Cells Expressing Cytochrome P450s for Assessing Metabolism-Associated Drug-Induced Liver Toxicity (Vývoj buniek odvodených od HepG2 exprimujúcich cytochróm P450 na hodnotenie toxicity pečene vyvolanej liekmi súvisiacimi s metabolizmom). Physiol. Behav. 2017, 176, 139-148.
- Ooka, M., Lynch, C., Xia, M. Application of in Vitro Metabolism Activation in High-Throughput Screening (Aplikácia aktivácie metabolizmu in vitro pri vysoko výkonnom skríningu). Int. J. Mol. Sci. 2020, 21, 8182.
- Huang, L., Coughtrie, M.W.H., Hsu, H. Down-Regulation of Dehydroepiandrosterone Sulfotransferase Gene in Human Hepatocellular Carcinoma (Znížená regulácia génu dehydroepiandrosterón sulfotransferázy v ľudskom hepatocelulárnom karcinóme). Mol. Cell. Endocrinol.
- Zhu, Z., Hao, X., Yan, M., et al. Cancer stem/progenitor cells are highly enriched in CD133 + CD44 + population in hepatocellular carcinoma. Int J Cancer. 2010; 126:2067-2078.
- Arbus, C., Benyamina, A., Llorca, P.-M., Baylé, F., Bromet, N., Massiere, F., Garay, R.P., Hameg, A. Characterization of human cytochrome P450 enzymes involved in the metabolism of cyamemazine. Eur J Pharm Sci. 2007 Dec;32(4-5):357-66.