Meios de cultura celular: Uma visão geral
No domínio das ciências da vida, uma das metodologias mais importantes é a cultura de células. A remoção de células, tecidos ou órgãos de um animal ou planta e a subsequente implantação dessas células, tecidos ou órgãos num ambiente artificial que seja favorável à sua sobrevivência e/ou crescimento é o que se entende por "cultura de células" As necessidades ambientais fundamentais para o desenvolvimento ótimo das células são a temperatura controlada, um substrato para a fixação das células, um meio de crescimento adequado e uma incubadora que mantenha o pH e a osmolalidade ideais. As células devem ter estas condições para poderem crescer em todo o seu potencial.
A seleção de um meio de crescimento adequado para o cultivo in vitro é a fase da cultura celular que é simultaneamente a mais crítica e a mais vital. Um meio de crescimento, também conhecido como meio de cultura, é um líquido ou gel formulado para encorajar o desenvolvimento de organismos a uma escala microscópica, celular ou vegetal. O meio utilizado para cultivar células contém frequentemente um fornecimento adequado de energia e substâncias que controlam o ciclo celular. Os principais componentes de um meio de cultura incluem aminoácidos, vitaminas, sais inorgânicos, glucose e soro. O soro é adicionado ao meio porque actua como uma fonte de factores de crescimento, hormonas e factores de fixação. Para além de fornecer nutrientes, o meio também contribui para a manutenção dos níveis de pH e osmolalidade.
Tipos de meios utilizados na cultura de células
Tanto as células humanas como as células animais podem ser cultivadas num meio artificial ou sintético ou num meio totalmente natural, complementado com elementos naturais. A seguir, damos-lhe uma visão geral dos diferentes tipos de meios atualmente disponíveis.
Meios naturais
Apenas os fluidos biológicos que existem no seu estado natural podem ser encontrados em meios naturais. Os meios naturais são muito úteis e fáceis para o cultivo de uma grande variedade de tipos de células animais. A falta de compreensão dos componentes exactos que constituem os meios naturais é o principal fator que contribui para a baixa repetibilidade dos resultados obtidos utilizando meios naturais.
Meios artificiais
A preparação de meios artificiais ou sintéticos envolve a adição de nutrientes (tanto orgânicos como inorgânicos), proteínas séricas, hidratos de carbono, cofactores, vitaminas e sais, bem como fases gasosas de O2 e CO2 [1].
Foram desenvolvidos vários tipos de meios artificiais com o objetivo de cumprir uma ou mais das seguintes funções 1) Sobrevivência imediata (uma solução salina equilibrada com um pH e uma pressão osmótica precisos). 2) Sobrevivência prolongada (uma solução salina equilibrada suplementada com diferentes formulações de produtos químicos orgânicos e/ou soro). 3) Desenvolvimento indefinido. 4) Funções especializadas.
Existem quatro classificações distintas para os meios artificiais:
Meios contendo soro
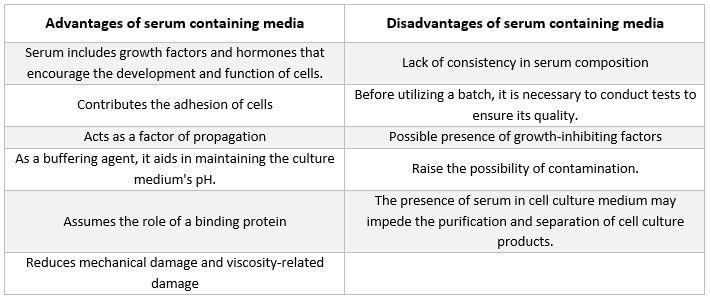
O tipo de suplemento mais frequente encontrado nos meios utilizados para o cultivo de células animais é o soro fetal bovino. É adicionado ao meio de cultura como um suplemento de baixo custo, de modo a obter as melhores condições de crescimento possíveis. Para além de atuar como transportador ou quelante de nutrientes instáveis ou insolúveis em água, hormonas e factores de crescimento, inibidores de proteases e outras substâncias, o soro também se liga e neutraliza moléculas nocivas.
Meio sem soro
A presença de soro nos meios tem uma série de desvantagens e tem o potencial de causar grandes erros de interpretação na investigação imunológica [2, 3]. Foi criada uma grande variedade de meios sem soro [4, 5]. Estes meios são geralmente formulados especificamente para apoiar a cultura de um único tipo de células, como o Knockout Serum Replacement e o Knockout DMEM da Thermo Fisher Scientific, e o meio mTESR da Stem Cell Technologies [6], para células estaminais [7].
Além disso, estes meios incorporam quantidades definidas de factores de crescimento purificados, lipoproteínas e outras proteínas, que são normalmente fornecidas pelo soro [8]. Estes meios são frequentemente referidos como "meios de cultura definidos", uma vez que os componentes que os constituem são bem conhecidos.
Meios quimicamente definidos
Estes meios incluem componentes inorgânicos e orgânicos ultra-puros que não foram contaminados por qualquer tipo de contaminação. Podem também incluir adições de proteínas puras, tais como factores de crescimento.
a modificação genética de bactérias ou leveduras, juntamente com a adição de determinados ácidos gordos, vitaminas, colesterol e aminoácidos, resulta na produção dos seus componentes [9].
Meios isentos de proteínas
Os meios isentos de proteínas são aqueles que não incluem qualquer proteína e, em vez disso, incluem apenas elementos não proteicos. Quando comparados com meios com adição de soro, a utilização de meios sem adição de proteínas promove uma maior proliferação celular e expressão proteica e facilita a purificação de qualquer produto gerado num processo a jusante [10-12]. As proteínas não são incluídas em formulações como MEM e RPMI-1640. No entanto, pode ser administrado um suplemento proteico se for necessário.
Meios de cultura e seus componentes básicos
Os meios de cultura comerciais podem ser adquiridos sob a forma de pó ou líquido e incluem frequentemente uma variedade de nutrientes, como aminoácidos, glucose, sais, vitaminas e outros suplementos alimentares.
As necessidades destes componentes são diferentes para cada linha celular, e estas variações são responsáveis pelo grande número de diferentes formulações de meios. Cada componente é responsável por uma determinada função, que será descrita nos parágrafos seguintes:
Sistemas tampão
Para manter condições óptimas de crescimento, o pH deve ser controlado, o que é frequentemente feito através de um de dois sistemas tampão:
Sistema tampão natural
A relação CO2/H2CO3 na atmosfera é igual à do meio, criando um mecanismo natural de tamponamento. Para preservar o seu mecanismo natural de tamponamento, as culturas devem ser mantidas num ambiente de ar com 5-10% de CO2, o que é frequentemente conseguido através da utilização de uma incubadora de CO2. Uma das melhores coisas sobre a utilização de um tampão natural é o facto de ser barato e seguro.
HEPES
O tamponamento químico utilizando o zwitterion HEPES tem uma maior capacidade de tamponamento na gama de pH de 7,2-7,4 e não necessita de um ambiente gasoso regulado. Para determinados tipos de células, uma dose maior de HEPES pode ser prejudicial. Os meios que contêm HEPES são também muito mais susceptíveis aos efeitos fototóxicos da luz fluorescente [13].
Vermelho de fenol
O indicador de pH vermelho de fenol é frequentemente incluído em meios de cultura comercialmente disponíveis, permitindo a monitorização contínua do pH. Ao expandir as células, os metabolitos produzidos por estas células provocam uma alteração do pH e, por conseguinte, uma mudança de cor do meio. O vermelho de fenol tem um efeito duplo na cor do meio, tornando-o amarelo em pH ácido e roxo em pH alcalino. O pH 7,4, o valor ótimo para a cultura de células, faz com que o meio apareça vermelho fluorescente.
Mas o vermelho de fenol tem alguns inconvenientes: Em primeiro lugar, o vermelho de fenol é capaz de simular o desempenho de uma série de hormonas esteróides, principalmente o estrogénio [14]. Por conseguinte, quando se estudam células sensíveis aos estrogénios, como o tecido mamário, recomenda-se um meio isento de vermelho de fenol. O equilíbrio sódio-potássio é perturbado pela presença de vermelho de fenol em várias formulações sem soro. A adição de soro ou de hormona pituitária bovina ao meio pode neutralizar este efeito [15]. Em terceiro lugar, a deteção em experiências de citometria de fluxo é dificultada pela presença de vermelho de fenol.
Sais inorgânicos
Os meios que contêm sais inorgânicos, como os iões de sódio, potássio e cálcio, ajudam a manter o equilíbrio osmótico e a regular o potencial da membrana.
Aminoácidos
Uma vez que os aminoácidos são os componentes fundamentais das proteínas, são um componente essencial de todos os meios de crescimento celular que alguma vez foram concebidos. Uma vez que as células são incapazes de produzir determinados aminoácidos por si próprias, é importante que o meio de cultura inclua aminoácidos essenciais. Estes são necessários para a proliferação das células e a concentração em que estão presentes determina a densidade celular máxima que pode ser atingida. Em particular, a L-glutamina, um aminoácido essencial, é especialmente crucial.
A L-glutamina funciona como uma fonte secundária de energia para o metabolismo e contribui com azoto para a produção de NAD, NADPH e nucleótidos. Devido ao facto de a L-glutamina ser um aminoácido instável que, com o tempo, se transforma numa forma que as células não conseguem utilizar, deve ser administrada ao meio.
Para além disso, podem ser fornecidos ao meio aminoácidos não essenciais para reabastecer os que foram consumidos durante o processo de crescimento. O crescimento das células é reforçado e a sua viabilidade aumenta quando o meio de crescimento é suplementado com aminoácidos não essenciais.
Hidratos de carbono
Os hidratos de carbono sob a forma de açúcares são a principal fonte de energia. Muitos dos meios de cultura incluem também maltose e frutose, para além dos açúcares mais comuns, a glucose e a galactose.
Proteínas e péptidos
A albumina, a transferrina e a fibronectina são as proteínas e os péptidos mais utilizados, sendo especialmente importantes nos meios que não incluem soro. A albumina, a transferrina, a aprotinina, a fetuina e a fibronectina são algumas das proteínas que podem ser encontradas no soro, que é um rico suprimento de proteínas.
A albumina é a principal proteína encontrada no sangue e a sua função é ligar e transportar várias substâncias, incluindo água, sais, ácidos gordos livres, hormonas e vitaminas, entre diferentes órgãos e células. A capacidade da albumina de se ligar a produtos químicos torna-a uma candidata eficaz para a remoção de compostos nocivos do meio em que as células são cultivadas.
A aprotinina é um agente protetor em sistemas de cultura de células, uma vez que é estável a pH neutro e ácido, bem como resistente a temperaturas elevadas e à destruição que pode ser causada por enzimas proteolíticas. É capaz de inibir um certo número de serino-proteases, incluindo a tripsina, entre outras.
A fetuina é uma glicoproteína que pode ser detectada em quantidades mais elevadas no soro de animais fetais e recém-nascidos do que no soro de adultos. Além disso, actua como um inibidor da serina protease. A proteína fibronectina é um componente essencial no processo de adesão celular. A transferrina é uma proteína que transporta o ferro e é responsável pela entrega do ferro às membranas das células.
Ácidos gordos e lípidos
Desempenham um papel crucial no meio isento de soro quando este está ausente.
Vitaminas
Numerosas vitaminas são necessárias para o desenvolvimento e proliferação celular. As vitaminas não podem ser produzidas em quantidades adequadas pelas células, pelo que são essenciais na cultura de tecidos como suplementos alimentares.
Na cultura de células, o soro é a principal fonte de vitaminas; no entanto, os meios também são tratados com várias vitaminas para os tornar adequados a um tipo específico de células. Normalmente, as vitaminas do grupo B são utilizadas para estimular o crescimento.
Oligoelementos
Elementos químicos como o cobre, o zinco, o selénio e os intermediários do ácido tricarboxílico são conhecidos como oligoelementos. Os oligoelementos são frequentemente adicionados a meios que não incluem soro, a fim de substituir os que estão normalmente presentes no soro. Estes elementos são componentes químicos importantes que são necessários para um desenvolvimento celular saudável. Muitas reacções bioquímicas dependem de certos micronutrientes, como a atividade enzimática.
Suplementos ao meio
O meio de crescimento completo sugerido para certas linhas celulares necessita de componentes extra que estão ausentes do meio de base e do soro. Estes suplementos alimentares apoiam o crescimento celular e a função metabólica adequada.
Embora as hormonas, os factores de crescimento e as moléculas de sinalização sejam essenciais para a proliferação adequada de determinadas linhas celulares, devem ser sempre tomadas as seguintes precauções: Uma vez que a adição de suplementos pode alterar a osmolalidade do meio de crescimento completo, o que pode inibir o desenvolvimento celular, é sempre aconselhável verificar a osmolalidade após a adição de suplementos. Para a maioria das linhas celulares, a osmolalidade óptima varia entre 260 e 320 mOSM/kg.
Antibióticos
Os antibióticos são frequentemente utilizados para inibir o desenvolvimento de poluentes bacterianos e fúngicos [16], embora não sejam essenciais para o crescimento celular. Uma vez que os antibióticos podem ocultar a contaminação por micoplasma e bactérias resistentes, a sua utilização de rotina não é sugerida para a cultura de células [17, 18].
Além disso, os antibióticos podem perturbar o metabolismo das células hipersensíveis. As combinações de penicilina-estreptomicina fabricadas pela MilliporeSigma e pela Life Technologies são frequentemente utilizadas. A plasmocina foi utilizada na cultura das linhas celulares de glioma TS603, TS516 e BT260 [19], e demonstrou ser eficaz na remoção da contaminação por micoplasma (20).
Soro
As albuminas, os factores de crescimento e os inibidores de crescimento estão todos presentes no soro. O soro é um dos componentes mais importantes do meio de cultura de células porque fornece aminoácidos, proteínas, vitaminas (especialmente vitaminas lipossolúveis como A, D, E e K), hidratos de carbono, lípidos, hormonas, factores de crescimento, minerais e oligoelementos.
O soro de fontes fetais e de vitelo bovino é frequentemente utilizado para promover o desenvolvimento de células em cultura. O soro fetal constitui uma fonte abundante de factores de crescimento e é adequado para a clonagem de células e o desenvolvimento de células sensíveis. Devido às suas reduzidas capacidades de promoção do crescimento, o soro de vitelo é utilizado em experiências de inibição do contacto. Os meios de cultura normais incluem frequentemente 2% a 10% de soro. A adição de soro ao meio de cultura tem os seguintes objectivos [21]:
-
O soro fornece os nutrientes essenciais para as células (tanto em solução como ligados a proteínas).
-
O soro contém vários factores de crescimento e hormonas envolvidos na promoção do crescimento e na atividade celular especializada.
-
O soro contém muitas proteínas de ligação, como a albumina e a transferrina, que transportam outros produtos químicos para a célula. Por exemplo, a albumina transporta gorduras, vitaminas, hormonas, etc. para o interior das células.
-
Também fornece proteínas, como a fibronectina, que aumentam a adesão das células ao substrato. Além disso, produz elementos de propagação que ajudam na expansão celular antes da divisão.
-
Fornece inibidores de protease que impedem a proteólise nas células.
-
Também contém minerais como Na+, K+, Zn2+ e Fe2+.
-
Aumenta a viscosidade do meio, protegendo assim as células de lesões mecânicas durante a agitação da cultura em suspensão.
-
É também um tampão.
Referências
[1] Morgan J, Morton H, Parker R. Nutrição de células animais em cultura de tecidos; estudos iniciais sobre um meio sintético. Proc Soc Exp Biol Med. 1950;73:1-8
[2] Kerbel R, Blakeslee D. Adsorção rápida de um componente do soro de vitelo fetal por células de mamíferos em cultura. Uma fonte potencial de artefactos em estudos de anti-soros para antigénios específicos de células. Immunology. 1976;31:881-91
[3] Sula K, Draber P, Nouza K. A adição de soro ao meio utilizado para a preparação de suspensões celulares como possível fonte de artefactos em reacções mediadas por células estudadas através do teste do nódulo linfático poplíteo. J Immunogenet. 1980;7:483-9
[4] Mariani E, Mariani A, Monaco M, Lalli E, Vitale M, Facchini A. Meios comerciais sem soro: crescimento de hibridomas e produção de anticorpos monoclonais. J Immunol Methods. 1991;145:175-83
[5] Barnes D, Sato G. Methods for growth of cultured cells in serum-free medium. Anal Biochem. 1980;102:255-70
[6] Yu H, Lu S, Gasior K, Singh D, Vazquez Sanchez S, Tapia O,et al. HSP70 chaperones RNA-free TDP-43 into anisotropic intranuclear liquid spherical shells. Ciência. 2021;371:
[7] Meharena H, Marco A, Dileep V, Lockshin E, Akatsu G, Mullahoo J,et al. A senescência induzida pela síndrome de Down interrompe a arquitetura nuclear dos progenitores neurais. Cell Stem Cell. 2022;29:116-130.e7
[8] Iscove N, Melchers F. Substituição completa do soro por albumina, transferrina e lípido de soja em culturas de linfócitos B reactivos a lipopolissacarídeos. J Exp Med. 1978;147:923-33
[9] Stoll T, Muhlethaler K, von Stockar U, Marison I. Systematic improvement of a chemically-defined protein-free medium for hybridoma growth and monoclonal antibody production. J Biotechnol. 1996;45:111-23
[10] Darfler F. A protein-free medium for the growth of hybridomas and other cells of the immune system. In Vitro Cell Dev Biol. 1990;26:769-78
[11] Barnes D, Sato G. Serum-free cell culture: a unifying approach. Cell. 1980;22:649-55
[12] Hamilton W, Ham R. Clonal growth of chinese hamster cell lines in protein-free media. In Vitro. 1977;13:537-47
[13] Zigler J, Lepe Zuniga J, Vistica B, Gery I. Analysis of the cytotoxic effects of light-exposed HEPES-containing culture medium. In Vitro Cell Dev Biol. 1985;21:282-7
[14] Berthois Y, Katzenellenbogen J, Katzenellenbogen B. Phenol red in tissue culture media is a weak estrogen: implications concerning the study of estrogen-responsive cells in culture. Proc Natl Acad Sci U S A. 1986;83:2496-500
[15] Karmiol S. Development of serum free media (Desenvolvimento de meios sem soro). In: Mestre JRW, editor. Animal Cell culture, 3rd ed., Oxford: Oxford University Press; 2000. Oxford: Oxford University Press; 2000.
[16] Perlman D. Use of antibiotics in cell culture media. Methods Enzymol. 1979;58:110-6
[17] McGarrity G. Spread and control of mycoplasmal infection of cell cultures. In Vitro. 1976;12:643-8
[18] Masters J, Stacey G. Changing medium and passaging cell lines. Nat Protoc. 2007;2:2276-84
[19] Chakraborty A, Laukka T, Myllykoski M, Ringel A, Booker M, Tolstorukov M,et al. Histone demethylase KDM6A directly senses oxygen to control chromatin and cell fate. Science. 2019;363:1217-1222
[20] Molla Kazemiha V, Azari S, Amanzadeh A, Bonakdar S, Shojaei Moghadam M, Habibi Anbouhi M,et al. Eficiência do Plasmocin™ em várias linhas celulares de mamíferos infectadas por mollicutes em comparação com antibióticos comumente usados em cultura de células: uma experiência local. Cytotechnology. 2011;63:609-20
[21] Kragh Hansen U. Molecular aspects of ligand binding to serum albumin. Pharmacol Rev. 1981;33:17-53