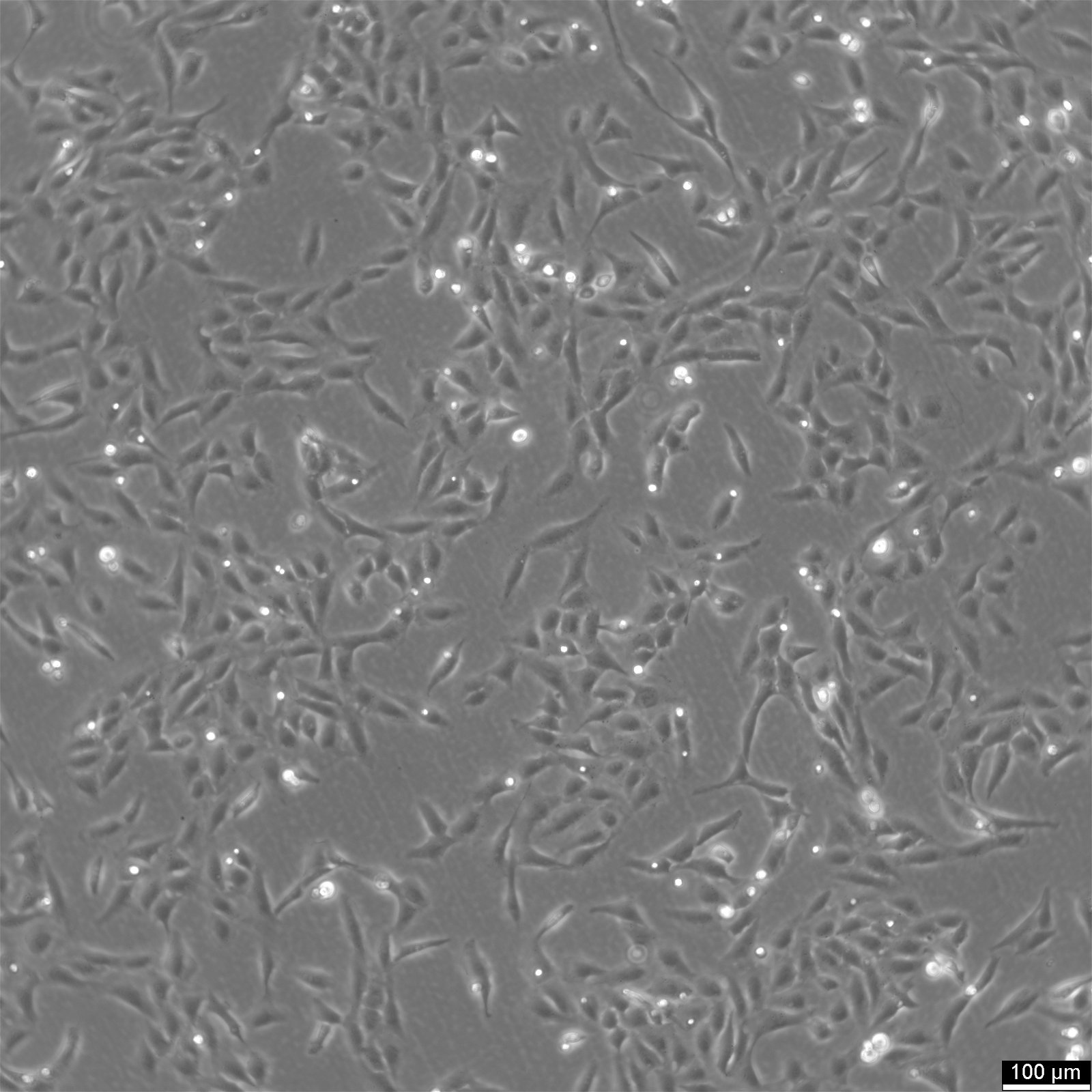
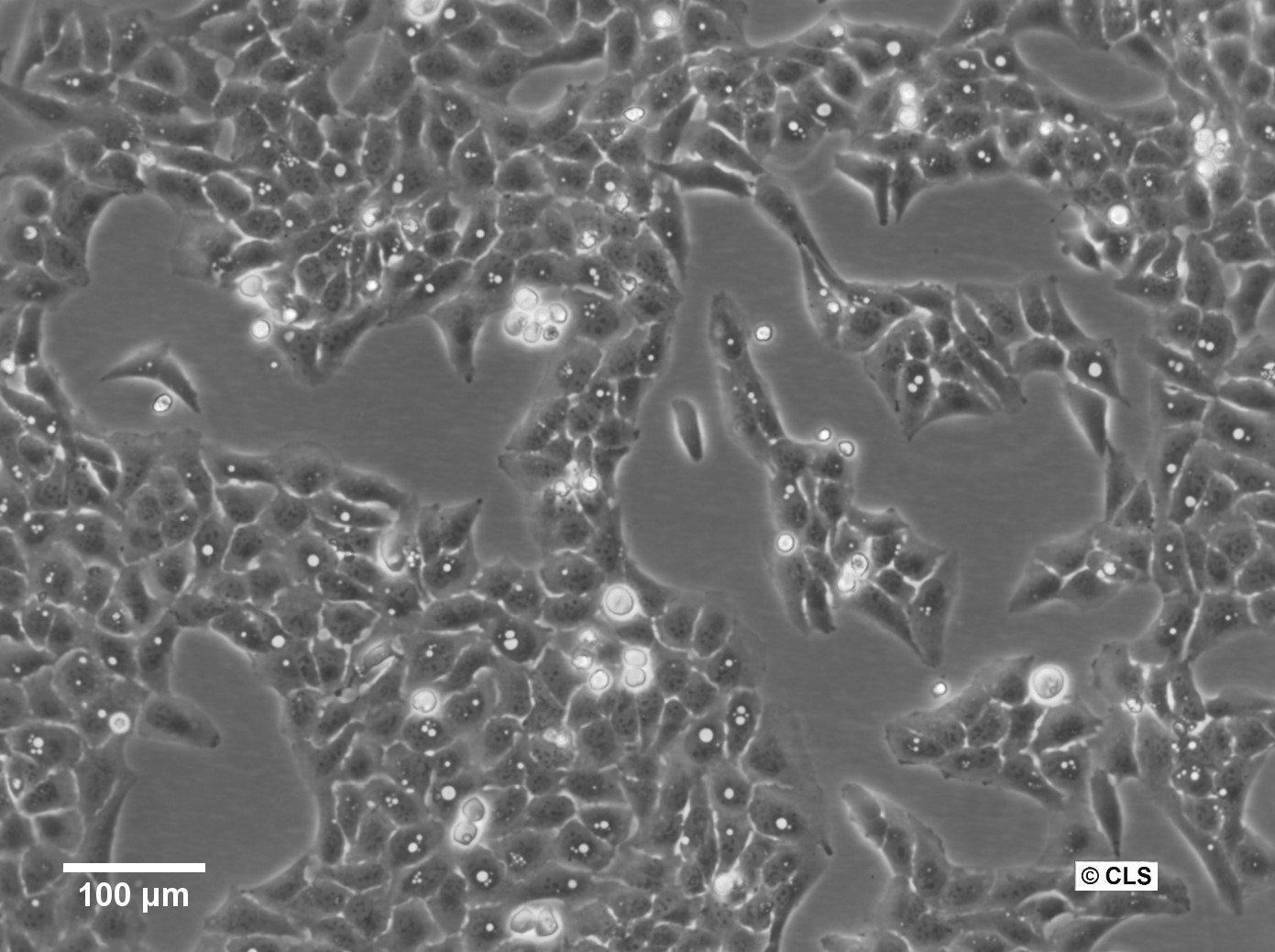
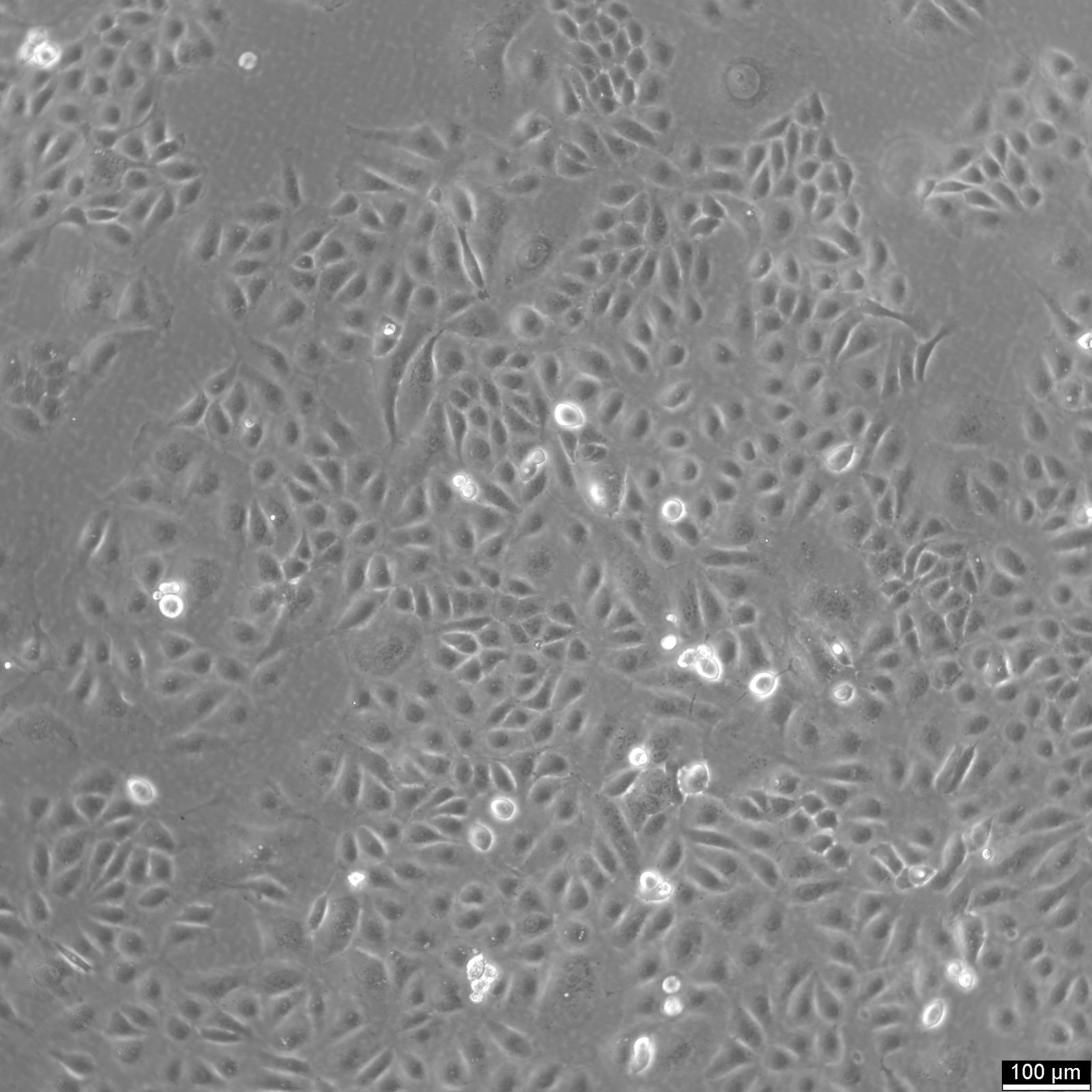
Células U2OS-CRISPR-SNAPf-Nup358/RanBP2















800,00 €*
Os produtos são enviados congelados em gelo seco em criotubos. Cada criotubo contém normalmente 3 × 10⁶ células para linhas aderentes ou 5 × 10⁶ células para linhas em suspensão (consulte o CoA do lote para obter detalhes).
Informações gerais
| Descrição | U2OS-CRISPR-SNAPf-Nup358/RanBP2 é uma linha celular de osteossarcoma humano editada genómicamente, derivada de células U2OS, na qual o locus endógeno RANBP2 (também conhecido como NUP358) foi modificado por CRISPR/Cas9 para codificar uma etiqueta SNAPf em quadro com a proteína nativa. Nup358/RanBP2 é uma grande nucleoporina localizada nos filamentos citoplasmáticos do complexo de poros nucleares (NPC) e desempenha papéis críticos no transporte nucleocitoplasmático, SUMOilação e processos mitóticos. A marcação endógena garante que SNAPf-Nup358 seja expresso sob o controlo fisiológico do promotor, mantendo os níveis de expressão nativos e minimizando artefactos associados a sistemas de superexpressão. A etiqueta SNAPf é uma variante de marcação rápida da etiqueta SNAP que se liga covalentemente a substratos conjugados com benzilguanina, permitindo a marcação fluorescente seletiva e estável de Nup358 em células vivas ou fixas. Nas células U2OS-CRISPR-SNAPf-Nup358/RanBP2, a proteína de fusão localiza-se no envelope nuclear numa distribuição pontilhada característica dos filamentos NPC citoplasmáticos. Esta configuração suporta imagens de fluorescência de alta resolução, microscopia de super-resolução, marcação pulse-chase e abordagens de rastreamento de moléculas únicas para estudar a arquitetura e a dinâmica do NPC. A morfologia plana e os núcleos grandes das células U2OS facilitam ainda mais a imagem quantitativa das estruturas do envelope nuclear. Este modelo permite a investigação das funções específicas da Nup358 na exportação nuclear dependente de CRM1/exportina, na regulação do ciclo da Ran GTPase e na organização espacial das plataformas de transporte citoplasmático. Dado o envolvimento da Nup358 na montagem do fuso mitótico e na função do cinetocoro, a linha celular também é adequada para estudar a redistribuição dependente do ciclo celular das nucleoporinas e a desmontagem/remontagem do NPC durante a mitose. O U2OS-CRISPR-SNAPf-Nup358/RanBP2 fornece uma plataforma fisiologicamente relevante para dissecar os aspetos estruturais e funcionais da face citoplasmática do complexo de poros nucleares em células humanas. |
|---|---|
| Organismo | Humano |
| Tecido | Osso |
| Doença | Osteossarcoma |
Caraterísticas
| Idade | 15 anos |
|---|---|
| Género | Feminino |
| Etnia | Caucasiano |
| Morfologia | De tipo epitelial |
| Propriedades de crescimento | Aderente |
Dados regulamentares
| Citação | U2OS-CRISPR-SNAPf-Nup358/RanBP2 (número de catálogo Cytion 300663) |
|---|---|
| Nível de biossegurança | 1 |
| NCBI_TaxID | 9606 |
| Depositor | O Laboratório Ellenberg (EMBL) |
| Estatuto dos OGM | GMO-S1: Esta linha celular de osteossarcoma humano (U2OS-CRISPR-SNAPf-Nup358/RanBP2) contém uma fusão SNAPf-Nup358/RanBP2 com engenharia CRISPR que permite a marcação exacta das fibrilhas citoplasmáticas do poro nuclear. A modificação está integrada de forma estável. Esta classificação aplica-se apenas na Alemanha e pode diferir noutros países. |
Dados biomoleculares
| Expressão proteica | Nup358/RanBP2, SNAPf-tag |
|---|
Manuseamento
| Meio de cultura | McCoys 5a, com: 3,0 g/L de glucose, com: glutamina estável, com: 2,0 mM de piruvato de sódio, com: 2,2 g/L de NaHCO3 (número de artigo Cytion 820200a) |
|---|---|
| Suplementos | Suplementar o meio com 10% de FBS, 3,0 g/L de glucose, glutamina estável, 2,0 mM de piruvato de sódio, 2,2 g/L de NaHCO3, 1% de NEAA |
| Reagente de dissociação | Accutase |
| Subcultura | Retirar o meio antigo das células aderentes e lavá-las com PBS sem cálcio e magnésio. Nos frascos T25, utilizar 3-5 ml de PBS e, nos frascos T75, 5-10 ml. Em seguida, cobrir completamente as células com Accutase, utilizando 1-2 ml para os frascos T25 e 2,5 ml para os frascos T75. Deixar as células incubar à temperatura ambiente durante 8-10 minutos para as destacar. Após a incubação, misturar suavemente as células com 10 ml de meio para as ressuspender e, em seguida, centrifugar a 300xg durante 3 minutos. Deitar fora o sobrenadante, ressuspender as células em meio fresco e transferi-las para novos frascos que já contenham meio fresco. |
| Congelar o meio | Como meio de criopreservação, utilizamos um meio de crescimento completo (incluindo FBS) + 10% DMSO para uma viabilidade pós-descongelamento adequada, ou CM-1 (número de catálogo Cytion 800100), que inclui osmoprotectores optimizados e estabilizadores metabólicos para melhorar a recuperação e reduzir o stress induzido pela crio. |
| Descongelamento e cultura de células |
|
| Atmosfera de incubação | 37°C, 5%CO2, atmosfera humidificada. |
| Revestimento de frascos | Nenhum |
| Procedimento de congelação | As linhas celulares criopreservadas são expedidas em gelo seco em embalagens validadas e isoladas com refrigerante suficiente para manter aproximadamente -78 °C durante o transporte. Aquando da receção, inspecionar imediatamente o recipiente e transferir sem demora os frascos para um local de armazenamento adequado. |
| Condições de envio | As linhas celulares criopreservadas são expedidas em gelo seco em embalagens validadas e isoladas com refrigerante suficiente para manter aproximadamente -78 °C durante o transporte. Aquando da receção, inspecionar imediatamente o recipiente e transferir sem demora os frascos para um local de armazenamento adequado. |
| Condições de armazenamento | Para conservação a longo prazo, colocar os frascos em azoto líquido em fase de vapor a uma temperatura entre -150 e -196 °C. O armazenamento a -80 °C é aceitável apenas como um curto passo intermédio antes da transferência para azoto líquido. |
Controlo de qualidade / Perfil genético / HLA
| Esterilidade | A contaminação por micoplasma é excluída utilizando ensaios baseados em PCR e métodos de deteção de micoplasma baseados em luminescência. Para garantir que não há contaminação bacteriana, fúngica ou de leveduras, as culturas de células são sujeitas a inspecções visuais diárias. |
|---|
Acordo com terceiros
Note-se que esta linha celular não está disponível ao abrigo de um MTA Cytion normalizado, uma vez que requer um acordo com terceiros e/ou está sujeita a negociação com o licenciante original.-
Produtos necessários
Produtos necessários
Meio de congelação CM-1 - 50 mlVariantes de meios de criopreservação: 50 mlO Freeze Medium CM-1 da Cytion é um meio de criopreservação de última geração concebido para garantir o mais alto nível de viabilidade e funcionalidade celular após o descongelamento. Este meio versátil é adequado para um amplo espetro de tipos de células, incluindo células humanas e animais, tornando-o uma ferramenta essencial para diversas aplicações de investigação. Formulado com uma combinação meticulosamente equilibrada de crioprotectores e nutrientes essenciais, o Freeze Medium CM-1 minimiza a formação de cristais de gelo e o stress celular durante o processo de congelação, preservando assim a integridade celular.
As principais caraterísticas do Freeze Medium CM-1 incluem:
Ampla compatibilidade: Eficaz para uma vasta gama de tipos de células, incluindo células primárias, células estaminais e linhas celulares estabelecidas.
Alta Viabilidade: Optimizado para maximizar a recuperação e a viabilidade das células pós-descongelamento, garantindo resultados experimentais fiáveis.
Pronto a utilizar: Convenientemente preparado e esterilizado para aplicação imediata, reduzindo o tempo de preparação e o risco de contaminação.
Estabilidade melhorada: Mantém um desempenho consistente sob condições padrão de criopreservação, garantindo resultados reprodutíveis.
Longo prazo de validade: O CM-1 é um meio de criopreservação pronto a utilizar que contém soro e que pode ser armazenado no frigorífico até um ano.
Utilização do CM-1 para congelação de células
Para utilizar o CM-1 para congelar células aderentes e em suspensão, siga estes passos
Para células aderentes, lavar e dissociar as células do substrato de cultura. No caso das células em suspensão, avançar diretamente para o passo seguinte.
Contar as células para garantir que estão na concentração correta.
Centrifugar as células para as pelletar e, em seguida, ressuspender em meio de congelação CM-1.
Transferir as células ressuspensas para frascos criogénicos.
Utilize um método de congelação lenta antes de transferir as células para armazenamento a longo prazo
Método
Descrição
Passos
❄️
Congelação manual
Um método passo a passo que envolve a redução gradual da temperatura para garantir a viabilidade das células
1️⃣ Colocar as células em meio de congelação num congelador a 4°C durante 40 minutos.
2️⃣ Transferir para um congelador a -80°C durante 24 horas.
3️⃣ Armazenar as células em azoto líquido para preservação a longo prazo
❄️
Utilização do Mr. Frosty
Um dispositivo conveniente que permite taxas de congelação controladas sem energia eléctrica
1️⃣ Preparar as células em frascos criogénicos com meio de congelação.
2️⃣ Colocar os frascos criogénicos no recipiente Mr. Frosty.
3️⃣ Armazenar a -80°C durante 24 horas antes de transferir para azoto líquido
❄️
Congelador de velocidade controlada
Um congelador de alta precisão da Thermo Fisher ou de outros fabricantes, concebido para a redução controlada da temperatura
1️⃣ Programar o dispositivo para diminuir gradualmente a temperatura.
2️⃣ Colocar as células preparadas no congelador.
3️⃣ Após o ciclo de congelação, transferir as células para azoto líquido
Armazenar os frascos criogénicos a temperaturas inferiores a -130°C ou em azoto líquido para preservação a longo prazo.
Ingredientes
Contém FBS, DMSO, Glucose, Sais
Capacidade tampão: pH = 7,2 a 7,6
O Freeze Medium CM-1 da Cytion oferece uma solução fiável para a criopreservação, garantindo uma elevada viabilidade celular e funcionalidade pós-descongelamento para uma vasta gama de aplicações de investigação.59,00 €*Meio McCoys 5A (modificado), com: 3,0 g/L Glucose, com: Glutamina estável, com: 2,0 mM Piruvato de sódio, com: 2,2 g/L NaHCO3O meio 5A da McCoy é um meio altamente recomendado e especializado, concebido para facilitar o crescimento e a replicação de vírus em culturas de células primárias. Ganhou reconhecimento significativo pelo seu desempenho excecional em várias aplicações de investigação biológica. Uma aplicação proeminente do meio McCoy's 5A é a sua utilização na cultura de linhas celulares de carcinoma do cólon humano. Especificamente, tem sido empregado no estudo do receptor acoplado à proteína G rico em repetições de leucina (LGR5) e o seu papel na metástase do cancro do cólon. Este meio tem sido efetivamente empregado no cultivo de várias linhas celulares de carcinoma do cólon, incluindo HCT116, RKO, FET, CBS, HCT116b e TENN, permitindo aos investigadores aprofundar os mecanismos subjacentes à metástase do cancro do cólon. Além da sua aplicação na investigação do cancro, o meio McCoy's 5A provou ser indispensável no estudo dos osteoblastos. Os investigadores que estudam a reatividade iónica da hidroxiapatita deficiente em cálcio em meios de cultura celular padrão têm utilizado este meio para cultivar osteoblastos. Esta aplicação facilitou uma melhor compreensão das interações entre os osteoblastos e a hidroxiapatita deficiente em cálcio, contribuindo para os avanços no campo da investigação óssea. O meio McCoy's 5A foi meticulosamente formulado através da modificação dos aminoácidos encontrados no meio basal Eagle para fornecer suporte ideal às células tumorais do fígado. Esta formulação enriquecida permite a sua adequação a uma gama diversificada de linhas celulares estabelecidas, bem como a células primárias, aumentando ainda mais a sua versatilidade e aplicabilidade em vários contextos de investigação. O meio McCoy's 5A estende os seus efeitos bioquímicos e fisiológicos para além das células tumorais do fígado. Tem sido utilizado com sucesso para apoiar o crescimento em culturas primárias de medula óssea, pele, gengiva, rim, omento, adrenal, pulmão, baço, embrião de rato e outros tipos de células. Esta ampla gama de aplicações atesta a grande utilidade do meio McCoy's 5A no apoio ao crescimento e manutenção de vários tipos de células para uma investigação biológica abrangente. Formulação Este meio McCoy's 5A (modificado) contém 3,0 g/L de glicose, glutamina estável, 2,0 mM de piruvato de sódio e 2,2 g/L de NaHCO3. Controlo de qualidade pH = 7,2 +/
- 0,02 a 20-25 °C. Cada lote foi testado quanto à esterilidade e ausência de micoplasma e bactérias. Manutenção Manter refrigerado entre +2 °C e +8 °C, ao abrigo da luz. A congelação e o aquecimento até +37 °C minimizam a qualidade do produto. Não aqueça o meio a mais de 37 °C nem utilize fontes de calor incontroláveis (por exemplo, aparelhos de micro-ondas). Se apenas uma parte do meio for utilizada, retire essa quantidade do frasco e aqueça-a à temperatura ambiente. O prazo de validade de qualquer meio, exceto o meio básico, é de 6 a 8 semanas a partir da data de abertura. Composição Componentes mg/L Sais inorgânicosCloreto de cálcio x 2H2O132,00 Sulfato de magnésio97,67 Cloreto de potássio400 Cloreto de sódio6.460,00 Hidrogenofosfato dissódico (anidro)504,00 Outros componentesD(+)-Glicose (anidro)3.000,00 Glutationa (reduzida)0,5 Peptona de carne600,00 Sal de sódio do vermelho fenol11 AminoácidosL-alanina13,36 L-arginina x HCl42,14 L-Asparagina x H2O45,03 Ácido L-aspártico19,97 L-Cisteína x HCl x H2O31,75 L-glutamina (estável)219,15 Ácido L-glutâmico22,07 Glicina7,51 L-histidina x HCl x H2O20,96 L-hidroxiprolina19,67 L-isoleucina39,36 L-leucina39,36 L-Lisina x HCl36,54 L-Metionina14,92 L-fenilalanina16,52 L-Prolina17,27 L-Serina26,28 L-treonina17,87 L-triptofano3,06 Sal dissódico de L-tirosina26,10 L-Valina17,57 VitaminasÁcido p-aminobenzóico1,0 Ácido ascórbico0,56 D(+)-Biotina0,20 D-Pantotenato de cálcio0,20 Cloreto de colina5,0 Ácido fólico10,0 Mio-inositol36,00 Nicotinamida0,50 Ácido nicotínico0,5 Cloridrato de piridoxal0,50 Cloridrato de piridoxina0,50 Riboflavina0,20 Cloridrato de tiamina0,20 Vitamina B122,030,00 €*AccutaseVariantes: 100 mlReagente de Dissociação Celular Accutase
- Uma Alternativa Suave à Tripsina
Accutase é uma solução de descolamento celular que está a revolucionar a indústria da cultura celular. É uma mistura de enzimas proteolíticas e colagenolíticas que imita a ação da tripsina e da colagenase. Ao contrário da tripsina, o Accutase não contém quaisquer componentes de mamíferos ou bactérias e é muito mais suave para as células, o que o torna uma solução ideal para o descolamento rotineiro de células de material plástico de cultura de tecidos padrão e material plástico revestido de adesão. Nesta publicação do blogue, vamos explorar as vantagens e utilizações do Accutase e a forma como está a mudar o jogo na cultura de células.
Vantagens do Accutase
A Accutase tem várias vantagens em relação às soluções tradicionais de tripsina. Em primeiro lugar, pode ser utilizado sempre que for necessário um descolamento suave e eficiente de qualquer linha celular aderente, o que o torna um substituto direto da tripsina. Em segundo lugar, a Accutase funciona extremamente bem em células estaminais embrionárias e neuronais, tendo sido demonstrado que mantém a viabilidade destas células após a passagem. Em terceiro lugar, a Accutase preserva a maioria dos epítopos para posterior análise por citometria de fluxo, tornando-a ideal para a análise de marcadores de superfície celular.
Além disso, a Accutase não necessita de ser neutralizada aquando da passagem das células aderentes. A adição de mais meios após a divisão das células dilui a Accutase de modo a que esta deixe de ser capaz de destacar as células. Isto elimina a necessidade de um passo de inativação e poupa tempo aos técnicos de cultura de células. Finalmente, o Accutase não precisa de ser aliquotado e um frasco mantém-se estável no frigorífico durante 2 meses.
Aplicações do Accutase
Accutase é um substituto direto da solução de tripsina e pode ser utilizado para a passagem de linhas celulares. Além disso, Accutase tem um bom desempenho na separação de células para a análise de muitos marcadores de superfície celular utilizando citometria de fluxo e para a seleção de células. Outras aplicações a jusante do tratamento com Accutase incluem a análise de marcadores de superfície celular, ensaio de crescimento de vírus, proliferação celular, ensaios de migração de células tumorais, passagem celular de rotina, aumento da escala de produção (bioreactor) e citometria de fluxo.
Composição do Accutase
Accutase não contém componentes de mamíferos ou bactérias e é uma mistura de enzimas naturais com atividade enzimática proteolítica e colagenolítica. É formulado numa concentração muito mais baixa do que a tripsina e a colagenase, tornando-o menos tóxico e mais suave, mas igualmente eficaz.
Eficácia do Accutase
O Accutase demonstrou ser eficiente na separação de células primárias e estaminais e na manutenção de uma elevada viabilidade celular em comparação com enzimas de origem animal, como a tripsina. 100% das células são recuperadas ao fim de 10 minutos e não há qualquer problema em deixar as células no Accutase até 45 minutos, graças à autodigestão do Accutase.
Em resumo
Em conclusão, o Accutase é uma solução poderosa que está a mudar o jogo na cultura de células. Com a sua natureza suave, eficiência e versatilidade, Accutase é a alternativa ideal à tripsina. Se procura uma solução fiável e eficiente para o descolamento de células, Accutase é a solução para si.75,00 €*Solução de antibiótico/antimicótico (100x)Visão geral do produto
Volume: 100 ml Armazenamento: ≤-15°C Esterilidade: Estéril-filtrado
A Solução Antibiótica/Antimicótica (100x) é um concentrado estéril, pronto a usar, concebido para reduzir os riscos de contaminação microbiana em culturas celulares e aplicações laboratoriais relacionadas. Esta solução 100x contém uma combinação bem estabelecida de penicilina, estreptomicina e anfotericina B, proporcionando uma atividade antimicrobiana de largo espetro contra bactérias Gram-positivas e Gram-negativas, leveduras e fungos filamentosos. A formulação é adequada para utilização em culturas de células eucarióticas, meios bacterianos e outros sistemas sensíveis à contaminação, apoiando operações laboratoriais limpas e consistentes.
Aplicação e benefícios Optimizada para protocolos de investigação de rotina, esta solução é amplamente utilizada para manter condições assépticas em fluxos de trabalho de cultura de células. Oferece um desempenho fiável em ambientes sensíveis à contaminação, ajudando os investigadores a reduzir o risco de crescimento microbiano excessivo sem comprometer a saúde das células ou a reprodutibilidade experimental. A formulação estéril-filtrada elimina a necessidade de etapas adicionais de solubilização, apoiando a preparação simplificada de meios e reduzindo a variabilidade nos procedimentos laboratoriais diários.
Utilização e compatibilidade Para obter concentrações de trabalho padrão, diluir a solução 1:100 no seu meio de cultura completo. O produto é compatível com uma vasta gama de linhas celulares de mamíferos e meios basais. Com uma disponibilidade de stock consistente, os investigadores beneficiam de uma continuidade de fornecimento fiável e de um planeamento logístico simplificado. A solução deve ser armazenada a ≤ -15 °C e protegida de ciclos repetidos de congelamento e descongelamento para manter a estabilidade. Apenas para uso em investigação. Não se destina a ser utilizado em procedimentos de diagnóstico ou terapêuticos. Não se destina a ser utilizado em seres humanos ou animais.45,00 €*PBSSolução salina tamponada com fosfato (PBS)
A solução salina tamponada com fosfato (PBS) é uma solução tampão amplamente utilizada na investigação biológica e química. Desempenha um papel crucial na manutenção do equilíbrio do pH e da osmolaridade durante vários procedimentos experimentais, incluindo o processamento de tecidos e a cultura de células. A nossa solução PBS é meticulosamente formulada com ingredientes de elevada pureza para garantir estabilidade e fiabilidade em todas as experiências. A osmolaridade e as concentrações de iões do nosso PBS imitam de perto as do corpo humano, tornando-o isotónico e não tóxico para a maioria das células.
Composição da nossa solução PBS
A nossa solução PBS é uma mistura com pH ajustado de tampões de fosfato de grau ultrapuro e soluções salinas. Numa concentração de trabalho 1X, contém
8000 mg/L de cloreto de sódio (NaCl)
200 mg/L de cloreto de potássio (KCl)
1150 mg/L Fosfato de sódio dibásico anidro (Na2HPO4)
200 mg/L Fosfato de potássio monobásico anidro (KH2PO4)
Esta composição assegura um pH e um equilíbrio iónico óptimos, adequados a uma vasta gama de aplicações biológicas.
Aplicações da nossa solução PBS
A nossa solução PBS é ideal para várias aplicações na investigação biológica. As suas propriedades isotónicas e não tóxicas tornam-na adequada para a diluição de substâncias e lavagem de recipientes de células. As soluções PBS que contêm EDTA são eficazes para desprender células ligadas e aglomeradas. No entanto, os metais divalentes, como o zinco, não devem ser adicionados ao PBS, uma vez que podem causar precipitação. Nestes casos, recomenda-se a utilização de tampões Good's. Além disso, a nossa solução de PBS é uma alternativa aceitável ao meio de transporte viral para o transporte e armazenamento de vírus de ARN, incluindo o SARS-CoV-2.
Controlo de qualidade
Estéril-filtrado
Armazenamento e prazo de validade
Armazenar entre +2°C e +25°C, protegido da luz.
Depois de aberto, conservar a uma temperatura entre 2°C e 25°C e utilizar no prazo de 24 meses.
Condições de transporte
Temperatura ambiente
Manutenção
Manter refrigerado a uma temperatura entre +2°C e +8°C, ao abrigo da luz. Evitar o congelamento e o aquecimento frequente a +37°C, uma vez que reduz a qualidade do produto.
Não aquecer o meio para além de 37°C nem utilizar fontes de calor não controladas, tais como aparelhos de micro-ondas.
Se apenas uma parte do meio for utilizada, retirar a quantidade necessária e aquecê-la à temperatura ambiente antes de a utilizar.
Composição
Categoria
Componentes
Concentração (mg/L)
Sais
Cloreto de potássio
200
Fosfato de potássio monobásico anidro
200
Cloreto de sódio
8000
Fosfato de sódio dibásico anidro
115020,00 €* -
Produtos relacionados
Produtos relacionados