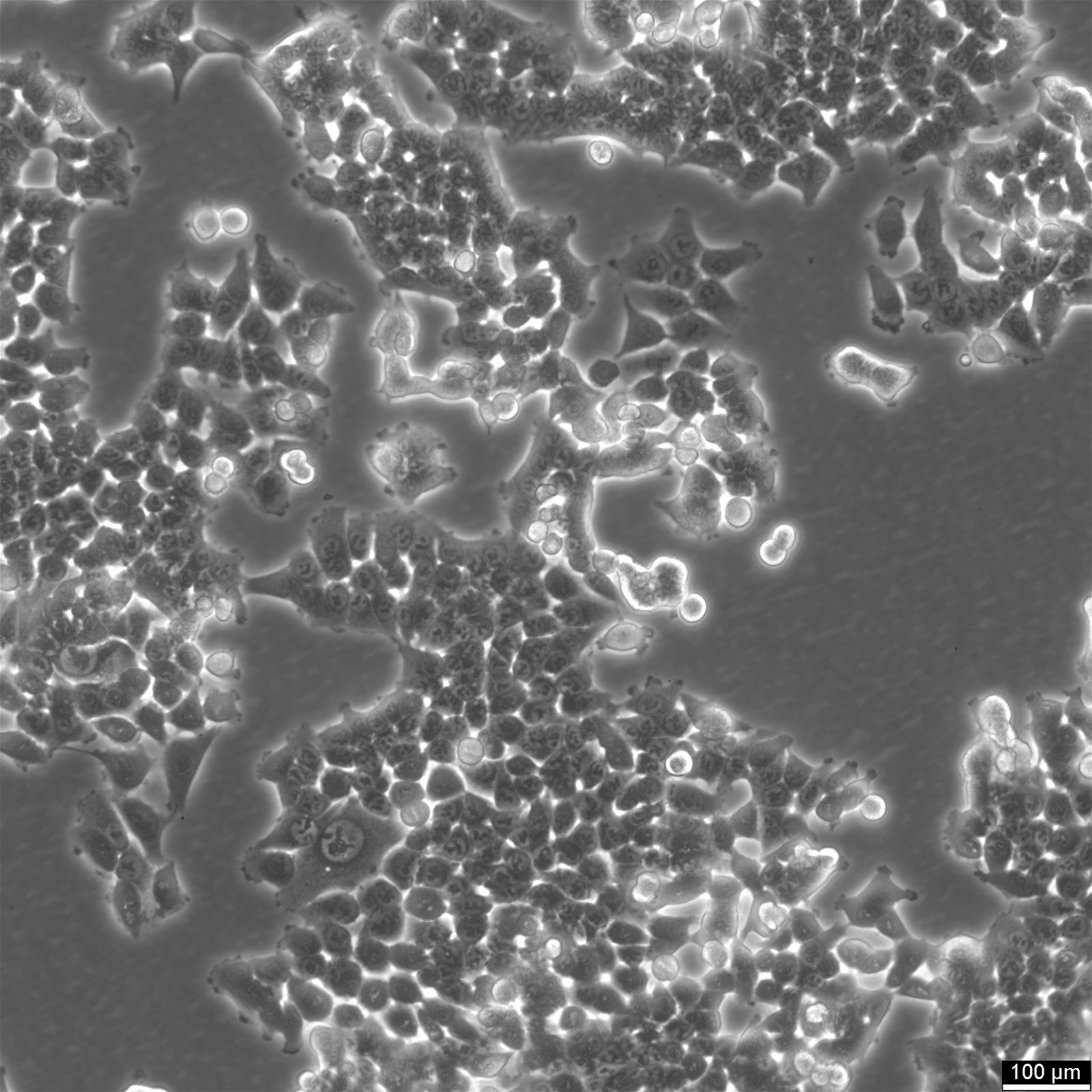
HCT116-cellelinjen: En hjørnestein i forskningen på kolorektal kreft
HCT116-cellelinjen er en hjørnestein i utforskningen av kolorektal kreft, og gir uvurderlig innsikt i sykdommens patogenese og potensielle terapeutiske muligheter. HCT116 er kjent for sin anvendelighet i kreftforskning og farmakologiske evalueringer, og gjør det mulig å gjennomføre viktige studier av tumoratferd og medikamenteffekt.
HCT116-cellenes opprinnelse og grunnleggende egenskaper
Å forstå HCT116-cellenes opprinnelse og grunnleggende egenskaper, som deres morfologiske trekk, genetiske sammensetning og cellulære dimensjoner, er avgjørende for forskere som skal gjennomføre studier med denne cellelinjen.
Opprinnelse oggenetisk landskap: HCT116-cellene stammer fra tykktarmen til en 48 år gammel kaukasisk mann som ble diagnostisert med kolorektal kreft, og de er kjennetegnet av en mutasjon i kodon 13 (G13D) i KRAS-genet, som er en del av RAS/RAF/MEK/ERK-signalveien. Denne spesielle mutasjonen er avgjørende for den onkogene transformasjonen av disse cellene, noe som understreker deres relevans i kreftforskningen.
Morfologi og vekstkarakteristika: HCT116-celler har en epitel-lignende morfologi og vokser vanligvis i monolagskulturer, men kan også danne sfæroider med en diameter på 150-400 µm. Denne tilpasningsdyktigheten i vekstmønsteret understreker deres allsidighet i ulike eksperimentelle oppsett.
Kromosomal profil: Kromosomsammensetningen i HCT116-celler er nesten diploid, og ca. 70 % av cellepopulasjonen har 45 kromosomer. Det er spesielt en tilbakevendende amplifikasjon i de lange armene av kromosom 8, 10, 16 og 17, mens kromosom Y er fraværende, noe som bidrar til deres unike genomiske signatur.
Sammenlignende analyse: HCT116 vs. HT29-cellelinjer
Når vi sammenligner HCT116 med HT29, en annen human kolorektal karsinomcellelinje, ser vi tydelige forskjeller i deres onkogene potensial og differensieringsevne:
Onkogen aggressivitet og differensiering: HCT116-celler kjennetegnes av høy onkogen aggressivitet og begrenset differensieringspotensial, noe som gjør dem til en modell for studier av aggressive tumorfenotyper. HT29-celler har derimot evnen til å differensiere seg til enterocyttlignende og mucinproduserende linjer, noe som gir en kontrasterende modell som etterligner ulike aspekter ved biologien til kolorektal kreft.
Denne komparative forståelsen av HCT116- og HT29-cellelinjene beriker forskernes verktøykasse, noe som muliggjør mer nyanserte undersøkelser av kolorektalkreftens mangefasetterte natur.
Håndtering av HCT116-celler
|
Fordoblingstid: |
Doblingstiden for HCT116-kreftceller varierer fra 25 til 35 timer. |
|
Adherent eller i suspensjon: |
HCT116-cellelinjen for tykktarmskreft er adherent, med celler som vokser i monolag. |
|
Såingstetthet: |
En såingstetthet på 2 x104 celler/cm2 anbefales for HCT116-cellekulturen. Ved subkulturering skal cellene løsnes ved hjelp av Accutase-løsning etter en 1x PBS-vask. Etter sentrifugering resuspenderes cellepelleten i nytt vekstmedium og overføres til en ny kolbe. |
|
Vekstmedium: |
McCoys 5a medium, supplert med 3,0 g/L L-glukose, 1,5 mM L-glutamin, 3,0 g/L NaHCO3 og 10 % føtalt bovint serum, er optimalt for dyrking av HCT116-celler. Det anbefales å fornye mediet 1 til 2 ganger per uke. |
|
Vekstbetingelser (temperatur,CO2): |
Dyrking foregår i en befuktet inkubator ved 37 °C med enCO2-atmosfære på 5 %. |
|
Oppbevaring: |
HCT116-celler kan oppbevares ved temperaturer under -150 °C i enten damp- eller væskefasen av flytende nitrogen. |
|
Fryseprosess og medium: |
Bruk CM-1- eller CM-ACF-medium til kryopreservering. Det anbefales å bruke en frysemetode med kontrollert hastighet, som gir en gradvis temperatursenkning på 1 °C per minutt, noe som bidrar til å opprettholde cellenes levedyktighet. |
|
Prosess for tining: |
Tine HCT116-celler i et vannbad på 37 °C. Etter tilsetning av vekstmedium, sentrifuger for å fjerne rester av frysemedium. Resuspender cellepelleten i nytt medium og dyrk i nye kolber. |
|
Biosikkerhetsnivå: |
Nivå 1 |
Fordeler med HCT116-cellelinjen
I dette avsnittet går vi nærmere inn på HCT116-cellelinjen, belyser dens sentrale rolle i kreftforskningen, spesielt i studier av kolorektal kreft, og diskuterer dens iboende fordeler.
HCT116-cellelinjen skiller seg ut i kreftforskningen på grunn av flere viktige fordeler:
Modell for kolorektal kreft: Den er en anerkjent in vitro-modell for kolorektal kreft, den tredje vanligste kreftformen på verdensbasis. Dens relevans for å etterligne kolorektal kreft hos mennesker gjør den uvurderlig for å forstå kreftbiologi og teste ut behandlingsstrategier.
Homogenitet: Det er bemerkelsesverdig at rundt 70 % av HCT116-cellene har konsistente genetiske profiler, noe som gir en relativt homogen populasjon. Denne ensartetheten er avgjørende for studier som fokuserer på genuttrykk, cellulære signalveier og vurdering av effekten av medikamentell behandling, ettersom den sikrer konsistens og pålitelighet i de eksperimentelle resultatene.
Transfeksjonseffektivitet: Et av HCT116-cellenes fremste kjennetegn er at de er svært lette å transfektere, spesielt med virale vektorer. Denne egenskapen er spesielt fordelaktig i genterapiforskning, ettersom den gjør det mulig å introdusere genetisk materiale med effektivitet og presisjon, noe som legger til rette for avanserte genetiske manipulasjoner og funksjonelle studier.
Gjør nye oppdagelser med vår autentiserte HCT116-cellelinje
Bruksområder for HCT116-cellelinjen i forskning
HCT116-cellelinjen har et bredt spekter av bruksområder innen kreftforskning. Noen fremtredende bruksområder er
Kreftbiologi
HCT116-cellelinjen brukes til å studere progresjon og utvikling av tykktarmskreft. I tillegg bidrar den til å belyse de underliggende mekanismene og signalveiene som er involvert i kreftspredning, migrasjon og invasjon. I en studie ble HCT116-celler brukt til å studere gener som er involvert i utvikling av legemiddelresistens. Forskerne overuttrykte MDR1-genet i tykktarmskreftceller og observerte uttrykket av NOX-isoformer (NADPH-oksid) og Nrf2. Studien avslørte at oppregulering av NOX2 og Nrf2 forårsaker kjemoresistens i kreftceller, og disse genene kan derfor brukes som mål for å overvinne resistensutvikling under kreftbehandling [1]. På samme måte rapporterte forskning utført i 2021 at NF-κB-signalveien er involvert i reguleringen av proliferasjon og migrasjon av tykktarmskreft. Dermed kan den brukes som mål for å utvikle nye og effektive behandlingsmetoder mot kolorektalt karsinom [2].
Innen onkologi er det grunnleggende å forstå de intrikate prosessene i cellesyklus, proliferasjon og vekst samt apoptose. Disse biologiske funksjonene er sentrale i studiet av humane cellelinjer, særlig de som stammer fra ondartede celler, som humane tykktarmskreftceller og bukspyttkjertelkreftmodeller. HCT116- og SW620-cellelinjene, for eksempel, er avgjørende for å utforske mekanismene som ligger til grunn for henholdsvis tykktarmskreft og bukspyttkjertelkreft. Ved hjelp av teknikker som flowcytometri og klonogene assays kan forskerne belyse genuttrykksprofilene og oppførselen til uavhengige celler i svulster, og dermed kaste lys over hvordan kreft kommuniserer i den ekstracellulære matrisen.
Apoptosens rolle i kreftprogresjon
Apoptose, eller programmert celledød, spiller en avgjørende rolle i opprettholdelsen av cellulær homeostase og er et sentralt forskningsområde innen kreftforskning. Det er avgjørende å skille mellom ikke-relatert apoptose og apoptose som er spesifikt indusert i forbindelse med kreft, for eksempel celledød ved tykktarmskreft. Denne prosessen handler ikke bare om eliminering av celler, men involverer et komplekst samspill av signaler som kan påvirke tumorvekst og metastase. Ved å undersøke apoptose og celledød i sammenheng med metastasesuppressorer og tumorsuppressoraktivitet kan forskerne få innsikt i hvilke veier som regulerer kreftprogresjon og metastatisk potensial.
Metastase og molekylære markører i kreft
Metastasering er fortsatt et av de mest utfordrende aspektene ved kreft, og hematogen metastasering er et viktig problem når det gjelder spredning av ondartede celler. Utforskningen av metastasering innebærer å studere kreftcellenes evne til å bevege seg og invadere, eller cellelokomotivasjon, og hvordan cellene samhandler med omgivelsene, inkludert den ekstracellulære matriksen. Molekylære markører som CD133-uttrykk og den epidermale vekstfaktorreseptoren er avgjørende for å identifisere og forstå atferden til positive tykktarmskreftceller og andre krefttyper. SIRT6-stien, for eksempel, har dukket opp som et område av interesse på grunn av sin potensielle rolle i modulering av tumorvekst og metastatisk tykktarmskreft.
Toksikologi/utvikling av legemidler
HCT116-cellelinjen brukes som screeningmodell for nye kreftlegemidler. Det er gjennomført flere studier for å vurdere effekt og toksisitet av kreftlegemidler, inkludert naturlige produkter og kjemisk syntetiserte nanopartikler. Forskerne vurderte cytotoksisiteten til syntetiserte sølvnanopartikler fra ekstrakter av et urtemedisin, Caesalpinia pulcherrima , i HCT116-celler [3]. I en studie brukte forskerne HCT116-kreftcellelinjen til å evaluere det krefthemmende potensialet til ekstrakt av kakao-tevann. De fant at kakaoteekstrakt reduserer spredning av tykktarmskreft og induserer celledød [4]. Enannen studie brukte HCT116-kreftceller og oppdaget at ekstrakter avluftpotet ,Dioscorea bulbifera, utviser pro-apoptotisk aktivitet i kolorektale karsinomceller via aktivering av JNK-signalkaskaden og undertrykkelse av ERK1/2-genet [5].
Metformins effekt på kreftceller, særlig i forbindelse med kreft i tykktarm og bukspyttkjertel, er et eksempel på hvordan forståelse av kreftcellenes biologiske funksjoner kan føre til potensielle behandlingsstrategier. Forskning på kreftcellers klonogene overlevelse, eller evne til å danne kloner, ved behandling med stoffer som metformin eller ved behandling rettet mot spesifikke signalveier som den epidermale vekstfaktorreseptoren, kan gi verdifull innsikt i effektive kreftbehandlinger. I tillegg gir bruken av HCT116-kloner og HCT116-cellepopulasjoner i disse studiene en nyansert forståelse av hvordan kreftceller reagerer på ulike terapeutiske intervensjoner, noe som baner vei for mer persontilpassede tilnærminger til kreftbehandling.
HCT116-celler: Forskningspublikasjoner
I dette avsnittet går vi gjennom noen av de viktigste og mest siterte publikasjonene med HCT116-cellelinjen.
Denne studien ble publisert i Journal of Photochemistry and Photobiology B: Biology (2017). Forskerne brukte HCT116 tykktarmskreft- og A549 lungekreftcellelinjer for å evaluere de cytotoksiske effektene av piper nigrum-frømedierte syntetiserte tinnoksydnanopartikler.
Denne forskningen i Cancer Letters (2018) foreslår at lncRNA SNHG15 fremmer migrasjon av tykktarmskreftceller i cellelinjer for tykktarmskreft, inkludert HCT116.
Overuttrykk av det lange ikke-kodende RNA-et TUG1 fremmer utviklingen av tykktarmskreft
Denne artikkelen ble publisert i tidsskriftet Medical Science Monitor i 2016. Studien fant at det onkogene LncRNA TUG1 fremmer spredning og migrasjon av HCT116 tykktarmskreftceller.
Denne forskningen i tidsskriftet Biochemical Pharmacology (2018) foreslår at utvikling av legemiddelresistens øker nivåene av H2S-produserende enzymer i HCT116 tykktarmskreftceller.
Denne forskningsartikkelen i International Journal of Environmental Health Research (2023) foreslår at Inula viscosa L. ekstrakt utøver en krefthemmende effekt på HCT116 tykktarmskreftceller via regulering av mikroRNA.
Ressurser for HCT116-celler
Nedenfor finner du noen ressurser om HCT116-celler.
- Transfeksjon av HCT116: Denne videoen er en trinnvis veiledning for transfeksjon av HCT116-kreftceller.
- Dyrking av HCT116-cellelinjen: Denne videoen viser subkultureringsprotokollen for HCT116-cellelinjen for tykktarmskreft.
- Subkulturering av HCT116-cellelinjen: Dette nettstedet inneholder mye nyttig informasjon om HCT116-dyrkingsmediet. I tillegg gir den prosedyrer for frysing, tining og subkulturering av celler.
Ofte stilte spørsmål om HCT116-celler
referanser
- Waghela, B.N., F.U. Vaidya og C. Pathak: Oppregulering av NOX-2 og Nrf-2 fremmer 5-fluorouracil-resistens i humane tykktarmskarsinomceller (HCT-116). Biokjemi (Moskva), 2021, 86, s. 262-274.
- Yang, M., et al., Astragalin hemmer spredning og migrasjon av humane tykktarmskreft HCT116-celler ved å regulere NF-κB-signalveien. Frontiers in Pharmacology, 2021, 12: s. 639256.
- Deepika, S., C.I. Selvaraj og S.M. Roopan, Screening av bioaktiviteter av Caesalpinia pulcherrima L. swartz og cytotoksisitet av ekstraktsyntetiserte sølvnanopartikler på HCT116-cellelinjen. Materialvitenskap og ingeniørfag, C, 2020, 106, s. 110279.
- Gao, X., et al., Kakao-te (Camellia ptilophylla) induserer mitokondriavhengig apoptose i HCT116-celler via ROS-generering og PI3K / Akt-signalveien. Food Research International, 2020, 129, s. 108854.
- Hidayat, AFA, et al., Dioscorea bulbifera induserte apoptose gjennom hemming av ERK 1/2 og aktivering av JNK-signalveier i HCT116 humane kolorektale karsinomceller. Biomedisin og farmakoterapi, 2018. 104: p. 806-816.