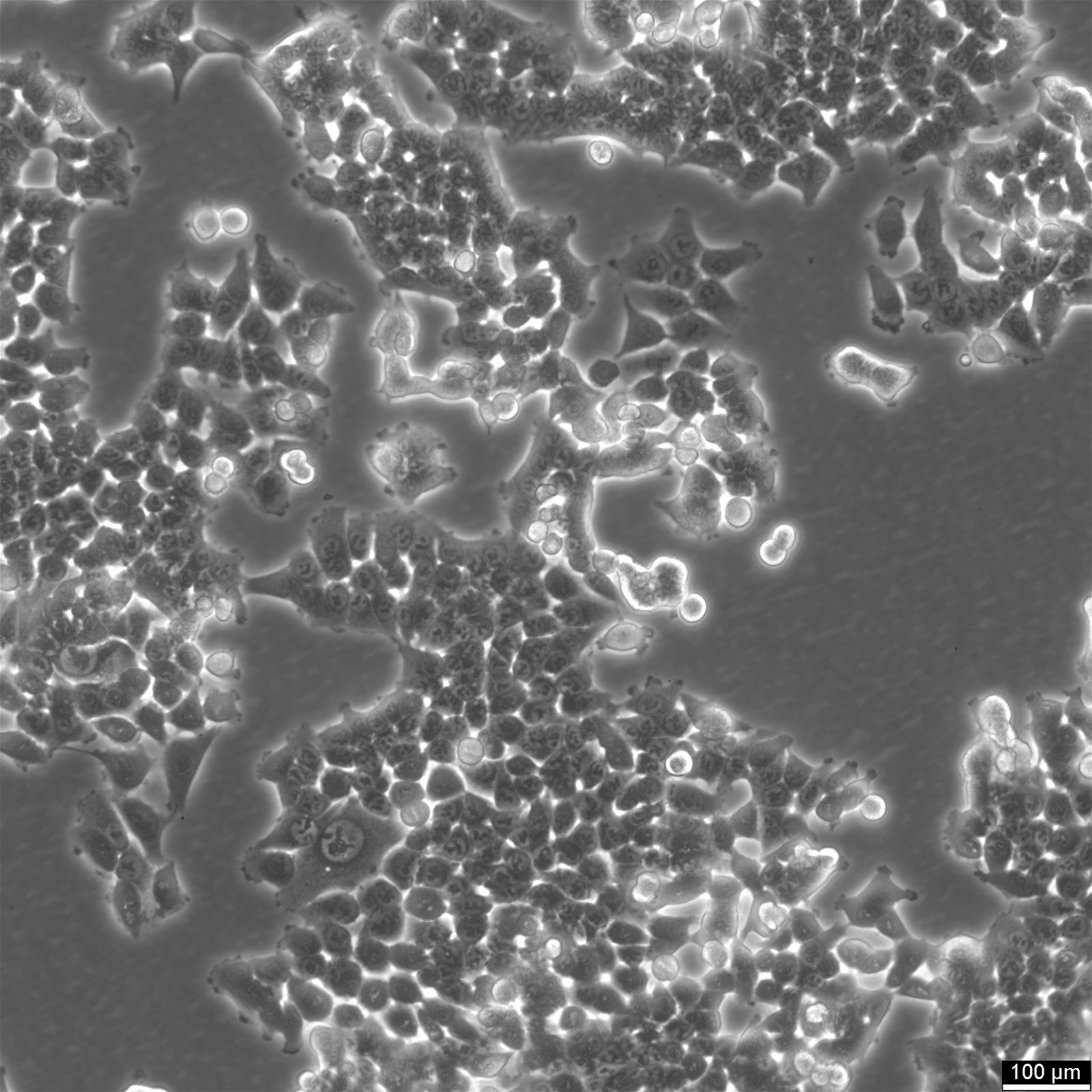
Клітинна лінія HCT116: Стовп у дослідженні колоректального раку
Клітинна лінія HCT116 слугує наріжним каменем у дослідженні колоректального раку, пропонуючи безцінну інформацію про патогенез захворювання та потенційні терапевтичні шляхи. Відома своєю корисністю в дослідженнях раку та фармакологічних оцінках, HCT116 сприяє проведенню ключових досліджень поведінки пухлини та ефективності ліків.
Походження та основні характеристики клітин HCT116
Розуміння походження та основних характеристик клітин HCT116, таких як морфологічні особливості, генетичний склад та розміри клітин, є важливим для дослідників, які розпочинають дослідження з використанням цієї клітинної лінії.
Походження та генетичний ландшафт: Клітини HCT116, отримані з товстої кишки 48-річного чоловіка європеоїдної раси з діагнозом колоректальний рак, відрізняються мутацією в кодоні 13 (G13D) гена KRAS, що є частиною сигнального шляху RAS/RAF/MEK/ERK. Саме ця мутація є ключовою в онкогенній трансформації цих клітин, що підкреслює їх актуальність для дослідження раку.
Морфологія та характеристики росту: Виявляючи епітеліальну морфологію, клітини HCT116 зазвичай ростуть в моношарових культурах, але також можуть утворювати сфероїди діаметром 150-400 мкм. Така пристосованість до різних форм росту підкреслює їхню універсальність у різних експериментальних умовах.
Хромосомний профіль: Хромосомний склад клітин HCT116 є майже диплоїдним, приблизно 70% клітинної популяції містить 45 хромосом. Примітно, що в довгих плечах хромосом 8, 10, 16 і 17 спостерігається реципрокна ампліфікація, тоді як хромосома Y відсутня, що сприяє їх унікальному геномному підпису.
Порівняльний аналіз: клітинні лінії HCT116 та HT29
При порівнянні HCT116 з HT29, іншою клітинною лінією колоректальної карциноми людини, виявляються чіткі відмінності в їх онкогенному потенціалі та здатності до диференціювання:
Онкогенна агресивність та диференціювання: Клітини HCT116 характеризуються високою онкогенною агресивністю та обмеженим диференціювальним потенціалом, що робить їх моделлю для вивчення агресивних фенотипів пухлин. На відміну від них, клітини HT29 демонструють здатність диференціюватися в ентероцитоподібні та муцин-продукуючі лінії, забезпечуючи контрастну модель, яка імітує різноманітні аспекти біології колоректального раку.
Таке порівняльне розуміння клітинних ліній HCT116 і HT29 збагачує інструментарій, доступний дослідникам, дозволяючи проводити більш тонкі дослідження багатогранної природи колоректального раку.
Робота з клітинами HCT116
|
Час подвоєння: |
Час подвоєння ракових клітин HCT116 становить від 25 до 35 годин. |
|
Адгезія або суспензія: |
Клітинна лінія раку товстої кишки HCT116 є адгезивною, тобто клітини ростуть моношаром. |
|
Щільність посіву: |
Для культури клітин HCT116 рекомендується щільність посіву 2 x104 клітин/см2. Для субкультивування клітини слід відокремити за допомогою розчину аккутази після відмивання 1х PBS. Після центрифугування осад клітин ресуспендують у свіжому живильному середовищі і переносять у нову колбу. |
|
Поживне середовище: |
Середовище McCoys 5a, доповнене 3,0 г/л L-глюкози, 1,5 мМ L-глутаміну, 3,0 г/л NaHCO3 та 10% ембріональної бичачої сироватки, є оптимальним для культивування клітин HCT116. Рекомендується оновлювати середовище 1-2 рази на тиждень. |
|
Умови росту (температура, CO2): |
Культивування відбувається у зволоженому інкубаторі при 37°C з 5%-ним вмістом CO2. |
|
Зберігання: |
Клітини HCT116 можна зберігати при температурі нижче -150°C у паровій або рідкій фазі рідкого азоту. |
|
Процес і середовище заморожування: |
Для кріоконсервування використовуйте середовище CM-1 або CM-ACF. Рекомендується метод заморожування з контрольованою швидкістю, що дозволяє поступово знижувати температуру на 1°C за хвилину, що допомагає підтримувати життєздатність клітин. |
|
Процес розморожування: |
Розморозьте клітини HCT116 на водяній бані при 37°C. Після додавання живильного середовища центрифугуйте, щоб видалити залишки замороженого середовища. Повторно суспендуйте гранули клітин у свіжому середовищі та культивуйте в нових колбах. |
|
Рівень біобезпеки: |
Рівень 1 |
Переваги клітинної лінії HCT116
У цьому розділі розглядається клітинна лінія HCT116, підкреслюється її ключова роль у дослідженнях раку, зокрема у вивченні колоректального раку, а також обговорюються притаманні їй переваги.
Клітинна лінія HCT116 виділяється в дослідженнях раку завдяки кільком ключовим перевагам:
Модель колоректального раку: Вона слугує широко визнаною моделлю колоректального раку in vitro, третьої за поширеністю онкологічної хвороби у світі. Його відповідність до імітації колоректального раку людини робить його безцінним для розуміння біології раку і тестування терапевтичних стратегій.
Однорідність: Примітно, що близько 70% клітин HCT116 мають однакові генетичні профілі, що забезпечує відносно однорідну популяцію. Ця однорідність має вирішальне значення для досліджень, спрямованих на вивчення експресії генів, клітинних сигнальних шляхів та оцінки ефективності медикаментозного лікування, оскільки вона забезпечує послідовність і надійність результатів експериментів.
Ефективність трансфекції: Однією з особливостей клітин HCT116 є їхня висока здатність до трансфекції, особливо за допомогою вірусних векторів. Ця характеристика є особливо корисною в дослідженнях генної терапії, дозволяючи вводити генетичний матеріал з ефективністю і точністю, полегшуючи таким чином проведення складних генетичних маніпуляцій і функціональних досліджень.
Здійснюйте свої відкриття з нашою аутентифікованою клітинною лінією HCT116
Дослідницькі застосування клітинної лінії HCT116
Клітинна лінія HCT116 має широкий спектр застосування в дослідженнях раку. Деякі з них є найбільш відомими:
Біологія раку
Клітинна лінія раку товстої кишки HCT116 використовується для вивчення прогресування та розвитку раку товстої кишки. Крім того, вона допомагає з'ясувати основні механізми та сигнальні шляхи, що беруть участь у проліферації, міграції та інвазії раку. В одному з досліджень клітини HCT116 використовували для вивчення генів, що беруть участь у розвитку резистентності до лікарських препаратів. Дослідники надмірно експресували ген MDR1 в клітинах раку товстої кишки і спостерігали за експресією ізоформ NOX (оксиду NADPH) та Nrf2. Дослідження показало, що підвищення регуляції NOX2 та Nrf2 спричиняє хіміорезистентність ракових клітин, а отже, ці гени можуть бути мішенями для подолання розвитку резистентності під час терапії раку [1]. Аналогічно, дослідження, проведене у 2021 році, показало, що сигнальний шлях NF-κB бере участь у регуляції проліферації та міграції раку товстої кишки. Таким чином, він може стати мішенню для розробки нових ефективних терапевтичних засобів проти колоректальної карциноми [2].
У сфері онкології розуміння складних процесів клітинного циклу, проліферації та росту, а також апоптозу є фундаментальним. Ці біологічні функції є ключовими у вивченні клітинних ліній людини, особливо тих, що отримані зі злоякісних клітин, таких як клітини раку товстої кишки людини та моделі раку підшлункової залози. Наприклад, клітинні лінії HCT116 і SW620 допомагають вивчати механізми, що лежать в основі раку товстої кишки і підшлункової залози відповідно. За допомогою таких методів, як проточна цитометрія та клоногенні аналізи, дослідники можуть з'ясувати профілі експресії генів та поведінку окремих клітин у пухлинах, проливаючи світло на те, як рак взаємодіє з позаклітинним матриксом.
Роль апоптозу в прогресуванні раку
Апоптоз, або запрограмована загибель клітин, відіграє важливу роль у підтримці клітинного гомеостазу і є ключовим напрямком дослідження раку. Різниця між не пов'язаним з раком апоптозом і апоптозом, специфічно індукованим в контексті раку, наприклад, загибеллю клітин раку товстої кишки, має вирішальне значення. Цей процес полягає не просто в усуненні клітин, а включає складну взаємодію сигналів, які можуть впливати на ріст пухлини і метастазування. Вивчаючи апоптоз і загибель клітин у поєднанні з супресорами метастазування і пухлинною супресорною активністю, вчені можуть отримати уявлення про шляхи, які регулюють прогресування раку і метастатичний потенціал.
Метастазування та молекулярні маркери при раку
Метастазування залишається одним з найбільш грізних аспектів раку, причому гематогенне метастазування викликає значне занепокоєння у поширенні злоякісних клітин. Дослідження метастазування передбачає вивчення здатності ракових клітин до переміщення та інвазії, або клітинної локомоції, а також того, як клітини взаємодіють з навколишнім середовищем, включаючи позаклітинний матрикс. Молекулярні маркери, такі як експресія CD133 і рецептор епідермального фактора росту, мають вирішальне значення для ідентифікації та розуміння поведінки позитивних клітин карциноми товстої кишки та інших типів раку. Наприклад, шлях SIRT6 став об'єктом інтересу через його потенційну роль у модулюванні росту пухлин і метастатичного раку товстої кишки.
Токсикологія/розробка ліків
Клітинну лінію HCT116 використовують як скринінгову модель для розробки нових протиракових препаратів. Було проведено кілька досліджень для оцінки ефективності та токсичності протиракових препаратів, включаючи природні продукти та хімічно синтезовані наночастинки. Так, у дослідженні оцінювали цитотоксичність синтезованих наночастинок срібла з екстрактів рослинного препарату Caesalpinia pulcherrima в клітинах HCT116 [3]. У дослідженні вчені використовували лінію ракових клітин HCT116 для оцінки протиракового потенціалу водного екстракту какао-чаю. Вони виявили, що екстракт какао-чаю зменшує проліферацію раку товстої кишки та індукує загибель клітин [4]. В іншому дослідженні на ракових клітинах HCT116 було виявлено, що екстрактиповітряної картоплі ( Dioscorea bulbifera ) проявляють проапоптотичну активність у клітинах колоректальної карциноми шляхом активації сигнального каскаду JNK та пригнічення гена ERK1/2 [5].
Вплив метформіну на ракові клітини, особливо в контексті раку товстої кишки та підшлункової залози, є прикладом того, як розуміння біологічних функцій ракових клітин може призвести до потенційних терапевтичних стратегій. Дослідження клоногенного виживання, або здатності утворювати клони, ракових клітин після лікування такими препаратами, як метформін, або впливу на конкретні шляхи, такі як рецептор епідермального фактору росту, можуть надати цінну інформацію для ефективного лікування раку. Крім того, використання клонів HCT116 і клітинних популяцій HCT116 у цих дослідженнях дозволяє краще зрозуміти, як ракові клітини реагують на різні терапевтичні втручання, що відкриває шлях до більш персоналізованих підходів у лікуванні раку.
Клітини HCT116: Дослідницькі публікації
У цьому розділі ми розглянемо декілька важливих і найбільш цитованих останніх публікацій, присвячених дослідженню клітинної лінії HCT116.
Це дослідження було опубліковано в Journal of Photochemistry and Photobiology B: Biology (2017). Дослідники використовували клітинні лінії раку товстої кишки HCT116 та раку легенів A549 для оцінки цитотоксичних ефектів синтезованих наночастинок оксиду олова, опосередкованих насінням дудника чорного (piper nigrum).
Це дослідження в Cancer Letters (2018) припускає, що lncRNA SNHG15 сприяє міграції клітин раку товстої кишки в клітинних лініях колоректального раку, включаючи HCT116.
Надмірна експресія довгої некодуючої РНК TUG1 сприяє прогресуванню раку товстої кишки
Ця робота була опублікована в журналі Medical Science Monitor у 2016 році. Дослідження показало, що онкогенна LncRNA TUG1 сприяє проліферації та міграції клітин раку товстої кишки HCT116.
Дослідження, опубліковане в журналі Biochemical Pharmacology (2018), свідчить про те, що розвиток резистентності до лікарських препаратів підвищує рівень H2S-продукуючих ферментів у клітинах раку товстої кишки HCT116.
У цій науковій статті, опублікованій у Міжнародному журналі досліджень екологічного здоров'я (2023), припускається, що екстракт Inula viscosa L. чинить протиракову дію на клітини колоректального раку HCT116 шляхом регуляції мікроРНК.
Ресурси для клітин HCT116
Нижче наведено кілька ресурсів про клітини HCT116.
- Трансфекція HCT116: Це відео є покроковим посібником з трансфекції ракових клітин HCT116.
- Культивування клітинної лінії HCT116: У цьому відео показано протокол субкультивування клітинної лінії раку товстої кишки HCT116.
- Субкультивування клітинної лінії HCT116: Цей веб-сайт містить багато корисної інформації про культуральне середовище HCT116. Крім того, на ньому описані процедури заморожування, розморожування та субкультивування клітин.
Часті запитання про клітини HCT116
посилання
- Вагела Б.Н., Ф.У. Вайдя та К. Патак: Підвищення регуляції NOX-2 та Nrf-2 сприяє резистентності до 5-фторурацилу в клітинах карциноми товстої кишки людини (HCT-116). Біохімія (Москва), 2021, 86, с. 262-274.
- Янг М. та ін., Астрагалін пригнічує проліферацію та міграцію клітин раку товстої кишки людини HCT116 шляхом регуляції сигнального шляху NF-κB. Frontiers in Pharmacology, 2021, 12: p. 639256.
- Діпіка С., Сельварадж К.І., Рупан С.М. Скринінг біоактивності кварцу Caesalpinia pulcherrima L. та цитотоксичності наночастинок срібла, синтезованих з екстракту, на клітинній лінії HCT116. Матеріалознавство та інженерія, C, 2020, 106, с. 110279.
- Гао, X. та ін., Какао-чай (Camellia ptilophylla) індукує мітохондріально-залежний апоптоз у клітинах HCT116 через генерацію АФК та сигнальний шлях PI3K/Akt. Food Research International, 2020, 129, с. 108854.
- Хідаят А.Ф.А. та ін., Dioscorea bulbifera індукує апоптоз через інгібування ERK 1/2 та активацію JNK сигнальних шляхів у клітинах колоректальної карциноми людини HCT116. Біомедицина і фармакотерапія, 2018. 104: p. 806-816.