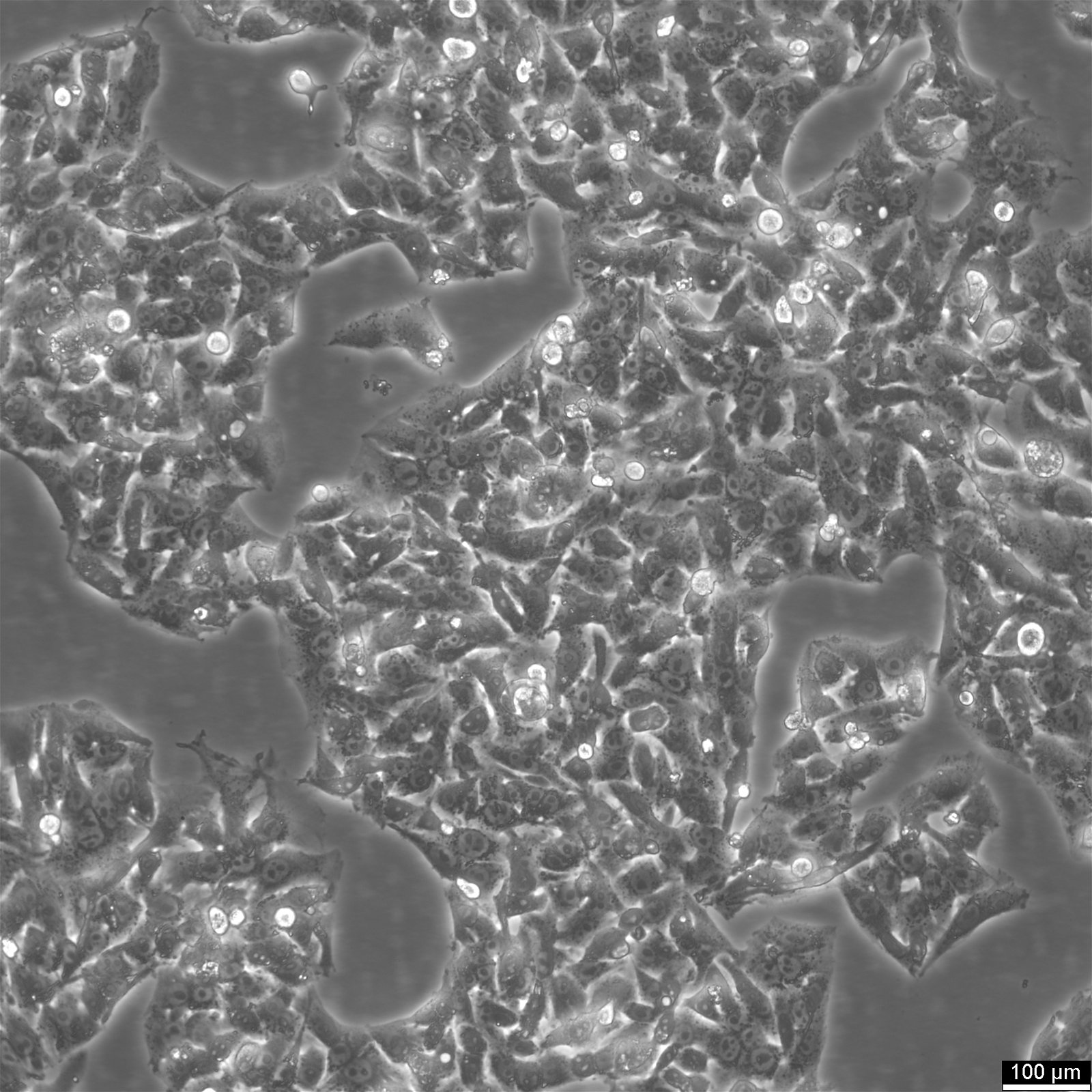
HepG2 rakud - maksavähi uurimisressurss
Hep-G2 on inimese maksavähi rakuliin, mis pärineb 15-aastase hepatotsellulaarse kartsinoomiga kaukaasia mehe maksakoes. Neid rakke kasutatakse sageli ravimite metabolismi ja hepatotoksilisuse uuringutes. Kuigi HepG2 rakkudel on kõrge proliferatsioonikiirus ja epiteelilaadne välimus, on nad mittetuumorigeensed ja täidavad mitmesuguseid diferentseeritud maksafunktsioone. 1975. aastal tuletasid teadlased HepG2 rakud hepatotsellulaarsest kartsinoomist, mis tegi sellest esimese maksarakkude liini, millel on hepatotsüütide kriitilised omadused. Erinevalt varem loodud SK-Hep1 rakuliinist, millel puuduvad olulised maksarakkude markerid, suudavad HepG2 rakud eritada erinevaid plasmavalku ja on väärtuslik mudel inimhepatotsüütide rakupinna domeenide rakusisese dünaamika uurimiseks. Neil rakkudel on epiteelilaadne morfoloogia, nende modaalne kromosoomide arv on 55 ja neid saab stimuleerida inimese kasvuhormooniga.
HepG2 omadused
Esmaste hepatotsüütide tüüpiline kuju on kuubikujuline ja sisaldab tavaliselt kahte tuuma. Seevastu HepG2 rakkudel on epiteelilaadne morfoloogia, millel on üks tuum ja kromosoomide arv 48-54 raku kohta. Kuigi HepG2 rakud võivad moodustada kuni 25% raku kogu valgu koguhulgast, on nende suurus suurem kui normaalsete hepatotsüütide oma, moodustades umbes 10% raku kogu valgu koguhulgast. Rakuvalkud on rakusisesed kriitilised osalejad, kes täidavad geenide poolt määratud funktsioone.
Kasvajarakkudes, sealhulgas kromosoomide ebahariliku arvuga rakkudes, on sageli suurenenud tuumade arv, kuni seitse raku kohta. Tänu oma kõrgele diferentseerumisastmele in vitro on HepG2 rakud ideaalne mudel inimhepatotsüütide sapiteede, sinusoidsete membraanvalkude ja lipiidide rakusisese liikumise ja dünaamika uurimiseks.
HepG2 raku keskmine läbimõõt on umbes 10-20 µm, mis on väiksem kui 15 µm läbimõõduga hepatotsüütidel, kuid sarnaneb hepatoblastoomi (HB) kasvajarakkudega, mille läbimõõt on 10-20 µm.
HepG2 geneetika
Hep-G2 rakuliinil esineb mitmeid translokatsioone, sealhulgas kromosoomide 1 ja 21 lühikeste harude vahel, kromosoomide 2, 16 ja 17 trisoomia ning kromosoomi 20 tetrasoomia. Täheldatakse ka kromosoomi 4q3 piirkonna kadumist, mis on seotud translokatsiooniga t(1;4), mida sageli täheldatakse hepatoblastoomi (HB) ja muude kromosoomianomaaliate, näiteks 2. ja 20. kromosoomi trisoomiate puhul. Kromosoomide arv HepG2 rakkudes on 50-60, mis viitab hüperdiploidsele karyotüübile, samas kui mõnel juhul on üle 100 kromosoomi ja neid iseloomustab tetraploidne laienemine. HepG2 rakud sisaldavad ligikaudu 7,5 pg DNA-d, mis on 15% rohkem kui keskmine somaatiline rakk. Võrreldes sellega on primaarsed hepatotsüüdid kuubikujulise raku kujuga ja sisaldavad tavaliselt kahte tuuma [1].
HepG2 rakkude mutatsiooniprofiil
HepG2 rakuliin kannab TERT promootorpiirkonna mutatsiooni C228T, mis esineb ka hepatotsellulaarsel kartsinoomil (HCC) ja hepatoblastoomil (HB). See mutatsioon aitab kaasa immortaliseerumisele, kaitstes vähirakkude telomeere. Lisaks on HepG2 rakkudel metsikut tüüpi TP53, mis on inimese vähktõve allasurumiseks kriitilise tähtsusega geen, kuna see mängib rolli rakutsükli peatamises, apoptoosis ja vananemises. Mutatsioonid selles geenis võivad soodustada rakkude proliferatsiooni.
HepG2 rakud osalevad mitmes rajas, sealhulgas rakkude kasvu, ellujäämisradade, nagu loote ja embrüo HB, ning Wnt/β-kateniini raja düsregulatsioonis. Lisaks on rakuliinil iseloomulik CTNNB1 geeni kolmanda eksoni deletsioon, mis on identne epiteeli tüüpi HB puhul täheldatuga [2,3].
HepG2 hepatotsellulaarse kartsinoomi rakkude ülevaade maksauuringutes
Inimese hepatoomist pärit HepG2 rakud on muutunud hindamatuks vahendiks maksa funktsioonide ja haiguste, sealhulgas hepatotsellulaarse kartsinoomi uurimisel. Need maksa rakuliinid annavad ülevaate inimese hepatotsüütide raku reaktsioonidest erinevates katsetustingimustes. Luciferaasi reporterplasmiidide kasutamine HepG2 rakkudes on olnud eriti tõhus geeniekspressiooni ja rakkude transfektsioonide jälgimiseks, mis on olulised ainevahetuse uurimisel, näiteks etanooli mõju uurimisel maksarakkudele
Viirusinfektsioonide ja maksahaiguste uuringud HepG2 rakkude abil
Immortaliseeritud maksakasvaja rakuliinid nagu HepG2 ja Huh7 on olulised viirusinfektsioonide uurimisel, näidates D-hepatiidi (HDV) täielikku rakutsükli replikatsiooni ja B-hepatiidi (HBV) ekspressiooni [5,6]. Paralleelselt mängivad HepaRG rakuliinid kriitilist rolli HBV sisenemismehhanismide selgitamisel [7]. HepG2 rakke kasutatakse ka mitmesuguste inimeste maksahaiguste uurimiseks, alates geneetilistest seisunditest, nagu progressiivne perekondlik intrahepaatiline kolestaas (PFIC) ja Dubin-Johnsoni sündroom, kuni tsütotoksiliste ja genotoksiliste ainetega seotud keskkonna- ja toitumisuuringute ning ravimite sihtotstarbelise kasutamise ja hepatokartsinogeneesi uuringuteni [8,9]. Nende kasutamine laieneb ka uuringutele bio-tehniliste maksaseadmetega
HepG2 rakkude ja biomaterjalide vastastikmõju kudede muundamisel
HepG2-rakkude koostoime erinevate biomaterjalidega on koetehnoloogias keskse tähtsusega. Sellised tehnikad nagu kolloidse sondi tehnika aitavad neid vastastikmõjusid mõista, mõõtes rakkude adhesiivseid omadusi, mis on olulised rakkude elujõulisuse määramisel tellingute ja täpsete maksakudede mudelite väljatöötamiseks
Rakkude käitumine ja uuendused HepG2-põhistes mudelites
Rakkude käitumise uurimine HepG2-põhistes mudelites on maksahaiguste uurimisel väga oluline. Kolmemõõtmeliste sferoidrakukultuuride areng on viinud HepG2 rakkude sferoidide loomisele, mis pakub füsioloogiliselt asjakohasemat mudelit, mis peegeldab täpselt normaalseid hepatotsüüte. Need 3D-mudelid, millel on suurenenud ainevahetuse aktiivsus, näitavad HepG2-rakkude potentsiaali hepatoblastoomi mudelina ja on olulised vähiraviuuringutes, eriti maksakasvajate simuleerimiseks ja uute ravimeetodite katsetamiseks [10-12]
HepG2 võrdlus ja omadused teiste tuumorirakuliinide seas
HepG2 on üks kõige laialdasemalt kasutatavaid maksakasvaja rakuliine, mis on valitud selle laialdase kasutusvõimaluse tõttu teaduslikes uuringutes umbes 40 olemasoleva maksakasvaja rakuliini hulgast [13]. Hoolimata sellest, et HepG2 rakuliinil on teatud tsütokroom P450 ensüümide ekspressioon võrreldes normaalsete hepatotsüütidega nõrk või puudub, on HepG2 metaboolne profiil ajendanud püüdlusi muuta seda rakuliini paremate ravimite metabolismiuuringute jaoks [13]. Võrreldes selliste kasvajarakkude liinidega nagu MCF7, PC3, 143B ja HEK293, on HepG2 rakkudel unikaalne aminohappesisalduse profiil, mis mõjutab oluliselt valkude sünteesi ja sekretsiooni, rõhutades nende unikaalseid ainevahetusradu [14]
Maksahaiguste uurimine HepG2 abil
HepG2 rakkude subkultiveerimine
Siin on viis sammu, kuidas eemaldada rakukultuurikolbidest Accutase'i abil adherentsed rakud:
- Eemaldage rakukultuurikolbist söötme ja loputage kleepunud rakud PBS-ga, mis ei sisalda kaltsiumi ega magneesiumi. Kasutage 3-5 ml PBS-i T25 kolbi puhul ja 5-10 ml T75 kolbi puhul.
- Lisage rakukultuurikolbi Accutase, kasutades 1-2 ml T25 ja 2,5 ml T75 kolvi kohta. Veenduge, et Accutase katab kogu rakukilbi.
- Inkubeerige kolbi toatemperatuuril 8-10 minutit.
- Resuspenseerige rakud ettevaatlikult söötmega, kasutades 10 ml värsket söötmeainet.
- Tsentrifuugige resuspendeeritud rakke 5 minutit 300xg juures, resuspendeerige need värskes söötmes ja doseerige need uutesse kolvidesse, mis sisaldavad värsket söötme.
HepG2 rakkude tulevikuväljavaated
HepG2 rakuliini täieliku potentsiaali ärakasutamine jätkub tänu murrangulistele edusammudele tsütokroomide ekspressiooni suurendamisel. Teadlased uurivad ka võimalust kasutada kolmemõõtmelisi sfäärilisi rakukultuure, mis pakuvad füsioloogiliselt asjakohasemat süsteemi. Metaboolne aktiivsus, sealhulgas tsütokroomide aktiivsus on 3D-sferoidsete HepG2-mudelite puhul märkimisväärselt suurem kui 2D-rakkude puhul, mis toob meid lähemale normaalseid hepatotsüüte peegeldava mudeli loomisele. Lisaks võib rakupinnavalkude ebaõige jaotumise aluseks olevate dünaamiliste protsesside uurimine sillutada teed maksahaiguste paremale mõistmisele
HepG2 rakud: KKK: Nende rolli ja erinevuste mõistmine biomeditsiinilistes uuringutes - KKK
Viited
- Vyas, R.C., Darroudi, F., Natarajan, A.T. Radiation-induced chromosomal breakage and rejoining in interphase-metaphase chromosomes of human lymphocytes, Mutat Res, 1991; 249(1):29-35.
- Woodfield, S.E., Shi, Y., Patel, R.H., Chen, Z., Shah, A.P., Srivastava, R.K., Whitlock, R.S., Ibarra, A.M., Larson, S.R., Sarabia, S.F., et al. MDM4 inhibeerimine: P53 reaktiveerimise uudne terapeutiline strateegia hepatoblastoomi korral. Sci. Rep. 2021, 11, 2967.
- Hussain, S.P., Schwank, J., Staib, F., Wang, X.W., Harris, C.C. TP53 Mutations and hepatocellular Carcinoma: Insights into the Etiology and Pathogenesis of Liver Cancer. Oncogene 2004.
- Schicht, G., Seidemann, L., Haensel, R., Seehofer, D., Damm, G. Hepatoomi rakuliinide HepG2 ja Huh7 kasutatavuse kriitiline uurimine hepatotsellulaarse kartsinoomi metaboolse kujutamise mudelina. Cancers 2022, 14(17), 4227.
- Verrier, E.R., Colpitts, C.C., Schuster, C., Zeisel, M.B., Baumert, T.F. Rakukultuurimudelid B- ja D-hepatiidi viiruse infektsiooni uurimiseks. Viruses 2016, 8, 261.
- Verrier, E.R., Colpitts, C.C., Bach, C., Heydmann, L., Weiss, A., Renaud, M., Durand, S.C., Habersetzer, F., Durantel, D., AbouJaoudé, G., et al. A Targeted Functional RNA Interference screen Uncovers Glypican 5 as an Entry Factor for Hepatitis B and D Viruses. Hepatology 2016, 63, 35-48.
- Gripon, P., Rumin, S., Urban, S., Le Seyec, J., Glaise, D., Cannie, I., Guyomard, C., Lucas, J., Trepo, C., Guguen-Guillouzo, C. Inimese hepatoomi rakuliini nakatumine B-hepatiidi viirusega. Proc. Natl. Acad. Sci. USA 2002, 99, 15655-15660.
- Mersch-Sundermann, V., Knasmüller, S., Wu, X.J., Darroudi, F., Kassie, F. Inimese maksa rakuliini kasutamine tsütoprotektiivsete, antigenotoksiliste ja kogenotoksiliste ainete avastamiseks. Toxicology. 2004; 198(1-3): 329-340.
- Fanelli, A. HepG2 (maksa hepatotsellulaarne kartsinoom): rakukultuur. HepG2. Välja otsitud 3. detsember 2017.
- Xuan, J., Chen, S., Ning, B., Tolleson, W.H., Guo, L. Tsütokroom P450-d ekspresseerivate HepG2-rakkude arendamine metabolismiga seotud ravimitest põhjustatud maksatoksilisuse hindamiseks. Physiol. Behav. 2017, 176, 139-148.
- Ooka, M., Lynch, C., Xia, M. In vitro ainevahetuse aktiveerimise rakendamine kõrgläbivoolulises skriiningus. Int. J. Mol. Sci. 2020, 21, 8182.
- Huang, L., Coughtrie, M.W.H., Hsu, H. Dehüdroepiandrosterooni sulfotransferaasi geeni allareguleerimine inimese hepatotsellulaarses kartsinoomis. Mol. Cell. Endocrinol.
- Zhu, Z., Hao, X., Yan, M., et al. Cancer stem/progenitor cells are highly enriched in CD133 + CD44 + population in hepatocellular carcinoma. Int J Cancer. 2010; 126:2067-2078.
- Arbus, C., Benyamina, A., Llorca, P.-M., Baylé, F., Bromet, N., Massiere, F., Garay, R.P., Hameg, A. Inimese tsütokroom P450 ensüümide iseloomustamine, mis osalevad tsüamemasiini metabolismis. Eur J Pharm Sci. 2007 Dec;32(4-5):357-66.