HCT116 rakuliin: Colorectal Cancer Research: A pillar in Colorectal Cancer Research: A pillar in Colorectal Cancer Research
HCT116 rakuliin on kolorektaalvähi uurimise nurgakivi, mis pakub hindamatut teavet haiguse patogeneesi ja võimalike ravivõimaluste kohta. HCT116 on tuntud oma kasulikkuse poolest vähiuuringutes ja farmakoloogilistes hindamistes ning see hõlbustab tuumori käitumise ja ravimite tõhususe olulisi uuringuid.
HCT116 rakkude päritolu ja põhiomadused
HCT116 rakkude juurte ja põhiomaduste, näiteks nende morfoloogiliste omaduste, geneetilise koostise ja rakumõõtmete mõistmine on oluline teadlastele, kes alustavad uuringuid selle rakuliiniga.
Päritolu ja geneetiline maastik: HCT116 rakud pärinevad 48-aastase kaukaasia mehe käärsoolest, kellel on diagnoositud kolorektaalvähk, ja need on märgatavad KRAS-geeni (RAS/RAF/MEK/ERK signaalirada) 13. koodoni (G13D) mutatsiooni tõttu. See konkreetne mutatsioon on nende rakkude onkogeenses muundumises keskse tähtsusega, mis rõhutab nende tähtsust vähiuuringutes.
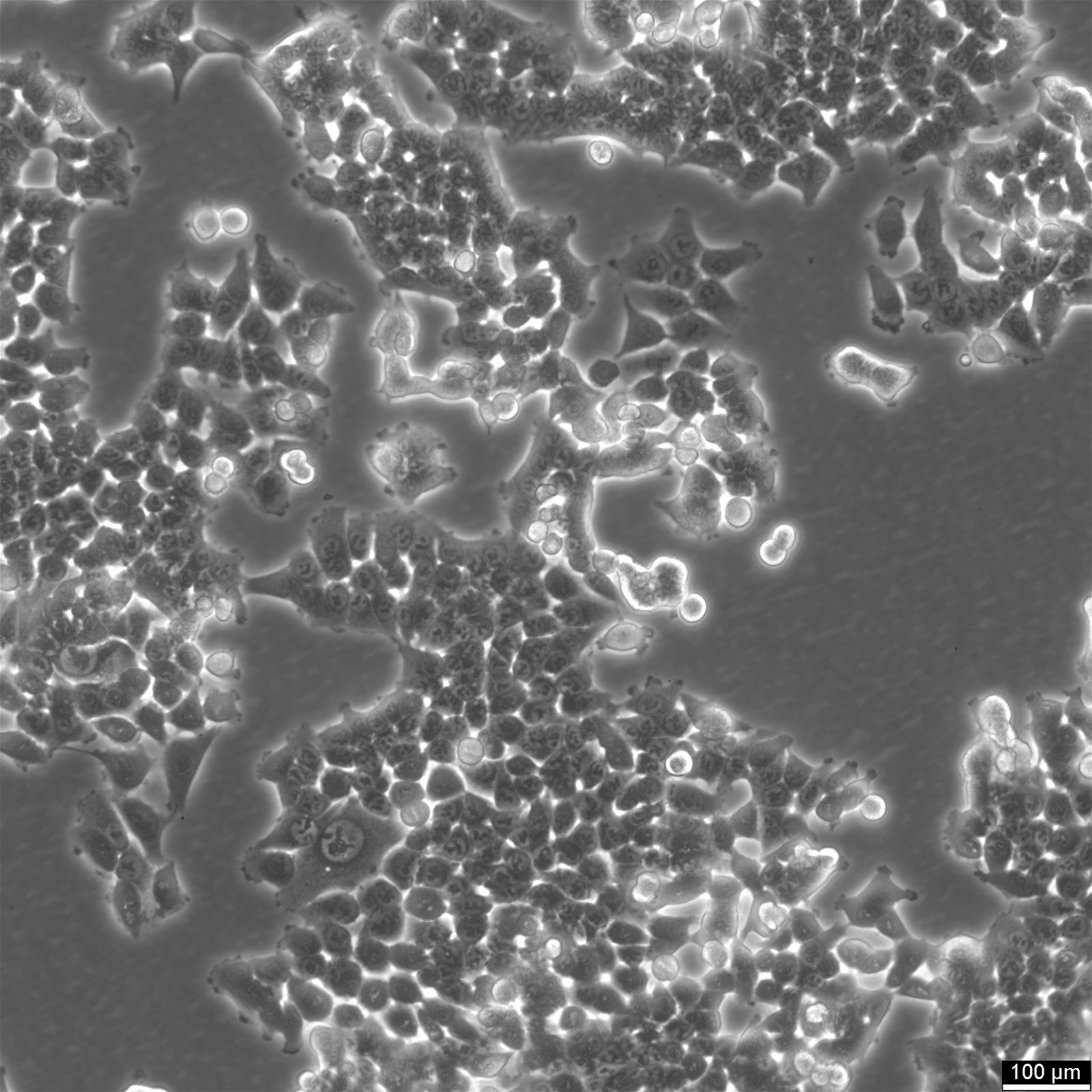
Morfoloogia ja kasvuomadused: HCT116 rakud, millel on epiteelilaadne morfoloogia, kasvavad tavaliselt monokihilistes kultuurides, kuid võivad moodustada ka 150-400 µm läbimõõduga sferoide. Selline kohanemisvõime kasvumustrite osas rõhutab nende mitmekülgsust erinevates katseseadeldistes.
Kromosoomiprofiil: HCT116 rakkude kromosoomiline koostis on peaaegu diploidne, ligikaudu 70% rakupopulatsioonist kannab 45 kromosoomi. Eriti märkimisväärne on kromosoomide 8, 10, 16 ja 17 pikkade harude korduv amplifikatsioon, samas kui kromosoom Y puudub, mis aitab kaasa nende unikaalsele genoomsele signatuurile.
Võrdlev analüüs: HCT116 vs. HT29 rakuliinid
HCT116 ja HT29, teise inimese kolorektaalkartsinoomi rakuliini kõrvutamisel ilmnevad selged erinevused nende onkogeenses potentsiaalis ja diferentseerumisvõimes:
Onkogeenne agressiivsus ja diferentseerumine: HCT116 rakke iseloomustab nende kõrge onkogeenne agressiivsus ja piiratud diferentseerumispotentsiaal, mis teeb neist agressiivsete kasvajate fenotüüpide uurimise mudeli. Seevastu HT29 rakkudel on võime diferentseeruda enterotsüütide sarnasteks ja limaskesta tootvateks liinideks, pakkudes kontrastset mudelit, mis jäljendab erinevaid kolorektaalvähi bioloogia aspekte.
HCT116 ja HT29 rakuliinide võrdlev arusaam rikastab teadlaste käsutuses olevaid vahendeid, võimaldades nüansirikkamaid uuringuid kolorektaalvähi mitmekülgsest olemusest.
HCT116 rakkude käitlemine
|
Kordistumisaeg: |
HCT116 vähirakkude kahekordistumisaeg on 25 kuni 35 tundi. |
|
Adherentselt või suspensioonis: |
HCT116 käärsoolevähi rakuliin on adherentne, rakud kasvavad monokihina. |
|
Külvikutihedus: |
HCT116 rakukultuuri puhul on soovitatav külvitihedus 2 x104 rakku/cm2. Subkultuuride kasvatamiseks tuleb rakud pärast 1x PBS pesu eraldada Accutase lahuse abil. Pärast tsentrifuugimist resuspenseeritakse rakupellet värskes kasvukeskkonnas ja viiakse uude kolbi. |
|
Kasvukeskkond: |
HCT116 rakkude kasvatamiseks on optimaalne McCoys 5a kasvukeskkond, mida on täiendatud 3,0 g/L L-glükoosi, 1,5 mM L-glutamiini, 3,0 g/L NaHCO3 ja 10% veiste loote seerumi sisaldusega. Soovitatav on vahetada söötme 1 kuni 2 korda nädalas. |
|
Kasvutingimused (temperatuur,CO2): |
Kultiveerimine toimub niisutatud inkubaatoris temperatuuril 37 °C ja 5%CO2 atmosfääris. |
|
Säilitamine: |
HCT116 rakke võib säilitada temperatuuril alla -150°C kas auru- või vedelas faasis vedelas lämmastikus. |
|
Külmutamisprotsess ja keskkond: |
Krüokonserveerimiseks kasutada CM-1 või CM-ACF keskkonda. Soovitatav on kasutada kontrollitud kiirusega külmutamise meetodit, mis võimaldab temperatuuri järkjärgulist langust 1 °C minutis, mis aitab säilitada rakkude elujõulisust. |
|
Sulatamisprotsess: |
HCT116 rakud sulatatakse 37 °C veevannis. Pärast kasvukeskkonna lisamist tsentrifuugige, et eemaldada külmutuskeskkonna jäägid. Resuspenseerige rakupellet värskes söötmes ja kasvatage uutes kolbides. |
|
Bioturvalisuse tase: |
Tase 1 |
HCT116 rakuliini eelised
Selles jaotises käsitletakse rakuliini HCT116, rõhutades selle keskset rolli vähiuuringutes, eelkõige kolorektaalvähi uurimisel, ja arutatakse selle eeliseid.
HCT116 rakuliin paistab vähiuuringutes silma mitme olulise eelise poolest:
Kolorektaalvähi mudel: See on laialt tunnustatud in vitro mudel kolorektaalvähi jaoks, mis on maailmas kolmas kõige levinum vähkkasvaja. Selle asjakohasus inimese kolorektaalvähi jäljendamisel muudab selle asendamatuks vähi bioloogia mõistmiseks ja ravistrateegiate katsetamiseks.
Homogeensus: Tähelepanuväärne on see, et umbes 70% HCT116 rakkude geneetiline profiil on järjepidev, mis tähendab, et tegemist on suhteliselt homogeense populatsiooniga. Selline ühetaolisus on oluline geeniekspressioonile, rakkude signaaliradadele ja ravimravi tõhususe hindamisele keskendunud uuringute jaoks, sest see tagab katsetulemuste järjepidevuse ja usaldusväärsuse.
Transfektsiooni tõhusus: HCT116 rakkude üks iseloomulikke omadusi on nende kõrge transfektsioonivõime, eriti viirusvektoritega. See omadus on eriti kasulik geeniteraapia uuringutes, võimaldades geneetilise materjali tõhusat ja täpset sisestamist, hõlbustades seeläbi täiustatud geneetilisi manipulatsioone ja funktsionaalseid uuringuid.
Edendada oma avastusi meie autentseeritud HCT116 rakuliiniga
HCT116 rakuliini teadusuuringute rakendused
HCT116 rakuliinil on mitmesuguseid rakendusi vähiuuringutes. Mõned silmapaistvad rakendused on järgmised:
Vähi bioloogia
HCT116 käärsoolevähi rakuliini kasutatakse käärsoolevähi progresseerumise ja arengu uurimiseks. Lisaks aitab see selgitada vähi proliferatsiooni, migratsiooni ja invasiivsuse aluseks olevaid mehhanisme ja signaaliradu. Ühes uuringus kasutati HCT116 rakke ravimresistentsuse arengus osalevate geenide uurimiseks. Teadlased üleekspresseerisid käärsoolevähirakkudes MDR1 geeni ja jälgisid NOX (NADPH oksiidi) isovormide ja Nrf2 ekspressiooni. Uuring näitas, et NOX2 ja Nrf2 ülereguleerimine põhjustab vähirakkude kemoresistentsust; seega saab neid geene suunata resistentsuse arengu ületamiseks vähiravi ajal [1]. Samuti teatasid 2021. aastal tehtud uuringud, et NF-κB signaalirada on seotud jämesoolevähi proliferatsiooni ja migratsiooni reguleerimisega. Seega saab seda suunata uute ja tõhusate ravimite väljatöötamiseks kolorektaalkartsinoomi vastu [2].
Onkoloogia valdkonnas on rakutsükli, proliferatsiooni ja kasvu ning apoptoosi keeruliste protsesside mõistmine väga oluline. Need bioloogilised funktsioonid on kesksel kohal inimese rakuliinide, eriti pahaloomuliste rakkude, nagu inimese käärsoolevähi rakud ja kõhunäärmevähi mudelid, uurimisel. Näiteks rakuliinid HCT116 ja SW620 on olulised vastavalt käärsoole- ja kõhunäärmevähi aluseks olevate mehhanismide uurimisel. Selliste meetodite abil nagu voolutsütomeetria ja klonogeensed testid saavad teadlased selgitada geeniekspressiooniprofiile ja sõltumatute rakkude käitumist kasvajates, mis heidab valgust sellele, kuidas vähk suhtleb rakuvälises maatriksis.
Apoptoosi roll vähi progresseerumises
Apoptoos ehk programmeeritud rakusurm mängib olulist rolli raku homöostaasi säilitamisel ja on vähiuuringute peamine uurimisvaldkond. Oluline on eristada mitteseotud apoptoosi ja spetsiaalselt vähi kontekstis esilekutsutud apoptoosi, näiteks käärsoolevähi rakusurma. See protsess ei seisne ainult rakkude hävitamises, vaid hõlmab signaalide keerukat koostoimet, mis võib mõjutada kasvajate kasvu ja metastaaside teket. Uurides apoptoosi ja rakusurma koos metastaaside supressorite ja kasvajasupressorite aktiivsusega, saavad teadlased ülevaate radadest, mis reguleerivad vähi progresseerumist ja metastaaside tekkimise potentsiaali.
Metastaasid ja molekulaarsed markerid vähktõves
Metastaasid on endiselt üks vähi kõige hirmsamaid aspekte, kusjuures hematogeenne metastaas on oluline probleem pahaloomuliste rakkude levikul. Metastaasi uurimine hõlmab vähirakkude liikumis- ja invasioonivõime ehk rakkude lokomotsiooni ning rakkude ja nende ümbritseva keskkonna, sealhulgas rakuvälise maatriksi vastastikmõju uurimist. Molekulaarsed markerid, nagu CD133 ekspressioon ja epidermise kasvufaktori retseptor, on kriitilise tähtsusega positiivsete käärsoole kartsinoomi rakkude ja teiste vähitüüpide käitumise tuvastamisel ja mõistmisel. Näiteks SIRT6 rada on esile kerkinud huvipakkuvaks valdkonnaks selle võimaliku rolli tõttu kasvaja kasvu ja metastaatilise käärsoolevähi moduleerimisel.
Toksikoloogia/ravimite väljatöötamine
HCT116 rakuliini kasutatakse uute vähiravimite skriiningmudelina. On tehtud mitmeid uuringuid, et hinnata vähivastaste ravimite, sealhulgas looduslike toodete ja keemiliselt sünteesitud nanoosakeste tõhusust ja toksilisust. Nii hinnati uuringus HCT116 rakkudes taimse ravimi Caesalpinia pulcherrima ekstraktidest sünteesitud hõbe nanoosakeste tsütotoksilisust [3]. Uuringus kasutasid teadlased HCT116 vähirakuliini, et hinnata kakaotee veeekstrakti vähivastast potentsiaali. Nad leidsid, et kakaotee ekstrakt vähendab käärsoolevähi proliferatsiooni ja kutsub esile rakusurma [4]. Teises uuringus kasutati HCT116 vähirakke ja avastati, et õhukartuli, Dioscorea bulbifera, ekstraktidel on pro-apoptootiline toime kolorektaalkartsinoomi rakkudes JNK signaalkaskaadi aktiveerimise ja ERK1/2 geeni allasurumise kaudu [5].
Metformiini mõju vähirakkudele, eriti jämesoole- ja kõhunäärmevähi kontekstis, näitab, kuidas vähirakkude bioloogiliste funktsioonide mõistmine võib viia potentsiaalsete ravistrateegiateni. Vähirakkude kloonilise ellujäämise ehk kloonide moodustamise võime uurimine pärast ravi selliste ainetega nagu metformiin või spetsiifiliste radade, näiteks epidermise kasvufaktori retseptori, sihtimisega võib anda väärtuslikke teadmisi tõhusate vähiravimeetodite kohta. Lisaks võimaldab HCT116 kloonide ja HCT116 rakupopulatsioonide kasutamine nendes uuringutes paremini mõista, kuidas vähirakud reageerivad erinevatele terapeutilistele sekkumistele, mis sillutab teed individuaalsematele lähenemisviisidele vähiravis.
HCT116 rakud: Uuringupublikatsioonid
Selles jaotises vaadeldakse mõningaid olulisi ja enim tsiteeritud hiljutisi publikatsioone, milles kasutatakse HCT116 rakuliini.
See uuring on avaldatud ajakirjas Journal of Photochemistry and Photobiology B: Biology (2017). Teadlased kasutasid HCT116 käärsoolevähi ja A549 kopsuvähi rakuliine, et hinnata piper nigrumi seemnete abil sünteesitud tinaoksiidi nanoosakeste tsütotoksilist mõju.
See uuring ajakirjas Cancer Letters (2018) pakub välja, et lncRNA SNHG15 soodustab jämesoolevähirakkude, sealhulgas HCT116 rakuliinide kolorektaalvähi rännet.
Pika mittekodeeriva RNA TUG1 üleekspressioon soodustab käärsoolevähi progresseerumist
See artikkel avaldati 2016. aastal ajakirjas Medical Science Monitor. Uuringus leiti, et onkogeenne LncRNA TUG1 soodustab HCT116 käärsoolevähirakkude proliferatsiooni ja migratsiooni.
Selles ajakirjas Biochemical Pharmacology (2018) avaldatud uuringus pakutakse välja, et ravimresistentsuse teke tõstab H2S-i tootvate ensüümide taset HCT116 käärsoolevähirakkudes.
Selles teadusartiklis ajakirjas International Journal of Environmental Health Research (2023) tehakse ettepanek, et Inula viscosa L. ekstrakt avaldab vähivastast toimet HCT116 käärsoolevähirakkudele mikroRNAde reguleerimise kaudu.
Ressursid HCT116 rakkude jaoks
Allpool on toodud mõned ressursid HCT116 rakkude kohta.
- HCT116 transfekteerimine: See video on HCT116 vähirakkude transfekteerimise samm-sammuline juhend.
- HCT116 rakuliini kultiveerimine: See video näitab HCT116 käärsoolevähi rakuliini subkultiveerimisprotokolli.
- HCT116 rakuliini subkultuurimine: See veebisait sisaldab palju kasulikku teavet HCT116-kultuurikeskkonna kohta. Lisaks on seal esitatud rakkude külmutamise, sulatamise ja subkultiveerimise protseduurid.
Korduma kippuvad küsimused HCT116 rakkude kohta
viited
- Waghela, B.N., F.U. Vaidya ja C. Pathak: NOX-2 ja Nrf-2 Upreguleerimine soodustab 5-fluorouratsiili resistentsust inimese käärsoole kartsinoomi (HCT-116) rakkudes. Biochemistry (Moscow), 2021, 86, lk 262-274.
- Yang, M., et al., Astragaliin pärsib inimese käärsoolevähi HCT116 rakkude proliferatsiooni ja migratsiooni, reguleerides NF-κB signaalirada. Frontiers in Pharmacology, 2021, 12: p. 639256.
- Deepika, S., C.I. Selvaraj ja S.M. Roopan, Caesalpinia pulcherrima L. swartz'i bioaktiivsuse skriining ja ekstrakti sünteesitud hõbeda nanoosakeste tsütotoksilisus HCT116 rakuliinile. Materials Science and Engineering, C, 2020, 106, lk 110279.
- Gao, X., et al., Kakaotee (Camellia ptilophylla) indutseerib HCT116 rakkudes mitokondritest sõltuvat apoptoosi ROS-i tekitamise ja PI3K/Akt signaalitee kaudu. Food Research International, 2020, 129, lk. 108854.
- Hidayat, A.F.A., et al., Dioscorea bulbifera indutseeris apoptoosi läbi ERK 1/2 inhibeerimise ja JNK signaaliradade aktiveerimise HCT116 inimese kolorektaalkartsinoomi rakkudes. Biomedicine & Pharmacotherapy, 2018. 104: p. 806-816.