Volumen: 100 ml
Opbevaring: ≤ –15 °C
Sterilitet: Sterilt filtreret
Stabil glutaminopløsning (L-Alanyl-L-Glutamin, 200 mM) er en meget stabil dipeptidform af L-glutamin, der er udviklet som en direkte erstatning for konventionel L-glutamin i cellekulturmedier. L-glutamin er en essentiel aminosyre og en vigtig energikilde for dyrkede celler, der spiller en afgørende rolle i cellevækst, stofskifte og proteinsyntese.
Anvendelse og fordele
I standardvæske medier nedbrydes L-glutamin relativt hurtigt ved 37 °C, hvilket fører til dannelsen af toksiske biprodukter såsom ammoniumioner, der kan have en negativ indvirkning på cellernes levedygtighed og eksperimentelle resultater. Stabil glutamin overvinder denne begrænsning ved at tilvejebringe en ikke-nedbrydelig dipeptidform, der forbliver intakt under dyrkningsbetingelser.
Celler spalter enzymatisk dipeptidbindingen for at frigive L-glutamin efter behov, hvilket sikrer en kontinuerlig frisk forsyning og samtidig forhindrer ophobning af skadelige affaldsprodukter. Dette gør opløsningen særligt fordelagtig til langvarige cellekulturer og vækstsystemer med høj densitet.
Formulering og anvendelse
L-Alanyl-L-Glutamin-opløsningen fremstilles i vand af cellekulturkvalitet i en koncentration på 200 mM og er sterilfiltreret til kontamineringsfølsomme anvendelser. Den kan fortyndes direkte i komplette medier i henhold til eksperimentelle krav. Opbevares ved ≤ –15 °C og undgå gentagne fryse-tø-cyklusser for at opretholde produktets stabilitet.
Kun til forskningsbrug. Ikke til brug i diagnostiske eller terapeutiske procedurer. Ikke til brug på mennesker eller dyr.
Volumen: 100 ml
Opbevaring: +2 °C til +8 °C
Sterilitet: Sterilt filtreret
HEPES-bufferopløsning (1 M), også kendt som N-2-hydroxyethylpiperazin-N-2-ethanesulfonsyre, er et zwitterionisk organisk buffermiddel, der er meget udbredt i cellekulturmedier. Det er designet til at opretholde stabile pH-forhold i det fysiologiske interval fra 6,7 til 8,6, hvilket understøtter optimal cellefunktion under in vitro-anvendelser.
Anvendelse og fordele
HEPES giver pålidelig bufferkapacitet i cellekultursystemer, især når celler håndteres uden for en CO₂-inkubator. Tilsætning af 10–25 mM HEPES til dyrkningsmedier giver forbedret pH-stabilitet under længerevarende manipulationsperioder, hvilket hjælper med at opretholde ensartede eksperimentelle betingelser.
Denne buffer er membranuigennemtrængelig, har minimal indvirkning på biokemiske reaktioner og udviser stærk kemisk og enzymatisk stabilitet. Disse egenskaber gør den velegnet til en bred vifte af cellekultur
- og biokemiske anvendelser.
Formulering og anvendelse
Opløsningen leveres som et 1 M koncentrat fremstillet i vand af cellekulturkvalitet og er sterilfiltreret til brug i kontamineringsfølsomme miljøer. Den kan fortyndes til den ønskede arbejdskoncentration afhængigt af anvendelseskravene. Opbevares ved +2 °C til +8 °C og håndteres under aseptiske forhold for at bevare produktets integritet.
Kun til forskningsbrug. Ikke til brug i diagnostiske eller terapeutiske procedurer. Ikke til brug på mennesker eller dyr.
Volumen: 50 ml
Opbevaring: +2 °C til +8 °C
Sterilitet: Sterilt filtreret
D-(+)-glukoseopløsning (dextroseopløsning) er et sterilt, brugsklart kosttilskud, der indeholder det naturligt forekommende sukker D-(+)-glukose, som er en central komponent i cellernes stofskifte. Glukose er involveret i vigtige biologiske processer såsom energiproduktion, glykosylering og dannelsen af glykaner, der bidrager til cellernes struktur og funktion.
Anvendelse og fordele
Denne glukoseopløsning er vidt anvendt som supplement i cellekulturmedier og i talrige cellulære og molekylærbiologiske anvendelser. Som primær kulstof
- og energikilde understøtter glukose cellevækst, proliferation og metabolisk aktivitet. Dens involvering i biosyntetiske veje gør den også afgørende for at opretholde normal cellulær fysiologi og eksperimentel konsistens.
Formulering og anvendelse
Opløsningen leveres i en høj koncentration på 250 g/l glukose, hvilket muliggør fleksibel fortynding i dyrkningsmedier i henhold til eksperimentelle krav. Den er sterilfiltreret for at sikre egnethed til kontamineringsfølsomme anvendelser. Opbevares ved +2 °C til +8 °C og håndteres aseptisk for at opretholde produktkvalitet og stabilitet.
Kun til forskningsbrug. Må ikke anvendes i diagnostiske eller terapeutiske procedurer. Må ikke anvendes på mennesker eller dyr.
Volumen: 10 ml
Opbevaring: +2 °C til +8 °C
Sterilitet: Sterilfiltreret
Insulin-Transferrin-Selenium (ITS) Solution (100x) er et kemisk defineret supplement udviklet til en bred vifte af cellekulturformål. Det anvendes oftest som tilsætningsstof til basale cellekulturmedier for at understøtte cellevækst under reducerede serum
- eller serumfrie betingelser.
Anvendelse og fordele
Vores ITS-tilskud leverer de essentielle komponenter, der kræves for optimal ydeevne i serumfrie medier. Ved at tilsætte ITS til konventionelle næringsmedier kan behovet for føtal bovint serum (FBS) til rutinemæssig vedligeholdelse af mange cellelinjer reduceres betydeligt. Dette hjælper med at minimere variabilitet forbundet med serumbrug, samtidig med at der opretholdes konsistent cellevækst og levedygtighed.
Insulin understøtter cellulær optagelse og metabolisme af vigtige næringsstoffer, transferrin letter jerntransporten, og selen bidrager til antioxidantforsvaret og enzymatisk aktivitet. Tilsammen fremmer disse komponenter en afbalanceret cellemetabolisme og forbedret reproducerbarhed i definerede dyrkningssystemer.
Sammensætning og anvendelse
Insulin-Transferrin-Selenium (ITS) leveres som en 100 gange koncentreret opløsning i Earle's Balanced Salt Solution (EBSS) uden fenolrødt. Til standardanvendelser fortyndes det 1:100 i det relevante basismedium for at opnå den anbefalede arbejdskoncentration. Opbevares ved +2 °C til +8 °C og håndteres under aseptiske forhold for at opretholde produktets stabilitet og sterilitet.
Kun til forskningsbrug. Må ikke anvendes til diagnostiske eller terapeutiske procedurer. Må ikke anvendes til mennesker eller dyr.
Volumen: 5 ml
Opbevaring: +2 °C til +8 °C
Sterilitet: Sterilfiltreret
Insulin Human Recombinant Solution er et kemisk defineret supplement, der almindeligvis anvendes til dyrkning af pattedyrscellelinjer, herunder Chinese Hamster Ovary (CHO)-celler. Denne opløsning i cellekulturkvalitet indeholder rekombinant humant insulin, der er udtrykt i Saccharomyces cerevisiae, hvilket sikrer høj renhed og ensartet ydeevne i forskningsanvendelser.
Anvendelse og fordele
Insulin tilsættes rutinemæssigt til serumfrie og kemisk definerede medier for at fremme cellevækst og produktivitet. Som et vigtigt regulerende hormon understøtter insulin cellulær optagelse, udnyttelse og lagring af glukose, aminosyrer og fedtsyrer. Det hæmmer også nedbrydningen af glykogen, proteiner og lipider, hvilket bidrager til forbedret cellelevedygtighed og metabolisk stabilitet i dyrkningssystemer. Den kemisk definerede formulering understøtter reproducerbarhed og minimerer variabilitet i følsomme cellekultur-arbejdsgange.
Biologiske egenskaber og anvendelse
Insulin er et to-kædet polypeptidhormon, der produceres naturligt af β-cellerne i bugspytkirtlens øer. Det har en molekylvægt på ca. 5.800 Da. α
- og β-kæderne er forbundet med to disulfidbindinger mellem kæderne, og α-kæden indeholder en disulfidbinding inden for kæden. Til cellekulturformål skal opløsningen håndteres under aseptiske forhold og opbevares ved +2 °C til +8 °C for at opretholde stabilitet og ydeevne.
Kun til forskningsbrug. Må ikke anvendes til diagnostiske eller terapeutiske procedurer. Må ikke anvendes på mennesker eller dyr.
Volumen: 100 ml
Opbevaring: +2 °C til +8 °C
Sterilitet: Sterilt filtreret
Natriumpyruvatopløsning (100 mM) er et sterilt, brugsklart tilskud, der er udviklet til at give en ekstra, let tilgængelig energikilde til cellekulturmedier. Natriumpyruvat spiller en vigtig rolle i cellernes energimetabolisme og understøtter væksten af metabolisk aktive og hurtigt prolifererende celler, såsom tumorceller. Tilskud kan øge cellernes levedygtighed og bidrage til at opretholde metabolisk stabilitet i kultursystemer.
Anvendelse og fordele
Denne opløsning er vidt anvendt i rutinemæssig cellekultur til at berige medier med pyruvat og fremme optimale vækstbetingelser. Den understøtter ATP-produktion, kan hjælpe med at reducere oxidativt stress og bidrager til forbedret metabolisk ydeevne hos dyrkede celler. Produktet er fremstillet i vand af cellekulturkvalitet og sterilt filtreret, hvilket sikrer ensartet kvalitet og reproducerbarhed i forskningsarbejdsgange.
Anvendelse og kompatibilitet
Den anbefalede endelige koncentration for de fleste cellekulturanvendelser er 1 mM natriumpyruvat, hvilket opnås ved at fortynde 100 mM stamopløsningen 1:100 i komplet dyrkningsmedium. Opløsningen er kompatibel med en bred vifte af basale medier og pattedyrcellelinjer. Opbevares ved +2 °C til +8 °C og beskyttes mod forurening for at opretholde produktets stabilitet.
Kun til forskningsbrug. Må ikke anvendes i diagnostiske eller terapeutiske procedurer. Må ikke anvendes på mennesker eller dyr.
Volumen: 100 ml Opbevaring: ≤-15°C Sterilitet: Sterilt filtreret
Antibiotic/Antimycotic Solution (100x) er et sterilt, brugsklart koncentrat, der er designet til at reducere risikoen for mikrobiel kontaminering i cellekulturer og relaterede laboratorieapplikationer. Denne 100x opløsning indeholder en veletableret kombination af penicillin, streptomycin og amfotericin B, der giver bredspektret antimikrobiel aktivitet mod grampositive og gramnegative bakterier, gær og filamentøse svampe. Formuleringen er velegnet til brug i eukaryote cellekulturer, bakteriemedier og andre forureningsfølsomme systemer, hvilket understøtter rene og ensartede laboratorieoperationer.
Anvendelse og fordele Denne løsning er optimeret til rutinemæssige forskningsprotokoller og bruges i vid udstrækning til at opretholde aseptiske forhold i arbejdsgange med cellekulturer. Den giver pålidelig ydeevne i kontamineringsfølsomme miljøer og hjælper forskere med at reducere risikoen for mikrobiel overvækst uden at gå på kompromis med cellernes sundhed eller forsøgets reproducerbarhed. Den sterilt filtrerede formulering eliminerer behovet for yderligere solubiliseringstrin, hvilket understøtter strømlinet medieforberedelse og reducerer variabiliteten i de daglige laboratorieprocedurer.
Anvendelse og kompatibilitet For at opnå standard arbejdskoncentrationer skal opløsningen fortyndes 1:100 i dit komplette kulturmedie. Produktet er kompatibelt med en bred vifte af pattedyrcellelinjer og basalmedier. Med konsekvent lagertilgængelighed drager forskere fordel af pålidelig forsyningskontinuitet og forenklet logistikplanlægning. Opløsningen skal opbevares ved ≤ -15 °C og beskyttes mod gentagne fryse-tø-cyklusser for at bevare stabiliteten. Kun til forskningsbrug. Ikke til brug i diagnostiske eller terapeutiske procedurer. Må ikke anvendes til mennesker eller dyr.
Volumen: 100 ml Opbevaring: +2°C til +8°C Sterilitet: Sterilt filtreret
MEM Non-Essential Amino Acids (100x) er et sterilt supplement, der er designet til at forbedre cellevækst og levedygtighed i pattedyrscellekultursystemer. Formuleringen svarer til et 100x koncentrat af de ikke-essentielle aminosyrer, der findes i standard Minimum Essential Medium (MEM), hvilket giver mulighed for direkte tilskud til basalmedier med minimal forberedelse.
Anvendelse og fordele Dette tilskud giver en ekstra aminosyrepulje til hurtigt voksende celler eller til cellelinjer, der har mistet evnen til at syntetisere ikke-essentielle aminosyrer de novo. Ved at lette den metaboliske byrde ved biosyntese understøtter det forbedret vækstkinetik, forlænget levedygtighed og større eksperimentel konsistens
- især i næringsstoffølsomme kulturer eller kulturer med høj densitet.
Sammensætning og anvendelse Opløsningen indeholder glycin, L-alanin, L-asparagin, L-asparaginsyre, L-glutaminsyre, L-prolin og L-serin. Den er kompatibel med MEM og de fleste andre standardmedier. Fortyndes 1:100 i det endelige kulturmedie. Dette produkt er sterilt filtreret og klar til brug uden yderligere håndteringstrin. Kun til forskningsbrug. Ikke til brug i diagnostiske eller terapeutiske procedurer. Må ikke anvendes til mennesker eller dyr.
Accutase er en brugsklar, sterilt filtreret celleafløsningsopløsning, der er udviklet som et skånsomt alternativ til trypsin/EDTA til at adskille vedhæftede pattedyrceller fra standard plastudstyr til vævskultur og overflader med vedhæftningsbelægning. Den kombinerer proteolytisk og kollagenolytisk enzymaktivitet i en afbalanceret saltopløsning for at sikre en effektiv, men kontrolleret adskillelse, der bevarer proteinerne på celleoverfladen og understøtter høj levedygtighed efter passage samt hurtig genvedhæftning.
Accutase-formuleringen er baseret på Dulbeccos phosphatbufferede saltvand (DPBS) med EDTA og fenolrødt som visuel pH-indikator. Enzymerne er af ikke-pattedyr
- og ikke-bakteriel oprindelse, hvilket gør Accutase særligt velegnet til stamcelleforskning, vaccinearbejdsgange og enhver anvendelse, hvor forurening fra dyr eller mikroorganismer skal minimeres. Opløsningen hæmmer sig selv ved 37 °C, så der kræves ingen neutraliserende reagens eller serumholdigt medium efter løsningen – cellerne kan overføres direkte til frisk medium.
Nøglefunktioner
Klar til brug 1x sterilt filtreret væske – ingen fortynding eller rekonstituering kræves
Kombineret proteolytisk og kollagenolytisk enzymaktivitet for skånsom dissociation
Hvert parti er standardiseret til en defineret dissociationsaktivitet for konsistens fra parti til parti
Enzymer af ikke-pattedyr og ikke-bakteriel oprindelse
Selvhæmmer ved 37 °C – ingen neutraliserende opløsning nødvendig
Formuleret i Dulbeccos PBS med EDTA
Fenolrødt inkluderet som visuel pH-indikator
pH 6,8 – 7,8
Typiske anvendelser
Accutase adskiller skånsomt en lang række adhærente og følsomme celletyper, herunder humane embryonale stamceller (hESCs), humane inducerede pluripotente stamceller (iPSCs), neurale stamceller, primære neuroner og rutinemæssigt dyrkede adhærente cellelinjer såsom HeLa, HEK 293, CHO, MDCK, Vero, NIH/3T3, BHK-21 og A549. Typiske anvendelsestilfælde omfatter:
Rutinemæssig subkultur og passering af adhærente pattedyrceller
Skånsom enkeltcelle-dissociation af hESC'er, iPSC'er og andre følsomme linjer
Prøveforberedelse til flowcytometri og FACS-analyse
Analyse af celleoverflademarkører, hvor epitopintegritet er afgørende
Assays af cellemigration, proliferation og apoptose
Hviletilstandsassays ved serumudtømning og onkogen-transfektionsstudier
Assays af tumorcelle
- og neuralkamcellemigration
Opskalering af produktionen i bioreaktor-arbejdsgange
Til rutinearbejde påføres ca. 10 ml Accutase pr. 75 cm2 kulturoverflade og inkuberes i 5–10 minutter ved stuetemperatur. Den optimale inkuberingstid bør bestemmes for hver cellelinje og bør ikke overstige en time. Før tilsætning skylles cellelaget med en Ca2+/Mg2+-fri saltopløsning, såsom DPBS uden calcium og magnesium, for at fjerne resterende serum og toværdige kationer.
Håndtering og opbevaring
Opbevar den uåbnede flaske frosset ved -15 °C eller derunder. Optø enten ved stuetemperatur eller natten over ved +2 °C til +8 °C. Optø ikke Accutase i et 37 °C vandbad, da forhøjede temperaturer reducerer enzymaktiviteten. Efter optøning kan opløsningen opbevares i op til 2 måneder ved +2 °C til +8 °C; opbevar ikke ved stuetemperatur. Reagenset må ikke forvarmes til 37 °C før anvendelse – tilsæt det direkte til vaskede celler ved stuetemperatur. For at opnå lang holdbarhed anbefales det at opdele reagenset i engangsportioner for at undgå gentagne optøningscyklusser. Arbejd altid under aseptiske forhold.
Kvalitet
Fremstillet under strenge kvalitetsstandarder. Hvert parti Accutase er sterilt filtreret og testet for sterilitet, pH, udseende og dissociationsaktivitet for at sikre ensartet, reproducerbar ydeevne fra parti til parti.
Produktspecifikationer
Specifikation
Detaljer
ProdukttypeReagens til celleafløsning/dissociation
FormatSterilfiltreret væske, klar til brug
Volumen100 ml
Arbejdskoncentration1x (klar til brug)
EnzymaktivitetKombineret proteolytisk og kollagenolytisk
Enzymets oprindelseIkke-pattedyr og ikke-bakterielt
BuffersystemDulbeccos PBS med EDTA
pH-indikatorFenolrød
pH-interval6,8 – 7,8
UdseendeKlar, lyserød til orange opløsning
Opbevaringstemperatur-15 °C eller derunder
Stabilitet efter optøningOp til 2 måneder ved +2 °C til +8 °C
Anbefalet anvendelsesvolumen~10 ml pr. 75 cm2 dyrkningsflade
Typisk inkubationstid5 – 10 minutter ved stuetemperatur
ForsendelsesbetingelserFrosset på tøris
Tilsigtet anvendelseUdelukkende til forskningsbrug og videreforarbejdning
Formulering (sammensætning pr. liter)
Komponent
Koncentration (mg/L)
Uorganiske salte
Natriumchlorid (NaCl)8000,00
Dinatriumhydrogenphosphat (Na2HPO4)1150,00
Kaliumchlorid (KCl)200,00
Kaliumdihydrogenphosphat (KH2PO4)200,00
Andre komponenter
EDTA · 4Na (tetranatrium-EDTA)220,00
Phenolrød3,00
Proprietær enzymblanding (proteolytisk og kollagenolytisk aktivitet)1x
Accutase er et registreret varemærke tilhørende Innovative Cell Technologies, Inc.
Denne brugsklare, sterilt filtrerede flydende formulering er tilsat Earle’s Balanced Salt Solution (EBSS), 2 mM L-glutamin, D-glukose (1,0 g/l) og 2,2 g/l natriumbicarbonat (NaHCO3), hvilket gør den velegnet til brug i en CO2-kontrolleret inkubatoratmosfære (typisk 5 % CO2). Det medfølgende fenolrød fungerer som en pH-indikator, hvilket muliggør praktisk visuel overvågning af mediets tilstand under cellekulturen.
Nøgleegenskaber
Klassisk Eagles MEM-formulering med Earle’s Balanced Salt Solution (EBSS)
2 mM L-glutamin inkluderet – klar til øjeblikkelig brug
2,2 g/L natriumbicarbonat – bufret til inkubation ved 5 % CO2
Med D-glukose (1,0 g/l) som primær kulstofkilde
Med fenolrødt som pH-indikator
Uden HEPES og uden natriumpyruvat
Sterilfiltreret flydende medium, klar til brug
pH 7,0 – 7,6
Typiske anvendelser
EMEM understøtter dyrkning af en lang række pattedyrcellelinjer, herunder HeLa, HEK 293, Vero, MRC-5, L-929, BHK-21 og mange primære celler. Almindelige anvendelser omfatter:
Rutinemæssig vedligeholdelse og ekspansion af adhærente cellelinjer
Arbejdsgange for virusformering og vaccineproduktion
Cytotoksicitet og bioassay-anvendelser
Transfektions
- og proteinekspressionsstudier
Grundlæggende forskning inden for cellebiologi og molekylærbiologi
For at opnå optimal cellevækst tilsættes der typisk 5–10 % føtal bovint serum (FBS) til EMEM og, afhængigt af cellelinjen, ikke-essentielle aminosyrer (NEAA) samt antibiotika såsom penicillin/streptomycin.
Håndtering og opbevaring
Opbevar den uåbnede flaske ved +2 °C til +8 °C, beskyttet mod lys. Efter åbning skal produktet anvendes under aseptiske forhold. L-glutamin i opløsning nedbrydes gradvist – vi anbefaler at anvende mediet inden for 4 uger efter åbning for at opnå den bedste ydeevne, eller at tilsætte frisk L-glutamin før brug, hvis det opbevares i længere perioder. Lad mediet opvarmes til 37 °C, før det tilsættes til cellerne.
Kvalitet
Fremstillet under strenge kvalitetsstandarder. Hver batch testes for sterilitet, pH, osmolalitet og endotoksinniveauer for at sikre ensartet ydeevne i cellekulturapplikationer.
Produktspecifikationer
Specifikation
Detaljer
ProdukttypeMEM
ProduktkategoriCellekulturmedier
FormatVæske
SterilYeees
Størrelse500 ml
L-glutaminMed L-glutamin (2 mM)
GlukoseMed glukose (1,0 g/l)
NatriumbicarbonatMed NaHCO3 (2,2 g/L)
HEPESUden HEPES
NatriumpyruvatUden natriumpyruvat
FenolrødMed fenolrødt
SaltopløsningEarle’s Balanced Salt Solution (EBSS)
pH7,0 – 7,6
EndotoksinindholdIkke angivet
Opbevaring+2 °C til +8 °C
Formulering (sammensætning pr. liter)
Komponent
Koncentration (mg/L)
Uorganiske salte
Calciumchlorid · 2H2O265,00
Magnesiumsulfat97,72
Kaliumchlorid400,00
Natriumchlorid6.800,00
Natriumdihydrogenphosphat, vandfrit122,00
Natriumbicarbonat (NaHCO3)2.200,00
Aminosyrer
L-arginin · HCl126,00
L-cystin · 2HCl31,30
L-glutamin292,00
L-histidin · HCl · H2O42,00
L-isoleucin52,00
L-leucin52,00
L-lysin · HCl72,50
L-methionin15,00
L-phenylalanin32,00
L-threonin48,00
L-tryptofan10,00
L-tyrosin · 2Na · 2H2O51,90
L-valin46,00
Vitaminer
D-Calciumpantothenat1,00
Cholinchlorid1,00
Folinsyre1,00
Myo-inositol2,00
Nikotinamid1,00
Pyridoxal · HCl1,00
Riboflavin0,10
Thiamin · HCl1,00
Andre komponenter
D(+)-Glukose1.000,00
Phenolrød10,00
De vigtigste funktioner i Freeze Medium CM-1 omfatter:
Bred kompatibilitet: Effektivt til en lang række celletyper, herunder primære celler, stamceller og etablerede cellelinjer.
Høj levedygtighed: Optimeret til at maksimere gendannelse og levedygtighed af celler efter optøning, hvilket sikrer pålidelige eksperimentelle resultater.
Klar til brug: Praktisk forberedt og steriliseret til øjeblikkelig anvendelse, hvilket reducerer forberedelsestiden og risikoen for kontaminering.
Forbedret stabilitet: Opretholder en ensartet ydeevne under standard kryopræserveringsforhold, hvilket sikrer reproducerbare resultater.
Lang holdbarhed: CM-1 er et serumholdigt kryopræserveringsmedium, der er klar til brug, og som kan opbevares i køleskabet i op til et år.
Brug af CM-1 til nedfrysning af celler
Følg disse trin for at bruge CM-1 til nedfrysning af både adhærente og suspenderede celler
For adhærente celler skal de vaskes og adskilles fra kultursubstratet. For suspensionsceller skal du fortsætte direkte til næste trin.
Tæl cellerne for at sikre, at de har den rette koncentration.
Centrifuger cellerne for at pelleter dem, og resuspender dem derefter i CM-1-frysemedium.
Overfør de resuspenderede celler til cryovials.
Brug en langsom nedfrysningsmetode, før du overfører cellerne til langtidsopbevaring
Metode
Beskrivelse
Skridt
❄️
Manuel nedfrysning
En trinvis metode, der involverer gradvis temperatursænkning for at sikre cellernes levedygtighed
1️⃣ Anbring cellerne i frysemediet i en fryser på 4 °C i 40 minutter.
2️⃣ Overfør til en fryser på -80 °C i 24 timer.
3️⃣ Opbevar cellerne i flydende nitrogen til langtidsopbevaring
❄️
Brug af Mr. Frosty
En praktisk anordning, der giver mulighed for kontrollerede frysehastigheder uden elektrisk strøm
1️⃣ Forbered celler i kryovialer med frysemedium.
2️⃣ Placer kryovials i Mr. Frosty-beholderen.
3️⃣ Opbevar ved -80 °C i 24 timer, før de overføres til flydende nitrogen
❄️
Fryser med kontrolleret hastighed
En højpræcisionsfryser fra Thermo Fisher eller andre producenter, der er designet til kontrolleret temperatursænkning
1️⃣ Programmer enheden til gradvist at sænke temperaturen.
2️⃣ Placer de forberedte celler i fryseren.
3️⃣ Efter frysecyklussen overføres cellerne til flydende nitrogen
Opbevar kryovialerne ved temperaturer under -130 °C eller i flydende kvælstof til langtidsopbevaring.
Ingredienser
Indeholder FBS, DMSO, glukose, salte
Bufferkapacitet: pH = 7,2 til 7,6
Cytions Freeze Medium CM-1 er en pålidelig løsning til kryopræservering, der sikrer høj cellelevedygtighed og funktionalitet efter optøning til en lang række forskningsformål.
- og kyllingeleverceller, især under forhold med reduceret serum.
Ham's F-12K (Kaighn's) Medium er omhyggeligt formuleret for at optimere betingelserne for celledyrkning. Det har en beriget sammensætning, der giver forhøjede niveauer af essentielle komponenter som aminosyrer og natriumpyruvat samt yderligere elementer, herunder putrescin, thymidin, hypoxanthin og zink. Disse tilføjelser gør det muligt for forskere at supplere mediet med minimalt serum eller definerede komponenter til specifikke celletyper, hvilket letter præcise forsøgsbetingelser.
Især indeholder Ham's F-12K (Kaighn's) Medium ikke proteiner eller vækstfaktorer. Derfor er det ofte nødvendigt at supplere med vækstfaktorer og Fetal Bovine Serum (FBS), så forskere kan skræddersy mediet til kravene i deres specifikke cellelinjer. For at opnå optimal ydeevne skal koncentrationen af FBS optimeres omhyggeligt for hver enkelt cellelinje for at sikre optimal vækst og funktionalitet.
For at opretholde en fysiologisk pH-værdi anvender Ham's F-12K (Kaighn's) Medium et natriumbicarbonat-buffersystem (2,5 g/L), hvilket kræver et kontrolleret 5-10 % CO2-miljø under dyrkningen. Dette sikrer, at mediets pH-værdi forbliver inden for det ideelle område for cellevækst og levedygtighed
Kvalitetskontrol
pH = 7,2 +/
- 0,02 ved 20-25 °C.
Hvert parti er blevet testet for sterilitet og fravær af mycoplasma og bakterier.
Vedligeholdelse
Opbevares på køl ved +2 °C til +8 °C i mørke. Nedfrysning og opvarmning til +37 °C minimerer produktets kvalitet.
Opvarm ikke mediet til mere end 37 °C, og brug ikke ukontrollerbare varmekilder (f.eks. mikrobølgeovne).
Hvis kun en del af mediet skal bruges, skal du tage denne mængde ud af flasken og varme den op ved stuetemperatur.
Holdbarheden for alle medier undtagen basismediet er 8 uger fra fremstillingsdatoen.
Sammensætning
Komponenter
mg/L
Uorganiske salte
Calciumklorid x 2H2O
135,24
Kobber(II)sulfat x 5H2O
0,00
Jern(II)-sulfat x 7H2O
0,83
Magnesiumklorid x 6H2O
105,72
Magnesiumsulfat x 7H2O
394,49
Kaliumklorid
283,29
Kaliumdihydrogenfosfat
58,52
Natriumklorid
7597,20
dinatriumhydrogenfosfatvandfri
115,02
Zinksulfat x 7H2O
0,14
Andre komponenter
D(+)-Glucose vandfri
1260,00
Hypoxanthin
4,08
DL-α-liponsyre
0,21
Fenol rød
3,00
Putrescin x 2HCl
0,32
Natriumpyruvat
220,00
NaHCO3
2500,00
Thymidin
0,73
Aminosyrer
L-Alanin
17,82
L-arginin x HCl
421,40
L-Asparagin x H2O
30,02
L-Asparaginsyre
26,62
L-cystein x HCl x H2O
70,24
L-glutamin
292,20
L-glutaminsyre
29,42
Glycin
15,01
L-Histidin x HCl x H2O
41,92
L-isoleucin
7,87
L-Leucin
26,24
L-Lysin x HCl
73,04
L-Methionin
8,95
L-Phenylalanin
9,91
L-prolin
69,06
L-Serin
21,02
L-Threonin
23,82
L-Tryptofan
4,08
L-Tyrosin
10,87
L-Valin
23,42
Vitaminer
D(+)-Biotin
0,07
D-Calcium-pantothenat
0,48
Cholinklorid
13,96
Folinsyre
1,32
myo-Inositol
18,02
Nikotinamid
0,04
Pyridoxin x HCl
0,06
Riboflavin
0,04
Thiamin x HCl
0,34
Vitamin B12
1,36
Fosfatbufferet saltvand (PBS) er en meget anvendt bufferopløsning inden for biologisk og kemisk forskning. Den spiller en afgørende rolle i opretholdelsen af pH-balancen og osmolariteten under forskellige eksperimentelle procedurer, herunder vævsbehandling og cellekultur. Vores PBS-opløsning er omhyggeligt formuleret med ingredienser af høj renhed for at sikre stabilitet og pålidelighed i hvert eksperiment. Osmolariteten og ionkoncentrationerne i vores PBS efterligner nøje dem i menneskekroppen, hvilket gør den isotonisk og ugiftig for de fleste celler.
Sammensætning af vores PBS-opløsning
Vores PBS-opløsning er en pH-justeret blanding af ultrarene fosfatbuffere og saltopløsninger. Ved en 1X arbejdskoncentration indeholder den:
8000 mg/L natriumklorid (NaCl)
200 mg/L kaliumklorid (KCl)
1150 mg/L Natriumfosfat dibasisk vandfri (Na2HPO4)
200 mg/L Vandfri monobasisk kaliumfosfat (KH2PO4)
Denne sammensætning sikrer en optimal pH
- og ionbalance, der er velegnet til en lang række biologiske anvendelser.
Anvendelser af vores PBS-opløsning
Vores PBS-opløsning er ideel til forskellige anvendelser inden for biologisk forskning. Dens isotoniske og ikke-toksiske egenskaber gør den velegnet til fortynding af stoffer og skylning af cellebeholdere. PBS-opløsninger, der indeholder EDTA, er effektive til at løsne fastgjorte og sammenklumpede celler. Der bør dog ikke tilsættes divalente metaller som f.eks. zink til PBS, da det kan forårsage udfældning. I sådanne tilfælde anbefales Good's buffere. Derudover er vores PBS-opløsning et acceptabelt alternativ til viralt transportmedium til transport og opbevaring af RNA-vira, herunder SARS-CoV-2.
Kvalitetskontrol
Sterilt filtreret
Opbevaring og holdbarhed
Opbevares ved +2°C til +25°C, beskyttet mod lys.
Når den er åbnet, skal den opbevares ved 2 °C til 25 °C og bruges inden for 24 måneder.
Betingelser for forsendelse
Omgivelsestemperatur
Vedligeholdelse
Opbevares på køl ved +2 °C til +8 °C i mørke. Undgå frysning og hyppig opvarmning til +37 °C, da det forringer produktkvaliteten.
Opvarm ikke mediet til mere end 37 °C, og brug ikke ukontrollerede varmekilder som f.eks. mikrobølgeovne.
Hvis kun en del af mediet skal bruges, skal du fjerne den nødvendige mængde og varme den op til stuetemperatur før brug.
Sammensætning
Kategori
Komponenter
Koncentration (mg/L)
Salte
Kaliumklorid
200
Vandfrit monobasisk kaliumfosfat
200
Natriumklorid
8000
Natriumfosfat dibasisk vandfri
1150
RPMI 1640 Medium blev oprindeligt designet til at understøtte væksten af humane leukæmiceller i både suspensions
- og monolagskulturer, men har udviklet sig gennem modifikationer af forskere og kommercielle leverandører til at være velegnet til en lang række pattedyrsceller. Det er usædvanligt kompatibelt med cellelinjer som HeLa, Jurkat, MCF-7, PC12, PBMC, astrocytter og karcinomer.
RPMI 1640 Medium adskiller sig fra andre cellekulturmedier på grund af sin unikke sammensætning. Det indeholder en betydelig mængde fosfat, aminosyrer og vitaminer. Det omfatter især biotin, B12-vitamin og PABA, som ikke findes i Eagle's Minimal Essential Medium eller Dulbecco's Modified Eagle Medium. Desuden udviser RPMI 1640 Medium betydeligt forhøjede koncentrationer af vitaminerne inositol og cholin. Det indeholder dog ikke proteiner, lipider eller vækstfaktorer. Derfor er det ofte nødvendigt at supplere med 10 % føtalt kvægserum (FBS) for at skabe optimale betingelser for cellevækst.
Buffersystemet i RPMI 1640 Medium er baseret på natriumbicarbonat og kræver et 5-10 % CO2-miljø for at opretholde en fysiologisk passende pH-værdi. Inkluderingen af reduktionsmidlet glutathion adskiller yderligere dette medium fra andre.
Kvalitetskontrol
Sterilt filtreret
Opbevaring og holdbarhed
Opbevares ved +2 °C til +8 °C, beskyttet mod lys.
Når det er åbnet, skal det opbevares ved 4 °C og bruges inden for 6-8 uger.
Betingelser for forsendelse
Omgivelsestemperatur
Vedligeholdelse
Opbevares på køl ved +2 °C til +8 °C i mørke. Undgå frysning og hyppig opvarmning til +37 °C, da det forringer produktkvaliteten.
Opvarm ikke mediet til mere end 37 °C, og brug ikke ukontrollerede varmekilder som f.eks. mikrobølgeovne.
Hvis kun en del af mediet skal bruges, skal du fjerne den nødvendige mængde og varme den op til stuetemperatur før brug.
Sammensætning
Kategori
Komponenter
Koncentration (mg/L)
Aminosyrer
Glycin
10.00
L-Alanyl-L-Glutamin
434.40
L-arginin
200.00
L-AsparaginH2O
56.82
L-Asparaginsyre
20.00
L-Cystin 2HCl
65.20
L-glutaminsyre
20.00
L-Histidin HClH2O
20.27
L-Hydroxy-L-Prolin
20.00
L-Isoleucin
50.00
L-Leucin
50.00
L-Lysin HCl
40.00
L-Methionin
15.00
L-Phenylalanin
15.00
L-Prolin
20.00
L-Serin
30.00
L-Threonin
20.00
L-Tryptofan
5.00
L-Tyrosin 2Na 2H2O
28.83
L-Valin
20.00
Vitaminer
p-Amino Benzoic Acid
1.00
D-Biotin
0.20
Cholinklorid
3.00
D-Calcium Pantothenat
0.25
Folinsyre
1.00
myo-Inositol
35.00
Nikotinamid
1.00
Pyridoxin HCl
1.00
Riboflavin
0.20
Thiamine HCl
1.00
Vitamin B12
0.005
Uorganiske salte
Ca(NO3)2 4H2O
100.00
KCl
400.00
MgSO4 7H2O
100.00
NaCl
6000.00
NaHCO3
2000.00
Na2HPO4
800.00
Andre komponenter
D-Glucose
2000.00
L-glutathion reduceret
1.00
Fenolrødt natriumsalt
5.30
Denne unikke formulering kombinerer Dulbeccos Modified Eagle Medium (DMEM) og Ham's F-12 (Ham's Nutrient Mixture F-12) i et præcist forhold på 1:1. Tilsætningen af L-glutamin forbedrer sammensætningen yderligere.
DMEM, der stammer fra Eagle's Minimal Essential Medium (EMEM), tilbyder en øget koncentration af aminosyrer og vitaminer sammenlignet med sin forgænger. I modsætning hertil er Ham's F-12 baseret på Ham's F-10-medium, hvilket giver et komplementært sæt af essentielle komponenter.
For at understøtte optimal cellevækst er det almindelig praksis at supplere DMEM:Ham's F12 med FBS i en typisk koncentration på 5-10 %. Denne tilsætning er nødvendig, da mediet mangler væksthormoner, lipider og proteiner, der er afgørende for celleudviklingen.
DMEM:Ham's F12 indeholder et pH-buffersystem og tilsættes ofte fenolrødt, en pH-indikator. Dyrkede celler i DMEM:Ham's F12 eller ethvert medium, der anvender bicarbonatbuffersystemet, kræver et kontrolleret CO2-miljø på 5-10 % for at opretholde passende pH-niveauer.
Kvalitetskontrol
Sterilfiltreret
Opbevaring og holdbarhed
Opbevares ved +2 °C til +8 °C, beskyttet mod lys.
Når produktet er åbnet, skal det opbevares ved 4 °C og bruges inden for 6–8 uger.
Forsendelsesbetingelser
Omgivelsestemperatur
Opbevaring
Opbevares i køleskab ved +2 °C til +8 °C i mørke. Undgå frysning og hyppig opvarmning til +37 °C, da dette nedsætter produktets kvalitet.
Mediet må ikke opvarmes til over 37 °C, og der må ikke anvendes ukontrollerede varmekilder, såsom mikrobølgeovne.
Hvis kun en del af mediet skal bruges, skal den nødvendige mængde tages ud og opvarmes til stuetemperatur før brug.
Sammensætning
Kategori
Bestanddele
Koncentration (mg/L)
Aminosyrer
Glycin
18,75
L-alanin
4,45
L-arginin-HCl
147,50
L-asparagin H₂O
7,50
L-asparaginsyre
6,65
L-cystein HCl H₂O
17,56
L-cystin 2 HCl
31,29
L-glutaminsyre
7,35
L-glutamin
365,00
L-histidin-HCl-H₂O
31,48
L-isoleucin
54,47
L-leucin
59,05
L-lysin-HCl
91,25
L-methionin
17,24
L-phenylalanin
35,48
L-prolin
17,25
L-serin
26,25
L-threonin
53,45
L-tryptofan
9,02
L-tyrosin 2 Na 2 H2O
55,79
L-valin
52,85
Vitaminer
D-biotin
0,0035
Cholinchlorid
8,98
D-calciumpantothenat
2,24
Folinsyre
2,66
myo-inositol
12,60
Nikotinamid
2,02
Pyridoxin-HCl
0,031
Pyridoxal-HCl
2,00
Riboflavin
0,219
Thiamin-HCl
2,17
Vitamin B12
0,68
Uorganiske salte
CaCl2 2 H2O
154,50
CuSO4 5 H2O
0,0013
Fe(NO3)3 9 H2O
0,05
FeSO4 7 H2O
0,417
KCl
311,80
MgCl2 6 H2O
61,20
MgSO4 7 H2O
100,00
NaCl
6996,00
NaHCO3
1200,00
Na2HPO4
71,02
NaH2PO4 2 H2O
70,87
ZnSO4 7 H2O
0,432
Andre komponenter
D-glukose
3151,00
Hypoxanthin
2,40
HEPES
3574,50
Linolsyre
0,042
Lipoinsyre
0,105
Fenolrødt natriumsalt
8,63
Putrescin-2-HCl
0,081
Natrium-pyruvat
55,00
Thymidin
0,365
- 0,02 ved 20-25 °C. Hvert parti er testet for sterilitet og fravær af mycoplasma og bakterier. Opbevaring Opbevares i køleskab ved +2 °C til +8 °C i mørke. Frysning og opvarmning til +37 °C forringer produktets kvalitet. Opvarm ikke mediet til over 37 °C, og brug ikke ukontrollerbare varmekilder (f.eks. mikrobølgeovne). Hvis kun en del af mediet skal bruges, skal denne mængde tages ud af flasken og opvarmes til stuetemperatur. Holdbarheden for alle medier undtagen basismediet er 6 til 8 uger fra åbningsdatoen. Sammensætning Komponenter mg/L Uorganiske salteCalciumchlorid x 2H2O132,00 Magnesiumsulfat97,67 Kaliumchlorid400 Natriumchlorid6.460,00 Dinatriumhydrogenphosphat (vandfrit)504,00 Andre komponenterD(+)-Glukose (vandfri)3.000,00 Glutathion (reduceret)0,5 Kødpeptone600,00 Phenolrødt natriumsalt11 AminosyrerL-alanin13,36 L-arginin x HCl42,14 L-asparagin x H2O45,03 L-asparaginsyre19,97 L-cystein x HCl x H2O31,75 L-glutamin (stabil)219,15 L-glutaminsyre22,07 Glycin7,51 L-histidin x HCl x H2O20,96 L-hydroxyprolin19,67 L-isoleucin39,36 L-leucin39,36 L-lysin x HCl36,54 L-methionin14,92 L-phenylalanin16,52 L-prolin17,27 L-serin26,28 L-threonin17,87 L-tryptofan3,06 L-tyrosin-dinatriumsalt26,10 L-valin17,57 Vitaminerp-Aminobenzoesyre1,0 Ascorbinsyre0,56 D(+)-biotin0,20 D-calciumpantothenat0,20 Kolinchlorid5,0 Folsyre10 Myo-inositol36 Nicotinamid0,5 Nikotinsyre0,5 Pyridoxal HCl0,5 Pyridoxin HCl0,50 Riboflavin0,2 Thiamin HCl0,2 Vitamin B122,0
Medium 199 har en række anvendelsesmuligheder inden for området. Det kan effektivt opretholde cumulus-oocyt-komplekset (COC) og understøtte in vitro-modning af oocytter. Derudover anvendes det til skylning af aspirationsslanger under ægopsamling fra tyske Holstein-køer. Desuden fungerer Medium 199 som et fremragende medium til dyrkning af hjerteendotelceller fra rotter. Disse anvendelser viser Medium 199's alsidighed og tilpasningsevne til forskellige eksperimentelle behov.
Historie
Udviklingen af Medium 199 i 1950'erne markerede et betydeligt fremskridt inden for vævskulturmedier. Før det blev introduceret, var mange dyrkningsmedier afhængige af produkter fra dyr og vævsekstrakter. Men Morgan og hans kolleger revolutionerede området ved at formulere en fuldstændig defineret ernæringskilde til cellekulturer. Gennem deres eksperimenter med forskellige kombinationer af vitaminer, aminosyrer og andre faktorer opdagede de de enestående vækstfremmende egenskaber ved Medium 199.
Kvalitetskontrol
pH = 7,2 +/
- 0,02 ved 20-25 °C.
Hvert parti er testet for sterilitet og fravær af mycoplasma og bakterier.
Vedligeholdelse
Opbevares på køl ved +2°C til +8°C i mørke. Frysning og opvarmning op til +37° C minimerer produktets kvalitet.
Opvarm ikke mediet til mere end 37 °C, og brug ikke ukontrollerbare varmekilder (f.eks. mikrobølgeovne).
Hvis kun en del af mediet skal bruges, skal du tage denne mængde ud af flasken og varme den op ved stuetemperatur.
Holdbarheden for alle medier undtagen basismediet er 8 uger fra fremstillingsdatoen.
Sammensætning
Komponenter
mg/L
Uorganiske salte
Calciumchlorid x 2H2O
264,92
Jern(III)-nitrat x 9H2O
0,72
Magnesiumsulfat
97,67
Kaliumklorid
400,00
Natriumacetat x 3H2O
82,95
Natriumklorid
6,800.00
Natriumdihydrogenfosfat x H2O
140,00
Andre komponenter
Adeninsulfat
10,00
AMP
0,20
ATP
1,00
Kolesterol
0,20
2'-Deoxyribose
0,50
D(+)-Glucose vandfri
1,000.00
Glutathion (rød)
0,05
Guanin x HCl
0,30
Hypoxanthin
0,30
Fenol rød
10,00
D-Ribose
0,50
Thymin
0,30
Tween 80
4,90
Uracil
0,30
Xanthin
0,30
NaHCO3
2,200.00
Aminosyrer
L-Alanin
25,00
L-Arginin x HCl
70,00
L-Asparaginsyre
30,00
L-Cystein x HCl x H2O
0,10
L-Cystein
20,00
L-Glutamin stabil
149,00
L-glutaminsyre
67,00
Glycin
50,00
L-Histidin x HCl x H2O
21,88
L-Hydroxyprolin
10,00
L-Isoleucin
20,00
L-Leucin
60,00
L-Lysin x HCl
70,00
L-Methionin
15,00
L-Phenylalanin
25,00
L-prolin
40,00
L-Serin
25,00
L-Threonin
30,00
L-Tryptofan
10,00
L-Tyrosin
40,00
L-Valin
25,00
Vitaminer
4-Amino benzoesyre
0,05
Ascorbinsyre
0,05
D(+)-Biotin
0,01
Calciferol
0,10
D-Calcium pantothenat
0,01
Cholinklorid
0,50
Folinsyre
0,01
myo-Inositol
0,05
Menadion
0,01
Nikotinsyre
0.025
Nikotinamid
0.025
Pyridoxal x HCl
0.025
Pyridoxol x HCl
0.025
Riboflavin
0,01
DL-α-tocopherolphosphat dinatriumsalt
0,01
Thiamin x HCl
0,01
Vitamin A-acetat
0,14
IMDM er velegnet til hurtigt voksende cellekulturer med høj densitet, herunder Jurkat-, COS-7
- og makrofagceller. De forskellige modifikationer af IMDM, der er tilgængelige til en række celledyrkningsapplikationer, kan findes ved hjælp af medievælgerværktøjet. Flydende medier giver vigtige næringsstoffer til alle celledyrkningsprogrammer. Alle vores celledyrkningsmedier af høj kvalitet fremstilles i henhold til den oprindeligt offentliggjorte formel eller de modifikationer, der er nødvendige for at sikre en ensartet ydeevne og stabilitet i dyrkningsmediet.
IMDM vs. DMEM
IMDM indeholder kaliumnitrat i stedet for jernnitrat samt HEPES og natriumpyruvat. De ekstra komponenter i IMDM gør det mere velegnet til specialiserede celletyper og specifikke anvendelser end DMEM.
IMDM vs. RPMI
IMDM og RPMI har forskellige formuleringer, som kan være relevante for PMA/ionomycin-stimulering. En væsentlig forskel er koncentrationen af Ca2+. Mens RPMI indeholder 0,42 mM Ca2+, indeholder IMDM 1,49 mM.
Kvalitetskontrol
pH = 7,2 +/
- 0,02 ved 20-25 °C.
Hvert parti er testet for sterilitet og fravær af mycoplasma og bakterier.
Vedligeholdelse
Opbevares på køl ved +2 °C til +8 °C i mørke. Frysning og opvarmning op til +37° C minimerer produktets kvalitet.
Opvarm ikke mediet til mere end 37 °C, og brug ikke ukontrollerbare varmekilder (f.eks. mikrobølgeovne).
Hvis kun en del af mediet skal bruges, skal du tage denne mængde ud af flasken og varme den op ved stuetemperatur.
Holdbarheden for alle medier undtagen basismediet er 8 uger fra fremstillingsdatoen.
Sammensætning
Komponenter
mg/L
Uorganiske salte
Calciumklorid x 2 H2O
219,00
Kaliumklorid
330,00
Kaliumnitrat
0.076
Vandfrit magnesiumsulfat
97,73
Natriumklorid
4,505.00
Vandfrit natriumdihydrogenfosfat
109,00
Natriumselenit
0,02
Andre komponenter
D(+)-Glucose vandfri
4,500.00
HEPES
5,958.00
Natriumpyruvat
110,00
Fenol rød
15,00
Aminosyrer
L-Alanin
25,00
L-Arginin x HCl
84,00
L-Asparagin x H2O
25,00
L-Asparaginsyre
30,00
L-Cystin x 2HCl
91,24
L-Glutamin
584,00
L-glutaminsyre
75,00
Glycin
30,00
L-Histidin x HCl x H2O
42,00
L-Isoleucin
104,80
L-Leucin
104,80
L-Lysin x HCl
146,20
L-Methionin
30,00
L-Phenylalanin
66,00
L-Prolin
40,00
L-Serin
42,00
L-Threonin
95,20
L-Tryptofan
16,00
L-Tyrosin x 2Na
104,20
L-Valin
93,60
Vitaminer
D(+)-Biotin
0.013
D-Calcium pantothenat
4,00
Cholinklorid
4,00
Folinsyre
4,00
myo-Inositol
7,20
Medier til cellekultur: Et overblik
Inden for biovidenskab er en af de vigtigste metoder cellekultur. Udtagning af celler, væv eller organer fra et dyr eller en plante og efterfølgende implantation af disse celler, væv eller organer i et kunstigt miljø, der er gunstigt for deres overlevelse og/eller vækst, er det, der menes med udtrykket "cellekultur" De grundlæggende miljømæssige behov for optimal celleudvikling er kontrolleret temperatur, et substrat til cellevedhæftning, et passende vækstmedium og en inkubator, der opretholder den optimale pH og osmolalitet. Cellerne skal have disse betingelser for at kunne vokse til deres fulde potentiale.
Valget af et passende vækstmedium til in vitro-dyrkning er den fase i cellekulturen, der både er den mest kritiske og den mest afgørende. Et vækstmedie, også kendt som dyrkningsmedie, er en væske eller gel, der er formuleret til at fremme organismers udvikling i mikroskopisk, cellulær eller plantelignende skala. Mediet, der bruges til dyrkning af celler, indeholder ofte en tilstrækkelig forsyning af energi og stoffer, der styrer cellecyklussen. Hovedkomponenterne i et dyrkningsmedie omfatter aminosyrer, vitaminer, uorganiske salte, glukose og serum. Serummet tilsættes mediet, fordi det fungerer som en kilde til vækstfaktorer, hormoner og vedhæftningsfaktorer. Ud over at levere næringsstoffer bidrager mediet også til at opretholde pH- og osmolalitetsniveauer.
Typer af medier, der bruges i cellekultur
Både menneske- og dyreceller har potentiale til at blive dyrket i enten et kunstigt eller syntetisk medium eller et helt naturligt medium, der er suppleret med naturlige elementer. I det følgende giver vi dig et overblik over de forskellige medietyper, der er tilgængelige i øjeblikket.
Naturlige medier
Kun biologiske væsker, der findes i deres naturlige tilstand, kan findes i naturlige medier. Naturlige medier er meget nyttige og nemme at bruge til dyrkning af en lang række dyrecelletyper. Den manglende forståelse af de præcise komponenter, der indgår i naturlige medier, er den primære faktor, der bidrager til den lave repeterbarhed af resultater, der opnås ved hjælp af naturlige medier.
Kunstige medier
Fremstilling af kunstige eller syntetiske medier indebærer tilsætning af næringsstoffer (både organiske og uorganiske), serumproteiner, kulhydrater, cofaktorer, vitaminer og salte samt O2- og CO2-gasfaser [1].
Forskellige typer kunstige medier er blevet udviklet for at opfylde en eller flere af de følgende funktioner: 1) Umiddelbar overlevelse (en afbalanceret saltopløsning med en præcis pH-værdi og osmotisk tryk). 2) Langvarig overlevelse (en afbalanceret saltopløsning suppleret med forskellige formuleringer af organiske kemikalier og/eller serum). 3) Ubestemt udvikling. 4) Specialiserede funktioner.
Der er fire forskellige klassifikationer for kunstige medier:
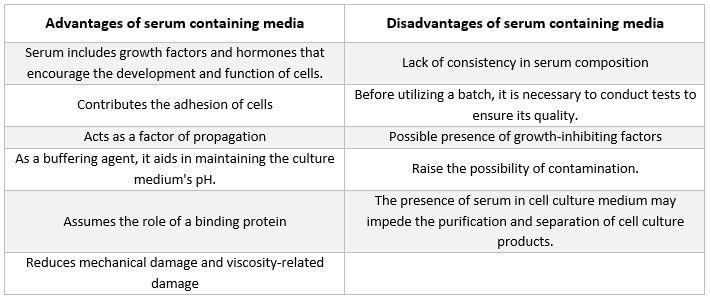
Serumholdige medier
Den hyppigste form for tilskud, der findes i medier, der bruges til dyrkning af dyreceller, er føtalt bovint serum. Det tilsættes til dyrkningsmediet som et billigt supplement for at opnå de bedst mulige vækstbetingelser. Ud over at fungere som transportør eller chelator for næringsstoffer, der er ustabile eller uopløselige i vand, hormoner og vækstfaktorer, proteasehæmmere og andre stoffer, binder og neutraliserer serummet også skadelige molekyler.
Serumfrit medium
Tilstedeværelsen af serum i medierne har en række ulemper og har potentiale til at forårsage store fortolkningsfejl i immunologisk forskning [2, 3]. Der er blevet udviklet en række forskellige serumfri medier [4, 5]. Disse medier er generelt specifikt formuleret til at understøtte dyrkningen af en enkelt celletype, såsom Knockout Serum Replacement og Knockout DMEM fra Thermo Fisher Scientific, og mTESR medium fra Stem Cell Technologies [6], til stamceller [7].
Derudover indeholder disse medier definerede mængder af oprensede vækstfaktorer, lipoproteiner og andre proteiner, som ellers typisk leveres af serummet [8]. Disse medier omtales ofte som "definerede kulturmedier", da de komponenter, der udgør disse medier, er velkendte.
Kemisk definerede medier
Disse medier omfatter ultrarene uorganiske og organiske komponenter, der ikke er blevet forurenet af nogen form for kontaminering. De kan også indeholde rene proteintilsætninger som f.eks. vækstfaktorer.
den genetiske modifikation af bakterier eller gær sammen med tilsætning af bestemte fedtsyrer, vitaminer, kolesterol og aminosyrer resulterer i produktion af deres bestanddele [9].
Proteinfrie medier
Proteinfrie medier er dem, der slet ikke indeholder noget protein, men i stedet kun indeholder ikke-proteinelementer. Sammenlignet med medier med tilsat serum fremmer brugen af medier uden tilsat protein større celleproliferation og proteinudtryk og gør det lettere at oprense ethvert produkt, der genereres i en downstream-proces [10-12]. Protein er ikke inkluderet i formuleringer som MEM og RPMI-1640. Der kan dog gives et proteintilskud, hvis det er nødvendigt.
Kulturmedier og deres grundlæggende komponenter
Kommercielle dyrkningsmedier kan købes som pulver eller væske og indeholder ofte en række næringsstoffer som aminosyrer, glukose, salte, vitaminer og andre kosttilskud.
Behovene for disse komponenter er forskellige for hver cellelinje, og disse variationer er ansvarlige for det store antal forskellige formuleringer af medier. Hver komponent er ansvarlig for en bestemt funktion, som vil blive beskrevet i de følgende afsnit:
Buffersystemer
For at opretholde optimale vækstbetingelser skal pH-værdien kontrolleres, hvilket ofte sker ved hjælp af et af to buffersystemer:
Naturligt buffersystem
CO2/H2CO3-forholdet i atmosfæren er det samme som i mediet, hvilket skaber en naturlig buffermekanisme. For at bevare den naturlige buffermekanisme skal kulturer holdes i et luftmiljø med 5-10 % CO2, hvilket ofte opnås ved at bruge en CO2-inkubator. En af de bedste ting ved at bruge en naturlig buffer er, hvor billig og sikker den er.
HEPES
Kemisk buffering ved hjælp af zwitterionen HEPES har en større bufferkapacitet i pH-området 7,2-7,4 og behøver ikke et reguleret gasformigt miljø. For bestemte celletyper kan en større dosis HEPES være skadelig. Medier, der indeholder HEPES, er også meget mere modtagelige for de fototoksiske virkninger af fluorescerende lys [13].
Fenolrød
PH-indikatoren fenolrødt er ofte inkluderet i kommercielt tilgængelige dyrkningsmedier, hvilket giver mulighed for kontinuerlig overvågning af pH. Ved at udvide cellerne forårsager de metabolitter, der produceres af disse celler, et skift i pH og derfor en farveændring i mediet. Fenolrødt har en dobbelt effekt på et mediums farve, idet det bliver gult ved sur pH og lilla ved basisk pH. pH 7,4, den optimale værdi for cellekultur, får mediet til at fremstå fluorescerende rødt.
Men fenolrødt har et par ulemper: For det første er fenolrødt i stand til at simulere virkningen af en række steroidhormoner, primært østrogen [14]. Når man studerer østrogenfølsomme celler som brystvæv, anbefales det derfor at bruge et medium uden fenolrødt. Natrium-kalium-balancen forstyrres af tilstedeværelsen af fenolrødt i flere serumfrie formuleringer. Tilsætning af serum eller bovint hypofysehormon til mediet kan modvirke denne effekt [15]. For det tredje forhindres detektion i flowcytometriske eksperimenter af tilstedeværelsen af fenolrødt.
Uorganiske salte
Medier, der indeholder uorganiske salte, såsom natrium-, kalium- og calciumioner, hjælper med at opretholde den osmotiske ligevægt og regulere membranpotentialet.
Aminosyrer
Da aminosyrer er de grundlæggende komponenter i protein, er de en vigtig komponent i hvert eneste cellevækstmedie, der nogensinde er blevet udtænkt. Da celler ikke er i stand til selv at producere visse aminosyrer, er det vigtigt, at dyrkningsmediet indeholder essentielle aminosyrer. De er nødvendige for cellernes spredning, og den koncentration, de er til stede i, bestemmer den maksimale celletæthed, der kan opnås. Især L-glutamin, som er en essentiel aminosyre, er afgørende.
L-glutamin fungerer som en sekundær energikilde til stofskiftet og bidrager med nitrogen til produktionen af NAD, NADPH og nukleotider. Da L-glutamin er en ustabil aminosyre, der med tiden ændrer sig til en form, som cellerne ikke kan udnytte, skal den gives til mediet.
Desuden kan der tilføres ikke-essentielle aminosyrer til mediet for at genopbygge dem, der er blevet brugt op i løbet af vækstprocessen. Cellernes vækst boostes, og deres levedygtighed øges, når vækstmediet suppleres med ikke-essentielle aminosyrer.
Kulhydrater
Kulhydrater i form af sukkerarter er den vigtigste energikilde. Mange af medierne indeholder også maltose og fruktose ud over de mere almindelige sukkerarter glukose og galaktose.
Proteiner og peptider
Albumin, transferrin og fibronektin er de mest almindeligt anvendte proteiner og peptider. De er især vigtige i medier, der ikke indeholder serum. Albumin, transferrin, aprotinin, fetuin og fibronektin er nogle af de proteiner, der kan findes i serum, som er en rig kilde til protein.
Albumin er det primære protein i blodet, og dets funktion er at binde og transportere forskellige stoffer, herunder vand, salte, frie fedtsyrer, hormoner og vitaminer, mellem forskellige organer og celler. Albumins evne til at binde sig til kemikalier gør det til en effektiv kandidat til at fjerne skadelige forbindelser fra det medium, som cellerne dyrkes i.
Aprotinin er et beskyttende middel i cellekultursystemer, da det er stabilt ved neutral og sur pH samt modstandsdygtigt over for høje temperaturer og den ødelæggelse, der kan forårsages af proteolytiske enzymer. Det er i stand til at hæmme en række serinproteaser, herunder bl.a. trypsin.
Fetuin er et glykoprotein, der kan påvises i større mængder i serum fra fostre og nyfødte dyr sammenlignet med voksnes serum. Derudover fungerer det som en serinproteasehæmmer. Proteinet fibronektin er en vigtig komponent i processen med celleadhæsion. Transferrin er et protein, der transporterer jern og er ansvarlig for at levere jern til cellernes membraner.
Fedtsyrer og lipider
De spiller en afgørende rolle i det serumfrie medium, når der ikke er noget serum.
Vitaminer
Mange vitaminer er nødvendige for cellernes udvikling og spredning. Vitaminer kan ikke produceres i tilstrækkelige mængder af cellerne og er derfor vigtige i vævskulturer som kosttilskud.
I cellekulturer er serum den primære kilde til vitaminer, men medierne behandles også med forskellige vitaminer for at gøre dem egnede til en bestemt celletype. Typisk bruges B-vitaminerne til vækststimulering.
Sporstoffer
Kemiske elementer som kobber, zink, selen og tricarboxylsyreintermediater er kendt som sporstoffer. Sporstoffer tilsættes ofte til medier, der ikke indeholder serum, for at erstatte dem, der typisk er til stede i serum. Disse elementer er vigtige kemiske komponenter, som er nødvendige for en sund celleudvikling. Mange biokemiske reaktioner er afhængige af visse mikronæringsstoffer, f.eks. enzymaktivitet.
Medietilskud
Det fulde vækstmedie, der foreslås til visse cellelinjer, har brug for ekstra komponenter, som ikke findes i basismediet og serum. Disse kosttilskud understøtter cellevækst og passende metabolisk funktion.
Selvom hormoner, vækstfaktorer og signalmolekyler er afgørende for en passende spredning af bestemte cellelinjer, skal følgende forholdsregler altid tages: Da tilsætning af kosttilskud kan ændre osmolaliteten i det komplette vækstmedium, hvilket kan hæmme celleudviklingen, anbefales det altid at kontrollere osmolaliteten efter tilsætning af kosttilskud. For de fleste cellelinjer ligger den optimale osmolalitet mellem 260 og 320 mOSM/kg.
Antibiotika
Antibiotika bruges ofte til at hæmme udviklingen af bakterie- og svampeforureninger [16], selvom de ikke er afgørende for cellevækst. Da antibiotika kan skjule forurening med mycoplasma og resistente bakterier, anbefales det ikke at bruge dem rutinemæssigt til celledyrkning [17, 18].
Desuden kan antibiotika forstyrre metabolismen i overfølsomme celler. Penicillin-streptomycin-kombinationerne fra MilliporeSigma og Life Technologies bruges ofte. Plasmocin er blevet brugt til dyrkning af gliomcellelinjerne TS603, TS516 og BT260 (19), og det har vist sig at være effektivt til at fjerne mycoplasmaforurening (20).
Serum
Albuminer, vækstfaktorer og væksthæmmere er alle til stede i serum. Serum er en af de vigtigste komponenter i cellekulturmediet, fordi det indeholder aminosyrer, proteiner, vitaminer (især fedtopløselige vitaminer som A, D, E og K), kulhydrater, lipider, hormoner, vækstfaktorer, mineraler og sporstoffer.
Serum fra fostre og kalve anvendes ofte til at fremme udviklingen af dyrkede celler. Fosterserum er en rigelig kilde til vækstfaktorer og er velegnet til cellekloning og udvikling af følsomme celler. På grund af dets mindre vækstfremmende egenskaber anvendes kalveserum i kontaktinhiberingsforsøg. Normale vækstmedier indeholder ofte 2-10 % serum. Tilsætning af serum til dyrkningsmediet tjener følgende formål [21]:
-
Serummet leverer de essentielle næringsstoffer til cellerne (både i opløsning og bundet til proteiner).
-
Flere vækstfaktorer og hormoner, der er involveret i vækstfremme og specialiseret celleaktivitet, er inkluderet i serum.
-
Det indeholder mange bindende proteiner, som albumin og transferrin, der transporterer andre kemikalier ind i cellen. For eksempel leverer albumin fedtstoffer, vitaminer, hormoner osv. ind i cellerne.
-
Det indeholder også proteiner som fibronektin, der øger cellernes vedhæftning til underlaget. Derudover producerer det spredningselementer, der hjælper med celleudvidelse før deling.
-
Det leverer proteasehæmmere, som forhindrer proteolyse i cellerne.
-
Det indeholder også mineraler som Na+, K+, Zn2+ og Fe2+.
-
Det øger mediets viskositet og beskytter dermed cellerne mod mekanisk skade under omrøring af suspensionskulturen.
-
Det er også en buffer.
Referencer
[1] Morgan J, Morton H, Parker R. Ernæring af dyreceller i vævskultur; indledende undersøgelser af et syntetisk medium. Proc Soc Exp Biol Med. 1950;73:1-8
[2] Kerbel R, Blakeslee D. Hurtig adsorption af en føtal kalveserumkomponent af pattedyrsceller i kultur. En potentiel kilde til artefakter i undersøgelser af antisera mod cellespecifikke antigener. Immunology. 1976;31:881-91
[3] Sula K, Draber P, Nouza K. Tilsætning af serum til det medium, der anvendes til fremstilling af cellesuspensioner, som en mulig kilde til artefakter i cellemedierede reaktioner undersøgt ved hjælp af den popliteale lymfeknudetest. J Immunogenet. 1980;7:483-9
[4] Mariani E, Mariani A, Monaco M, Lalli E, Vitale M, Facchini A. Kommercielle serumfrie medier: vækst af hybridomer og produktion af monoklonale antistoffer. J Immunol Methods. 1991;145:175-83
[5] Barnes D, Sato G. Metoder til vækst af dyrkede celler i serumfrit medium. Anal Biochem. 1980;102:255-70
[6] Yu H, Lu S, Gasior K, Singh D, Vazquez Sanchez S, Tapia O,et al. HSP70 chaperoner RNA-fri TDP-43 ind i anisotropiske intranukleare flydende sfæriske skaller. Videnskab. 2021;371:
[7] Meharena H, Marco A, Dileep V, Lockshin E, Akatsu G, Mullahoo J,et al. Down-syndrome-induceret senescens forstyrrer den nukleare arkitektur af neurale progenitorer. Cell Stem Cell. 2022;29:116-130.e7
[8] Iscove N, Melchers F. Fuldstændig erstatning af serum med albumin, transferrin og sojabønne-lipid i kulturer af lipopolysaccharid-reaktive B-lymfocytter. J Exp Med. 1978;147:923-33
[9] Stoll T, Muhlethaler K, von Stockar U, Marison I. Systematisk forbedring af et kemisk defineret proteinfrit medium til vækst af hybridomer og produktion af monoklonale antistoffer. J Biotechnol. 1996;45:111-23
[10] Darfler F. Et proteinfrit medium til vækst af hybridomer og andre celler i immunsystemet. In Vitro Cell Dev Biol. 1990;26:769-78
[11] Barnes D, Sato G. Serumfri cellekultur: en samlende tilgang. Cell. 1980;22:649-55
[12] Hamilton W, Ham R. Klonal vækst af cellelinjer fra kinesisk hamster i proteinfrie medier. In Vitro. 1977;13:537-47
[13] Zigler J, Lepe Zuniga J, Vistica B, Gery I. Analyse af de cytotoksiske virkninger af lyseksponeret HEPES-holdigt kulturmedium. In Vitro Cell Dev Biol. 1985;21:282-7
[14] Berthois Y, Katzenellenbogen J, Katzenellenbogen B. Fenolrødt i vævskulturmedier er et svagt østrogen: implikationer vedrørende studiet af østrogenresponsive celler i kultur. Proc Natl Acad Sci U S A. 1986;83:2496-500
[15] Karmiol S. Udvikling af serumfrie medier. In: Master JRW, editor. Animal Cell culture, 3. udgave. Oxford:Oxford University Press; 2000.
[16] Perlman D. Brug af antibiotika i cellekulturmedier. Methods Enzymol. 1979;58:110-6
[17] McGarrity G. Spredning og kontrol af mykoplasmainfektion i cellekulturer. In Vitro. 1976;12:643-8
[18] Masters J, Stacey G. Changing medium and passaging cell lines. Nat Protoc. 2007;2:2276-84
[19] Chakraborty A, Laukka T, Myllykoski M, Ringel A, Booker M, Tolstorukov M,et al. Histone demethylase KDM6A senses directly oxygen to control chromatin and cell fate. Science. 2019;363:1217-1222
[20] Molla Kazemiha V, Azari S, Amanzadeh A, Bonakdar S, Shojaei Moghadam M, Habibi Anbouhi M,et al. Efficiency of Plasmocin™ on various mammalian cell lines infected by mollicutes in comparison with commonly used antibiotics in cell culture: a local experience. Cytotechnology. 2011;63:609-20
[21] Kragh Hansen U. Molekylære aspekter af ligandbinding til serumalbumin. Pharmacol Rev. 1981;33:17-53