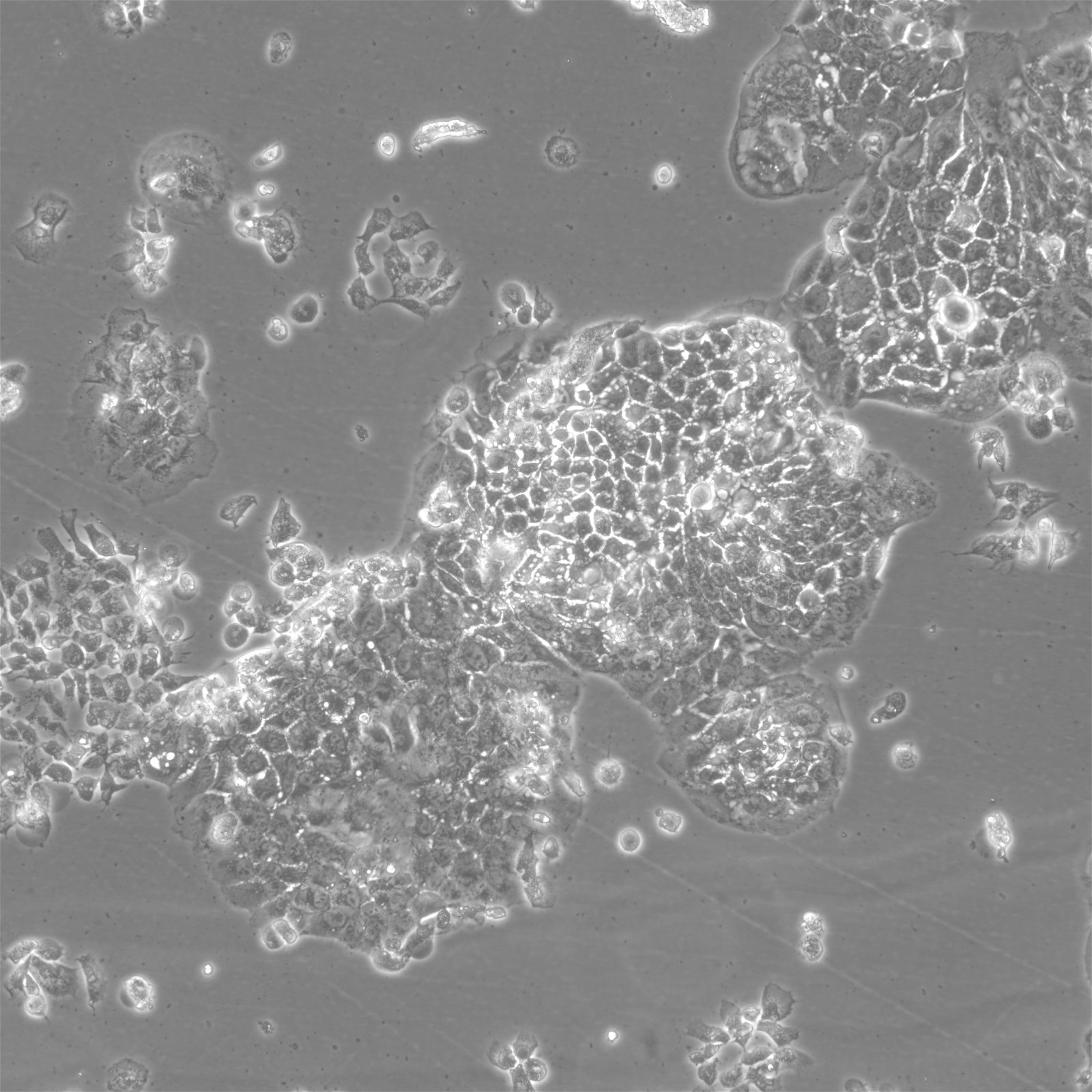
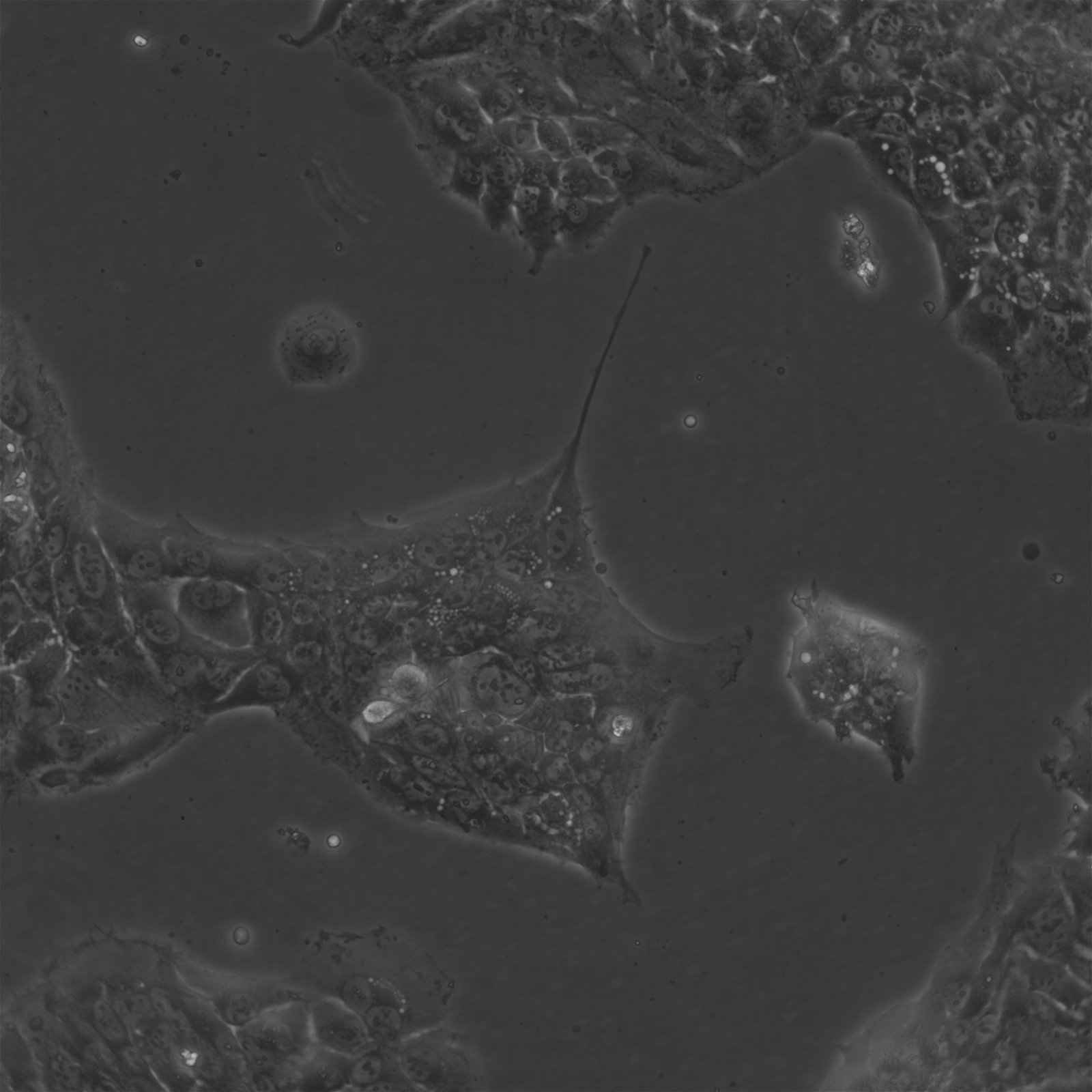
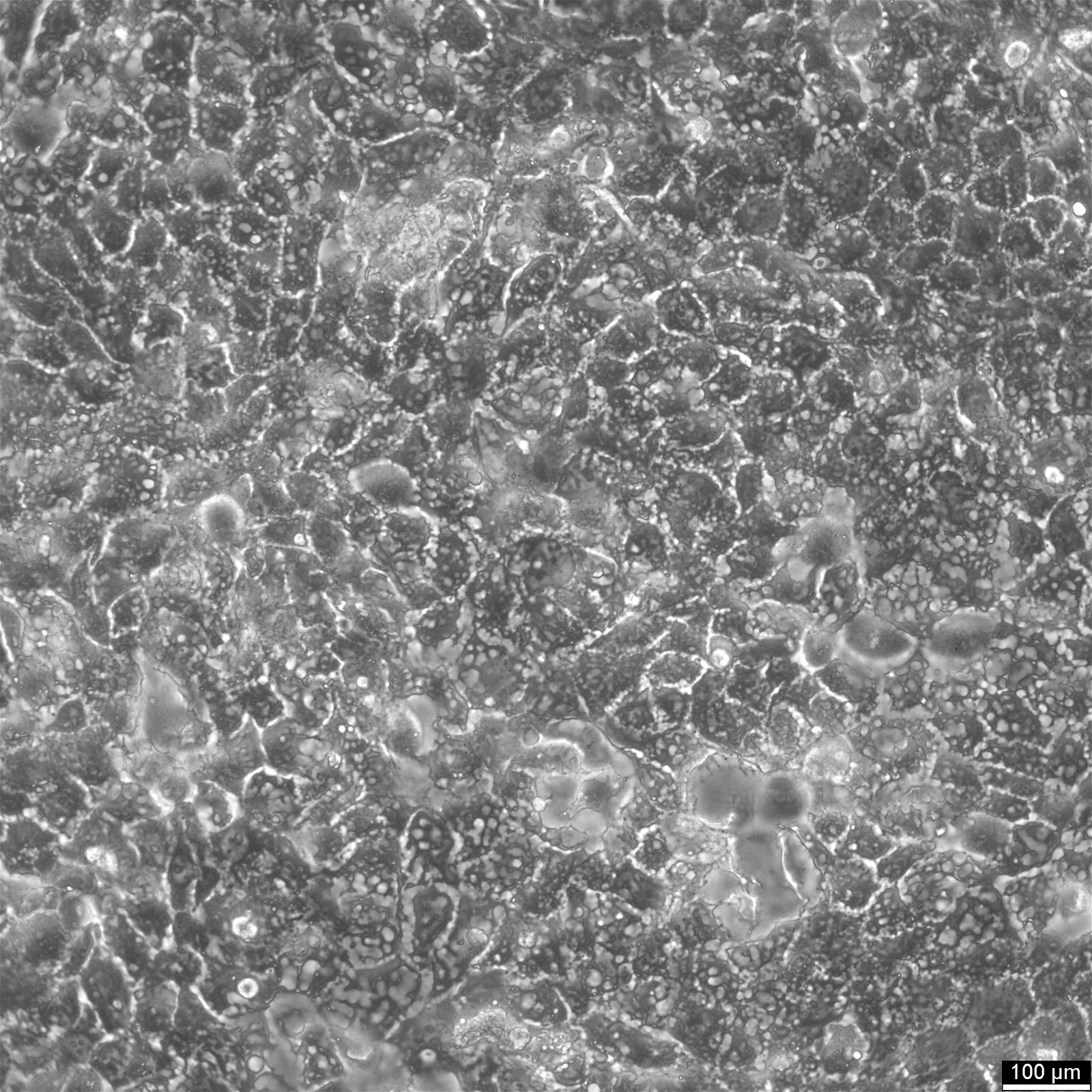
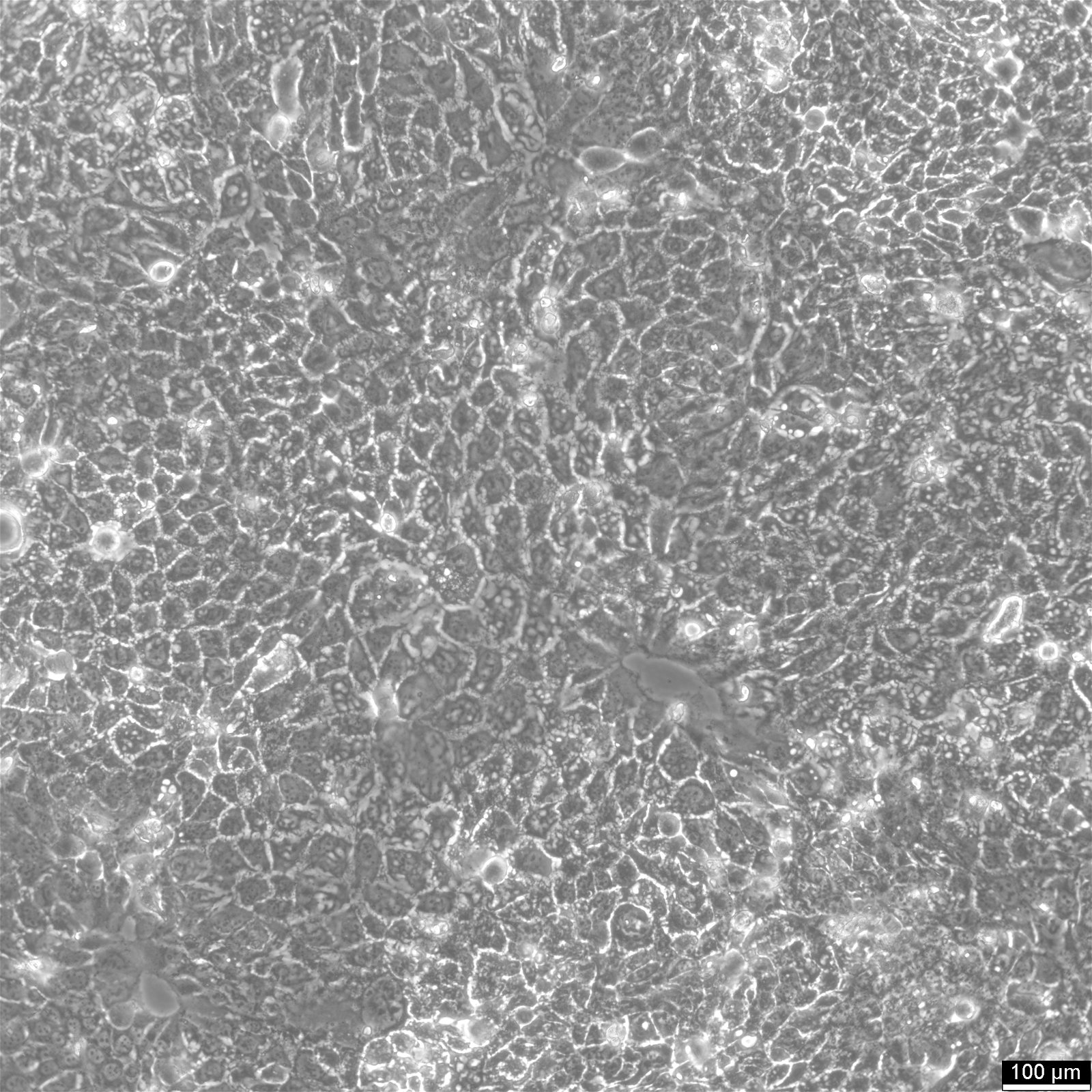
Клітини BEWO












430,00 EUR*
Продукти відправляються в замороженому вигляді на сухому льоді в кріопробірках. Кожна кріопробірка зазвичай містить 3 × 10 6 клітин для адгезивних ліній або 5 × 106 клітин для суспензійних ліній (детальніше див. сертифікат аналізу партії).
Загальна інформація
| Опис | Клітини BeWo, клітинні лінії, отримані зі злоякісної гестаційної хоріокарциноми плаценти плода чоловічої статі, стали широко використовуваною моделлю in vitro для вивчення плаценти. Злиття клітин під час фази синцитіалізації трофобласта під час розвитку плаценти у людини є однією з найважливіших, але найменш вивчених подій. Через складність вивчення цього процесу в плаценті in vivo, клітини BeWo використовуються як модель культури клітин для моделювання синцитіалізації ворсинчастого трофобласту плаценти in vivo. Ці клітини мають епітеліоподібний фенотип і є адгезивними. Субклон b30 клітин BeWo особливо корисний для вивчення поглинання і транспорту поживних речовин завдяки щільному росту на проникних мембранах. CK 7 та E-кадгерин - молекулярні маркери, які експресуються клітинами BeWo. VE-кадгерин міститься в клітинах BeWo і посилюється при обробці форсколіном. Клітини також експресують кератин і є позитивними до ізоферменту G6PD, B. Каріотип клітин BeWo має модальне число = 86, з діапазоном від 71 до 178, а стеблове число є гіпотетраплоїдним. Каріотип є відносно стабільним в межах стовбурового числа. Клітини BeWo секретують різні гормони, включаючи хоріонічний гонадотропін людини (ХГЛ), хоріонічний соматомамотропін людини (плацентарний лактоген) і стероїдні гормони, такі як естрон, естріол та естрадіол. Однак рівні β-ХГЛ та естрадіолу, що секретуються клітинами BeWo, нижчі, ніж ті, що секретуються іншими клітинними лініями, отриманими з хоріокарциноми, такими як JEG-3. Після лікування Форсколіном секреція β-ХГЛ у клітинах BeWo збільшується до рівня, подібного до того, що спостерігається в інших клітинних лініях, отриманих з хоріокарциноми. Крім того, лікування форсколіном також підвищує рівень прогестерону, що секретується клітинами BeWo. Таким чином, клітини BeWo є широко використовуваною моделлю in vitro для вивчення розвитку плаценти і процесу синцитіалізації трофобласта людини. Вони демонструють епітеліоподібний фенотип, експресують різні молекулярні маркери і секретують різні гормони, включаючи ХГЛ, плацентарний лактоген і стероїдні гормони. В цілому, клітини BeWo є цінним інструментом для дослідження складних процесів, пов'язаних з розвитком плаценти. |
|---|---|
| Організм | Людина |
| Тканина | Плацента |
| Хвороба | Хоріокарцинома |
| Місце метастазування | Мозок |
| Синоніми | BeWo, Be Wo, Be-Wo |
Характеристики
| Вік | Плід |
|---|---|
| Стать | Чоловік |
| Морфологія | Епітеліальноподібні |
| Ростові властивості | Адепт |
Нормативні дані
| Цитування | BEWO (номер за каталогом 300123) |
|---|---|
| Рівень біобезпеки | 1 |
| NCBI_TaxID | 9606 |
| ЦелозаврПриєднання | CVCL_0044 |
Біомолекулярні дані
| Ізоферменти | G6PD, B |
|---|---|
| Сприйнятливість до вірусів | Поліовірус 3, везикулярний стоматит (Індіана) |
| Зворотна транскриптаза | Негативно |
| Продукти | Прогестерон, хоріонічний соматомамотропін людини (плацентарний лактоген), естроген, естрон, естріол, естрадіол, кератин |
Обробка
| Поживне середовище | Середовище Ham's F12K, w: 2,0 мМ L-глутамін, w: 2,0 мМ піруват натрію, w: 2,5 г/л NaHCO3 (цит. номер 820608a) |
|---|---|
| Додатки | Додайте до середовища 10% FBS |
| Реагент для дисоціації | Аккутаза |
| Субкультура | Видаліть старе середовище з прилиплих клітин і промийте їх PBS, в якому бракує кальцію і магнію. Для колб T25 використовуйте 3-5 мл PBS, а для колб T75 - 5-10 мл. Потім повністю покрийте клітини аккутазою, використовуючи 1-2 мл для колб Т25 і 2,5 мл для колб Т75. Залиште клітини інкубуватися при кімнатній температурі протягом 8-10 хвилин, щоб відокремити їх. Після інкубації обережно змішайте клітини з 10 мл середовища, щоб ресуспендувати їх, а потім центрифугуйте при 300xg протягом 3 хвилин. Викиньте надосадову рідину, ресуспендуйте клітини у свіжому середовищі та перенесіть їх у нові колби, які вже містять свіже середовище. |
| Густота посіву | Рекомендується щільність посіву 1 x 104 клітин/см2. |
| Оновлення рідини | 2-3 рази на тиждень |
| Відновлення після відлиги | Після розморожування висійте клітини з щільністю 5 x 104 клітин/см2 і дайте клітинам відновитися після процесу заморожування та прикріпитися протягом щонайменше 24 годин. |
| Заморожуюче середовище | Як середовище кріоконсервування ми використовуємо повне живильне середовище (включаючи FBS) + 10% ДМСО для адекватної життєздатності після відтавання або CM-1 (номер за каталогом Cytion 800100), до складу якого входять оптимізовані осмопротектори та метаболічні стабілізатори для прискорення відновлення та зменшення кріоіндукованого стресу. |
| Розморожування та культивування клітин |
|
| Інкубаційна атмосфера | 37°C, 5% CO2, волога атмосфера. |
| Покриття колби | Для оптимального прикріплення та життєздатності після розморожування ми рекомендуємо використовувати колби або пластини з колагеновим покриттям. |
| Процедура заморожування | Кріоконсервовані клітинні лінії транспортуються на сухому льоду в перевіреній ізольованій упаковці з достатньою кількістю холодоагенту для підтримання температури приблизно -78 °C під час транспортування. При отриманні негайно огляньте контейнер і негайно перемістіть віали у відповідне місце для зберігання. |
| Умови доставки | Кріоконсервовані клітинні лінії транспортуються на сухому льоду в перевіреній ізольованій упаковці з достатньою кількістю холодоагенту для підтримання температури приблизно -78 °C під час транспортування. При отриманні негайно огляньте контейнер і негайно перемістіть віали у відповідне місце для зберігання. |
| Умови зберігання | Для тривалого зберігання помістіть флакони в парофазний рідкий азот при температурі від -150 до -196 °C. Зберігання при -80 °C допустиме лише як короткий проміжний етап перед перенесенням у рідкий азот. |
Контроль якості / Генетичний профіль / HLA
| Стерильність | Зараження мікоплазмою виключається за допомогою аналізів на основі ПЛР та люмінесцентних методів виявлення мікоплазми. Щоб переконатися у відсутності бактеріального, грибкового або дріжджового забруднення, клітинні культури піддаються щоденному візуальному контролю. |
|---|---|
| HLA алелі |
A*: '01:01:01, '11:01:01
B*: '08:13, '35:01:01
C*: '04:01:01, '07:01:01
DRB1*: '01:03:01, '03:01:01
DQA1*: '01:01:01, '05:01:01
DQB1*: '02:01:01, '05:01:01
DPB1*: '01:01:01, '04:01:01
E: '01:01:01
|
Сертифікат аналізу (CoA)
| Номер лота | Тип сертифікату | Дата | Номер за каталогом |
|---|---|---|---|
| 300123-010425 | Сертифікат аналізу | 23. May. 2025 | 300123 |
| 300123-1022 | Сертифікат аналізу | 23. May. 2025 | 300123 |
Угода про передачу матеріалів
Якщо ви маєте намір використовувати клітинні лінії Cytion виключно для внутрішніх досліджень в одному дослідницькому центрі, заповніть та підпишіть нашу Угоду про передачу матеріалів (MTA) і надішліть її разом із вашим замовленням.
Для будь-яких комерційних застосувань, включаючи, але не обмежуючись, роботу за плату, тестування контролю якості, випуск продукції, діагностичне використання або регуляторні дослідження, заповніть форму передбачуваного використання, щоб ми могли підготувати відповідну угоду, адаптовану до вашого проекту.
Зверніть увагу: угода MTA застосовується лише до певних клітинних ліній. Якщо це повідомлення та документ MTA з'являються на сторінці продукту, угода є чинною. Для клітинних ліній, на які не поширюється дія угоди MTA, посилання на угоду не відображається. Угода MTA не є чинною для клієнтів в Америці, Китаї або Тайвані. Зверніться до нашого представництва в США, щоб отримати відповідну угоду.
