Milieux de culture cellulaire : Une vue d'ensemble
Dans le domaine des sciences de la vie, l'une des méthodologies les plus importantes est la culture cellulaire. L'expression "culture cellulaire" désigne le prélèvement de cellules, de tissus ou d'organes sur un animal ou une plante et l'implantation ultérieure de ces cellules, tissus ou organes dans un environnement artificiel favorable à leur survie et/ou à leur croissance Les besoins environnementaux fondamentaux pour un développement cellulaire optimal sont une température contrôlée, un substrat pour la fixation des cellules, un milieu de croissance adéquat et un incubateur qui maintient un pH et une osmolalité optimaux. Les cellules doivent bénéficier de ces conditions pour se développer au maximum de leur potentiel.
La sélection d'un milieu de croissance adéquat pour la culture in vitro est l'étape de la culture cellulaire qui est à la fois la plus critique et la plus vitale. Un milieu de croissance, également appelé milieu de culture, est un liquide ou un gel formulé pour favoriser le développement des organismes à l'échelle microscopique, cellulaire ou végétale. Le milieu utilisé pour la culture des cellules contient souvent un apport adéquat d'énergie et de substances qui contrôlent le cycle cellulaire. Les principaux composants d'un milieu de culture sont les acides aminés, les vitamines, les sels inorganiques, le glucose et le sérum. Le sérum est ajouté au milieu car il constitue une source de facteurs de croissance, d'hormones et de facteurs d'attachement. Outre l'apport de nutriments, le milieu contribue également au maintien des niveaux de pH et d'osmolalité.
Types de milieux utilisés en culture cellulaire
Les cellules humaines et animales peuvent être cultivées soit dans un milieu artificiel ou synthétique, soit dans un milieu entièrement naturel complété par des éléments naturels. Dans ce qui suit, nous vous donnons un aperçu des différents types de milieux actuellement disponibles.
Milieu naturel
Seuls les fluides biologiques existant à l'état naturel peuvent être trouvés dans les milieux naturels. Les milieux naturels sont très utiles et faciles pour la culture d'une grande variété de types de cellules animales. Le manque de compréhension des composants précis qui constituent les milieux naturels est le principal facteur contribuant à la faible répétabilité des résultats obtenus en utilisant les milieux naturels.
Milieux artificiels
La préparation de milieux artificiels ou synthétiques implique l'ajout de nutriments (organiques et inorganiques), de protéines sériques, d'hydrates de carbone, de cofacteurs, de vitamines et de sels, ainsi que de phases gazeuses d'O2 et de CO2 [1].
Différents types de milieux artificiels ont été développés pour remplir une ou plusieurs des fonctions suivantes : 1) Survie immédiate (une solution saline équilibrée avec un pH et une pression osmotique précis). 2) Survie prolongée (une solution saline équilibrée complétée par différentes formulations de produits chimiques organiques et/ou de sérum). 3) Développement indéfini. 4) Fonctions spécialisées.
Il existe quatre classifications distinctes pour les milieux artificiels :
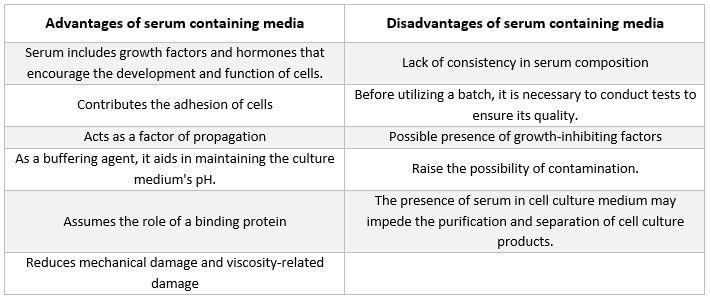
Milieux contenant du sérum
Le type de supplément le plus fréquent dans les milieux utilisés pour la culture de cellules animales est le sérum bovin fœtal. Il est ajouté au milieu de culture en tant que supplément peu coûteux afin d'obtenir les meilleures conditions de croissance possibles. Outre son rôle de transporteur ou de chélateur pour les nutriments instables ou insolubles dans l'eau, les hormones et les facteurs de croissance, les inhibiteurs de protéase et d'autres substances, le sérum lie et neutralise les molécules nocives.
Milieu sans sérum
La présence de sérum dans les milieux présente un certain nombre d'inconvénients et peut entraîner des erreurs d'interprétation majeures dans la recherche immunologique [2, 3]. Différents milieux sans sérum ont été créés [4, 5]. Ces milieux sont généralement formulés spécifiquement pour favoriser la culture d'un seul type de cellule, comme le Knockout Serum Replacement et le Knockout DMEM de Thermo Fisher Scientific, et le milieu mTESR de Stem Cell Technologies [6], pour les cellules souches [7].
En outre, ces milieux incorporent des quantités définies de facteurs de croissance purifiés, de lipoprotéines et d'autres protéines, qui sont généralement fournies par le sérum [8]. Ces milieux sont souvent appelés "milieux culturels définis" car leurs composants sont bien connus.
Milieux chimiquement définis
Ces milieux comprennent des composants inorganiques et organiques ultra-purs qui n'ont été contaminés par aucun type de contamination. Ils peuvent également comprendre des ajouts de protéines pures, telles que des facteurs de croissance.
la modification génétique des bactéries ou des levures, ainsi que l'ajout d'acides gras, de vitamines, de cholestérol et d'acides aminés particuliers, aboutissent à la production de leurs composants [9].
Milieux sans protéines
Les milieux sans protéines sont ceux qui ne contiennent aucune protéine, mais uniquement des éléments non protéiques. Par rapport aux milieux contenant du sérum, les milieux sans protéines favorisent la prolifération cellulaire et l'expression des protéines et facilitent la purification de tout produit généré dans un processus en aval [10-12]. Les protéines ne sont pas incluses dans les préparations telles que MEM et RPMI-1640. Toutefois, un supplément de protéines peut être administré si cela s'avère nécessaire.
Le milieu de culture et ses composants de base
Les milieux de culture commerciaux peuvent être achetés sous forme de poudre ou de liquide et comprennent souvent une variété de nutriments tels que des acides aminés, du glucose, des sels, des vitamines et d'autres compléments alimentaires.
Les besoins en ces composants sont différents pour chaque lignée cellulaire, et ces variations sont à l'origine du grand nombre de formulations différentes de milieux. Chaque composant est responsable d'une certaine fonction, qui sera décrite dans les paragraphes suivants :
Systèmes tampons
Pour maintenir des conditions de croissance optimales, le pH doit être contrôlé, ce qui est souvent fait par l'un des deux systèmes tampons suivants :
Système tampon naturel
Le rapport CO2/H2CO3 dans l'atmosphère est égal à celui du milieu, ce qui crée un mécanisme tampon naturel. Afin de préserver leur mécanisme tampon naturel, les cultures doivent être maintenues dans un environnement atmosphérique contenant 5 à 10 % de CO2, ce qui est souvent réalisé à l'aide d'un incubateur à CO2. L'un des avantages de l'utilisation d'un tampon naturel est qu'il est bon marché et sûr.
HEPES
Le tamponnage chimique à l'aide du zwitterion HEPES a une plus grande capacité de tamponnage dans la plage de pH de 7,2 à 7,4 et n'a pas besoin d'un environnement gazeux réglementé. Pour certains types de cellules, une dose plus importante d'HEPES peut être nocive. Les milieux contenant de l'HEPES sont également beaucoup plus sensibles aux effets phototoxiques de la lumière fluorescente [13].
Rouge de phénol
L'indicateur de pH, le rouge de phénol, est souvent inclus dans les milieux de culture disponibles dans le commerce, ce qui permet un contrôle continu du pH. En faisant grossir les cellules, les métabolites produits par ces cellules provoquent un changement de pH et donc un changement de couleur du milieu. Le rouge de phénol a un double effet sur la couleur du milieu : il le rend jaune à un pH acide et violet à un pH alcalin. Le pH 7,4, la valeur optimale pour la culture cellulaire, fait apparaître le milieu en rouge fluorescent.
Le rouge de phénol présente toutefois quelques inconvénients : Tout d'abord, le rouge de phénol est capable de simuler la performance d'un certain nombre d'hormones stéroïdiennes, principalement les œstrogènes [14]. Par conséquent, il est recommandé d'utiliser un milieu exempt de rouge de phénol lors de l'étude de cellules sensibles aux œstrogènes, comme le tissu mammaire. L'équilibre sodium-potassium est perturbé par la présence de rouge de phénol dans plusieurs formulations sans sérum. L'ajout de sérum ou d'hormone hypophysaire bovine au milieu peut contrecarrer cet effet [15]. Troisièmement, la détection dans les expériences de cytométrie de flux est entravée par la présence de rouge de phénol.
Sels inorganiques
Les milieux contenant des sels inorganiques, tels que les ions sodium, potassium et calcium, contribuent à maintenir l'équilibre osmotique et à réguler le potentiel membranaire.
Acides aminés
Les acides aminés étant les composants fondamentaux des protéines, ils sont un élément essentiel de tous les milieux de croissance cellulaire jamais conçus. Les cellules étant incapables de produire elles-mêmes certains acides aminés, il est important que le milieu de culture contienne des acides aminés essentiels. Ils sont nécessaires à la prolifération des cellules et leur concentration détermine la densité cellulaire maximale qui peut être atteinte. En particulier, la L-glutamine, un acide aminé essentiel, est particulièrement cruciale.
La L-glutamine fonctionne comme une source secondaire d'énergie pour le métabolisme et contribue à la production de NAD, de NADPH et de nucléotides. Étant donné que la L-glutamine est un acide aminé instable qui, avec le temps, se transforme en une forme que les cellules ne peuvent pas utiliser, elle doit être apportée au milieu.
En outre, des acides aminés non essentiels peuvent être apportés au milieu afin de réapprovisionner ceux qui ont été utilisés au cours du processus de croissance. La croissance des cellules est stimulée et leur viabilité est accrue lorsque le milieu de croissance est supplémenté en acides aminés non essentiels.
Glucides
Les hydrates de carbone sous forme de sucres sont la principale source d'énergie. De nombreux milieux de culture contiennent du maltose et du fructose en plus des sucres plus courants que sont le glucose et le galactose.
Protéines et peptides
L'albumine, la transferrine et la fibronectine sont les protéines et les peptides les plus couramment utilisés. Ils sont particulièrement importants dans les milieux qui ne contiennent pas de sérum. L'albumine, la transferrine, l'aprotinine, la fétuine et la fibronectine sont quelques-unes des protéines que l'on peut trouver dans le sérum, qui est une source riche en protéines.
L'albumine est la principale protéine du sang et sa fonction est de lier et de transporter diverses substances, y compris l'eau, les sels, les acides gras libres, les hormones et les vitamines, entre les différents organes et cellules. La capacité de l'albumine à se lier aux produits chimiques en fait un candidat efficace pour éliminer les composés nocifs du milieu dans lequel les cellules sont cultivées.
L'aprotinine est un agent protecteur dans les systèmes de culture cellulaire, car elle est stable aux pH neutres et acides, et résiste aux températures élevées et à la destruction causée par les enzymes protéolytiques. Elle est capable d'inhiber un certain nombre de protéases à sérine, dont la trypsine, entre autres.
La fétuine est une glycoprotéine qui peut être détectée en plus grande quantité dans le sérum des fœtus et des nouveau-nés que dans le sérum des adultes. En outre, elle agit comme un inhibiteur de protéase à sérine. La protéine fibronectine est un composant essentiel dans le processus d'adhésion cellulaire. La transferrine est une protéine qui transporte le fer et qui est responsable de l'apport de fer aux membranes des cellules.
Acides gras et lipides
Ils jouent un rôle crucial dans le milieu sans sérum en cas d'absence de sérum.
Les vitamines
De nombreuses vitamines sont nécessaires au développement et à la prolifération des cellules. Les vitamines ne peuvent pas être produites en quantités suffisantes par les cellules et sont donc essentielles dans la culture de tissus en tant que compléments alimentaires.
Dans la culture cellulaire, le sérum est la principale source de vitamines ; cependant, les milieux sont également traités avec diverses vitamines pour les adapter à un type de cellule spécifique. Le plus souvent, les vitamines du groupe B sont utilisées pour stimuler la croissance.
Oligo-éléments
Les éléments chimiques tels que le cuivre, le zinc, le sélénium et les intermédiaires d'acide tricarboxylique sont connus sous le nom d'oligo-éléments. Les oligo-éléments sont souvent ajoutés aux milieux qui ne contiennent pas de sérum afin de remplacer ceux qui sont généralement présents dans le sérum. Ces éléments sont des composants chimiques importants qui sont nécessaires au bon développement des cellules. De nombreuses réactions biochimiques dépendent de certains micronutriments, comme l'activité enzymatique.
Suppléments au milieu
Le milieu de croissance complet proposé pour certaines lignées cellulaires nécessite des composants supplémentaires qui sont absents du milieu de base et du sérum. Ces compléments alimentaires soutiennent la croissance cellulaire et les fonctions métaboliques appropriées.
Bien que les hormones, les facteurs de croissance et les molécules de signalisation soient essentiels à la prolifération appropriée de certaines lignées cellulaires, les précautions suivantes doivent toujours être prises : L'ajout de suppléments pouvant modifier l'osmolalité du milieu de croissance complet, ce qui peut inhiber le développement cellulaire, il est toujours conseillé de vérifier l'osmolalité après l'ajout de suppléments. Pour la majorité des lignées cellulaires, l'osmolalité optimale se situe entre 260 et 320 mOSM/kg.
Antibiotiques
Les antibiotiques sont souvent utilisés pour inhiber le développement de polluants bactériens et fongiques [16], bien qu'ils ne soient pas essentiels à la croissance cellulaire. Comme les antibiotiques peuvent dissimuler une contamination par des mycoplasmes et des bactéries résistantes, leur utilisation systématique n'est pas recommandée pour la culture cellulaire [17, 18].
En outre, les antibiotiques peuvent perturber le métabolisme des cellules hypersensibles. Les combinaisons pénicilline-streptomycine fabriquées par MilliporeSigma et Life Technologies sont souvent utilisées. La plasmocine a été utilisée dans la culture des lignées cellulaires de gliome TS603, TS516 et BT260 [19], et elle s'est avérée efficace pour éliminer la contamination par les mycoplasmes (20).
Sérum
Les albumines, les facteurs de croissance et les inhibiteurs de croissance sont tous présents dans le sérum. Le sérum est l'un des composants les plus importants du milieu de culture cellulaire car il fournit des acides aminés, des protéines, des vitamines (en particulier des vitamines liposolubles telles que A, D, E et K), des hydrates de carbone, des lipides, des hormones, des facteurs de croissance, des minéraux et des oligo-éléments.
Le sérum fœtal et le sérum de veau bovin sont souvent utilisés pour favoriser le développement des cellules cultivées. Le sérum fœtal est une source abondante de facteurs de croissance et convient au clonage cellulaire et au développement de cellules sensibles. En raison de ses capacités réduites de promotion de la croissance, le sérum de veau est utilisé dans les expériences d'inhibition de contact. Les milieux de croissance normaux contiennent souvent de 2 à 10 % de sérum. L'ajout de sérum au milieu de culture répond aux objectifs suivants [21] :
-
Le sérum fournit les nutriments essentiels aux cellules (à la fois en solution et attachés aux protéines).
-
Plusieurs facteurs de croissance et hormones impliqués dans la promotion de la croissance et l'activité cellulaire spécialisée sont inclus dans le sérum.
-
Il contient de nombreuses protéines de liaison, comme l'albumine et la transferrine, qui transportent d'autres substances chimiques dans la cellule. Par exemple, l'albumine transporte les graisses, les vitamines, les hormones, etc. dans les cellules.
-
Elle fournit également des protéines, telles que la fibronectine, qui augmentent l'adhésion des cellules au substrat. En outre, elle produit des éléments d'étalement qui favorisent l'expansion cellulaire avant la division.
-
Elle fournit des inhibiteurs de protéase qui empêchent la protéolyse dans les cellules.
-
Il contient également des minéraux tels que Na+, K+, Zn2+ et Fe2+.
-
Il augmente la viscosité du milieu, protégeant ainsi les cellules des lésions mécaniques lors de l'agitation des cultures en suspension.
-
C'est également un tampon.
Références
[1] Morgan J, Morton H, Parker R. Nutrition of animal cells in tissue culture ; initial studies on a synthetic medium. Proc Soc Exp Biol Med. 1950;73:1-8
[2] Kerbel R, Blakeslee D. Rapid adsorption of a foetal calf serum component by mammalian cells in culture. A potential source of artifacts in studies of antisera to cell-specific antigens. Immunology. 1976;31:881-91
[3] Sula K, Draber P, Nouza K. Addition of serum to the medium used for preparation of cell suspensions as a possible source of artefacts in cell-mediated reactions studied by means of the popliteal lymph node test. J Immunogenet. 1980;7:483-9
[4] Mariani E, Mariani A, Monaco M, Lalli E, Vitale M, Facchini A. Commercial serum-free media : hybridoma growth and monoclonal antibody production. J Immunol Methods. 1991;145:175-83
[5] Barnes D, Sato G. Methods for growth of cultured cells in serum-free medium. Anal Biochem. 1980;102:255-70
[6] Yu H, Lu S, Gasior K, Singh D, Vazquez Sanchez S, Tapia O,et al. HSP70 chaperones RNA-free TDP-43 into anisotropic intranuclear liquid spherical shells. Science. 2021;371 :
[7] Meharena H, Marco A, Dileep V, Lockshin E, Akatsu G, Mullahoo J,et al. Down-syndrome-induced senescence disrupts the nuclear architecture of neural progenitors. Cell Stem Cell. 2022;29:116-130.e7
[8] Iscove N, Melchers F. Complete replacement of serum by albumin, transferrin, and soybean lipid in cultures of lipopolysaccharide-reactive B lymphocytes. J Exp Med. 1978;147:923-33
[9] Stoll T, Muhlethaler K, von Stockar U, Marison I. Systematic improvement of a chemically-defined protein-free medium for hybridoma growth and monoclonal antibody production. J Biotechnol. 1996;45:111-23
[10] Darfler F. A protein-free medium for the growth of hybridomas and other cells of the immune system. In Vitro Cell Dev Biol. 1990;26:769-78
[11] Barnes D, Sato G. Serum-free cell culture : a unifying approach. Cell. 1980;22:649-55
[12] Hamilton W, Ham R. Clonal growth of chinese hamster cell lines in protein-free media. In Vitro. 1977;13:537-47
[13] Zigler J, Lepe Zuniga J, Vistica B, Gery I. Analysis of the cytotoxic effects of light-exposed HEPES-containing culture medium. In Vitro Cell Dev Biol. 1985;21:282-7
[14] Berthois Y, Katzenellenbogen J, Katzenellenbogen B. Phenol red in tissue culture media is a weak estrogen : implications concerning the study of estrogen-responsive cells in culture. Proc Natl Acad Sci U S A. 1986;83:2496-500
[15] Karmiol S. Development of serum free media. In : Master JRW, éditeur. Animal Cell culture, 3rd ed. Oxford:Oxford University Press ; 2000.
[16] Perlman D. Use of antibiotics in cell culture media. Methods Enzymol. 1979;58:110-6
[17] McGarrity G. Spread and control of mycoplasmal infection of cell cultures. In Vitro. 1976;12:643-8
[18] Masters J, Stacey G. Changing medium and passaging cell lines. Nat Protoc. 2007;2:2276-84
[19] Chakraborty A, Laukka T, Myllykoski M, Ringel A, Booker M, Tolstorukov M,et al. Histone demethylase KDM6A directly senses oxygen to control chromatin and cell fate. Science. 2019;363:1217-1222
[20] Molla Kazemiha V, Azari S, Amanzadeh A, Bonakdar S, Shojaei Moghadam M, Habibi Anbouhi M,et al. Efficacité du Plasmocin™ sur diverses lignées cellulaires de mammifères infectées par des mollicutes en comparaison avec des antibiotiques couramment utilisés dans la culture cellulaire : une expérience locale. Cytotechnology. 2011;63:609-20
[21] Kragh Hansen U. Aspects moléculaires de la liaison des ligands à l'albumine sérique. Pharmacol Rev. 1981;33:17-53