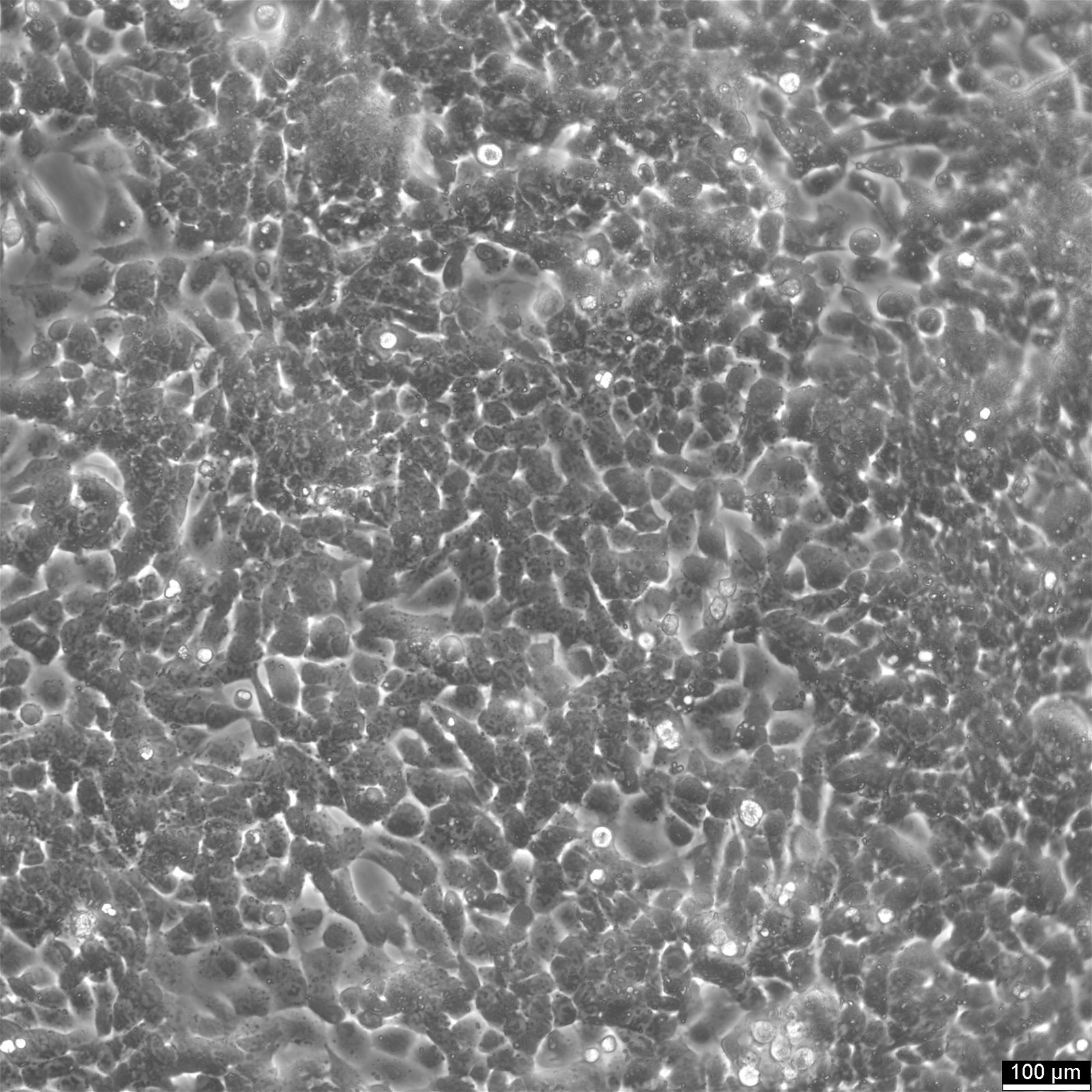
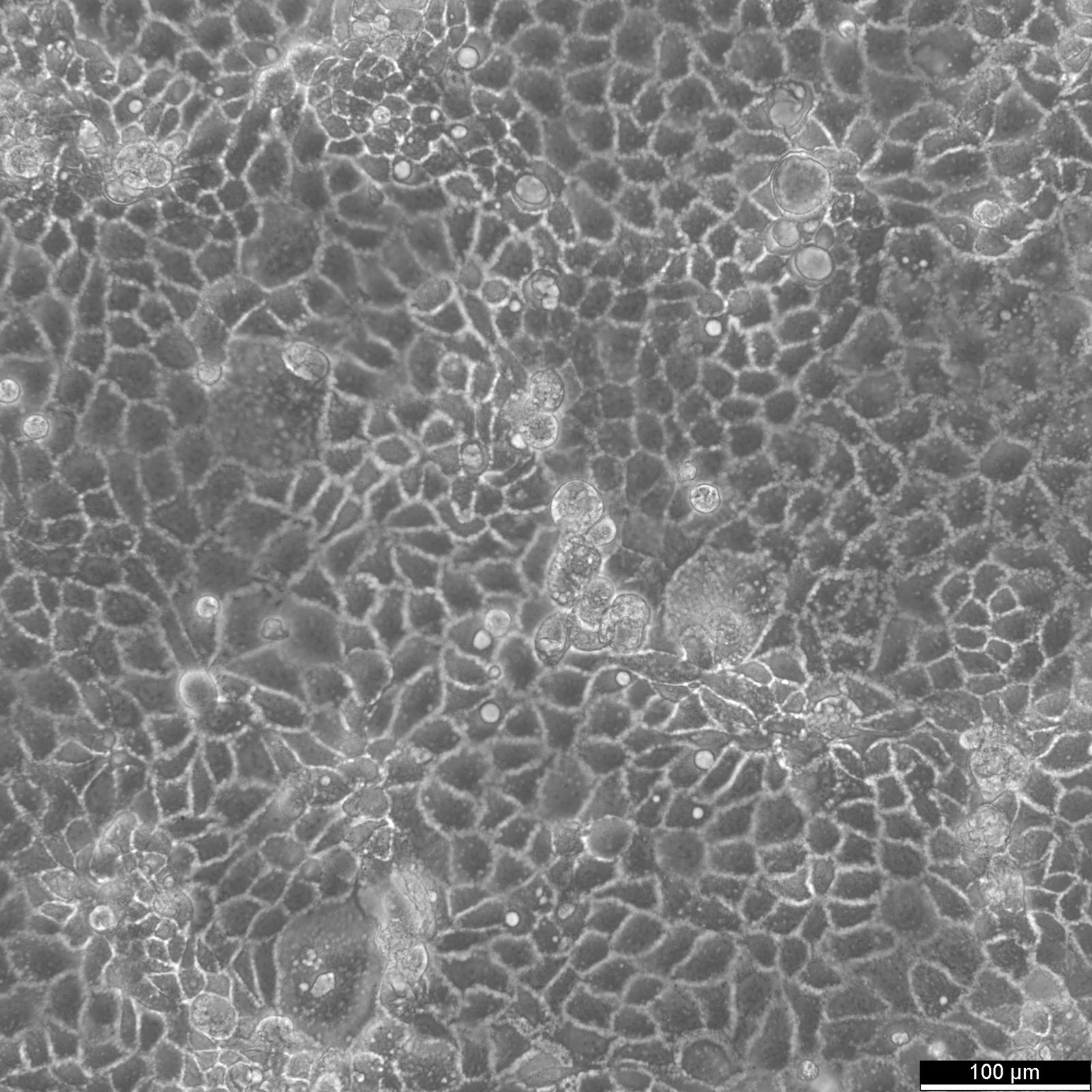
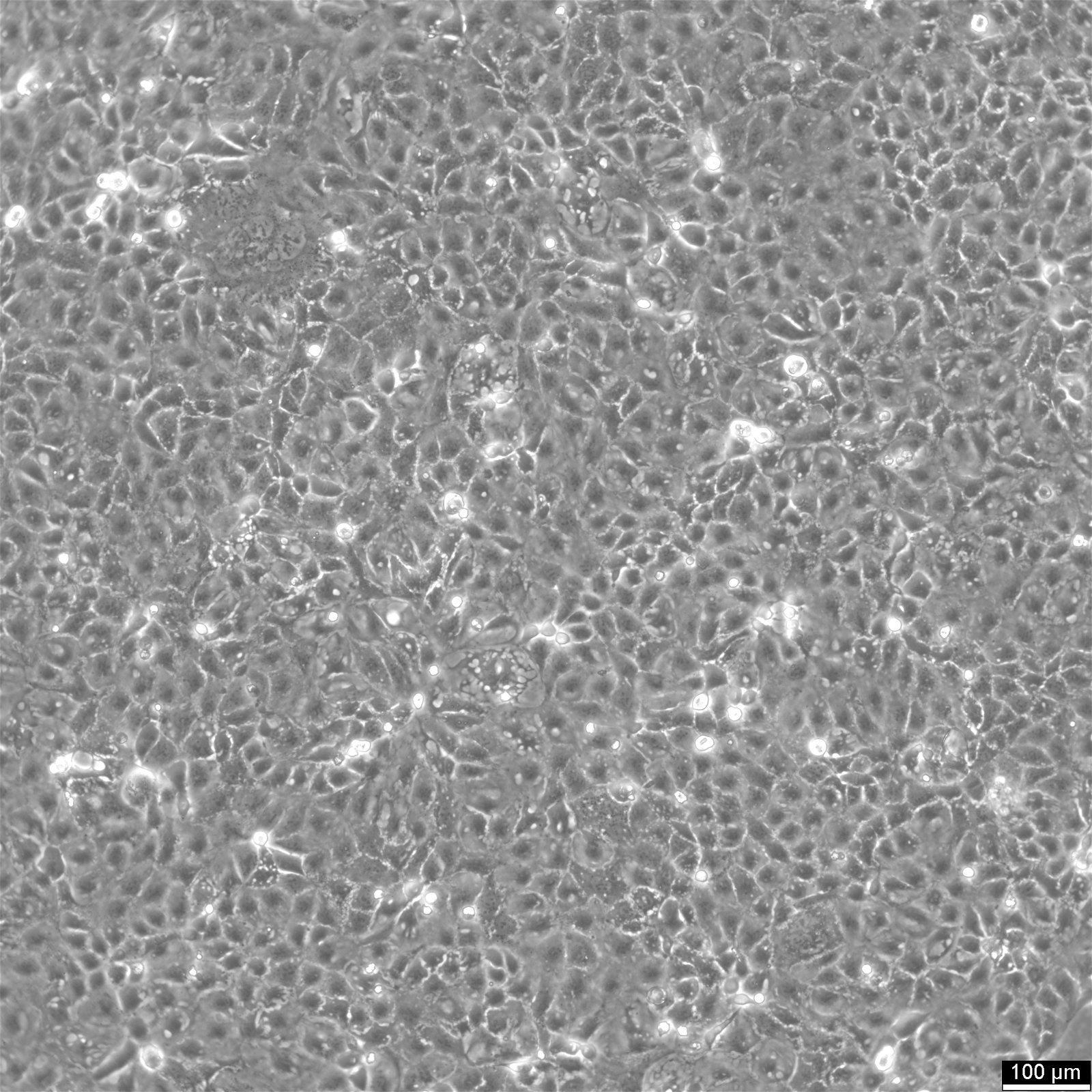
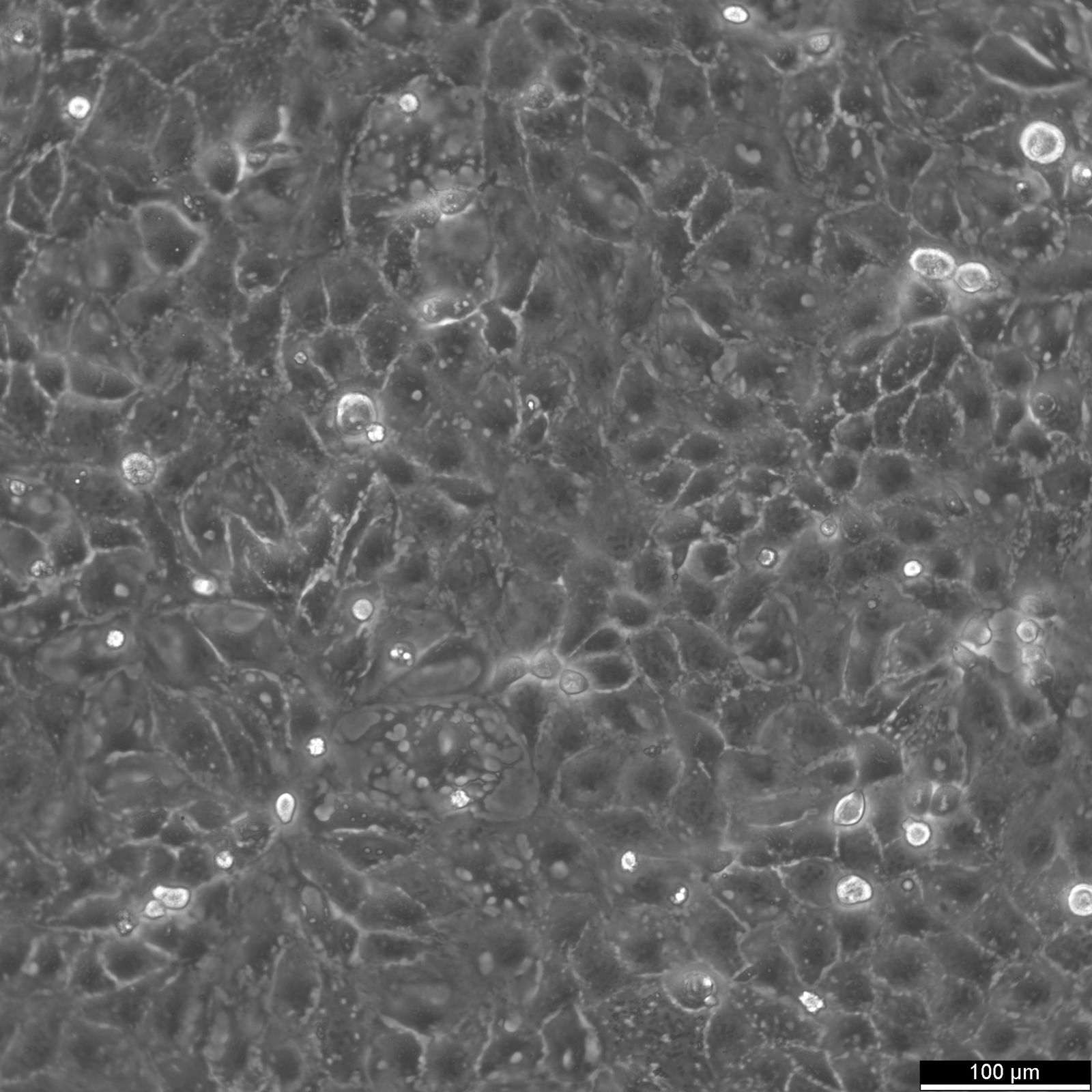
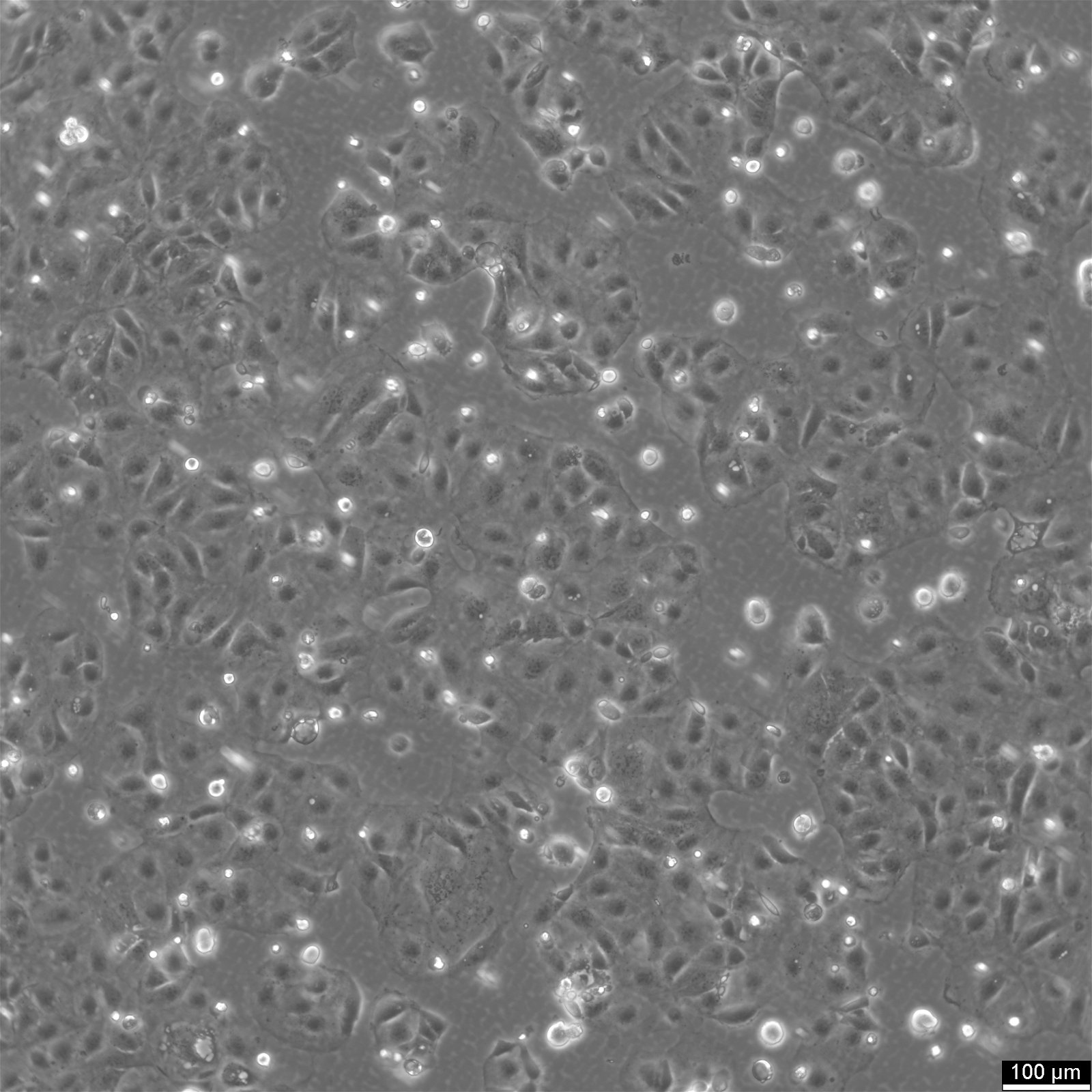
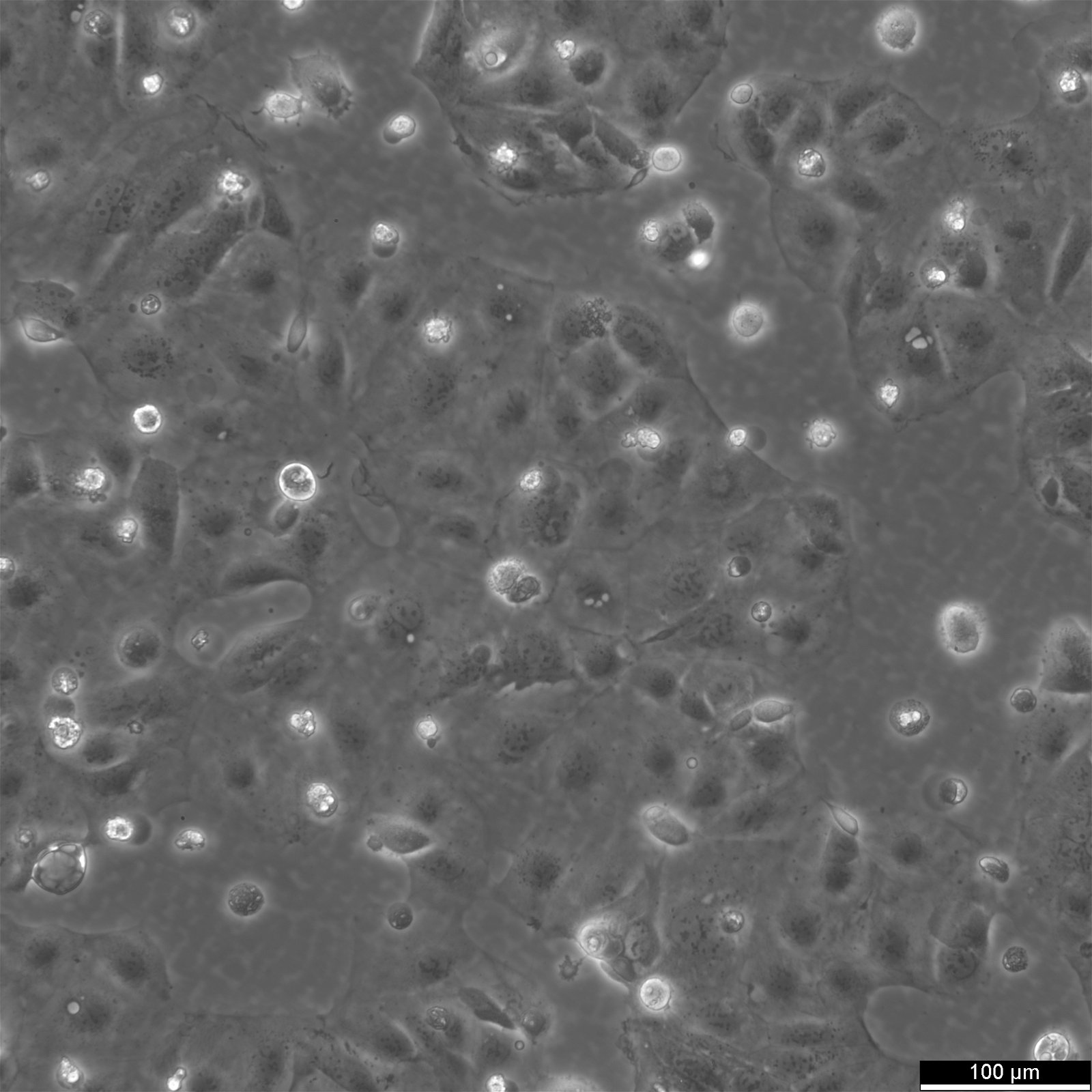
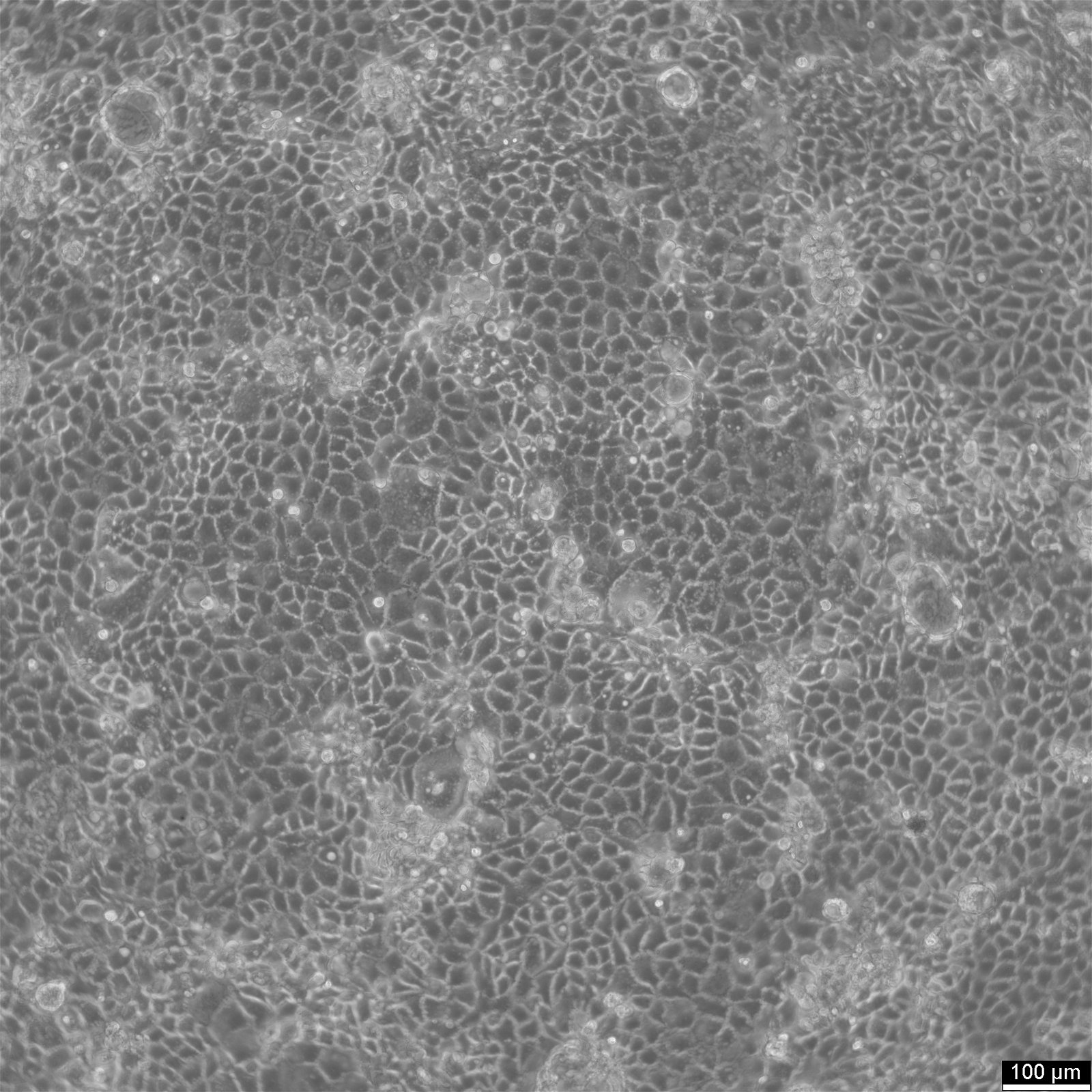
Cellules Caco-2






















430,00 €*
Les produits sont expédiés congelés dans de la glace carbonique dans des cryotubes. Chaque cryotube contient généralement 3 × 10 6 cellules pour les lignées adhérentes ou 5 × 106 cellules pour les lignées en suspension (voir le certificat d'analyse du lot pour plus de détails).
Introduction aux cellules Caco-2
| Description | Les cellules Caco-2 servent de modèle in vitro avancé pour la barrière intestinale humaine, principalement en raison de leur différenciation en une monocouche cellulaire qui ressemble étroitement aux entérocytes qui tapissent l'intestin grêle. Lors de la culture de la lignée cellulaire Caco2 sur des inserts de filtre de culture tissulaire avec des filtres en polycarbonate, les cellules Caco2 subissent une différenciation spontanée. La différenciation des cellules Caco2 se traduit par l'expression de types cellulaires spécialisés, dotés de microvillosités, d'enzymes et de transporteurs, parallèlement aux caractéristiques et mécanismes complexes observés dans une situation in vivo. Dans le contexte des modèles d'étude de l'absorption intestinale, les cellules Caco-2, dérivées d'un adénocarcinome colorectal humain, jouent un rôle essentiel en raison de leur capacité à développer des valeurs TEER élevées, ce qui signifie que les jonctions serrées et la fonction de barrière épithéliale sont intactes. Ces propriétés sont cruciales pour des essais tels que l'essai d'efflux de cholestérol et les recherches sur le transport cellulaire, y compris le mouvement des nanoparticules lipidiques et la détection des interactions protéiques. Les cellules Caco-2 sont essentielles pour les études sur l'absorption intestinale, car elles constituent une approximation in vitro fiable de l'épithélium intestinal. Mimant les entérocytes intestinaux, ces cellules facilitent l'analyse de l'absorption orale des médicaments en simulant la barrière intestinale. Les chercheurs utilisent les cellules Caco-2 pour prédire comment les substances traversent la muqueuse intestinale, ce qui est essentiel pour l'établissement du profil pharmacocinétique des médicaments administrés par voie orale. En outre, les cellules Caco-2 sont un outil essentiel pour étudier l'absorption, l'homéostasie et le transport du cholestérol dans l'intestin, des processus vitaux pour comprendre le métabolisme des lipides et les maladies qui y sont associées. Les cellules Caco-2 restent une pierre angulaire de la recherche sur le carcinome du côlon et la toxicologie, non seulement en raison de leur pertinence pour les études gastro-intestinales humaines, mais aussi parce qu'elles fournissent des informations détaillées sur la voie biliaire, le métabolisme des xénobiotiques dans le côlon, la recherche sur le cancer et la toxicologie. |
|---|---|
| Organisme | Humain |
| Tissus | Colon |
| Maladie | Adénocarcinome |
| Applications | Modèle du tractus gastro-intestinal, mesure de la résistance électrique transépithéliale/endothéliale (TEER). Les cellules Caco-2 développent des valeurs TEER élevées allant jusqu'à 2000 cm2 (mesurées par CLS à l'aide du CellZscope, nanoAnalytics, Münster, Allemagne). |
| Synonymes | CaCo-2, CACO-2, Caco 2, CACO 2, CACO2, CaCo2, CaCO2, Caco2, Caco-II |
Détails
| L'âge | 72 ans |
|---|---|
| Genre | Homme |
| Ethnicité | Caucasien |
| Morphologie | De type épithélial |
| Propriétés de croissance | Adhérent |
Documentation
| Citation | CaCo-2 (numéro de catalogue 300137 de Cytion) |
|---|---|
| Niveau de biosécurité | 1 |
| NCBI_TaxID | 9606 |
| CellosaurusAccession | CVCL_0025 |
Composition génétique de la lignée cellulaire Caco-2
| Récepteurs exprimés | Entérotoxine thermostable (Sta, E. coli), facteur de croissance épidermique (EGF), protéine I de liaison à l'acide rétinoïque et protéine II de liaison au rétinol, kératine positive. |
|---|---|
| Expression de l'antigène | Groupe sanguin O, Rh+, HLA classe II négatif |
| Isoenzymes | Me-2, 1, PGM3, 1, PGM1, 1, ES-D, 1, AK-1, 1, GLO-1, 1, G6PD, B. |
| Tumorigène | Oui, chez la souris nude. Forme des adénocarcinomes modérément bien différenciés correspondant à un cancer primaire du côlon (grade II) |
| Résistance aux virus | Virus de l'immunodéficience humaine (VIH, LAV) |
| Statut de ploïdie | (P14), hypertétraploïde |
| État MSI | Stable (MSS) |
Manipulation
| Milieu de culture | EMEM (MEM Eagle), w : 2 mM L-Glutamine, w : 2.2 g/L NaHCO3, w : EBSS (numéro d'article Cytion 820100a) |
|---|---|
| Suppléments | Compléter le milieu avec 10 % de FBS et 1 % de NEAA |
| Réactif de dissociation | Accutase |
| Temps de doublement | 60 à 70 heures |
| Sous-culture | Retirer l'ancien milieu des cellules adhérentes et les laver avec du PBS dépourvu de calcium et de magnésium. Pour les flacons T25, utiliser 3-5 ml de PBS, et pour les flacons T75, 5-10 ml. Ensuite, recouvrir complètement les cellules avec Accutase, en utilisant 1 à 2 ml pour les flacons T25 et 2,5 ml pour les flacons T75. Laisser les cellules incuber à température ambiante pendant 8-10 minutes pour les détacher. Après incubation, mélanger délicatement les cellules avec 10 ml de milieu pour les remettre en suspension, puis centrifuger à 300xg pendant 3 minutes. Jeter le surnageant, remettre les cellules en suspension dans du milieu frais et les transférer dans de nouveaux flacons contenant déjà du milieu frais. |
| Taux de fractionnement | Un rapport de 1:2 à 1:3 est recommandé |
| Densité de semis | 1 x 104 cellules/cm2 donnera lieu à une monocouche confluente à 90 % en environ 4 jours. |
| Récupération après dégel | Après décongélation, ensemencer les cellules à raison de 5 x 104 cellules/cm2 et laisser les cellules se remettre du processus de congélation et adhérer pendant au moins 24 heures. |
| Congélation du milieu | Comme milieu de cryoconservation, nous utilisons un milieu de croissance complet (comprenant du FBS) + 10 % de DMSO pour une viabilité adéquate après décongélation, ou CM-1 (numéro de catalogue 800100 de Cytion), qui comprend des osmoprotectants et des stabilisateurs métaboliques optimisés pour améliorer la récupération et réduire le stress induit par la cryogénisation. |
| Décongélation et culture des cellules |
|
| Atmosphère d'incubation | 37°C, 5%CO2, atmosphère humidifiée. |
| Revêtement des flacons | Aucun |
| Procédure de congélation | Les lignées cellulaires cryoconservées sont expédiées sur glace sèche dans des emballages isolés et validés, avec suffisamment de réfrigérant pour maintenir une température d'environ -78 °C tout au long du transport. À la réception, inspecter immédiatement le conteneur et transférer sans délai les flacons dans un lieu de stockage approprié. |
| Conditions d'expédition | Les lignées cellulaires cryoconservées sont expédiées sur glace sèche dans des emballages isolés et validés, avec suffisamment de réfrigérant pour maintenir une température d'environ -78 °C tout au long du transport. À la réception, inspecter immédiatement le conteneur et transférer sans délai les flacons dans un lieu de stockage approprié. |
| Conditions de stockage | Pour une conservation à long terme, placer les flacons dans de l'azote liquide en phase vapeur à une température comprise entre -150 et -196 °C environ. Le stockage à -80 °C n'est acceptable qu'en tant qu'étape intermédiaire de courte durée avant le transfert dans l'azote liquide. |
Contrôle de la qualité
| Stérilité | La contamination par les mycoplasmes est exclue à l'aide de tests basés sur la PCR et de méthodes de détection des mycoplasmes basées sur la luminescence. Pour s'assurer de l'absence de contamination bactérienne, fongique ou levurienne, les cultures cellulaires font l'objet d'inspections visuelles quotidiennes. |
|---|---|
| Profil STR |
Amélogénine: x,x
CSF1PO: 11
D13S317: 11, 13, 14
D16S539: 12, 13
D5S818: 12, 13
D7S820: 11, 12
TH01: 6
TPOX: 9, 11
vWA: 16, 18
D3S1358: 14, 17
D21S11: 30, 32
D18S51: 12
D8S1179: 12, 14
FGA: 19
D1S1656: 15, 16
D2S1338: 17, 25
D12S391: 17, 23
D19S433: 15
|
| Allèles HLA |
A*: '02:01:01
B*: '15:01:01
C*: '04:01:01
DRB1*: '04:04:01
DQA1*: '03:01:01
DQB1*: '03:02:01
DPB1*: '04:01:01
E: '01:03:02
|
Certificat d'analyse (CoA)
| Numéro de lot | Type de certificat | Date | Numéro de catalogue |
|---|---|---|---|
| 300137-220424 | Certificat d'analyse | 23. May. 2025 | 300137 |
| 300137-170625 | Certificat d'analyse | 18. Aug. 2025 | 300137 |
Accord de transfert de matériel
Si vous avez l'intention d'utiliser les lignées cellulaires Cytion uniquement pour la recherche interne sur un seul site de recherche, veuillez remplir et signer notre accord de transfert de matériel (MTA) et le joindre à votre commande.
Pour toute application commerciale, y compris, mais sans s'y limiter, les travaux rémunérés, les tests de contrôle qualité, la mise sur le marché de produits, l'utilisation à des fins diagnostiques ou les études réglementaires, veuillez remplir le formulaire d'utilisation prévue afin que nous puissions préparer un accord adapté à votre projet.
Remarque : le MTA s'applique uniquement à certaines lignées cellulaires. Si cet avis et le document MTA apparaissent sur une page produit, l'accord est applicable. Pour les lignées cellulaires non couvertes par le MTA, aucune référence à l'accord ne sera affichée. Le MTA n'est pas valable pour les clients situés en Amérique, en Chine ou à Taïwan. Veuillez contacter notre entité américaine pour recevoir l'accord approprié.
-
Produits requis
Produits requis
Milieu de congélation CM-1 - 50 mlVariantes de milieux de cryoconservation: 50 mlLe milieu de congélation CM-1 de Cytion est un milieu de cryoconservation de pointe conçu pour garantir le plus haut niveau de viabilité et de fonctionnalité des cellules après la décongélation. Ce milieu polyvalent convient à un large éventail de types de cellules, y compris les cellules humaines et animales, ce qui en fait un outil essentiel pour diverses applications de recherche. Formulé avec une combinaison méticuleusement équilibrée de cryoprotecteurs et de nutriments essentiels, le milieu de congélation CM-1 minimise la formation de cristaux de glace et le stress cellulaire pendant le processus de congélation, préservant ainsi l'intégrité cellulaire.
Les principales caractéristiques du milieu de congélation CM-1 sont les suivantes :
Large compatibilité: Efficace pour une large gamme de types de cellules, y compris les cellules primaires, les cellules souches et les lignées cellulaires établies.
Haute viabilité: Optimisé pour maximiser la récupération et la viabilité des cellules après décongélation, garantissant des résultats expérimentaux fiables.
Prêt à l'emploi: Pratiquement préparé et stérilisé pour une application immédiate, réduisant le temps de préparation et le risque de contamination.
Stabilité améliorée: Maintient des performances constantes dans des conditions de cryoconservation standard, garantissant des résultats reproductibles.
Longue durée de conservation: CM-1 est un milieu de cryoconservation contenant du sérum, prêt à l'emploi, qui peut être conservé au réfrigérateur jusqu'à un an.
Utilisation du CM-1 pour la congélation des cellules
Pour utiliser le CM-1 pour congeler des cellules adhérentes ou en suspension, suivre les étapes suivantes
Pour les cellules adhérentes, les laver et les dissocier du substrat de culture. Pour les cellules en suspension, passer directement à l'étape suivante.
Compter les cellules pour s'assurer qu'elles ont la bonne concentration.
Centrifuger les cellules pour les culotter, puis les remettre en suspension dans le milieu de congélation CM-1.
Transférer les cellules remises en suspension dans des cryovials.
Utiliser une méthode de congélation lente avant de transférer les cellules pour un stockage à long terme
Méthode de congélation
Description
Etapes
❄️
Congélation manuelle
Méthode progressive impliquant une réduction graduelle de la température pour assurer la viabilité des cellules
1️⃣ Placer les cellules dans un milieu de congélation dans un congélateur à 4°C pendant 40 minutes.
2️⃣ Transférer dans un congélateur à -80°C pendant 24 heures.
3️⃣ Stocker les cellules dans de l'azote liquide pour une conservation à long terme
❄️
Utilisation de Mr. Frosty
Un appareil pratique qui permet de contrôler les taux de congélation sans alimentation électrique
1️⃣ Préparer les cellules dans des cryovials avec du milieu de congélation.
2️⃣ Placer les cryovials dans le récipient Mr. Frosty.
3️⃣ Conserver à -80°C pendant 24 heures avant de les transférer dans l'azote liquide
❄️
Congélateur à débit contrôlé
Un congélateur de haute précision de Thermo Fisher ou d'autres fabricants, conçu pour une réduction contrôlée de la température
1️⃣ Programmer l'appareil pour réduire progressivement la température.
2️⃣ Placer les cellules préparées dans le congélateur.
3️⃣ Après le cycle de congélation, transférer les cellules dans l'azote liquide
Stocker les cryovials à des températures inférieures à -130°C ou dans de l'azote liquide pour une conservation à long terme.
Ingrédients
Contient du FBS, du DMSO, du glucose et des sels
Pouvoir tampon : pH = 7,2 à 7,6
Le milieu de congélation CM-1 de Cytion offre une solution fiable pour la cryoconservation, garantissant une viabilité cellulaire et une fonctionnalité élevées après décongélation pour une large gamme d'applications de recherche.59,00 €*EMEM (MEM Eagle), w : 2 mM L-Glutamine, w : 2,2 g/L NaHCO3, w : EBSSLe milieu minimal essentiel d'Eagle (EMEM) est l'un des milieux de base les plus couramment utilisés pour la culture d'un large éventail de cellules mammifères, en particulier les lignées cellulaires adhérentes. Développée à l'origine par Harry Eagle, cette formulation classique contient les acides aminés essentiels, les vitamines et les sels inorganiques nécessaires à la croissance des cellules primaires et des lignées cellulaires établies dans des conditions de culture standard.
Cette formulation liquide prête à l'emploi et filtrée de manière stérile est enrichie en solution saline équilibrée d'Earle (EBSS), en L-glutamine 2 mM, en D-glucose (1,0 g/L) et en bicarbonate de sodium (NaHCO₃) à 2,2 g/L, ce qui la rend adaptée à une utilisation dans une atmosphère d'incubateur à CO₂ contrôlé (généralement 5 % de CO₂). Le rouge de phénol inclus sert d’indicateur de pH, permettant un contrôle visuel pratique de l’état du milieu pendant la culture cellulaire.
Caractéristiques principales
Formulation MEM classique d’Eagle avec la solution saline équilibrée d’Earle (EBSS)
2 mM de L-glutamine inclus – prêt à l'emploi
2,2 g/L de bicarbonate de sodium – tamponné pour une incubation à 5 % de CO₂
Avec du D-glucose (1,0 g/L) comme source principale de carbone
Avec du rouge de phénol comme indicateur de pH
Sans HEPES et sans pyruvate de sodium
Milieu liquide filtré stérile, prêt à l'emploi
pH 7,0 – 7,6
Applications typiques
L'EMEM permet la culture d'une grande variété de lignées cellulaires mammifères, notamment HeLa, HEK 293, Vero, MRC-5, L-929, BHK-21 et de nombreuses cellules primaires. Les applications courantes comprennent :
L'entretien et la multiplication de routine de lignées cellulaires adhérentes
Les processus de propagation virale et de production de vaccins
Applications de cytotoxicité et de bioessais
Études de transfection et d'expression protéique
La recherche fondamentale en biologie cellulaire et en biologie moléculaire
Pour une croissance cellulaire optimale, l'EMEM est généralement complété par 5 à 10 % de sérum fœtal bovin (FBS) et, selon la lignée cellulaire, par des acides aminés non essentiels (NEAA) et des antibiotiques tels que la pénicilline/streptomycine.
Manipulation et conservation
Conserver le flacon non ouvert entre +2 °C et +8 °C, à l'abri de la lumière. Après ouverture, utiliser dans des conditions aseptiques. La L-glutamine en solution est sujette à une dégradation progressive ; nous recommandons d'utiliser le milieu dans les 4 semaines suivant l'ouverture pour obtenir les meilleures performances, ou de le compléter avec de la L-glutamine fraîche avant utilisation en cas de stockage prolongé. Laisser le milieu se réchauffer à 37 °C avant de l'ajouter aux cellules.
Qualité
Fabriqué selon des normes de qualité strictes. Chaque lot est testé pour vérifier sa stérilité, son pH, son osmolalité et ses niveaux d'endotoxines afin de garantir des performances constantes dans les applications de culture cellulaire.
Spécifications du produit
Spécifications
Détails
Type de produitMEM
Catégorie de produitMilieux de culture cellulaire
FormatLiquide
StérileOui
Contenance500 ml
L-glutamineAvec L-glutamine (2 mM)
GlucoseAvec du glucose (1,0 g/L)
Bicarbonate de sodiumAvec NaHCO3 (2,2 g/L)
HEPESSans HEPES
Pyruvate de sodiumSans pyruvate de sodium
Rouge de phénolAvec rouge de phénol
Solution salineSolution saline équilibrée d'Earle (EBSS)
pH7,0 – 7,6
Teneur en endotoxinesNon spécifiée
Conservation+2 °C à +8 °C
Formulation (composition par litre)
Composant
Concentration (mg/L)
Sels inorganiques
Chlorure de calcium · 2H₂O265,00
Sulfate de magnésium97,72
Chlorure de potassium400,00
Chlorure de sodium6 800,00
Dihydrogénophosphate de sodium, anhydre122,00
Bicarbonate de sodium (NaHCO3)2 200,00
Acides aminés
L-Arginine · HCl126,00
L-cystine · 2HCl31,30
L-Glutamine292,00
L-histidine · HCl · H₂O42,00
L-isoleucine52,00
L-Leucine52,00
L-Lysine · HCl72,50
L-méthionine15,00
L-phénylalanine32,00
L-thréonine48,00
L-tryptophane10,00
L-Tyrosine · 2Na · 2H2O51,90
L-Valine46,00
Vitamines
D-pantothénate de calcium1,00
Chlorure de choline1,00
Acide folique1,00
Myo-inositol2,00
Nicotinamide1,00
Pyridoxal · HCl1,00
Riboflavine0,10
Thiamine · HCl1,00
Autres composants
D(+)-Glucose1 000,00
Rouge de phénol10,0025,00 €*Solution de détachement cellulaire Accutase - 100 mlVariantes: 100 mlSolution de détachement cellulaire Accutase avec EDTA et rouge de phénol – 100 ml
Accutase est une solution de détachement cellulaire prête à l'emploi et filtrée de manière stérile, conçue comme une alternative douce à la trypsine/EDTA pour dissocier les cellules mammifères adhérentes des récipients en plastique standard pour culture tissulaire et des surfaces revêtues d'un agent d'adhérence. Elle combine une activité enzymatique protéolytique et collagénolytique dans une solution saline équilibrée pour offrir une dissociation efficace mais contrôlée, préservant les protéines de surface cellulaire et favorisant une viabilité élevée après passage ainsi qu'une réadhérence rapide.
La formulation d'Accutase est basée sur une solution saline tamponnée au phosphate de Dulbecco (DPBS) avec de l'EDTA et du rouge de phénol comme indicateur visuel de pH. Les enzymes sont d'origine non mammifère et non bactérienne, ce qui rend Accutase particulièrement adapté à la recherche sur les cellules souches, aux processus de fabrication de vaccins et à toute application où les contaminants d'origine animale ou microbienne doivent être minimisés. La solution s'auto-inhibe à 37 °C ; aucun réactif neutralisant ni milieu contenant du sérum n'est donc nécessaire après le détachement – les cellules peuvent être transférées directement dans un milieu frais.
Caractéristiques principales
Liquide 1x stérilisé par filtration, prêt à l'emploi – aucune dilution ni reconstitution requise
Activité enzymatique combinée protéolytique et collagénolytique pour une dissociation en douceur
Chaque lot est standardisé à une activité de dissociation définie pour garantir la cohérence d'un lot à l'autre
Enzymes d'origine non mammifère et non bactérienne
S'auto-inhibe à 37 °C – aucune solution neutralisante n'est nécessaire
Formulé dans du PBS de Dulbecco avec de l'EDTA
Rouge de phénol inclus comme indicateur visuel de pH
pH 6,8 – 7,8
Applications typiques
Accutase dissocie en douceur une grande variété de types de cellules adhérentes et sensibles, notamment les cellules souches embryonnaires humaines (hESC), les cellules souches pluripotentes induites humaines (iPSC), les cellules souches neurales, les neurones primaires et les lignées adhérentes couramment cultivées telles que HeLa, HEK 293, CHO, MDCK, Vero, NIH/3T3, BHK-21 et A549. Exemples d'utilisation :
La sous-culture et le repiquage courants de cellules mammifères adhérentes
Dissociation douce de cellules individuelles issues de hESC, d'iPSC et d'autres lignées sensibles
Préparation d'échantillons pour la cytométrie en flux et l'analyse FACS
L'analyse des marqueurs de surface cellulaire où l'intégrité de l'épitope est cruciale
Tests de migration, de prolifération et d'apoptose cellulaires
Tests de quiescence par privation de sérum et études de transfection d'oncogènes
Tests de migration des cellules tumorales et des cellules de la crête neurale
Augmentation de la production dans les flux de travail en bioréacteur
Pour les travaux de routine, appliquez environ 10 ml d'Accutase par 75 cm² de surface de culture et incubez pendant 5 à 10 minutes à température ambiante. La durée d'incubation optimale doit être déterminée pour chaque lignée cellulaire et ne doit pas dépasser une heure. Avant l'ajout, rincez la couche cellulaire avec une solution saline exempte de Ca²⁺/Mg²⁺, telle que du DPBS sans calcium ni magnésium, afin d'éliminer le sérum résiduel et les cations divalents.
Manipulation et conservation
Conserver le flacon non ouvert congelé à -15 °C ou moins. Décongeler soit à température ambiante, soit pendant une nuit entre +2 °C et +8 °C. Ne pas décongeler Accutase dans un bain-marie à 37 °C, car les températures élevées réduisent l’activité enzymatique. Après décongélation, la solution peut être conservée jusqu’à 2 mois entre +2 °C et +8 °C ; ne pas conserver à température ambiante. Ne préchauffez pas le réactif à 37 °C avant utilisation – ajoutez-le directement aux cellules lavées à température ambiante. Pour une conservation à long terme, il est recommandé de prélever des aliquotes à usage unique afin d'éviter les cycles de décongélation répétés. Travaillez toujours dans des conditions aseptiques.
Qualité
Fabriqué selon des normes de qualité strictes. Chaque lot d'Accutase est filtré à stérilité et testé pour vérifier sa stérilité, son pH, son aspect et son activité de dissociation afin de garantir des performances constantes et reproductibles d'un lot à l'autre.
Spécifications du produit
Spécifications
Détails
Type de produitRéactif de détachement/dissociation cellulaire
FormatLiquide filtré stérile, prêt à l'emploi
Volume100 ml
Concentration d'utilisation1x (prêt à l'emploi)
Activité enzymatiqueProtéolytique et collagénolytique combinées
Origine de l'enzymeNon mammifère et non bactérienne
Système tamponPBS de Dulbecco avec EDTA
Indicateur de pHRouge de phénol
Plage de pH6,8 – 7,8
AspectSolution limpide, de couleur rouge pâle à orange
Température de stockage-15 °C ou moins
Stabilité après décongélationJusqu'à 2 mois entre +2 °C et +8 °C
Volume d'utilisation recommandé~10 ml par 75 cm² de surface de culture
Durée d'incubation typique5 à 10 minutes à température ambiante
Conditions d'expéditionCongelé dans de la glace carbonique
Utilisation prévueÀ usage exclusif pour la recherche et la fabrication ultérieure
Formulation (composition par litre)
Composant
Concentration (mg/L)
Sels inorganiques
Chlorure de sodium (NaCl)8000,00
Hydrogénophosphate disodique (Na₂HPO₄)1150,00
Chlorure de potassium (KCl)200,00
Dihydrogénophosphate de potassium (KH₂PO₄)200,00
Autres composants
EDTA · 4Na (EDTA tétrasodique)220,00
Rouge de phénol3,00
Mélange enzymatique exclusif (activité protéolytique et collagénolytique)1x
Accutase est une marque déposée d'Innovative Cell Technologies, Inc.75,00 €*Solution antibiotique/antimycosique (100x)Aperçu du produit
Volume : 100 ml Stockage : ≤-15°C Stérilité : Filtration stérile
Lasolution antibiotique/antimycosique (100x) est un concentré stérile, prêt à l'emploi, conçu pour réduire les risques de contamination microbienne dans les cultures cellulaires et les applications de laboratoire connexes. Cette solution 100x contient une combinaison bien établie de pénicilline, de streptomycine et d'amphotéricine B, qui fournit une activité antimicrobienne à large spectre contre les bactéries Gram-positives et Gram-négatives, les levures et les champignons filamenteux. La formulation convient aux cultures de cellules eucaryotes, aux milieux bactériens et à d'autres systèmes sensibles à la contamination, ce qui favorise des opérations de laboratoire propres et cohérentes.
Applications et avantages Optimisée pour les protocoles de recherche de routine, cette solution est largement utilisée pour maintenir des conditions aseptiques dans les flux de culture cellulaire. Elle offre des performances fiables dans les environnements sensibles à la contamination, aidant les chercheurs à réduire le risque de prolifération microbienne sans compromettre la santé des cellules ou la reproductibilité des expériences. La formulation stérile-filtrée élimine le besoin d'étapes de solubilisation supplémentaires, ce qui permet de rationaliser la préparation des milieux et de réduire la variabilité des procédures de laboratoire quotidiennes.
Utilisation et compatibilité Pour obtenir des concentrations de travail standard, diluer la solution au 1:100 dans votre milieu de culture complet. Le produit est compatible avec une large gamme de lignées cellulaires de mammifères et de milieux de base. Grâce à la disponibilité constante des stocks, les chercheurs bénéficient d'une continuité d'approvisionnement fiable et d'une planification logistique simplifiée. La solution doit être conservée à une température ≤ -15 °C et protégée des cycles répétés de congélation-décongélation pour maintenir sa stabilité. Réservé à la recherche. Ne pas utiliser dans des procédures diagnostiques ou thérapeutiques. Ne pas utiliser chez l'homme ou l'animal.45,00 €*PBSSolution saline tamponnée au phosphate (PBS)
La solution saline tamponnée au phosphate (PBS) est une solution tampon largement utilisée dans la recherche biologique et chimique. Elle joue un rôle crucial dans le maintien de l'équilibre du pH et de l'osmolarité au cours de diverses procédures expérimentales, y compris le traitement des tissus et la culture cellulaire. Notre solution PBS est méticuleusement formulée avec des ingrédients de haute pureté afin de garantir la stabilité et la fiabilité de chaque expérience. L'osmolarité et les concentrations d'ions de notre PBS imitent étroitement celles du corps humain, ce qui la rend isotonique et non toxique pour la plupart des cellules.
Composition de notre solution PBS
Notre solution PBS est un mélange de tampons phosphatés et de solutions salines de qualité supérieure dont le pH est ajusté. À une concentration de travail de 1X, elle contient :
8000 mg/L de chlorure de sodium (NaCl)
200 mg/L Chlorure de potassium (KCl)
1150 mg/L phosphate de sodium dibasique anhydre (Na2HPO4)
200 mg/L Phosphate de potassium monobasique anhydre (KH2PO4)
Cette composition assure un pH et un équilibre ionique optimaux, convenant à une large gamme d'applications biologiques.
Applications de notre solution PBS
Notre solution PBS est idéale pour diverses applications dans la recherche biologique. Ses propriétés isotoniques et non toxiques la rendent appropriée pour la dilution de substances et le rinçage de récipients cellulaires. Les solutions PBS contenant de l'EDTA sont efficaces pour désengager les cellules attachées et agglutinées. Cependant, les métaux divalents tels que le zinc ne doivent pas être ajoutés au PBS, car ils peuvent provoquer une précipitation. Dans ce cas, les tampons Good's sont recommandés. En outre, notre solution PBS est une alternative acceptable au milieu de transport viral pour le transport et le stockage des virus à ARN, y compris le SARS-CoV-2.
Contrôle de la qualité
Filtré stérilement
Stockage et durée de conservation
Stocker entre +2°C et +25°C, à l'abri de la lumière.
Après ouverture, conserver entre 2°C et 25°C et utiliser dans les 24 mois.
Conditions d'expédition
Température ambiante
Entretien
Conserver au réfrigérateur entre +2°C et +8°C à l'abri de la lumière. Éviter la congélation et le réchauffement fréquent jusqu'à +37°C, car cela réduit la qualité du produit.
Ne pas chauffer le milieu au-delà de 37°C ou utiliser des sources de chaleur non contrôlées telles que les micro-ondes.
Si une partie seulement du milieu doit être utilisée, prélever la quantité nécessaire et la réchauffer à température ambiante avant de l'utiliser.
Composition
Catégorie
Composants
Concentration (mg/L)
Sels
Chlorure de potassium
200
Phosphate de potassium monobasique anhydre
200
Chlorure de sodium
8000
Phosphate de sodium dibasique anhydre
115020,00 €* -
Produits apparentés
Produits apparentés