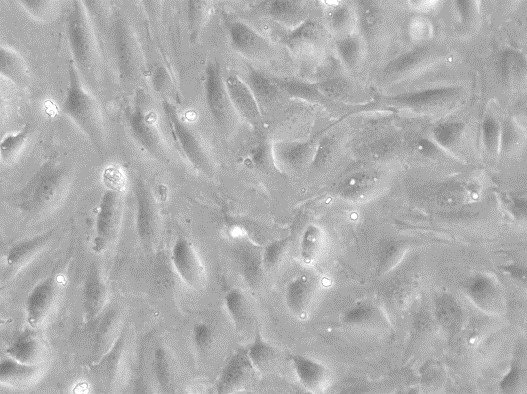
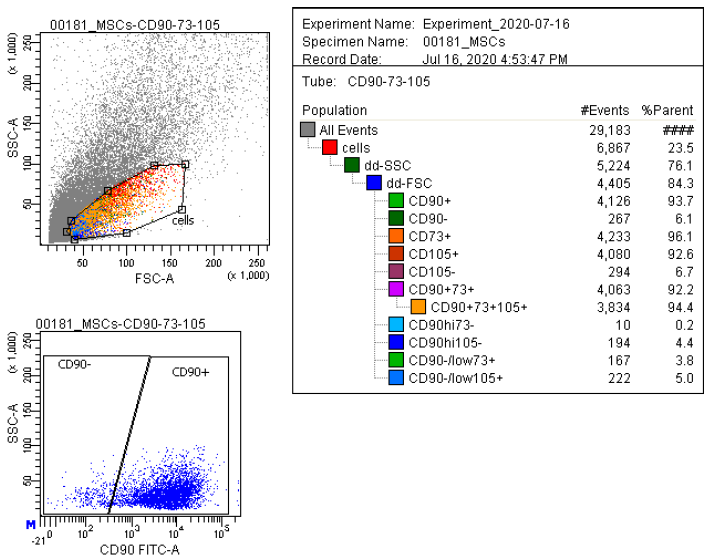
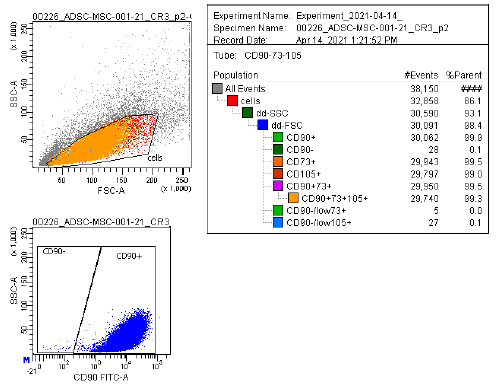
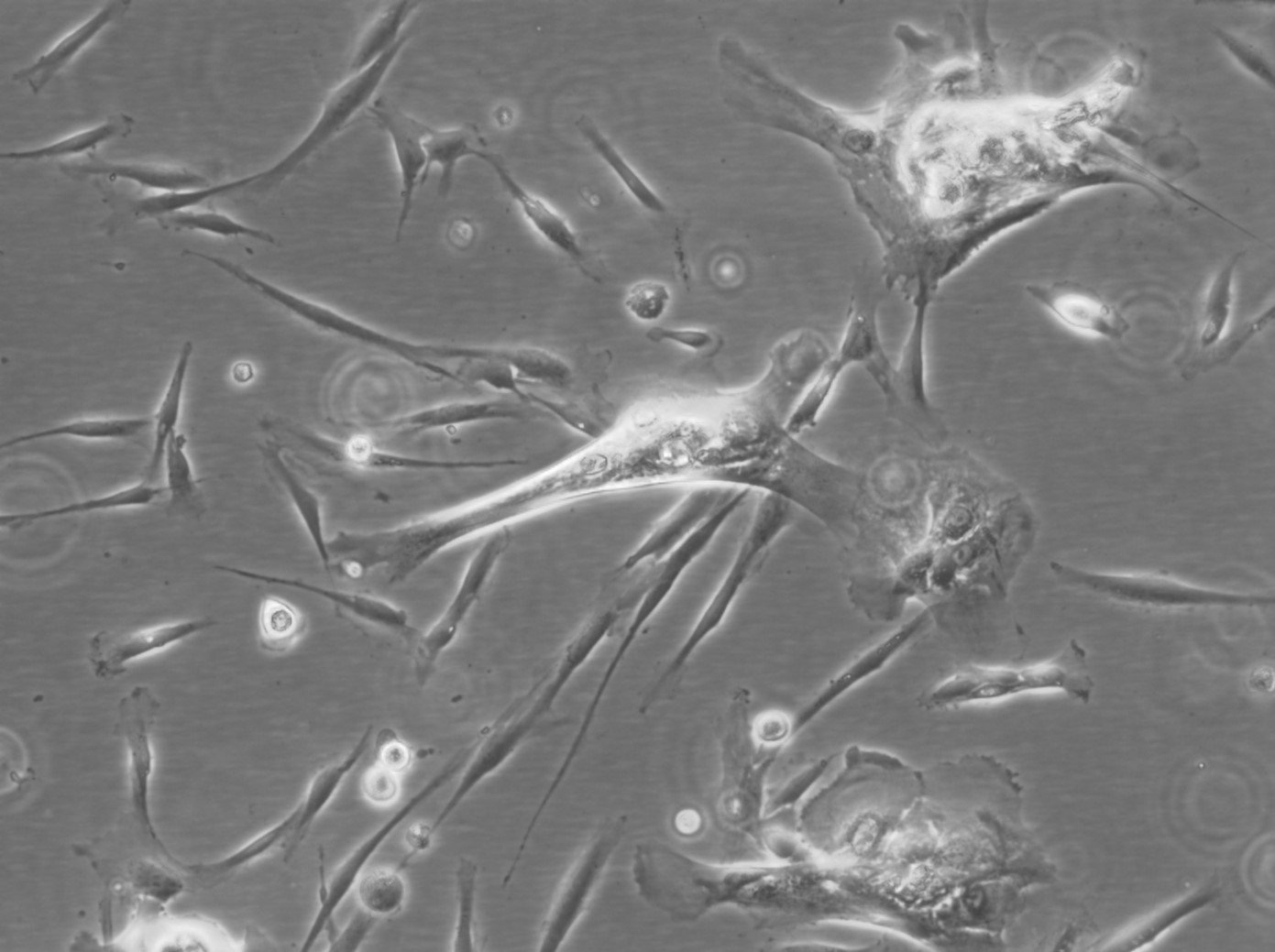
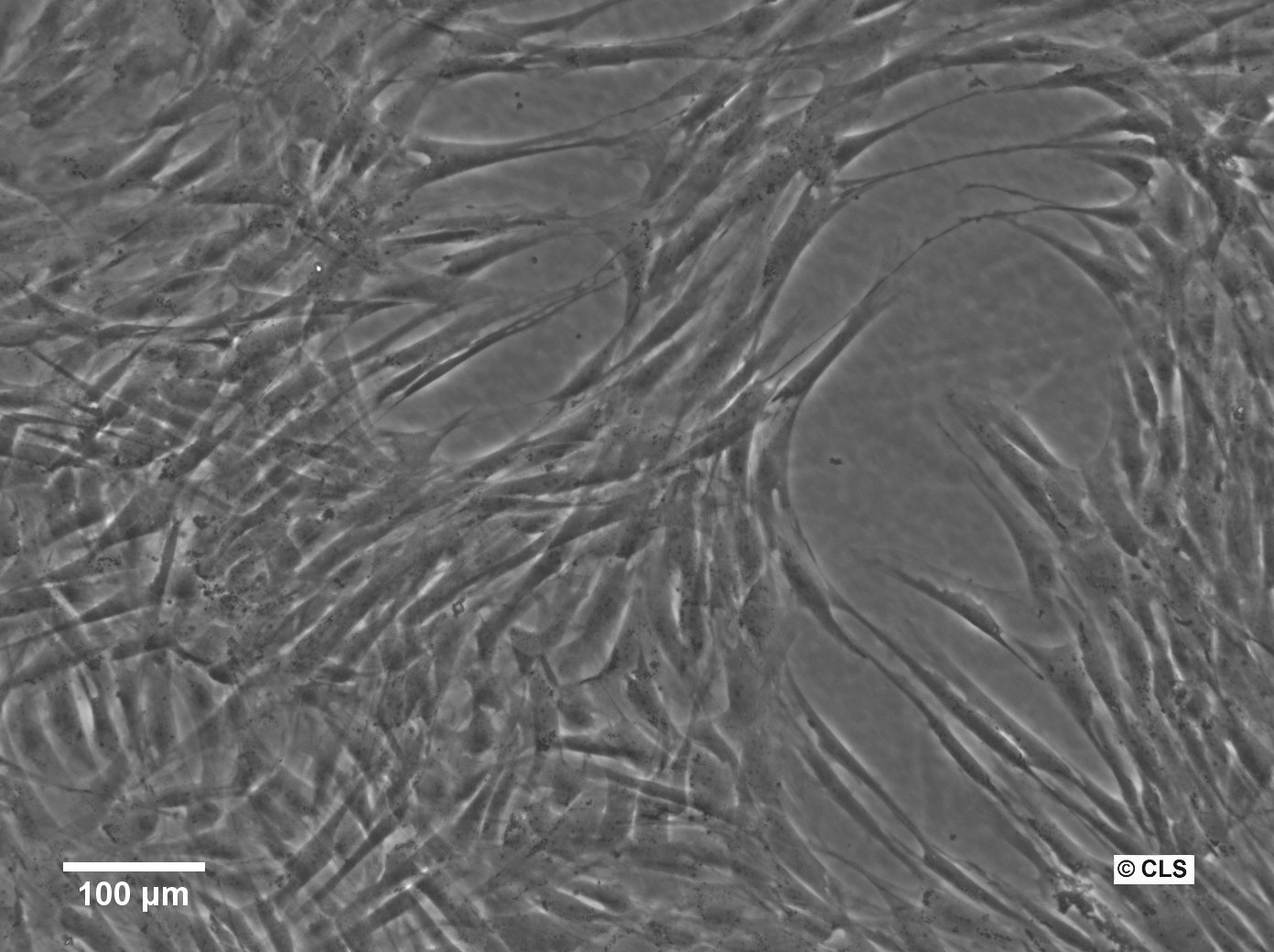
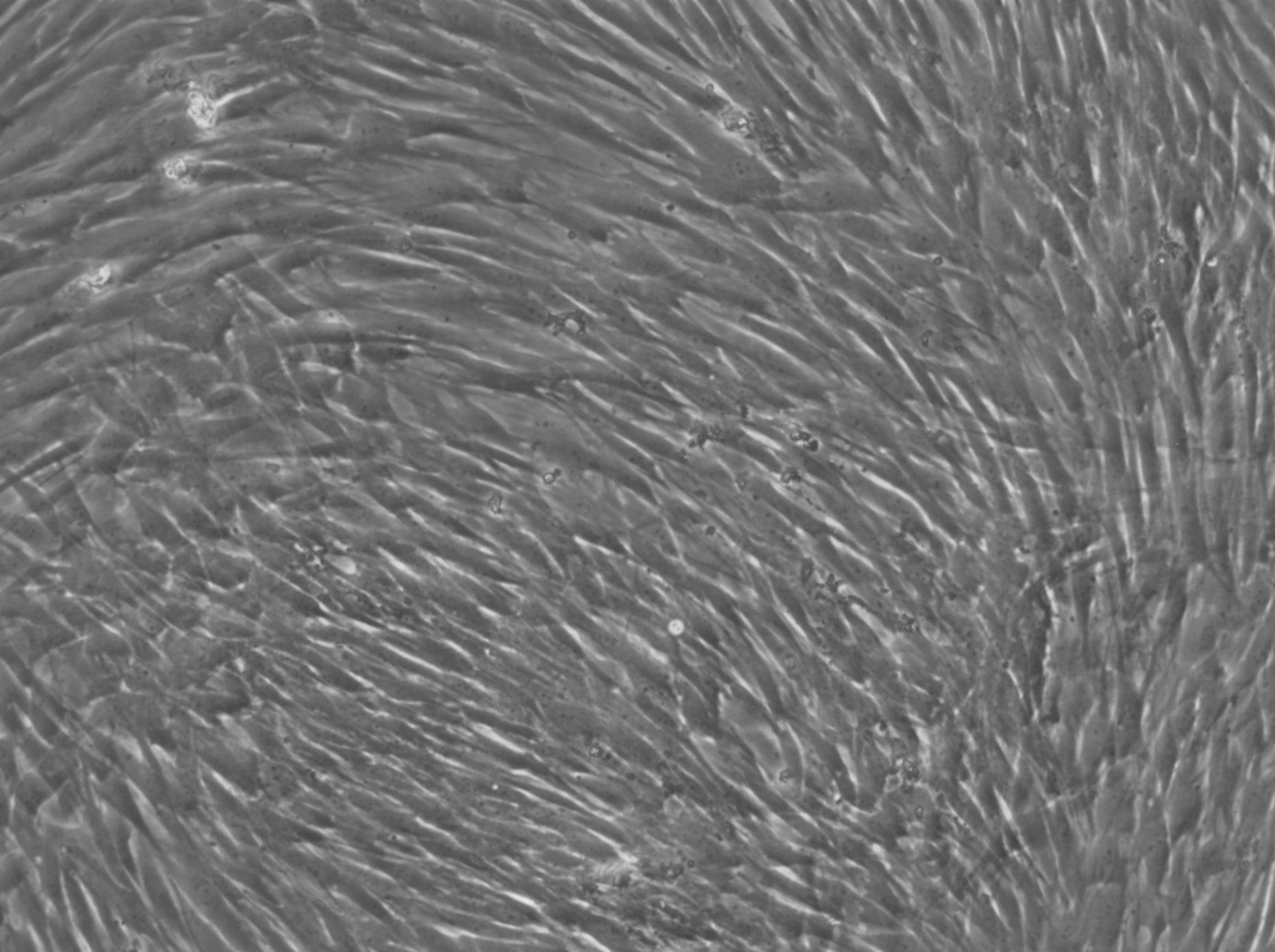
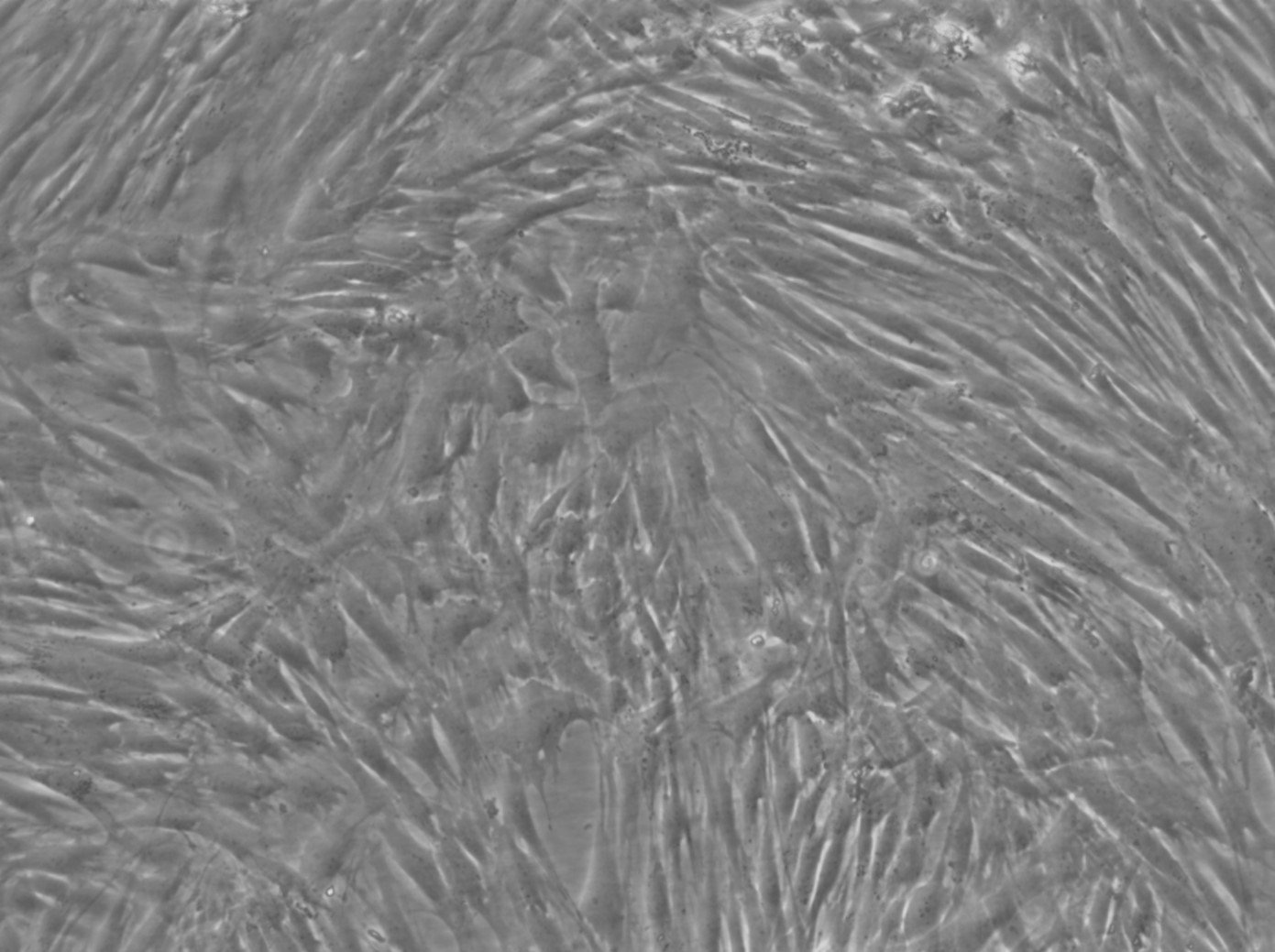
Células madre de la pulpa dental humana (hDPSC)






800,00 €*
Los productos se envían congelados en hielo seco en criotubos. Cada criotubo contiene normalmente 5 × 10 5 células para líneas celulares primarias (consulte el certificado de análisis del lote para obtener más detalles).
Información general
| Descripción | Las células madre de la pulpa dental humana (DPSC, hDPSC) son células madre multipotentes aisladas de la pulpa dental de dientes adultos, normalmente terceros molares. Estas células son especialmente valiosas en medicina regenerativa debido a su capacidad para diferenciarse en una gran variedad de tipos celulares, incluidos los que forman hueso, cartílago, grasa y tejidos dentales. Las DPSC destacan por su elevada capacidad proliferativa, lo que las convierte en una opción sólida para la ingeniería de tejidos y las aplicaciones terapéuticas basadas en células. Las DPSC también poseen importantes propiedades inmunomoduladoras, que contribuyen a su uso potencial en el tratamiento de afecciones inflamatorias. Además de la regeneración de tejidos dentales, se ha investigado su capacidad para reparar defectos óseos y su aplicación en terapias neurológicas. Su accesibilidad relativamente fácil y su capacidad para mantener la viabilidad tras la crioconservación hacen de las DPSC una opción atractiva para la investigación clínica y el desarrollo terapéutico, especialmente en los ámbitos de la odontología regenerativa, la ortopedia y las enfermedades neurodegenerativas. |
|---|---|
| Organismo | Humano |
| Tejido | Dental |
| Aplicaciones | Análisis de fármacos, medicina regenerativa, investigación de enfermedades |
Características
| Propiedades de crecimiento | Adherente |
|---|
Datos reglamentarios
| Cita | Células madre de la pulpa dental humana (DPSC, hDPSC) (número de catálogo 300702 de Cytion) |
|---|---|
| Nivel de bioseguridad | 1 |
| NCBI_TaxID | 9606 |
Datos biomoleculares
Manejo de
| Medio de cultivo | MEM alfa, con: 2,0 mM de glutamina estable, sin Ribonucleósidos, w/o: Desoxirribonucleósidos, w: 1,0 mM Piruvato sódico, w: 2,2g/L NaHCO3 |
|---|---|
| Suplementos | Suplementar el medio con 10% FBS, 2 ng/mL bFGF |
| Reactivo de disociación | Accutase |
| Subcultivo | Retire el medio antiguo de las células adheridas y lávelas con PBS que carezca de calcio y magnesio. Para matraces T25, utilice 3-5 ml de PBS, y para matraces T75, utilice 5-10 ml. A continuación, cubra completamente las células con Accutase, utilizando 1-2 ml para matraces T25 y 2,5 ml para matraces T75. Deje incubar las células a temperatura ambiente durante 8-10 minutos para desprenderlas. Tras la incubación, mezclar suavemente las células con 10 ml de medio para resuspenderlas y, a continuación, centrifugar a 300xg durante 3 minutos. Desechar el sobrenadante, resuspender las células en medio fresco y transferirlas a nuevos matraces que ya contengan medio fresco. |
| Medio de congelación | Como medio de criopreservación, utilizamos FBS al 90% + DMSO al 10% para mantener la viabilidad, o CM-1 (número de catálogo 800100 de Cytion), que incluye osmoprotectores optimizados y estabilizadores metabólicos para mejorar la recuperación y reducir el estrés crioinducido. |
| Descongelación y cultivo de células |
|
| Atmósfera de incubación | 37°C, 5%CO2, atmósfera humidificada. |
| Recubrimiento de matraces | Ninguno |
| Procedimiento de congelación | Las líneas celulares crioconservadas se envían en hielo seco en envases validados y aislados con suficiente refrigerante para mantener aproximadamente -78 °C durante el tránsito. A la recepción, inspeccione el envase inmediatamente y transfiera los viales sin demora al almacenamiento adecuado. |
| Condiciones de envío | Las líneas celulares crioconservadas se envían en hielo seco en envases validados y aislados con suficiente refrigerante para mantener aproximadamente -78 °C durante el tránsito. A la recepción, inspeccione el envase inmediatamente y transfiera los viales sin demora al almacenamiento adecuado. |
| Condiciones de almacenamiento | Para la conservación a largo plazo, coloque los viales en nitrógeno líquido en fase vapor a una temperatura aproximada de -150 a -196 °C. El almacenamiento a -80 °C sólo es aceptable como breve paso intermedio antes de la transferencia al nitrógeno líquido. |
Control de calidad / Perfil genético / HLA
| Esterilidad | La contaminación por micoplasma se excluye utilizando tanto ensayos basados en la PCR como métodos de detección de micoplasma basados en la luminiscencia. Para garantizar la ausencia de contaminación bacteriana, fúngica o por levaduras, los cultivos celulares se someten a inspecciones visuales diarias. |
|---|
Acuerdo de transferencia de material
Si tiene intención de utilizar las líneas celulares Cytion exclusivamente para investigación interna en un único centro de investigación, rellene y firme nuestro Acuerdo de transferencia de material (MTA) y envíelo junto con su pedido.
Para cualquier aplicación comercial, incluyendo, entre otras, trabajos remunerados, pruebas de control de calidad, lanzamiento de productos, uso diagnóstico o estudios normativos, rellene el formulario de uso previsto para que podamos preparar un acuerdo adecuado a su proyecto.
Tenga en cuenta que el MTA solo se aplica a determinadas líneas celulares. Si este aviso y el documento MTA aparecen en la página de un producto, el acuerdo es aplicable. En el caso de las líneas celulares no cubiertas por el MTA, no se mostrará ninguna referencia al acuerdo. El MTA no es válido para clientes de América, China o Taiwán. Póngase en contacto con nuestra entidad en EE. UU. para recibir el acuerdo correspondiente.
-
Productos necesarios
Productos necesarios
Medio de congelación CM-1 - 50 mlVariantes de medios de crioconservación: 50 mlEl medio de congelación CM-1 de Cytion es un medio de criopreservación de última generación diseñado para garantizar el máximo nivel de viabilidad y funcionalidad celular tras la descongelación. Este medio versátil es adecuado para un amplio espectro de tipos celulares, incluyendo células humanas y animales, lo que lo convierte en una herramienta esencial para diversas aplicaciones de investigación. Formulado con una combinación meticulosamente equilibrada de crioprotectores y nutrientes esenciales, Freeze Medium CM-1 minimiza la formación de cristales de hielo y el estrés celular durante el proceso de congelación, preservando así la integridad celular.
Las principales características de Freeze Medium CM-1 incluyen:
Amplia compatibilidad: Eficaz para una amplia gama de tipos celulares, incluyendo células primarias, células madre y líneas celulares establecidas.
Alta Viabilidad: Optimizado para maximizar la recuperación y viabilidad celular tras la descongelación, garantizando resultados experimentales fiables.
Listo para usar: Cómodamente preparadas y esterilizadas para su aplicación inmediata, reduciendo el tiempo de preparación y el riesgo de contaminación.
Estabilidad mejorada: Mantiene un rendimiento constante en condiciones de criopreservación estándar, garantizando resultados reproducibles.
Larga vida útil: CM-1 es un medio de criopreservación que contiene suero, listo para usar y que puede almacenarse en el frigorífico hasta un año.
Uso de CM-1 para congelar células
Para utilizar CM-1 para congelar células tanto adherentes como en suspensión, siga estos pasos
Para células adherentes, lavarlas y disociarlas del sustrato de cultivo. Para células en suspensión, proceder directamente al paso siguiente.
Contar las células para asegurarse de que tienen la concentración adecuada.
Centrifugar las células para granularlas y, a continuación, resuspenderlas en medio de congelación CM-1.
Transfiera las células resuspendidas a crioviales.
Utilizar un método de congelación lenta antes de transferir las células al almacenamiento a largo plazo
Método
Descripción
Pasos
❄️
Congelación manual
Un método paso a paso que implica la reducción gradual de la temperatura para garantizar la viabilidad celular
1️⃣ Colocar las células en medio de congelación en un congelador a 4°C durante 40 minutos.
2️⃣ Transferir a un congelador a -80°C durante 24 horas.
3️⃣ Almacenar las células en nitrógeno líquido para su conservación a largo plazo
❄️
Utilización de Mr. Frosty
Un práctico dispositivo que permite velocidades de congelación controladas sin energía eléctrica
1️⃣ Preparar las células en crioviales con medio de congelación.
2️⃣ Colocar los crioviales en el contenedor Mr. Frosty.
3️⃣ Almacenar a -80°C durante 24 horas antes de transferir al nitrógeno líquido
❄️
Congelador de velocidad controlada
Congelador de alta precisión de Thermo Fisher u otros fabricantes diseñado para la reducción controlada de la temperatura
1️⃣ Programar el aparato para que disminuya gradualmente la temperatura.
2️⃣ Colocar las células preparadas en el congelador.
3️⃣ Tras el ciclo de congelación, transfiera las células a nitrógeno líquido
Almacenar los crioviales a temperaturas inferiores a -130°C o en nitrógeno líquido para su conservación a largo plazo.
Ingredientes
Contiene FBS, DMSO, glucosa, sales
Capacidad tampón: pH = 7,2 a 7,6
El Medio de Congelación CM-1 de Cytion ofrece una solución fiable para la criopreservación, asegurando una alta viabilidad celular y funcionalidad post-descongelación para una amplia gama de aplicaciones de investigación.59,00 €*Solución para el desprendimiento celular Accutase - 100 mlVariantes: 100 mlSolución de desprendimiento celular Accutase con EDTA y rojo de fenol – 100 ml
Accutase es una solución de desprendimiento celular lista para usar y filtrada estérilmente, diseñada como una alternativa suave a la tripsina/EDTA para disociar células mamíferas adherentes de material plástico estándar para cultivo de tejidos y superficies recubiertas para la adhesión. Combina la actividad enzimática proteolítica y colagenolítica en una solución salina equilibrada para proporcionar una disociación eficaz pero controlada, preservando las proteínas de la superficie celular y favoreciendo una alta viabilidad tras el paso y una rápida readhesión.
La formulación de Accutase se basa en la solución salina tamponada con fosfato de Dulbecco (DPBS) con EDTA y rojo de fenol como indicador visual del pH. Las enzimas son de origen no mamífero y no bacteriano, lo que hace que Accutase sea especialmente adecuado para la investigación con células madre, los procesos de desarrollo de vacunas y cualquier aplicación en la que sea necesario minimizar los contaminantes de origen animal o microbiano. La solución se autoinhibe a 37 °C, por lo que no se requiere ningún reactivo neutralizante ni medio que contenga suero tras la desadhesión: las células pueden transferirse directamente a un medio fresco.
Características principales
Líquido 1x filtrado estéril listo para usar: no requiere dilución ni reconstitución
Actividad enzimática combinada proteolítica y colagenolítica para una disociación suave
Cada lote está estandarizado con una actividad de disociación definida para garantizar la consistencia entre lotes
Enzimas de origen no mamífero y no bacteriano
Se autoinhibe a 37 °C: no se necesita solución neutralizante
Formulado en PBS de Dulbecco con EDTA
Incluye rojo de fenol como indicador visual de pH
pH 6,8 – 7,8
Aplicaciones típicas
Accutase disocia suavemente una amplia variedad de tipos de células adherentes y sensibles, incluidas las células madre embrionarias humanas (hESC), las células madre pluripotentes inducidas humanas (iPSC), las células madre neurales, las neuronas primarias y las líneas adherentes cultivadas habitualmente, como HeLa, HEK 293, CHO, MDCK, Vero, NIH/3T3, BHK-21 y A549. Entre los casos de uso típicos se incluyen:
Subcultivo y pases rutinarios de células mamíferas adherentes
Disociación suave de células individuales de hESC, iPSC y otras líneas sensibles
Preparación de muestras para citometría de flujo y análisis FACS
Análisis de marcadores de superficie celular en los que la integridad del epítopo es importante
Ensayos de migración, proliferación y apoptosis celular
Ensayos de quiescencia mediante privación de suero y estudios de transfección de oncogenes
Ensayos de migración de células tumorales y de la cresta neural
Ampliación de la producción en flujos de trabajo con biorreactores
Para el trabajo rutinario, aplique aproximadamente 10 ml de Accutase por cada 75 cm² de superficie de cultivo e incube durante 5-10 minutos a temperatura ambiente. El tiempo de incubación óptimo debe determinarse para cada línea celular y no debe superar una hora. Antes de la adición, enjuague la capa celular con una solución salina libre de Ca²⁺/Mg²⁺, como DPBS sin calcio ni magnesio, para eliminar el suero residual y los cationes divalentes.
Manipulación y almacenamiento
Almacene el frasco sin abrir congelado a -15 °C o menos. Descongele a temperatura ambiente o durante la noche a una temperatura de entre +2 °C y +8 °C. No descongele Accutase en un baño de agua a 37 °C, ya que las temperaturas elevadas reducen la actividad enzimática. Tras la descongelación, la solución puede almacenarse hasta 2 meses a una temperatura de entre +2 °C y +8 °C; no la almacene a temperatura ambiente. No precaliente el reactivo a 37 °C antes de su aplicación; añádalo directamente a las células lavadas a temperatura ambiente. Para una vida útil prolongada, se recomienda el fraccionamiento en alícuotas de un solo uso para evitar ciclos de descongelación repetidos. Trabaje siempre en condiciones asépticas.
Calidad
Fabricado bajo estrictas normas de calidad. Cada lote de Accutase se filtra en condiciones estériles y se somete a pruebas de esterilidad, pH, aspecto y actividad de disociación para garantizar un rendimiento constante y reproducible de un lote a otro.
Especificaciones del producto
Especificaciones
Detalle
Tipo de productoReactivo de desprendimiento/disociación celular
FormatoLíquido filtrado estéril, listo para usar
Volumen100 ml
Concentración de trabajo1x (listo para usar)
Actividad enzimáticaProteolítica y colagenolítica combinadas
Origen de la enzimaNo mamífero y no bacteriano
Sistema tampónPBS de Dulbecco con EDTA
Indicador de pHRojo de fenol
Rango de pH6,8 – 7,8
AspectoSolución transparente, de color rojo pálido a naranja
Temperatura de almacenamiento-15 °C o menos
Estabilidad tras la descongelaciónHasta 2 meses a una temperatura de entre +2 °C y +8 °C
Volumen de uso recomendado~10 ml por cada 75 cm² de superficie de cultivo
Tiempo de incubación habitual5 – 10 minutos a temperatura ambiente
Condiciones de envíoCongelado en hielo seco
Uso previstoSolo para uso en investigación y fabricación posterior
Formulación (composición por litro)
Componente
Concentración (mg/L)
Sales inorgánicas
Cloruro de sodio (NaCl)8000,00
Hidrogenofosfato disódico (Na₂HPO₄)1150,00
Cloruro de potasio (KCl)200,00
Dihidrogenofosfato de potasio (KH₂PO₄)200,00
Otros componentes
EDTA · 4Na (EDTA tetrasódico)220,00
Rojo de fenol3,00
Mezcla enzimática patentada (actividad proteolítica y colagenolítica)1x
Accutase es una marca registrada de Innovative Cell Technologies, Inc.75,00 €*Solución antibiótica/antimicótica (100x)Descripción general del producto
Volumen: 100 ml Almacenamiento: ≤-15°C Esterilidad: Filtrado estéril
La Solución Antibiótica/Antimicótica (100x ) es un concentrado estéril, listo para usar, diseñado para reducir los riesgos de contaminación microbiana en cultivos celulares y aplicaciones de laboratorio relacionadas. Esta solución 100x contiene una combinación bien establecida de penicilina, estreptomicina y anfotericina B, que proporciona una actividad antimicrobiana de amplio espectro contra bacterias Gram-positivas y Gram-negativas, levaduras y hongos filamentosos. La formulación es adecuada para su uso en cultivos de células eucariotas, medios bacterianos y otros sistemas sensibles a la contaminación, lo que favorece unas operaciones de laboratorio limpias y consistentes.
Aplicación y ventajas Optimizada para protocolos de investigación rutinarios, esta solución se utiliza ampliamente para mantener condiciones asépticas en flujos de trabajo de cultivos celulares. Ofrece un rendimiento fiable en entornos sensibles a la contaminación, ayudando a los investigadores a reducir el riesgo de sobrecrecimiento microbiano sin comprometer la salud celular o la reproducibilidad experimental. La formulación filtrada estéril elimina la necesidad de pasos adicionales de solubilización, lo que permite una preparación racionalizada de los medios y reduce la variabilidad en los procedimientos diarios de laboratorio.
Uso y compatibilidad Para alcanzar concentraciones de trabajo estándar, diluya la solución 1:100 en su medio de cultivo completo. El producto es compatible con una amplia gama de líneas celulares de mamíferos y medios basales. Con una disponibilidad de stock constante, los investigadores se benefician de una continuidad de suministro fiable y una planificación logística simplificada. La solución debe almacenarse a ≤ -15 °C y protegerse de ciclos repetidos de congelación-descongelación para mantener la estabilidad. Sólo para uso en investigación. No para uso en procedimientos diagnósticos o terapéuticos. No para uso en humanos o animales.45,00 €*PBSSolución salina tamponada con fosfato (PBS)
La solución salina tamponada con fosfato (PBS) es una solución tampón muy utilizada en la investigación biológica y química. Desempeña un papel crucial en el mantenimiento del equilibrio del pH y la osmolaridad durante diversos procedimientos experimentales, como el procesamiento de tejidos y el cultivo celular. Nuestra solución PBS está meticulosamente formulada con ingredientes de gran pureza para garantizar la estabilidad y fiabilidad en cada experimento. La osmolaridad y las concentraciones de iones de nuestra PBS imitan fielmente las del cuerpo humano, por lo que es isotónica y no tóxica para la mayoría de las células.
Composición de nuestra solución PBS
Nuestra solución PBS es una mezcla de soluciones salinas y tampones de fosfato de grado ultrapuro con pH ajustado. A una concentración de trabajo de 1X, contiene:
8000 mg/L de cloruro sódico (NaCl)
200 mg/L Cloruro potásico (KCl)
1150 mg/L Fosfato sódico dibásico anhidro (Na2HPO4)
200 mg/L Fosfato potásico monobásico anhidro (KH2PO4)
Esta composición garantiza un pH y un equilibrio iónico óptimos, adecuados para una amplia gama de aplicaciones biológicas.
Aplicaciones de nuestra solución PBS
Nuestra solución PBS es ideal para diversas aplicaciones en investigación biológica. Sus propiedades isotónicas y no tóxicas la hacen adecuada para la dilución de sustancias y el enjuague de contenedores celulares. Las soluciones de PBS que contienen EDTA son eficaces para desprender células adheridas y aglomeradas. Sin embargo, los metales divalentes como el zinc no deben añadirse al PBS, ya que pueden provocar precipitación. En tales casos, se recomiendan los tampones de Good. Además, nuestra solución de PBS es una alternativa aceptable al medio de transporte viral para el transporte y almacenamiento de virus de ARN, incluido el SARS-CoV-2.
Control de calidad
Filtrado estéril
Almacenamiento y vida útil
Almacenar a +2°C a +25°C, protegido de la luz.
Una vez abierto, conservar entre 2°C y 25°C y utilizar antes de 24 meses.
Condiciones de envío
Temperatura ambiente
Conservación
Conservar refrigerado a +2°C a +8°C en la oscuridad. Evitar la congelación y el calentamiento frecuente a +37°C, ya que reduce la calidad del producto.
No calentar el medio a más de 37°C ni utilizar fuentes de calor no controladas, como aparatos de microondas.
Si sólo se va a utilizar una parte del medio, retirar la cantidad necesaria y calentarla a temperatura ambiente antes de su uso.
Composición
Categoría
Componentes
Concentración (mg/L)
Sales
Cloruro de potasio
200
Fosfato potásico monobásico anhidro
200
Cloruro sódico
8000
Fosfato sódico dibásico anhidro
115020,00 €* -
Productos relacionados
Productos relacionados
Células madre mesenquimales humanas - Tejido adiposoOrganismo Humano Tejido Tejido adiposo 690,00 €*Células madre mesenquimales humanas - Médula ósea (HMSC-BM)Organismo Humano Tejido Médula ósea 690,00 €*