Hacim: 100 ml
Saklama: ≤ –15°C
Sterilite: Steril filtrelenmiş
Stabil Glutamin Çözeltisi (L-Alanyl-L-Glutamine, 200 mM), hücre kültürü ortamlarında geleneksel L-glutaminin yerine doğrudan kullanılmak üzere tasarlanmış, oldukça stabil bir dipeptid formundaki L-glutamindir. L-glutamin, kültürlenmiş hücreler için temel bir amino asit ve önemli bir enerji kaynağıdır ve hücre büyümesi, metabolizma ve protein sentezinde kritik bir rol oynar.
Uygulama ve Avantajları
Standart sıvı ortamlarda, L-glutamin 37 °C'de nispeten hızlı bir şekilde bozunur ve hücre canlılığını ve deney sonuçlarını olumsuz etkileyebilecek amonyum iyonları gibi toksik yan ürünlerin oluşmasına neden olur. Stabil glutamin, kültür koşullarında bozulmayan bir dipeptid formu sağlayarak bu sınırlamayı ortadan kaldırır.
Hücreler, dipeptid bağını enzimatik olarak parçalayarak gerektiğinde L-glutamin salar ve zararlı atık ürünlerin birikmesini önlerken sürekli taze bir tedarik sağlar. Bu, çözeltiyi uzun süreli hücre kültürleri ve yüksek yoğunluklu büyüme sistemleri için özellikle avantajlı hale getirir.
Formülasyon ve Kullanım
L-Alanyl-L-Glutamine çözeltisi, hücre kültürü sınıfı suda 200 mM konsantrasyonda hazırlanır ve kontaminasyona duyarlı uygulamalar için steril filtreden geçirilir. Deney gereksinimlerine göre doğrudan tam besiyerine seyreltilebilir. Ürün stabilitesini korumak için ≤ –15°C'de saklayın ve tekrarlı donma-çözülme döngülerinden kaçının.
Yalnızca araştırma amaçlıdır. Teşhis veya tedavi prosedürlerinde kullanılmaz. İnsanlarda veya hayvanlarda kullanılmaz.
Hacim: 100 ml
Saklama: +2°C ila +8°C
Sterilite: Steril filtrelenmiş
HEPES Tampon Çözeltisi (1 M), N-2-hidroksietilpiperazin-N-2-etansülfonik asit olarak da bilinir ve hücre kültürü ortamlarında yaygın olarak kullanılan bir zwitteriyonik organik tamponlama maddesidir. Fizyolojik aralıkta 6,7 ila 8,6 arasında stabil pH koşullarını korumak üzere tasarlanmıştır ve in vitro uygulamalar sırasında optimal hücre fonksiyonunu destekler.
Uygulama ve Avantajları
HEPES, özellikle hücreler CO₂ inkübatörü dışında işlendiğinde, hücre kültürü sistemlerinde güvenilir tamponlama kapasitesi sağlar. Kültür ortamına 10–25 mM HEPES ilavesi, uzun manipülasyon süreleri boyunca pH stabilitesini artırarak tutarlı deney koşullarının korunmasına yardımcı olur.
Bu tampon, membran geçirgen değildir, biyokimyasal reaksiyonlarla minimum düzeyde etkileşime girer ve güçlü kimyasal ve enzimatik stabilite gösterir. Bu özellikleri, onu çok çeşitli hücre kültürü ve biyokimyasal uygulamalar için uygun hale getirir.
Formülasyon ve Kullanım
Çözelti, hücre kültürü sınıfı suyla hazırlanmış 1 M konsantre olarak tedarik edilir ve kontaminasyona duyarlı ortamlarda kullanılmak üzere steril filtreden geçirilir. Uygulama gereksinimlerine bağlı olarak istenen çalışma konsantrasyonuna seyreltilebilir. Ürün bütünlüğünü korumak için +2°C ila +8°C arasında saklayın ve aseptik koşullarda kullanın.
Yalnızca araştırma amaçlıdır. Teşhis veya tedavi prosedürlerinde kullanılmaz. İnsanlarda veya hayvanlarda kullanılmaz.
Hacim: 50 ml
Saklama: +2°C ila +8°C
Sterilite: Steril filtrelenmiş
D-(+)-Glikoz Solüsyonu (Dekstroz Solüsyonu), hücresel metabolizmanın merkezi bir bileşeni olan doğal olarak bulunan D-(+)-glikoz şekerini içeren, steril, kullanıma hazır bir takviyedir. Glikoz, enerji üretimi, glikozilasyon ve hücresel yapı ve fonksiyona katkıda bulunan glikanların oluşumu gibi temel biyolojik süreçlerde rol oynar.
Uygulama ve Faydaları
Bu glikoz çözeltisi, hücre kültürü ortamlarında ve çok sayıda hücresel ve moleküler biyoloji uygulamasında takviye olarak yaygın olarak kullanılmaktadır. Birincil karbon ve enerji kaynağı olarak glikoz, hücre büyümesini, çoğalmasını ve metabolik aktiviteyi destekler. Biyosentetik yollarda rol oynaması, normal hücresel fizyolojiyi ve deneysel tutarlılığı korumak için de kritik öneme sahiptir.
Formülasyon ve Kullanım
Çözelti, 250 g/L glikoz gibi yüksek bir konsantrasyonda sağlanır ve deney gereksinimlerine göre kültür ortamına esnek bir şekilde seyreltilebilir. Kontaminasyona duyarlı uygulamalar için uygunluğunu sağlamak amacıyla steril filtreden geçirilir. Ürün kalitesini ve stabilitesini korumak için +2°C ila +8°C arasında saklayın ve aseptik olarak kullanın.
Yalnızca araştırma amaçlıdır. Teşhis veya tedavi prosedürlerinde kullanılmaz. İnsanlarda veya hayvanlarda kullanılmaz.
Hacim: 10 ml
Saklama: +2°C ila +8°C
Sterilite: Steril filtrelenmiş
İnsülin-Transferrin-Selenyum (ITS) Çözeltisi (100x), çok çeşitli hücre kültürü uygulamaları için tasarlanmış, kimyasal olarak tanımlanmış bir takviyedir. En yaygın olarak, düşük serumlu veya serumsuz koşullarda hücre büyümesini desteklemek için bazal hücre kültürü ortamlarına katkı maddesi olarak kullanılır.
Uygulama ve Avantajlar
ITS takviyemiz, serumsuz ortamların optimum performansı için gerekli olan temel bileşenleri sağlar. Geleneksel besin ortamlarına ITS takviyesi yapılarak, birçok hücre hattının rutin bakımı için gerekli olan fetal sığır serumu (FBS) ihtiyacı önemli ölçüde azaltılabilir. Bu, tutarlı hücre büyümesi ve canlılığını korurken, serum kullanımıyla ilişkili değişkenliği en aza indirmeye yardımcı olur.
İnsülin, temel besin maddelerinin hücre tarafından alınmasını ve metabolizmasını destekler, transferrin demir taşınmasını kolaylaştırır ve selenyum, antioksidan savunmaya ve enzimatik aktiviteye katkıda bulunur. Bu bileşenler birlikte, tanımlanmış kültür sistemlerinde dengeli hücre metabolizmasını ve daha iyi tekrarlanabilirliği destekler.
Formülasyon ve Kullanım
İnsülin-Transferrin-Selenyum (ITS), fenol kırmızısı içermeyen Earle's Balanced Salt Solution (EBSS) içinde 100 kat konsantre bir çözelti olarak sunulur. Standart uygulamalar için, önerilen çalışma konsantrasyonuna ulaşmak üzere uygun bazal besiyerinde 1:100 oranında seyreltin. Ürün stabilitesini ve sterilliğini korumak için +2°C ila +8°C arasında saklayın ve aseptik koşullar altında kullanın.
Yalnızca araştırma amaçlıdır. Teşhis veya tedavi prosedürlerinde kullanılmamalıdır. İnsanlarda veya hayvanlarda kullanılmamalıdır.
Hacim: 5 ml
Saklama: +2°C ila +8°C
Sterilite: Steril filtrelenmiş
İnsan Rekombinant İnsülin Çözeltisi, Çin Hamster Yumurtalık (CHO) hücreleri dahil olmak üzere memeli hücre hatlarının kültivasyonunda yaygın olarak kullanılan, kimyasal olarak tanımlanmış bir takviyedir. Bu hücre kültürü sınıfı çözelti, Saccharomyces cerevisiae'de eksprese edilen rekombinant insan insülini içerir ve araştırma uygulamalarında yüksek saflık ve tutarlı performans sağlar.
Uygulama ve Avantajlar
İnsülin, hücre büyümesini ve üretkenliğini teşvik etmek için rutin olarak serumsuz ve kimyasal olarak tanımlanmış besiyerlerine eklenir. Önemli bir düzenleyici hormon olan insülin, glikoz, amino asitler ve yağ asitlerinin hücre tarafından alınmasını, kullanılmasını ve depolanmasını destekler. Ayrıca glikojen, proteinler ve lipitlerin parçalanmasını engeller, böylece kültür sistemlerinde hücre canlılığının ve metabolik stabilitenin iyileştirilmesine katkıda bulunur. Kimyasal olarak tanımlanmış formülasyon, hassas hücre kültürü iş akışlarında tekrarlanabilirliği destekler ve değişkenliği en aza indirir.
Biyolojik Özellikler ve Kullanım
İnsülin, pankreas adacıklarının β hücreleri tarafından doğal olarak üretilen iki zincirli bir polipeptit hormondur. Moleküler ağırlığı yaklaşık 5.800 Da'dır. α ve β zincirleri, iki zincirler arası disülfid bağı ile birbirine bağlanmıştır ve α zinciri, bir zincir içi disülfid bağı içerir. Hücre kültürü uygulamaları için, stabilite ve performansı korumak amacıyla çözelti aseptik koşullar altında kullanılmalı ve +2°C ile +8°C arasında saklanmalıdır.
Yalnızca araştırma amaçlıdır. Teşhis veya tedavi prosedürlerinde kullanılmamalıdır. İnsanlarda veya hayvanlarda kullanılmamalıdır.
Hacim: 100 ml
Saklama: +2°C ila +8°C
Sterilite: Steril filtrelenmiş
Sodyum Piruvat Çözeltisi (100 mM), hücre kültürü ortamları için ek, kolay erişilebilir bir enerji kaynağı sağlamak üzere tasarlanmış, steril, kullanıma hazır bir takviyedir. Sodyum piruvat, hücresel enerji metabolizmasında önemli bir rol oynar ve tümör hücreleri gibi metabolik olarak aktif ve hızla çoğalan hücrelerin büyümesini destekler. Takviye, hücre canlılığını artırabilir ve kültür sistemlerinde metabolik stabiliteyi korumaya yardımcı olabilir.
Uygulama ve Faydaları
Bu çözelti, piruvat ile ortamı zenginleştirmek ve optimal büyüme koşullarını desteklemek için rutin hücre kültüründe yaygın olarak kullanılır. ATP üretimini destekler, oksidatif stresi azaltmaya yardımcı olabilir ve kültürlenmiş hücrelerin metabolik performansının iyileştirilmesine katkıda bulunur. Hücre kültürü sınıfı su ile üretilen ve steril filtrelenmiş olan ürün, araştırma iş akışlarında tutarlı kalite ve tekrarlanabilirlik sağlar.
Kullanım ve Uyumluluk
Çoğu hücre kültürü uygulaması için önerilen nihai konsantrasyon, 100 mM stok çözeltisini 1:100 oranında tam kültür ortamında seyreltmek suretiyle elde edilen 1 mM sodyum piruvat'tır. Çözelti, çok çeşitli bazal ortamlar ve memeli hücre hatları ile uyumludur. Ürün stabilitesini korumak için +2°C ila +8°C arasında saklayın ve kontaminasyondan koruyun.
Yalnızca araştırma amaçlıdır. Teşhis veya tedavi prosedürlerinde kullanılmaz. İnsanlarda veya hayvanlarda kullanılmaz.
Hacim: 100 ml Depolama: ≤-15°C Sterilite: Steril filtrelenmiş
Antibiyotik/Antimikotik Solüsyon (100x), hücre kültürü ve ilgili laboratuvar uygulamalarında mikrobiyal kontaminasyon risklerini azaltmak için tasarlanmış steril, kullanıma hazır bir konsantredir. Bu 100x çözelti, Gram-pozitif ve Gram-negatif bakterilere, mayalara ve filamentli mantarlara karşı geniş spektrumlu antimikrobiyal aktivite sağlayan iyi bilinen bir penisilin, streptomisin ve amfoterisin B kombinasyonu içerir. Formülasyon, ökaryotik hücre kültürlerinde, bakteriyel besiyerlerinde ve kontaminasyona duyarlı diğer sistemlerde kullanıma uygundur ve temiz ve tutarlı laboratuvar işlemlerini destekler.
Uygulama ve Faydaları Rutin araştırma protokolleri için optimize edilen bu çözüm, hücre kültürü iş akışlarında aseptik koşulları korumak için yaygın olarak kullanılmaktadır. Kontaminasyona duyarlı ortamlarda güvenilir performans sunarak araştırmacıların hücre sağlığından veya deneysel tekrarlanabilirlikten ödün vermeden mikrobiyal aşırı büyüme riskini azaltmalarına yardımcı olur. Steril filtreli formülasyon, ek çözündürme adımlarına olan ihtiyacı ortadan kaldırarak kolaylaştırılmış besiyeri hazırlığını destekler ve günlük laboratuvar prosedürlerindeki değişkenliği azaltır.
Kullanım ve Uyumluluk Standart çalışma konsantrasyonları elde etmek için çözeltiyi 1:100 oranında tam kültür ortamınızda seyreltin. Ürün çok çeşitli memeli hücre hatları ve bazal besiyerleri ile uyumludur. Tutarlı stok mevcudiyeti sayesinde araştırmacılar güvenilir tedarik sürekliliğinden ve basitleştirilmiş lojistik planlamasından faydalanır. Çözelti ≤ -15 °C'de saklanmalı ve stabiliteyi korumak için tekrarlanan dondurma-çözme döngülerinden korunmalıdır. Yalnızca araştırma amaçlı kullanım içindir. Tanısal veya terapötik prosedürlerde kullanım için değildir. İnsanlarda veya hayvanlarda kullanım için değildir.
Hacim: 100 ml Depolama: +2°C ila +8°C Sterilite: Steril filtreli
MEM Esansiyel Olmayan Amino Asitler (100x), memeli hücre kültürü sistemlerinde hücre büyümesini ve canlılığını artırmak için tasarlanmış steril bir takviyedir. Formülasyon, standart Minimum Essential Medium'da (MEM) bulunan esansiyel olmayan amino asitlerin 100 kat konsantresine karşılık gelir ve minimum hazırlık ile bazal ortamın doğrudan takviye edilmesine olanak tanır.
Uygulama ve Faydaları Bu takviye, hızla çoğalan hücreler veya esansiyel olmayan amino asitleri de novo sentezleme kapasitesini kaybetmiş hücre hatları için ek bir amino asit havuzu sağlar. Biyosentezin metabolik yükünü hafifleterek, özellikle besin maddelerine duyarlı veya yüksek yoğunluklu kültürlerde gelişmiş büyüme kinetiğini, uzun süreli canlılığı ve daha fazla deneysel tutarlılığı destekler.
Bileşimi ve Kullanımı Çözelti glisin, L-alanin, L-asparajin, L-aspartik asit, L-glutamik asit, L-prolin ve L-serin içerir. MEM ve diğer standart ortamların çoğu ile uyumludur. Kullanmak için, nihai kültür ortamına 1:100 oranında seyreltin. Bu ürün steril olarak filtrelenmiştir ve ek işlem adımları olmadan kullanıma hazırdır. Sadece araştırma amaçlı kullanım içindir. Tanısal veya terapötik prosedürlerde kullanım için değildir. İnsanlarda veya hayvanlarda kullanım için değildir.
Accutase, yapışkan memeli hücrelerini standart doku kültürü plastik kaplarından ve yapışma kaplı yüzeylerden ayırmak için tripsin/EDTA'ya nazik bir alternatif olarak tasarlanmış, kullanıma hazır, steril filtrelenmiş bir hücre ayırma çözeltisidir. Dengeli bir tuz çözeltisi içinde proteolitik ve kollajenolitik enzim aktivitesini birleştirerek etkili ancak kontrollü bir ayrışma sağlar, hücre yüzeyi proteinlerini korur ve yüksek pasaj sonrası canlılık ve hızlı yeniden yapışmayı destekler.
Accutase formülasyonu, görsel pH göstergesi olarak EDTA ve fenol kırmızısı içeren Dulbecco fosfat tamponlu salin (DPBS) bazlıdır. Enzimler memeli ve bakteriyel kökenli değildir, bu da Accutase'i kök hücre araştırmaları, aşı iş akışları ve hayvan veya mikrobiyal kaynaklı kontaminantların en aza indirilmesi gereken tüm uygulamalar için özellikle uygun hale getirir. Çözelti 37 °C'de kendiliğinden inhibe olur, bu nedenle ayrılma işleminden sonra nötralize edici reaktif veya serum içeren ortam gerekmez – hücreler doğrudan taze ortama aktarılabilir.
Temel Özellikler
Kullanıma hazır 1x steril filtrelenmiş sıvı – seyreltme veya sulandırma gerekmez
Nazik ayrışma için birleşik proteolitik ve kollajenolitik enzim aktivitesi
Partiler arası tutarlılık için her parti, tanımlanmış bir ayrışma aktivitesine göre standartlaştırılmıştır
Memeli ve bakteri kaynaklı olmayan enzim
37 °C'de kendiliğinden inhibe olur – nötralize edici çözeltiye gerek yoktur
EDTA içeren Dulbecco’s PBS içinde formüle edilmiştir
Görsel pH göstergesi olarak fenol kırmızısı içerir
pH 6,8 – 7,8
Tipik Uygulamalar
Accutase, insan embriyonik kök hücreleri (hESC'ler), insan indüklenmiş pluripotent kök hücreleri (iPSC'ler), nöral kök hücreler, birincil nöronlar ve HeLa, HEK 293, CHO, MDCK, Vero, NIH/3T3, BHK-21 ve A549 gibi rutin olarak kültürlenen yapışkan hücre hatları dahil olmak üzere çok çeşitli yapışkan ve hassas hücre tiplerini nazikçe ayrıştırır. Tipik kullanım örnekleri şunlardır:
Yapışkan memeli hücrelerinin rutin alt kültürü ve pasajlanması
hESC'lerin, iPSC'lerin ve diğer hassas hatların nazik tek hücre ayrıştırması
Akış sitometrisi ve FACS analizi için numune hazırlığı
Epitop bütünlüğünün önemli olduğu hücre yüzeyi belirteçlerinin analizi
Hücre göçü, proliferasyon ve apoptoz testleri
Serum açlığı ve onkogen transfeksiyon çalışmaları ile durgunluk testleri
Tümör hücresi ve nöral kret hücresi göç testleri
Biyoreaktör iş akışlarında üretim ölçeğinin büyütülmesi
Rutin çalışmalar için, 75 cm2 kültür yüzeyi başına yaklaşık 10 ml Accutase uygulayın ve oda sıcaklığında 5–10 dakika inkübe edin. Optimum inkübasyon süresi her hücre hattı için ayrı ayrı belirlenmelidir ve bir saati geçmemelidir. İlave etmeden önce, kalıntı serum ve iki değerlikli katyonları gidermek için hücre tabakasını kalsiyum ve magnezyum içermeyen DPBS gibi Ca2+/Mg2+ içermeyen bir tuz çözeltisiyle durulayın.
Kullanım ve Saklama
Açılmamış şişeyi -15 °C veya altında dondurulmuş olarak saklayın. Oda sıcaklığında veya +2 °C ile +8 °C arasında bir gece boyunca çözdürün. Yüksek sıcaklıklar enzim aktivitesini azalttığından, Accutase'i 37 °C'lik su banyosunda çözdürmeyin. Çözdürme işleminden sonra, çözelti +2 °C ile +8 °C arasında 2 aya kadar saklanabilir; oda sıcaklığında saklamayın. Uygulamadan önce reaktifi 37 °C'ye önceden ısıtmayın – oda sıcaklığında yıkanmış hücrelere doğrudan ekleyin. Uzun süreli raf ömrü için, tekrarlanan çözme döngülerinden kaçınmak amacıyla tek kullanımlık alıkoyma önerilir. Her zaman aseptik koşullar altında çalışın.
Kalite
Sıkı kalite standartları altında üretilmiştir. Accutase'in her partisi, partiden partiye tutarlı ve tekrarlanabilir performans sağlamak için steril filtreden geçirilir ve sterilite, pH, görünüm ve ayrışma aktivitesi açısından test edilir.
Ürün Özellikleri
Özellik
Ayrıntı
Ürün türüHücre ayrıştırma / disosiyasyon reaktifi
BiçimSteril filtrelenmiş sıvı, kullanıma hazır
Hacim100 ml
Çalışma konsantrasyonu1x (kullanıma hazır)
Enzim aktivitesiKombine proteolitik ve kollajenolitik
Enzim kaynağıMemeli ve bakteri kaynaklı olmayan
Tampon sistemiEDTA içeren Dulbecco’s PBS
pH göstergesiFenol kırmızısı
pH aralığı6,8 – 7,8
GörünümBerrak, soluk kırmızı ila turuncu renkli çözelti
Saklama sıcaklığı-15 °C veya altında
Çözüldükten sonra stabilite+2 °C ila +8 °C arasında 2 aya kadar
Önerilen kullanım hacmi75 cm2 kültür yüzeyi başına ~10 ml
Tipik inkübasyon süresiOda sıcaklığında 5 – 10 dakika
Nakliye koşullarıKuru buzda dondurulmuş
Kullanım amacıYalnızca araştırma amaçlı ve ileri üretim için
Formülasyon (Litre Başına Bileşim)
Bileşen
Konsantrasyon (mg/L)
İnorganik Tuzlar
Sodyum klorür (NaCl)8000,00
Disodyum hidrojen fosfat (Na2HPO4)1150,00
Potasyum klorür (KCl)200,00
Potasyum dihidrojen fosfat (KH2PO4)200,00
Diğer Bileşenler
EDTA · 4Na (tetrasodyum EDTA)220,00
Fenol kırmızısı3,00
Özel enzim karışımı (proteolitik ve kollajenolitik aktivite)1x
Accutase, Innovative Cell Technologies, Inc. şirketinin tescilli ticari markasıdır.
Kullanıma hazır, steril filtrelenmiş bu sıvı formülasyon, Earle’s Balanced Salt Solution (EBSS), 2 mM L-glutamin, D-glukoz (1,0 g/L) ve 2,2 g/L sodyum bikarbonat (NaHCO3) ile takviye edilmiştir, bu da onu CO2 kontrollü inkübatör atmosferinde (tipik olarak %5 CO2). İçerdiği fenol kırmızısı, pH göstergesi görevi görerek hücre kültürü sırasında besiyeri durumunun kolayca görsel olarak izlenmesini sağlar.
Temel Özellikler
Earle’s Dengeli Tuz Çözeltisi (EBSS) içeren klasik Eagle’s MEM formülasyonu
2 mM L-glutamin içerir – hemen kullanıma hazırdır
2,2 g/L sodyum bikarbonat – %5 CO2 inkübasyonu için tamponlanmıştır
Birincil karbon kaynağı olarak D-glukoz (1,0 g/L) içerir
pH göstergesi olarak fenol kırmızısı içerir
HEPES ve sodyum piruvat içermez
Steril filtrelenmiş sıvı besiyeri, kullanıma hazır
pH 7,0 – 7,6
Tipik Uygulamalar
EMEM, HeLa, HEK 293, Vero, MRC-5, L-929, BHK-21 ve birçok birincil hücre dahil olmak üzere çok çeşitli memeli hücre hatlarının kültürlenmesini destekler. Yaygın uygulamalar şunlardır:
Yapışkan hücre hatlarının rutin bakımı ve çoğaltılması
Virüs çoğaltma ve aşı üretimi iş akışları
Sitotoksisite ve biyoanaliz uygulamaları
Transfeksiyon ve protein ekspresyonu çalışmaları
Hücre biyolojisi ve moleküler biyoloji alanındaki temel araştırmalar
Optimum hücre büyümesi için EMEM'e tipik olarak %5–10 fetal sığır serumu (FBS) ve hücre hattına bağlı olarak esansiyel olmayan amino asitler (NEAA) ve penisilin/streptomisin gibi antibiyotikler eklenir.
Kullanım ve Saklama
Açılmamış şişeyi +2 °C ila +8 °C arasında, ışıktan korunarak saklayın. Açıldıktan sonra aseptik koşullar altında kullanın. Çözeltideki L-glutamin kademeli olarak bozulmaya maruz kalır – en iyi performans için açıldıktan sonra 4 hafta içinde kullanmanızı veya daha uzun süre saklanacaksa kullanımdan önce taze L-glutamin ilave etmenizi öneririz. Hücrelere eklemeden önce besiyerinin 37 °C'ye ısınmasını bekleyin.
Kalite
Sıkı kalite standartları altında üretilmiştir. Hücre kültürü uygulamalarında tutarlı performans sağlamak için her parti sterillik, pH, osmolalite ve endotoksin seviyeleri açısından test edilir.
Ürün Özellikleri
Özellik
Ayrıntı
Ürün türüMEM
Ürün kategorisiHücre kültürü besiyeri
BiçimSıvı
SterilEvet
Boyut500 ml
L-GlutaminL-glutamin (2 mM) içerir
GlikozGlikoz içerir (1,0 g/L)
Sodyum bikarbonatNaHCO3 (2,2 g/L) ile
HEPESHEPES içermez
Sodyum piruvatSodyum piruvat içermez
Fenol kırmızısıFenol kırmızısı ile
Tuz çözeltisiEarle’s Dengeli Tuz Çözeltisi (EBSS)
pH7,0 – 7,6
Endotoksin içeriğiBelirtilmemiştir
Saklama+2 °C ila +8 °C
Formülasyon (Litre Başına Bileşim)
Bileşen
Konsantrasyon (mg/L)
İnorganik Tuzlar
Kalsiyum klorür · 2H2O265,00
Magnezyum sülfat97,72
Potasyum klorür400,00
Sodyum klorür6.800,00
Sodyum dihidrojen fosfat, susuz122,00
Sodyum bikarbonat (NaHCO3)2.200,00
Amino Asitler
L-Arginin · HCl126,00
L-Sistin · 2HCl31,30
L-Glutamin292,00
L-Histidin · HCl · H2O42,00
L-İzolösin52,00
L-Lösin52,00
L-Lizin · HCl72,50
L-Metiyonin15,00
L-Fenilalanin32,00
L-Treonin48,00
L-Triptofan10,00
L-Tirozin · 2Na · 2H2O51,90
L-Valin46,00
Vitaminler
D-Kalsiyum pantotenat1,00
Kolin klorür1,00
Folik asit1,00
Miyo-inositol2,00
Nikotinamid1,00
Piridoksal · HCl1,00
Riboflavin0,10
Tiamin · HCl1,00
Diğer Bileşenler
D(+)-Glikoz1.000,00
Fenol kırmızısı10,00
Freeze Medium CM-1'in temel özellikleri şunlardır:
Geniş Uyumluluk: Birincil hücreler, kök hücreler ve yerleşik hücre hatları dahil olmak üzere çok çeşitli hücre tipleri için etkilidir.
Yüksek Canlılık: Çözülme sonrası hücre iyileşmesini ve canlılığını en üst düzeye çıkarmak için optimize edilmiş olup güvenilir deneysel sonuçlar sağlar.
Kullanıma Hazır: Hemen uygulama için uygun şekilde hazırlanır ve sterilize edilir, hazırlık süresini ve kontaminasyon riskini azaltır.
Geliştirilmiş Stabilite: Standart kriyoprezervasyon koşulları altında tutarlı performansı koruyarak tekrarlanabilir sonuçlar sağlar.
Uzun Raf Ömrü: CM-1, buzdolabında bir yıla kadar saklanabilen, serum içeren, kullanıma hazır bir kriyoprezervasyon ortamıdır.
Hücreleri Dondurmak için CM-1 Kullanımı
CM-1'i hem yapışık hem de süspansiyon hücrelerini dondurmak için kullanmak üzere aşağıdaki adımları izleyin
Yapışık hücreler için hücreleri yıkayın ve kültür substratından ayırın. Süspansiyon hücreleri için doğrudan bir sonraki adıma geçin.
Uygun konsantrasyonda olduklarından emin olmak için hücreleri sayın.
Hücreleri santrifüjleyerek peletleyin, ardından CM-1 dondurma ortamında yeniden süspanse edin.
Yeniden süspanse edilen hücreleri kriyoviyallere aktarın.
Hücreleri uzun süreli depolamaya aktarmadan önce yavaş dondurma yöntemi kullanın
Yöntem
Açıklama
Adımlar
❄️
Manuel Dondurma
Hücre canlılığını sağlamak için kademeli sıcaklık düşüşünü içeren adım adım bir yöntem
1️⃣ Hücreleri 40 dakika boyunca 4°C dondurucuda dondurma ortamına yerleştirin.
2️⃣ 24 saat boyunca -80°C dondurucuya aktarın.
3️⃣ Uzun süreli koruma için hücreleri sıvı nitrojen içinde saklayın
❄️
Bay Frosty'yi Kullanmak
Elektrik gücü olmadan kontrollü dondurma oranlarına izin veren kullanışlı bir cihaz
1️⃣ Hücreleri dondurma ortamı ile kriyoviyallerde hazırlayın.
2️⃣ Kriyoviyalleri Mr. Frosty kabına yerleştirin.
3️⃣ Sıvı nitrojene aktarmadan önce -80°C'de 24 saat saklayın
❄️
Kontrollü Fiyatlı Dondurucu
Thermo Fisher veya diğer üreticiler tarafından kontrollü sıcaklık düşürme için tasarlanmış yüksek hassasiyetli bir dondurucu
1️⃣ Cihazı sıcaklığı kademeli olarak düşürecek şekilde programlayın.
2️⃣ Hazırlanan hücreleri dondurucuya yerleştirin.
3️⃣ Dondurma döngüsünden sonra hücreleri sıvı nitrojene aktarın
Kriyoviyalleri -130°C'nin altındaki sıcaklıklarda veya uzun süreli muhafaza için sıvı nitrojen içinde saklayın.
İçindekiler
FBS, DMSO, Glikoz, Tuzlar içerir
Tamponlama kapasitesi: pH = 7,2 ila 7,6
Cytion Freeze Medium CM-1, kriyoprezervasyon için güvenilir bir çözüm sunarak çok çeşitli araştırma uygulamaları için çözülme sonrası yüksek hücre canlılığı ve işlevselliği sağlar.
Ham's F-12K (Kaighn's) Medium, hücre kültürü koşullarını optimize etmek için özenle formüle edilmiştir. Amino asitler ve sodyum piruvat gibi temel bileşenlerin yanı sıra putresin, timidin, hipoksantin ve çinko gibi ek elementlerin yüksek seviyelerini sağlayan zenginleştirilmiş bir bileşime sahiptir. Bu eklemeler, araştırmacıların besiyerini minimal serumla veya belirli hücre tipleri için tanımlanmış bileşenlerle desteklemesini sağlayarak hassas deneysel koşulları kolaylaştırır.
Özellikle, Ham's F-12K (Kaighn's) Medium protein veya büyüme faktörü içermez. Sonuç olarak, büyüme faktörleri ve Fetal Sığır Serumu (FBS) ile takviye genellikle gereklidir, bu da araştırmacıların ortamı kendi spesifik hücre hatlarının gereksinimlerine göre uyarlamasına olanak tanır. Optimum performans için, FBS konsantrasyonu her hücre hattı için dikkatlice optimize edilmeli, böylece optimum büyüme ve işlevsellik sağlanmalıdır.
Fizyolojik pH'ı korumak için Ham's F-12K (Kaighn's) Medium, bir sodyum bikarbonat tampon sistemi (2,5 g/L) kullanır ve ekim sırasında kontrollü bir %5-10 CO2 ortamı gerektirir. Bu, ortamın pH değerinin hücre büyümesi ve canlılığı için ideal aralıkta kalmasını sağlar
Kalite kontrol
20-25°C'de pH = 7,2 +/
- 0,02.
Her parti sterilite ve mikoplazma ve bakteri yokluğu açısından test edilmiştir.
Bakım
2°C ila +8°C arasında karanlıkta buzdolabında saklayın. Dondurma ve +37°C'ye kadar ısıtma ürünün kalitesini en aza indirir.
Besiyerini 37°C'den fazla ısıtmayın veya kontrol edilemeyen ısı kaynakları (örn. mikrodalga cihazlar) kullanmayın.
Besiyerinin sadece bir kısmı kullanılacaksa, bu miktarı şişeden çıkarın ve oda sıcaklığında ısıtın.
Temel besiyeri hariç tüm besiyerlerinin raf ömrü üretim tarihinden itibaren 8 haftadır.
Kompozisyon
Bileşenler
mg/L
İnorganik Tuzlar
Kalsiyum klorür x 2H2O
135,24
Bakır(II) sülfat x 5H2O
0,00
Demir (II) sülfat x 7H2O
0,83
Magnezyum klorür x 6H2O
105,72
Magnezyum sülfat x 7H2O
394,49
Potasyum klorür
283,29
Potasyum dihidrojen fosfat
58,52
Sodyum klorür
7597,20
di-Sodyum hidrojen fosfatsusuz
115,02
Çinko sülfat x 7H2O
0,14
Diğer Bileşenler
D(+)-Glikoz susuz
1260,00
Hipoksantin
4,08
DL-α-Lipoik asit
0,21
Fenol kırmızısı
3,00
Putresin x 2HCl
0,32
Sodyum piruvat
220,00
NaHCO3
2500,00
Timidin
0,73
Amino Asitler
L-Alanin
17,82
L-Arginin x HCl
421,40
L-Asparagin x H2O
30,02
L-Aspartik asit
26,62
L-Sistein x HCl x H2O
70,24
L-Glutamin
292,20
L-Glutamik asit
29,42
Glisin
15,01
L-Histidin x HCl x H2O
41,92
L-İzolösin
7,87
L-Lösin
26,24
L-Lizin x HCl
73,04
L-Metiyonin
8,95
L-Fenilalanin
9,91
L-Proline
69,06
L-Serin
21,02
L-Threonine
23,82
L-Triptofan
4,08
L-Tirozin
10,87
L-Valine
23,42
Vitaminler
D(+)-Biyotin
0,07
D-Kalsiyum pantotenat
0,48
Kolin klorür
13,96
Folik asit
1,32
miyo-İnositol
18,02
Nikotinamid
0,04
Piridoksin x HCl
0,06
Riboflavin
0,04
Tiamin x HCl
0,34
B12 Vitamini
1,36
Fosfat tamponlu salin (PBS) biyolojik ve kimyasal araştırmalarda yaygın olarak kullanılan bir tampon çözeltisidir. Doku işleme ve hücre kültürü dahil olmak üzere çeşitli deneysel prosedürler sırasında pH dengesinin ve ozmolaritenin korunmasında çok önemli bir rol oynar. PBS çözeltimiz, her deneyde stabilite ve güvenilirlik sağlamak için yüksek saflıkta bileşenlerle titizlikle formüle edilmiştir. PBS'mizin ozmolaritesi ve iyon konsantrasyonları insan vücudundakileri yakından taklit eder, bu da onu izotonik ve çoğu hücre için toksik olmayan hale getirir.
PBS Solüsyonumuzun Bileşimi
PBS çözeltimiz, ultra saf dereceli fosfat tamponları ve tuzlu su çözeltilerinin pH ayarlı bir karışımıdır. 1X çalışma konsantrasyonunda şunları içerir:
8000 mg/L Sodyum klorür (NaCl)
200 mg/L Potasyum klorür (KCl)
1150 mg/L Sodyum fosfat dibazik susuz (Na2HPO4)
200 mg/L Potasyum fosfat monobazik susuz (KH2PO4)
Bu bileşim, çok çeşitli biyolojik uygulamalar için uygun optimum pH ve iyonik denge sağlar.
PBS Çözeltimizin Uygulamaları
PBS solüsyonumuz biyolojik araştırmalarda çeşitli uygulamalar için idealdir. İzotonik ve toksik olmayan özellikleri onu madde seyreltme ve hücre kabı durulama için uygun hale getirir. EDTA içeren PBS çözeltileri bağlı ve kümelenmiş hücrelerin ayrılması için etkilidir. Ancak, çinko gibi iki değerlikli metaller çökelmeye neden olabileceğinden PBS'ye eklenmemelidir. Bu gibi durumlarda Good's tamponları tavsiye edilir. Ayrıca, PBS solüsyonumuz SARS-CoV-2 dahil olmak üzere RNA virüslerinin taşınması ve saklanması için viral taşıma ortamına kabul edilebilir bir alternatiftir.
Kalite Kontrol
Steril filtreli
Depolama ve Raf Ömrü
2°C ila +25°C arasında, ışıktan koruyarak saklayın.
Açıldıktan sonra 2°C ila 25°C'de saklayın ve 24 ay içinde kullanın.
Nakliye Koşulları
Ortam sıcaklığı
Bakım
2°C ila +8°C arasında karanlıkta buzdolabında saklayın. Ürün kalitesini düşürdüğü için dondurmaktan ve sık sık +37°C'ye kadar ısıtmaktan kaçının.
Besiyerini 37°C'nin üzerinde ısıtmayın veya mikrodalga fırın gibi kontrolsüz ısı kaynakları kullanmayın.
Ortamın sadece bir kısmı kullanılacaksa, gerekli miktarı çıkarın ve kullanmadan önce oda sıcaklığına kadar ısıtın.
Kompozisyon
Kategori
Bileşenler
Konsantrasyon (mg/L)
Tuzlar
Potasyum klorür
200
Potasyum fosfat monobazik susuz
200
Sodyum klorür
8000
Sodyum fosfat dibazik susuz
1150
Başlangıçta hem süspansiyon hem de tek tabakalı kültürlerde insan lösemik hücrelerinin büyümesini desteklemek için tasarlanan RPMI 1640 Besiyeri, araştırmacılar ve ticari tedarikçiler tarafından yapılan modifikasyonlarla çok çeşitli memeli hücreleri için uygun hale gelmiştir. HeLa, Jurkat, MCF-7, PC12, PBMC, astrositler ve karsinomlar gibi hücre hatlarıyla son derece uyumludur.
RPMI 1640 Medium, benzersiz bileşimi nedeniyle diğer hücre kültürü ortamlarından ayrılır. Önemli miktarda fosfat, amino asit ve vitamin içerir. Özellikle, Eagle's Minimal Essential Medium veya Dulbecco's Modified Eagle Medium'da bulunmayan biyotin, B12 vitamini ve PABA içerir. Ayrıca, RPMI 1640 Medium önemli ölçüde yüksek konsantrasyonlarda inositol ve kolin vitaminleri sergiler. Ancak protein, lipid veya büyüme faktörü içermez. Sonuç olarak, hücre büyümesi için en uygun koşulları sağlamak üzere genellikle %10 Fetal Sığır Serumu (FBS) ile takviye gereklidir.
RPMI 1640 Medium'un tamponlama sistemi sodyum bikarbonata dayanır ve fizyolojik olarak uygun bir pH'ı korumak için %5-10 CO2 ortamı gerektirir. İndirgeyici ajan glutatyonun dahil edilmesi, bu ortamı diğerlerinden daha da ayırır.
Kalite Kontrol
Steril filtreli
Depolama ve Raf Ömrü
2°C ila +8°C arasında, ışıktan koruyarak saklayın.
Açıldıktan sonra 4°C'de saklayın ve 6-8 hafta içinde kullanın.
Nakliye Koşulları
Ortam sıcaklığı
Bakım
2°C ila +8°C arasında karanlıkta buzdolabında saklayın. Ürün kalitesini düşürdüğü için dondurmaktan ve sık sık +37°C'ye kadar ısıtmaktan kaçının.
Besiyerini 37°C'nin üzerinde ısıtmayın veya mikrodalga cihazlar gibi kontrolsüz ısı kaynakları kullanmayın.
Ortamın sadece bir kısmı kullanılacaksa, gerekli miktarı çıkarın ve kullanmadan önce oda sıcaklığına kadar ısıtın.
Kompozisyon
Kategori
Bileşenler
Konsantrasyon (mg/L)
Amino Asitler
Glisin
10.00
L-Alanil-L-Glutamin
434.40
L-Arginin
200.00
L-AsparaginH2O
56.82
L-Aspartik Asit
20.00
L-Sistin 2HCl
65.20
L-Glutamik Asit
20.00
L-Histidin HClH2O
20.27
L-Hidroksi-L-Prolin
20.00
L-İzolösin
50.00
L-Lösin
50.00
L-Lizin HCl
40.00
L-Metiyonin
15.00
L-Fenilalanin
15.00
L-Proline
20.00
L-Serin
30.00
L-Threonine
20.00
L-Triptofan
5.00
L-Tirozin 2Na 2H2O
28.83
L-Valine
20.00
Vitaminler
p-Amino Benzoik Asit
1.00
D-Biotin
0.20
Kolin Klorür
3.00
D-Kalsiyum Pantotenat
0.25
Folik Asit
1.00
miyo-İnositol
35.00
Nikotinamid
1.00
Piridoksin HCl
1.00
Riboflavin
0.20
Tiamin HCl
1.00
B12 Vitamini
0.005
İnorganik Tuzlar
Ca(NO3)2 4H2O
100.00
KCl
400.00
MgSO4 7H2O
100.00
NaCl
6000.00
NaHCO3
2000.00
Na2HPO4
800.00
Diğer Bileşenler
D-Glikoz
2000.00
İndirgenmiş L-Glutatyon
1.00
Fenol Kırmızı Sodyum Tuzu
5.30
Bu benzersiz formülasyon, Dulbecco'nun Modifiye Eagle Ortamı (DMEM) ile Ham's F-12'yi (Ham's Besin Karışımı F-12) tam olarak 1:1 oranında birleştirir. L-glutamin ilavesi, bileşimini daha da güçlendirir.
Eagle's Minimal Essential Medium (EMEM) kaynaklı DMEM, önceki versiyonuna kıyasla daha yüksek konsantrasyonda amino asit ve vitamin sunar. Buna karşılık, Ham's F-12, Ham's F-10 besiyerine dayanır ve tamamlayıcı bir dizi temel bileşen sağlar.
Optimal hücre büyümesini desteklemek için, DMEM:Ham's F12'ye tipik olarak %5-10 konsantrasyonda FBS ilave edilmesi yaygın bir uygulamadır. Ortada hücresel gelişim için hayati önem taşıyan büyüme hormonları, lipitler ve proteinler bulunmadığından bu ilave gereklidir.
DMEM:Ham's F12, bir pH tampon sistemi içerir ve genellikle bir pH göstergesi olan fenol kırmızısı ile takviye edilir. DMEM:Ham's F12'de veya bikarbonat tampon sistemini kullanan herhangi bir ortamda kültürlenen hücreler, uygun pH seviyelerini korumak için %5-10 oranında kontrollü bir CO2 ortamına ihtiyaç duyar.
Kalite Kontrol
Steril filtrelenmiş
Saklama ve Raf Ömrü
Işıktan korunarak +2°C ila +8°C arasında saklayın.
Açıldıktan sonra 4°C'de saklayın ve 6–8 hafta içinde kullanın.
Nakliye Koşulları
Ortam sıcaklığı
Saklama
Karanlık bir ortamda +2°C ile +8°C arasında buzdolabında saklayın. Ürün kalitesini düşürdüğü için donmasını ve sık sık +37°C'ye ısıtılmasını önleyin.
Ortamı 37°C'nin üzerine ısıtmayın veya mikrodalga fırın gibi kontrolsüz ısı kaynakları kullanmayın.
Ortamın sadece bir kısmı kullanılacaksa, gerekli miktarı çıkarın ve kullanmadan önce oda sıcaklığına ısıtın.
Bileşim
Kategori
Bileşenler
Konsantrasyon (mg/L)
Amino Asitler
Glisin
18,75
L-alanin
4,45
L-Arginin HCl
147,50
L-Asparagin H₂O
7,50
L-Aspartik Asit
6,65
L-Sistein HCl H₂O
17,56
L-Sistin 2 HCl
31,29
L-Glutamik Asit
7,35
L-Glutamin
365,00
L-Histidin HCl H₂O
31,48
L-İzolösin
54,47
L-Lösin
59,05
L-Lizin HCl
91,25
L-Metiyonin
17,24
L-Fenilalanin
35,48
L-Prolin
17,25
L-Serin
26,25
L-Treonin
53,45
L-Triptofan
9,02
L-Tirozin 2 Na 2 H2O
55,79
L-Valin
52,85
Vitaminler
D-Biotin
0,0035
Kolin Klorür
8,98
D-Kalsiyum Pantotenat
2,24
Folik Asit
2,66
Miyo-inositol
12,60
Nikotinamid
2,02
Piridoksin HCl
0,031
Piridoksal HCl
2,00
Riboflavin
0,219
Tiamin HCl
2,17
B12 vitamini
0,68
İnorganik Tuzlar
CaCl2 2 H2O
154,50
CuSO4 5 H2O
0,0013
Fe(NO3)3 9 H2O
0,05
FeSO4 7 H2O
0,417
KCl
311,80
MgCl2 6 H2O
61,20
MgSO4 7 H2O
100,00
NaCl
6996,00
NaHCO3
1200,00
Na2HPO4
71,02
NaH2PO4 2 H2O
70,87
ZnSO4 7 H2O
0,432
Diğer Bileşenler
D-Glikoz
3151,00
Hipoksantin
2,40
HEPES
3574,50
Linoleik Asit
0,042
Lipoik Asit
0,105
Fenol Kırmızısı Sodyum Tuzu
8,63
Putresin 2 HCl
0,081
Sodyum Piruvat
55,00
Timidin
0,365
- 0,02, 20-25 °C'de. Her parti sterillik ve mikoplazma ve bakteri bulunmadığı konusunda test edilmiştir. Saklama Karanlıkta +2°C ila +8°C arasında buzdolabında saklayın. Dondurma ve +37°C'ye kadar ısıtma, ürünün kalitesini en aza indirir. Ortamı 37°C'nin üzerine ısıtmayın veya kontrol edilemeyen ısı kaynakları (örn. mikrodalga fırınlar) kullanmayın. Ortamın sadece bir kısmı kullanılacaksa, bu miktarı şişeden çıkarın ve oda sıcaklığında ısıtın. Temel besiyeri hariç tüm besiyerlerinin raf ömrü, açılma tarihinden itibaren 6 ila 8 haftadır. Bileşim Bileşenler mg/L İnorganik TuzlarKalsiyum klorür x 2H2O132,00 Magnezyum sülfat97,67 Potasyum klorür400 Sodyum klorür6.460 Disodyum hidrojen fosfat (susuz)504,00 Diğer BileşenlerD(+)-Glikoz (susuz)3.000 Glutatyon (indirgenmiş)0 Et Peptonu600 Fenol kırmızısı sodyum tuzu11 Amino AsitlerL-Alanin13 L-Arginin x HCl42,1 L-Asparagin x H2O45,03 L-Aspartik asit19,97 L-Sistein x HCl x H2O31,75 L-Glutamin (kararlı)21 L-Glutamik asit22 Glisin7,51 L-Histidin x HCl x H2O20,96 L-Hidroksiprolin19,67 L-İzolösin39,3 L-Lösin39,36 L-Lizin x HCl36,54 L-Metiyonin14,92 L-Fenilalanin16,52 L-Prolin17,27 L-Serin26,28 L-Treonin17,87 L-Triptofan3,06 L-Tirozin disodyum tuzu26,10 L-Valin17,57 Vitaminlerp-Aminobenzoik asit1 Askorbik asit0,56 D(+)-Biotin0 D-Kalsiyum pantotenat0,2 Kolin klorür5 Folik asit10 Miyo-inositol36 Nikotinamid0,5 Nikotinik asit0 Piridoksal HCl0,5 Piridoksin HCl0,5 Riboflavin0 Tiamin HCl0 B12 vitamini2
Medium 199 bu alanda bir dizi uygulama sunmaktadır. Kümülüs-oosit kompleksini (COC) etkili bir şekilde muhafaza edebilir ve oositlerin in vitro olgunlaşmasını destekleyebilir. Ayrıca, Alman Holstein ineklerinden ovum toplanması sırasında aspirasyon hatlarının durulanmasında kullanılır. Ayrıca, Medium 199 sıçanlardan elde edilen kardiyak endotelyal hücrelerin kültürü için mükemmel bir ortam görevi görmektedir. Bu uygulamalar, Medium 199'un çok yönlülüğünü ve çeşitli deneysel ihtiyaçlara uyarlanabilirliğini göstermektedir.
Tarihçe
1950'lerde Medium 199'un geliştirilmesi doku kültürü ortamlarında önemli bir ilerlemeye işaret etmiştir. Bu ürünün piyasaya sürülmesinden önce, birçok kültür ortamı hayvan kaynaklı ürünlere ve doku özlerine dayanıyordu. Ancak Morgan ve meslektaşları hücre kültürleri için tamamen tanımlanmış bir besin kaynağı formüle ederek bu alanda devrim yarattı. Vitaminlerin, amino asitlerin ve diğer faktörlerin farklı kombinasyonlarını içeren deneyleri sayesinde, Medium 199'un olağanüstü büyümeyi teşvik edici özelliklerini keşfettiler.
Kalite kontrol
20-25°C'de pH = 7,2 +/
- 0,02.
Her parti sterilite ve mikoplazma ve bakteri yokluğu açısından test edilmiştir.
Bakım
2°C ila +8°C arasında karanlıkta buzdolabında saklayın. Dondurma ve +37° C'ye kadar ısıtma ürünün kalitesini en aza indirir.
Besiyerini 37° C'den daha fazla ısıtmayın veya kontrol edilemeyen ısı kaynakları (örn. mikrodalga cihazlar) kullanmayın.
Besiyerinin sadece bir kısmı kullanılacaksa, bu miktarı şişeden çıkarın ve oda sıcaklığında ısıtın.
Temel besiyeri dışındaki tüm besiyerlerinin raf ömrü üretim tarihinden itibaren 8 haftadır.
Kompozisyon
Bileşenler
mg/L
İnorganik Tuzlar
Kalsiyum klorür x 2H2O
264,92
Demir (III) nitrat x 9H2O
0,72
Magnezyum sülfat
97,67
Potasyum klorür
400,00
Sodyum asetat x 3H2O
82,95
Sodyum klorür
6,800.00
Sodyum dihidrojen fosfat x H2O
140,00
Diğer Bileşenler
Adenin sülfat
10,00
AMP
0,20
ATP
1,00
Kolesterol
0,20
2'-Deoksiriboz
0,50
D(+)-Glikoz susuz
1,000.00
Glutatyon (kırmızı)
0,05
Guanin x HCl
0,30
Hipoksantin
0,30
Fenol kırmızısı
10,00
D-Riboz
0,50
Timin
0,30
Tween 80
4,90
Urasil
0,30
Ksantin
0,30
NaHCO3
2,200.00
Amino Asitler
L-Alanin
25,00
L-Arginin x HCl
70,00
L-Aspartik asit
30,00
L-Sistein x HCl x H2O
0,10
L-Sistin
20,00
L-Glutamin stabil
149,00
L-Glutamik asit
67,00
Glisin
50,00
L-Histidin x HCl x H2O
21,88
L-Hidroksiprolin
10,00
L-İzolösin
20,00
L-Lösin
60,00
L-Lizin x HCl
70,00
L-Metiyonin
15,00
L-Fenilalanin
25,00
L-Proline
40,00
L-Serin
25,00
L-Threonine
30,00
L-Triptofan
10,00
L-Tirozin
40,00
L-Valine
25,00
Vitaminler
4-Amino benzoik asit
0,05
Askorbik asit
0,05
D(+)-Biyotin
0,01
Kalsiferol
0,10
D-Kalsiyum pantotenat
0,01
Kolin klorür
0,50
Folik asit
0,01
miyo-İnositol
0,05
Menadion
0,01
Nikotinik asit
0.025
Nikotinamid
0.025
Piridoksal x HCl
0.025
Piridoksol x HCl
0.025
Riboflavin
0,01
DL-α-Tokoferol fosfat disodyum tuzu
0,01
Tiamin x HCl
0,01
A Vitamini asetat
0,14
IMDM, Jurkat, COS-7 ve makrofaj hücreleri dahil olmak üzere hızla çoğalan, yüksek yoğunluklu hücre kültürleri için çok uygundur. Bir dizi hücre kültürü uygulaması için mevcut olan çeşitli IMDM modifikasyonları, ortam seçici aracı kullanılarak bulunabilir. Sıvı besiyerleri tüm hücre kültürü uygulamaları için gerekli besinleri sağlar. Yüksek kaliteli hücre kültürü ortamlarımızın her biri, kültür ortamının tutarlı performansı ve stabilitesi için gerekli olan ilk yayınlanan formüle veya modifikasyonlara göre üretilmektedir.
IMDM ve DMEM
IMDM ferrik nitrat yerine potasyum nitrat, HEPES ve sodyum piruvat içerir. IMDM'deki ek bileşenler onu özel hücre tipleri ve spesifik uygulamalar için DMEM'den daha uygun hale getirir.
IMDM vs RPMI
IMDM ve RPMI, PMA/iyonomisin stimülasyonu ile ilgili olabilecek farklı formülasyonlara sahiptir. Önemli bir fark Ca2+ konsantrasyonudur. RPMI 0,42 mM Ca2+ içerirken IMDM 1,49 mM içerir.
Kalite kontrol
20-25°C'de pH = 7,2 +/
- 0,02.
Her parti sterilite ve mikoplazma ve bakteri yokluğu açısından test edilmiştir.
Bakım
2°C ila +8°C arasında karanlıkta buzdolabında saklayın. Dondurma ve +37° C'ye kadar ısıtma ürünün kalitesini en aza indirir.
Besiyerini 37° C'den daha fazla ısıtmayın veya kontrol edilemeyen ısı kaynakları (örn. mikrodalga cihazlar) kullanmayın.
Besiyerinin sadece bir kısmı kullanılacaksa, bu miktarı şişeden çıkarın ve oda sıcaklığında ısıtın.
Temel besiyeri dışındaki tüm besiyerlerinin raf ömrü üretim tarihinden itibaren 8 haftadır.
Kompozisyon
Bileşenler
mg/L
İnorganik Tuzlar
Kalsiyum klorür x 2 H2O
219,00
Potasyum klorür
330,00
Potasyum nitrat
0.076
Magnezyum sülfat susuz
97,73
Sodyum klorür
4,505.00
Sodyum dihidrojen fosfat susuz
109,00
Sodyum selenit
0,02
Diğer Bileşenler
D(+)-Glikoz susuz
4,500.00
HEPES
5,958.00
Sodyum piruvat
110,00
Fenol kırmızısı
15,00
Amino Asitler
L-Alanin
25,00
L-Arginin x HCl
84,00
L-Asparagin x H2O
25,00
L-Aspartik asit
30,00
L-Sistin x 2HCl
91,24
L-Glutamin
584,00
L-Glutamik asit
75,00
Glisin
30,00
L-Histidin x HCl x H2O
42,00
L-İzolösin
104,80
L-Lösin
104,80
L-Lizin x HCl
146,20
L-Metiyonin
30,00
L-Fenilalanin
66,00
L-Proline
40,00
L-Serin
42,00
L-Threonine
95,20
L-Triptofan
16,00
L-Tirozin x 2Na
104,20
L-Valine
93,60
Vitaminler
D(+)-Biyotin
0.013
D-Kalsiyum pantotenat
4,00
Kolin klorür
4,00
Folik asit
4,00
miyo-İnositol
7,20
Hücre kültürü ortamı: Genel bir bakış
Yaşam bilimleri alanında en önemli metodolojilerden biri hücre kültürüdür. Hücrelerin, dokuların veya organların bir hayvan veya bitkiden alınması ve daha sonra bu hücrelerin, dokuların veya organların hayatta kalmaları ve/veya büyümeleri için uygun olan yapay bir ortama yerleştirilmesi, "hücre kültürü" ifadesiyle kastedilen şeydir Optimum hücre gelişimi için temel çevresel ihtiyaçlar kontrollü sıcaklık, hücre tutunması için bir substrat, yeterli bir büyüme ortamı ve optimum pH ve osmolaliteyi koruyan bir inkübatördür. Hücrelerin tam potansiyellerine ulaşabilmeleri için bu koşullara sahip olmaları gerekir.
İn vitro ekim için yeterli bir büyüme ortamının seçilmesi, hücre kültüründe hem en kritik hem de en hayati aşamadır. Kültür ortamı olarak da bilinen bir büyüme ortamı, organizmaların mikroskobik, hücresel veya bitki benzeri bir ölçekte gelişimini teşvik etmek için formüle edilmiş bir sıvı veya jeldir. Hücreleri yetiştirmek için kullanılan ortam genellikle yeterli miktarda enerji ve hücre döngüsünü kontrol eden maddeler içerir. Bir kültür ortamının ana bileşenleri arasında amino asitler, vitaminler, inorganik tuzlar, glikoz ve serum bulunur. Serum ortama eklenir çünkü büyüme faktörleri, hormonlar ve bağlanma faktörleri kaynağı olarak işlev görür. Besiyeri, besin sağlamanın yanı sıra pH ve osmolalite seviyelerinin korunmasına da katkıda bulunur.
Hücre kültüründe kullanılan besiyeri türleri
Hem insan hem de hayvan hücreleri yapay veya sentetik bir ortamda ya da doğal elementlerle desteklenmiş tamamen doğal bir ortamda yetiştirilme potansiyeline sahiptir. Aşağıda, şu anda mevcut olan farklı medya türlerine genel bir bakış sunacağız.
Doğal ortam
Doğal besiyerlerinde yalnızca doğal halleriyle var olan biyolojik sıvılar bulunabilir. Doğal besiyerleri çok çeşitli hayvan hücresi türlerinin yetiştirilmesi için çok yararlı ve kolaydır. Doğal ortamı oluşturan bileşenlerin tam olarak anlaşılamaması, doğal ortam kullanılarak elde edilen sonuçların düşük tekrarlanabilirliğine katkıda bulunan birincil faktördür.
Yapay besiyerleri
Yapay veya sentetik ortamların hazırlanması, besin maddelerinin (hem organik hem de inorganik), serum proteinlerinin, karbonhidratların, kofaktörlerin, vitaminlerin ve tuzların yanı sıra O2 ve CO2 gaz fazlarının eklenmesini içerir [1].
Aşağıdaki işlevlerden birini veya daha fazlasını yerine getirmek için çeşitli yapay ortam türleri geliştirilmiştir: 1) Anında hayatta kalma (kesin bir pH ve ozmotik basınca sahip dengeli bir tuz çözeltisi). 2) Uzun süreli hayatta kalma (farklı organik kimyasal formülasyonları ve/veya serum ile desteklenmiş dengeli bir tuz çözeltisi). 3) Belirsiz gelişim. 4) Özelleşmiş işlevler.
Yapay ortamlar için dört farklı sınıflandırma vardır:
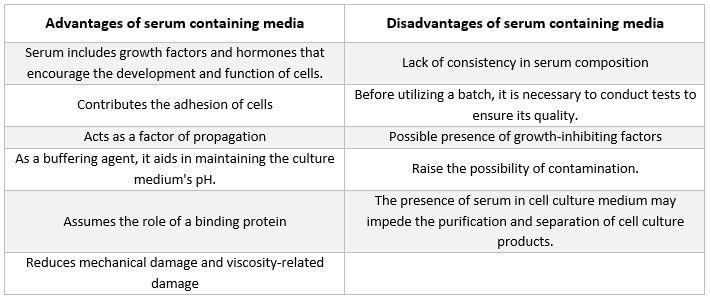
Serum içeren besiyerleri
Hayvan hücrelerini büyütmek için kullanılan ortamda en sık bulunan takviye türü fetal sığır serumudur. Mümkün olan en iyi büyüme koşullarını elde etmek için kültür ortamına düşük maliyetli bir takviye olarak eklenir. Serum, kararsız veya suda çözünmeyen besinler, hormonlar ve büyüme faktörleri, proteaz inhibitörleri ve diğer maddeler için bir taşıyıcı veya şelatör görevi görmenin yanı sıra, zararlı molekülleri de bağlar ve nötralize eder.
Serumsuz Ortam
Ortamda serum bulunmasının bir dizi dezavantajı vardır ve immünolojik araştırmalarda yorumlamada büyük hatalara neden olma potansiyeline sahiptir [2, 3]. Serum içermeyen çeşitli ortamlar oluşturulmuştur [4, 5]. Bu ortamlar genellikle Thermo Fisher Scientific'ten Knockout Serum Replacement ve Knockout DMEM ve kök hücreler için Stem Cell Technologies'ten mTESR ortamı [6] gibi tek bir hücre türünün kültürünü desteklemek için özel olarak formüle edilmiştir [7].
Ayrıca bu besiyerleri, tipik olarak serum tarafından sağlanan saflaştırılmış büyüme faktörleri, lipoproteinler ve diğer proteinleri belirli miktarlarda içermektedir [8]. Bu ortamlar genellikle "tanımlanmış kültürel ortamlar" olarak adlandırılır çünkü bu ortamları oluşturan bileşenler iyi anlaşılmıştır.
Kimyasal olarak tanımlanmış besiyerleri
Bu besiyerleri, herhangi bir kontaminasyonla kirlenmemiş ultra saf inorganik ve organik bileşenler içerir. Ayrıca büyüme faktörleri gibi saf protein ilaveleri de içerebilirler.
belirli yağ asitleri, vitaminler, kolesterol ve amino asitlerin eklenmesiyle birlikte bakteri veya mayanın genetik modifikasyonu, bileşen parçalarının üretilmesiyle sonuçlanır [9].
Protein içermeyen ortamlar
Proteinsiz besiyerleri, hiç protein içermeyen ve bunun yerine sadece protein olmayan elementler içeren besiyerleridir. Serum eklenmiş besiyerleriyle karşılaştırıldığında, protein eklenmemiş besiyerlerinin kullanımı daha fazla hücre çoğalmasını ve protein ekspresyonunu teşvik eder ve sonraki bir süreçte üretilen herhangi bir ürünün saflaştırılmasını kolaylaştırır [10-12]. MEM ve RPMI-1640 gibi formülasyonlara protein dahil değildir. Ancak, gerekli olması halinde protein takviyesi yapılabilir.
Kültür ortamı ve temel bileşenleri
Ticari kültür ortamı toz veya sıvı olarak satın alınabilir ve genellikle amino asitler, glikoz, tuzlar, vitaminler ve diğer besin takviyeleri gibi çeşitli besin maddeleri içerir.
Bu bileşenlere duyulan ihtiyaç her hücre hattı için farklıdır ve bu varyasyonlar çok sayıda farklı ortam formülasyonundan sorumludur. Her bileşen, aşağıdaki paragraflarda özetlenecek olan belirli bir işlevden sorumludur:
Tamponlama sistemleri
Optimum yetiştirme koşullarını korumak için pH kontrol edilmelidir ve bu genellikle iki tamponlama sisteminden biri ile yapılır:
Doğal tamponlama sistemi
Atmosferdeki CO2/H2CO3 oranı ortamdakine eşittir ve doğal bir tamponlama mekanizması oluşturur. Doğal tamponlama mekanizmasını korumak için kültürler %5-10 CO2 içeren bir hava ortamında tutulmalıdır, bu da genellikle bir CO2 inkübatörü kullanılarak elde edilir. Doğal bir tampon kullanmanın en iyi yanlarından biri ucuz ve güvenli olmasıdır.
HEPES
Zwitterion HEPES kullanılarak yapılan kimyasal tamponlama, 7.2-7.4 pH aralığında daha büyük bir tamponlama kapasitesine sahiptir ve düzenlenmiş bir gaz ortamına ihtiyaç duymaz. Belirli hücre tipleri için daha yüksek dozda HEPES zararlı olabilir. HEPES içeren ortamlar da aynı şekilde floresan ışığın fototoksik etkilerine karşı çok daha hassastır [13].
Fenol Kırmızısı
PH göstergesi fenol kırmızısı genellikle ticari olarak temin edilebilen kültür ortamına dahil edilir ve pH'ın sürekli izlenmesine olanak tanır. Hücrelerin genişlemesiyle, bu hücreler tarafından üretilen metabolitler pH'da bir kaymaya ve dolayısıyla besiyerinde bir renk değişimine neden olur. Fenol kırmızısının besiyerinin rengi üzerinde ikili bir etkisi vardır; asidik pH'da sarıya, alkali pH'da mora dönüştürür. Hücre kültürü için en uygun değer olan pH 7,4, besiyerinin floresan kırmızısı görünmesine neden olur.
Ancak fenol kırmızısının birkaç dezavantajı vardır: İlk olarak, fenol kırmızısı, başta östrojen olmak üzere bir dizi steroid hormonunun performansını taklit edebilir [14]. Bu nedenle, meme dokusu gibi östrojene duyarlı hücreleri incelerken, fenol kırmızısı içermeyen bir ortam önerilir. Sodyum-potasyum dengesi, serum içermeyen çeşitli formülasyonlarda fenol kırmızısının varlığıyla bozulur. Ortama serum veya sığır hipofiz hormonu eklenmesi bu etkiyi ortadan kaldırabilir [15]. Üçüncü olarak, akış sitometrik deneylerde tespit, fenol kırmızısının varlığı nedeniyle engellenmektedir.
İnorganik tuzlar
Sodyum, potasyum ve kalsiyum iyonları gibi inorganik tuzlar içeren ortamlar ozmotik dengenin korunmasına yardımcı olur ve membran potansiyelini düzenler.
Amino asitler
Amino asitler proteinin temel bileşenleri olduğundan, şimdiye kadar tasarlanmış olan her bir hücre büyütme ortamının temel bir bileşenidir. Hücreler belirli amino asitleri kendi başlarına üretemedikleri için kültür ortamının esansiyel amino asitleri içermesi önemlidir. Hücrelerin çoğalması için gereklidirler ve mevcut oldukları konsantrasyon, ulaşılabilecek maksimum hücre yoğunluğunu belirler. Özellikle, esansiyel bir amino asit olan L-glutamin özellikle çok önemlidir.
L-glutamin metabolizma için ikincil bir enerji kaynağı olarak işlev görür ve NAD, NADPH ve nükleotid üretimine nitrojen katkısında bulunur. L-glutaminin zamanla hücrelerin kullanamayacağı bir forma dönüşen kararsız bir amino asit olması nedeniyle ortama verilmesi gerekir.
Buna ek olarak, büyüme süreci boyunca tüketilen amino asitleri yeniden doldurmak için ortama esansiyel olmayan amino asitler de verilebilir. Büyüme ortamı esansiyel olmayan amino asitlerle desteklendiğinde hücrelerin büyümesi hızlanır ve canlılıkları artar.
Karbonhidratlar
Şeker formundaki karbonhidratlar temel enerji kaynağıdır. Ortamların çoğu, daha yaygın olan glikoz ve galaktoz şekerlerine ek olarak maltoz ve fruktoz da içerir.
Proteinler ve peptitler
Albümin, transferrin ve fibronektin en yaygın kullanılan proteinler ve peptitlerdir. Bunlar özellikle serum içermeyen ortamlarda önemlidir. Albümin, transferrin, aprotinin, fetuin ve fibronektin, zengin bir protein kaynağı olan serumda bulunabilen proteinlerden bazılarıdır.
Albümin kanda bulunan birincil proteindir ve işlevi su, tuzlar, serbest yağ asitleri, hormonlar ve vitaminler de dahil olmak üzere çeşitli maddeleri bağlamak ve farklı organlar ve hücreler arasında taşımaktır. Albüminin kimyasallara bağlanma yeteneği, onu hücrelerin kültürlendiği ortamdan zararlı bileşiklerin uzaklaştırılması için etkili bir aday haline getirir.
Aprotinin, nötr ve asidik pH'da stabil olmasının yanı sıra yüksek sıcaklıklara ve proteolitik enzimlerin neden olabileceği tahribata karşı dirençli olması nedeniyle hücre kültürü sistemlerinde koruyucu bir maddedir. Diğerlerinin yanı sıra tripsin de dahil olmak üzere bir dizi serin proteazı inhibe edebilir.
Fetuin, fetal ve yeni doğan hayvanların serumunda yetişkin serumuna kıyasla daha yüksek miktarlarda tespit edilebilen bir glikoproteindir. Buna ek olarak, bir serin proteaz inhibitörü olarak işlev görür. Fibronektin proteini, hücre yapışması sürecinde önemli bir bileşendir. Transferrin, demiri taşıyan bir proteindir ve demirin hücrelerin zarlarına iletilmesinden sorumludur.
Yağ asitleri ve lipitler
Serum bulunmadığında serumsuz ortamda çok önemli bir rol oynarlar.
Vitaminler
Hücre gelişimi ve çoğalması için çok sayıda vitamin gereklidir. Vitaminler hücreler tarafından yeterli miktarda üretilemez ve bu nedenle doku kültüründe diyet takviyesi olarak gereklidir.
Hücre kültüründe, serum birincil vitamin kaynağıdır; ancak, ortam da belirli bir hücre tipine uygun hale getirmek için çeşitli vitaminlerle işlenir. En tipik olarak, B grubu vitaminler büyümenin uyarılması için kullanılır.
Eser elementler
Bakır, çinko, selenyum ve trikarboksilik asit ara ürünleri gibi kimyasal elementler eser elementler olarak bilinir. Eser elementler genellikle serumda tipik olarak bulunanların yerini almak için serum içermeyen ortamlara eklenir. Bu elementler sağlıklı bir hücre gelişimi için gerekli olan önemli kimyasal bileşenlerdir. Birçok biyokimyasal reaksiyon, enzim aktivitesi gibi belirli mikro besin maddelerine bağlıdır.
Besiyeri takviyeleri
Belirli hücre hatları için önerilen tam büyüme ortamı, temel ortam ve serumda bulunmayan ekstra bileşenlere ihtiyaç duyar. Bu diyet takviyeleri hücre büyümesini ve uygun metabolik fonksiyonu destekler.
Hormonlar, büyüme faktörleri ve sinyal molekülleri belirli hücre hatlarının uygun şekilde çoğalması için gerekli olsa da aşağıdaki önlemler her zaman alınmalıdır: Takviyelerin eklenmesi tüm büyüme ortamının ozmolalitesini değiştirebileceğinden ve bu da hücre gelişimini engelleyebileceğinden, takviyeler eklendikten sonra ozmolalitenin doğrulanması her zaman tavsiye edilir. Hücre hatlarının çoğu için optimum osmolalite 260 ila 320 mOSM/kg arasında değişmektedir.
Antibiyotikler
Antibiyotikler, hücre büyümesi için gerekli olmamalarına rağmen, bakteriyel ve fungal kirleticilerin gelişimini engellemek için sıklıkla kullanılmaktadır [16]. Antibiyotikler mikoplazma ve dirençli bakteriler tarafından kontaminasyonu gizleyebileceğinden, hücre kültürü için rutin kullanımları önerilmemektedir [17, 18].
Ayrıca antibiyotikler aşırı duyarlı hücrelerin metabolizmasını bozabilir. MilliporeSigma ve Life Technologies tarafından üretilen penisilin-streptomisin kombinasyonları sıklıkla kullanılmaktadır. Plazmosin, TS603, TS516 ve BT260 [19] glioma hücre hatlarının kültüründe kullanılmış ve mikoplazma kontaminasyonunun giderilmesinde etkili olduğu gösterilmiştir (20).
Serum
Albüminler, büyüme faktörleri ve büyüme inhibitörlerinin hepsi serumda mevcuttur. Serum hücre kültürü ortamının en önemli bileşenlerinden biridir çünkü amino asitler, proteinler, vitaminler (özellikle A, D, E ve K gibi yağda çözünen vitaminler), karbonhidratlar, lipidler, hormonlar, büyüme faktörleri, mineraller ve eser elementler sağlar.
Fetal ve dana sığır kaynaklarından elde edilen serum genellikle kültürlenmiş hücrelerin gelişimini desteklemek için kullanılır. Fetal serum bol miktarda büyüme faktörü kaynağıdır ve hücre klonlama ve hassas hücrelerin geliştirilmesi için uygundur. Büyümeyi teşvik etme kabiliyetinin azalması nedeniyle, temas inhibisyonu deneylerinde dana serumu kullanılır. Normal büyüme ortamları genellikle %2 ila %10 serum içerir. Kültür ortamına serum eklenmesi aşağıdaki amaçlara hizmet eder [21]:
-
Serum, hücreler için gerekli besinleri sağlar (hem çözelti içinde hem de proteinlere bağlı olarak).
-
Büyümenin desteklenmesinde ve özelleşmiş hücre aktivitesinde rol oynayan çeşitli büyüme faktörleri ve hormonlar seruma dahildir.
-
Albümin ve transferrin gibi diğer kimyasalları hücre içine taşıyan birçok bağlayıcı protein sunar. Örneğin, albümin yağları, vitaminleri, hormonları vb. hücrelere iletir.
-
Ayrıca fibronektin gibi hücrenin alt tabakaya yapışmasını artıran proteinler de sağlar. Ek olarak, bölünmeden önce hücre genişlemesine yardımcı olan yayılma elemanları üretir.
-
Hücrelerde proteolizi önleyen proteaz inhibitörleri sağlar.
-
Ayrıca Na+, K+, Zn2+ ve Fe2+ gibi mineraller içerir.
-
Ortamın viskozitesini artırır, böylece süspansiyon kültürü çalkalaması sırasında hücreleri mekanik yaralanmalardan korur.
-
Aynı zamanda bir tampon.
Referanslar
[1] Morgan J, Morton H, Parker R. Doku kültüründeki hayvan hücrelerinin beslenmesi; sentetik bir ortam üzerinde ilk çalışmalar. Proc Soc Exp Biol Med. 1950;73:1-8
[2] Kerbel R, Blakeslee D. Bir fötal buzağı serumu bileşeninin kültürdeki memeli hücreleri tarafından hızlı adsorpsiyonu. Hücreye özgü antijenlere karşı antiserum çalışmalarında potansiyel bir artefakt kaynağı. İmmünoloji. 1976;31:881-91
[3] Sula K, Draber P, Nouza K. Popliteal lenf nodu testi ile incelenen hücre aracılı reaksiyonlarda olası bir artefakt kaynağı olarak hücre süspansiyonlarının hazırlanması için kullanılan ortama serum eklenmesi. J Immunogenet. 1980;7:483-9
[4] Mariani E, Mariani A, Monaco M, Lalli E, Vitale M, Facchini A. Ticari serumsuz besiyerleri: hibridoma büyümesi ve monoklonal antikor üretimi. J Immunol Methods. 1991;145:175-83
[5] Barnes D, Sato G. Serum içermeyen ortamda kültürlenmiş hücrelerin büyümesi için yöntemler. Anal Biyokimya. 1980;102:255-70
[6] Yu H, Lu S, Gasior K, Singh D, Vazquez Sanchez S, Tapia O,vd. HSP70, RNA içermeyen TDP-43'ü anizotropik intranükleer sıvı küresel kabuklara şaperonlar. Bilim. 2021;371:
[7] Meharena H, Marco A, Dileep V, Lockshin E, Akatsu G, Mullahoo J,et al. Down sendromunun neden olduğu yaşlanma, nöral progenitörlerin nükleer mimarisini bozar. Hücre Kök Hücre. 2022;29:116-130.e7
[8] Iscove N, Melchers F. Lipopolisakkarit reaktif B lenfosit kültürlerinde serumun albümin, transferrin ve soya fasulyesi lipidi ile tamamen değiştirilmesi. J Exp Med. 1978;147:923-33
[9] Stoll T, Muhlethaler K, von Stockar U, Marison I. Hibridoma büyümesi ve monoklonal antikor üretimi için kimyasal olarak tanımlanmış protein içermeyen bir ortamın sistematik olarak geliştirilmesi. J Biotechnol. 1996;45:111-23
[10] Darfler F. Hibridomların ve bağışıklık sisteminin diğer hücrelerinin büyümesi için proteinsiz bir ortam. In Vitro Cell Dev Biol. 1990;26:769-78
[11] Barnes D, Sato G. Serumsuz hücre kültürü: birleştirici bir yaklaşım. Cell. 1980;22:649-55
[12] Hamilton W, Ham R. Çin hamster hücre hatlarının proteinsiz ortamda klonal büyümesi. In Vitro. 1977;13:537-47
[13] Zigler J, Lepe Zuniga J, Vistica B, Gery I. Işığa maruz bırakılmış HEPES içeren kültür ortamının sitotoksik etkilerinin analizi. In Vitro Cell Dev Biol. 1985;21:282-7
[14] Berthois Y, Katzenellenbogen J, Katzenellenbogen B. Doku kültürü ortamındaki fenol kırmızısı zayıf bir östrojendir: kültürde östrojene duyarlı hücrelerin incelenmesine ilişkin çıkarımlar. Proc Natl Acad Sci U S A. 1986;83:2496-500
[15] Karmiol S. Serum içermeyen besiyerlerinin geliştirilmesi. İçinde: Master JRW, editör. Hayvan Hücre kültürü, 3. baskı. Oxford:Oxford University Press; 2000.
[16] Perlman D. Hücre kültürü ortamlarında antibiyotik kullanımı. Yöntemler Enzimol. 1979;58:110-6
[17] McGarrity G. Hücre kültürlerinde mikoplazma enfeksiyonunun yayılması ve kontrolü. In Vitro. 1976;12:643-8
[18] Masters J, Stacey G. Ortam değiştirme ve hücre dizilerini pasajlama. Nat Protoc. 2007;2:2276-84
[19] Chakraborty A, Laukka T, Myllykoski M, Ringel A, Booker M, Tolstorukov M,vd. Histon demetilaz KDM6A, kromatin ve hücre kaderini kontrol etmek için oksijeni doğrudan algılar. Bilim. 2019;363:1217-1222
[20] Molla Kazemiha V, Azari S, Amanzadeh A, Bonakdar S, Shojaei Moghadam M, Habibi Anbouhi M,et al. Plasmocin™'in hücre kültüründe yaygın olarak kullanılan antibiyotiklerle karşılaştırıldığında mollicutes tarafından enfekte edilen çeşitli memeli hücre hatları üzerindeki etkinliği: yerel bir deneyim. Sitoteknoloji. 2011;63:609-20
[21] Kragh Hansen U. Serum albüminine ligand bağlanmasının moleküler yönleri. Pharmacol Rev. 1981;33:17-53