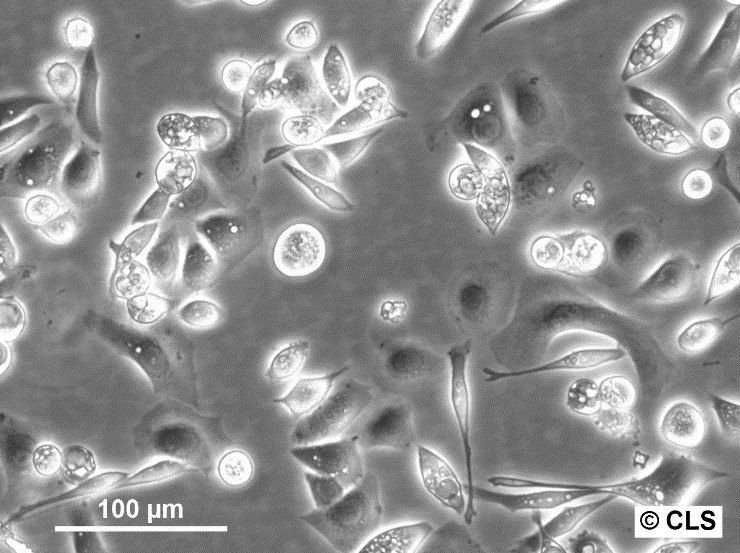
AGS-celler - Utforskning av gastriskt adenokarcinom AGS-celler i cancerstudier
AGS-celler är en cellinje från humant gastriskt adenokarcinom som används flitigt inom biomedicinsk forskning. Den används framför allt för att studera gastrisk cancerbiologi, inklusive tumörtillväxt, utveckling, progression och terapeutiska ingrepp. Dessutom används den för att undersöka värd-patogen-interaktioner.
Denna artikel kommer att diskutera grunderna för gastriska epiteliala AGS-celler. I synnerhet kommer den att omfatta följande:
- AGS-cellernas allmänna egenskaper och ursprung
- Information om odling av AGS-cellinje
- AGS-cellinje: Fördelar och begränsningar
- Tillämpningar av AGS-celler
- Forskningspublikationer om AGS-cellinje
- Resurser för AGS-cellinje: Protokoll, videor och mer
1.allmänna egenskaper och ursprung för AGS-celler
Det är nödvändigt att känna till en cellinjes ursprung och allmänna egenskaper innan du börjar arbeta med den. Detta avsnitt kommer att täcka följande: Vad är AGS-celler? Vad är AGS-cellens ursprung? Vad är morfologin hos AGS-cellinjen för cancer?
- AGS-cellinjen härstammar från magvävnaden hos en 54-årig kaukasisk kvinna med gastriskt adenokarcinom. Den isolerades 1979 [1].
- AGS-cellerna har en epitelliknande morfologi.
- De gastriska epiteliala AGS-cellerna är hyperdiploida. Det modala kromosomantalet för AGS-celler är 49, vilket förekommer i nästan 60% av cellerna. Polyploidi förekommer också i cirka 3,6% av cellerna.
2.information om odling av AGS-cellinjen
För korrekt hantering och skötsel av en cellinje måste du känna till dess grundläggande odlingskoncept. Du bör särskilt lära dig följande: Vad är AGS-cellens fördubblingstid? Vad är AGS-cellmediet? Hur subkulturerar man AGS-celler? Vilka frysmedier används för AGS-celler från gastriska epitel?
Viktiga punkter för odling av AGS-celler
|
Fördubblingstid: |
AGS-cellernas fördubblingstid varierar mellan 24 och 48 timmar. |
|
Adherent eller i suspension: |
AGS-celler är adherenta. De växer till monolager. |
|
Utsädesdensitet: |
AGS-celler utsädes med en celldensitet på 1 x104 celler/cm2. Cellerna bildar ett sammanflytande monolager vid denna densitet inom 3 till 5 dagar. Efter avlägsnande av gamla medier sköljdes cellerna med 1 x PBS och inkuberades med Accutase dissociationslösning. Avskilda celler resuspenderades i odlingsmedium och centrifugerades. Cellpelleten resuspenderades igen, och efter AGS-cellräkning fördelades de i den nya kolven för tillväxt. |
|
Tillväxtmedium: |
DMEM-media innehållande 10% FBS, 4 mM L-Glutamin, 4,5 g/L Glukos, 1,5 g/L NaHCO3 och 1,0 mM Natriumpyruvat används för odling av AGS-celler. Media bör bytas ut 2 till 3 gånger i veckan. |
|
Tillväxtförhållanden: |
AGS-cellerna förvaras i en luftfuktad inkubator (vid 37°C) med 5% CO2-tillförsel. |
|
Förvaring: |
Frysta AGS-celler förvaras i elektriska frysar vid en temperatur under -150°C eller i ångfasen av flytande kväve under en längre tid. |
|
Frysningsprocess och medium: |
CM-1- eller CM-ACF-medium används för att frysa AGS-celler. Cellfrysningen sker genom en långsam frysningsprocess som endast tillåter en temperatursänkning på 1°C per minut och som skyddar cellernas livskraft. |
|
Upptiningsprocess: |
Frysta gastriska epitelceller omrörs snabbt i ett 37°C vattenbad under 40 till 60 sekunder. Upptinade celler resuspenderas i färskt odlingsmedium och hälls över i nya kolvar för tillväxt. Efter 24 timmars inkubation förnyas mediet för att avlägsna frysande mediakomponenter. I motsats till detta centrifugeras upptinade celler och frysmedieelement avlägsnas. Därefter resuspenderas de skördade cellerna igen och fördelas i kolven som innehåller odlingsmediet. |
|
Biosäkerhetsnivå: |
Laboratorieinställningar på biosäkerhetsnivå 2 är nödvändiga för odling av AGS-celler. |
3.aGS cellinje: Fördelar och begränsningar
I detta artikelavsnitt belyses några av de viktigaste fördelarna och begränsningarna med AGS-celler.
Fördelar med AGS-celler
De främsta fördelarna med AGS-celler från magsäcksepitel är
|
Lätt att odla |
AGS-cellinjen för gastriskt karcinom är lätt att underhålla i cellodlingslaboratorier. Den har inte några komplicerade och krångliga cellodlingskrav. Dessutom uppvisar den goda tillväxtegenskaper, vilket gör den till ett idealiskt val för att studera gastrisk cancerbiologi. |
|
Relevans för magsäckscancer |
AGS-celler härrör från humant gastriskt adenokarcinom, vilket gör att de ofta används för att studera gastrisk cancerbiologi och terapeutiska interventioner. |
Begränsningar
Den begränsning som är förknippad med AGS-cellinjen är:
|
In vitro-cellmodell |
AGS-celler odlas i biomedicinska forskningslaboratorier under artificiella förhållanden. Därför kanske de inte helt replikerar mikromiljön för gastrisk cancer in vivo och andra cell- och molekylära interaktioner. |
4.tillämpningar av AGS-celler
AGS-celler används specifikt för att studera gastrisk cancerbiologi. De har många andra lovande tillämpningar inom det biomedicinska området. Några av de intressanta forskningsapplikationerna för AGS-celler är
- Studie av magsäckscancer: AGS-celler är ett utmärkt forskningsverktyg för att undersöka cell- och molekylära mekanismer som ligger bakom tillväxt, metastasering och invasion av magcancer. Forskare använder också AGS-celler från magsäcksepitel för att studera olika cellulära processer, genetiska mutationer och signalvägar i utvecklingen av magsäckscancer. En studie i Oncology Reports (2019) visade att mikroRNA-183-5p.1 främjar tumörcellers proliferation, migration och invasion genom att hämma Bcl 2/P53-signalkaskaden. Dessutom nedreglerar det också TPM1-genen för att utöva dessa effekter. Både mikroRNA och TPM1 föreslås därför som effektiva molekylära mål för utveckling av riktade behandlingar mot gastrisk cancer [2].
- Screening av läkemedel: AGS-celler har ofta använts för att screena nya och effektiva läkemedel mot magsäckscancer. Forskare utvärderar cytotoxiciteten och effekten av potentiella läkemedel med hjälp av AGS-cellinjen. Studier har också genomförts för att identifiera nya molekylära mål och utveckla nya riktade terapier för att bekämpa magsäckscancer. I forskning som genomfördes 2021 användes AGS magcancerceller och den terapeutiska effekten av läkemedlet paklitaxel studerades. Resultaten visade att paklitaxel inducerar en mitotisk katastrof, en integrerad mekanism för apoptos eller celldöd i AGS-celler. Dessutom främjade det autofagi i gastriska cancerceller [3].
- Interaktioner mellan värd och patogen: AGS-cancercellinjen studerar också interaktioner mellan värd och patogen. Detta hjälper forskare att förstå de cellulära mekanismer och svar som är involverade i en infektion. I en studie som genomfördes 2020 observerades till exempel att små icke-kodande RNA som finns i yttermembranvesiklar från Helicobacter pylori minskar utsöndringen av interleukin 8 i mänskliga AGS-celler [4].
5.forskningspublikationer om AGS-cellinje
Detta avsnitt av artikeln kommer att behandla några intressanta och mest citerade forskningspublikationer som innehåller AGS-celler.
Denna studie i Biomedicine & Pharmacotherapy (2020) föreslog att salidroside, en naturlig förening, inducerar skyddande autofagi och celldöd i gastriska epiteliala AGS-celler via modulering av PI3K / AKT / mTOR-signalvägen.
Denna studie publicerades i Biomedicine & Pharmacotherapy (2018). Den undersökte de synergistiska anticancereffekterna av astragalus polysackarid och läkemedlet apatinib i AGS-celler. Studiens resultat visade att astragalus förstärker apatinibs antitumöreffekter genom att undertrycka AKT-signalering.
I denna forskning i Journal of Ethnopharmacology (2018) föreslås att curcuzedoalide, en naturlig förening från växten Curcuma zedoaria Roscoe, bidrar till dess cytotoxiska potential mot AGS-celler.
Överuttryck av FOXA1 hämmar cellproliferation och EMT hos AGS-celler från magcancer hos människa
I denna publikation i Gene (2018) föreslås att uppreglering av FOXA1 undertrycker AGS gastriska adenokarcinomcellers proliferation och epitelial till mesenkymal övergång (EMT) och invasion.
Denna forskningsartikel publicerades i International Journal of Medical Microbiology 2020. I denna studie användes AGS-celler för att studera värd-patogen-interaktioner. Resultaten visade att Helicobacter pylori innehåller vissa icke-kodande RNA i sina yttre membranvesiklar som påverkar IL-8-nivåerna i AGS-celler.
6.resurser för AGS cellinje: Protokoll, videor och mer
Nedan följer några resurser som handlar om AGS-celler.
- Protokoll för transfektion av AGS-celler: Den här videon är en stegvis guide för att lära sig transfektionsprotokoll för gastriska epiteliala AGS-celler.
Följande länk innehåller AGS-cellodlingsprotokollet.
- AGS cellodlingsprotokoll: Den här webbplatsen innehåller användbar information om AGS-cellmedier och cellodlingsprotokoll. I korthet innehåller den ett protokoll för subkulturering av AGS-celler från gastriska epitel och hantering av prolifererande och kryokonserverade AGS-kulturer.
- Subodling av AGS-celler: På den här webbplatsen förklaras subodlingsförfarandet för AGS-celler i detalj.
Referenser
- Phuc, B.H., et al., Comparative genomics of two Vietnamese Helicobacter pylori strains, CHC155 from a non-cardia gastric cancer patient and VN1291 from a duodenal ulcer patient. Vetenskapliga rapporter, 2023. 13(1): p. 8869.
- Lin, J., et al, miRNA-183-5p. 1 främjar migration och invasion av AGS-celler med magcancer genom att rikta in sig på TPM1 Rättelse i/10.3892/or. 2020.7902. Onkologiska rapporter, 2019. 42(6): p. 2371-2381.
- Khing, T.M., et al, Effekten av paklitaxel på apoptos, autofagi och mitotisk katastrof i AGS-celler. Vetenskapliga rapporter, 2021. 11(1): p. 23490.
- Zhang, H., et al., sncRNA förpackade av Helicobacter pylori yttre membranvesiklar dämpar IL-8-sekretion i humana celler. International Journal of Medical Microbiology, 2020. 310(1): p. 151356.