Mediile de cultură celulară: O prezentare generală
În domeniul științelor vieții, una dintre cele mai importante metodologii este cultura celulară. Prin sintagma "cultură celulară" se înțelege prelevarea de celule, țesuturi sau organe de la un animal sau de la o plantă și implantarea ulterioară a acestor celule, țesuturi sau organe într-un mediu artificial care este favorabil supraviețuirii și/sau creșterii lor Necesitățile fundamentale de mediu pentru dezvoltarea optimă a celulelor sunt temperatura controlată, un substrat pentru fixarea celulelor, un mediu de creștere adecvat și un incubator care menține pH-ul și osmolalitatea optime. Celulele trebuie să aibă aceste condiții pentru a se dezvolta la potențialul lor maxim.
Selectarea unui mediu de creștere adecvat pentru cultivarea in vitro este etapa cea mai critică și cea mai vitală din cultura celulară. Un mediu de creștere, cunoscut și ca mediu de cultură, este un lichid sau un gel formulat pentru a încuraja dezvoltarea organismelor la scară microscopică, celulară sau vegetală. Mediul utilizat pentru cultivarea celulelor conține adesea un aport adecvat de energie și substanțe care controlează ciclul celular. Principalele componente ale unui mediu de cultură includ aminoacizii, vitaminele, sărurile anorganice, glucoza și serul. Serul este adăugat la mediu deoarece acționează ca o sursă de factori de creștere, hormoni și factori de atașare. Pe lângă aportul de substanțe nutritive, mediul contribuie și la menținerea pH-ului și a nivelului de osmolalitate.
Tipuri de medii utilizate în cultura celulară
Atât celulele umane, cât și cele animale au potențialul de a fi cultivate fie într-un mediu artificial sau sintetic, fie într-un mediu complet natural care este suplimentat cu elemente naturale. În cele ce urmează, vă vom oferi o prezentare generală a diferitelor tipuri de medii disponibile în prezent.
Mediile naturale
Numai fluidele biologice care există în starea lor naturală pot fi găsite în medii naturale. Mediile naturale sunt foarte utile și ușoare pentru cultivarea unei mari varietăți de tipuri de celule animale. Lipsa de înțelegere a componentelor exacte care alcătuiesc mediile naturale este principalul factor care contribuie la repetabilitatea scăzută a rezultatelor obținute cu ajutorul mediilor naturale.
Mediile artificiale
Prepararea mediilor artificiale sau sintetice implică adăugarea de nutrienți (atât organici, cât și anorganici), proteine serice, carbohidrați, cofactoare, vitamine și săruri, precum și faze gazoase de O2 și CO2 [1].
Au fost dezvoltate diverse tipuri de medii artificiale pentru a îndeplini una sau mai multe dintre următoarele funcții: 1) Supraviețuirea imediată (o soluție salină echilibrată cu un pH și o presiune osmotică precise). 2) Supraviețuire prelungită (o soluție salină echilibrată suplimentată cu diferite formulări de substanțe chimice organice și/sau ser). 3) Dezvoltare nelimitată. 4) Funcții specializate.
Există patru clasificări distincte pentru mediile artificiale:
Medii care conțin ser
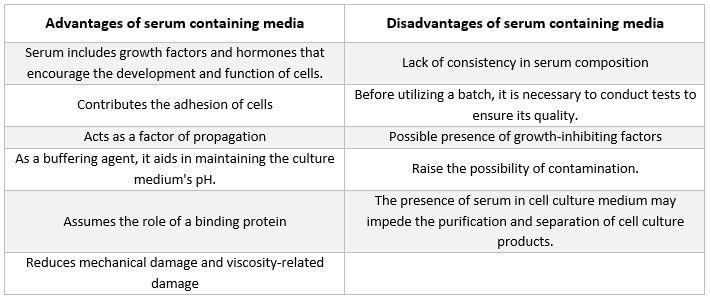
Cel mai frecvent tip de supliment găsit în mediile utilizate pentru cultivarea celulelor animale este serul fetal bovin. Acesta se adaugă la mediul de cultură ca supliment cu costuri reduse pentru a obține cele mai bune condiții de creștere posibile. Pe lângă faptul că acționează ca un transportor sau chelator pentru nutrienții instabili sau insolubili în apă, hormoni și factori de creștere, inhibitori de protează și alte substanțe, serul leagă și neutralizează moleculele dăunătoare.
Mediul fără ser
Prezența serului în mediu are o serie de dezavantaje și are potențialul de a cauza erori majore de interpretare în cercetarea imunologică [2, 3]. Au fost create o varietate de medii diferite fără ser [4, 5]. În general, aceste medii sunt formulate special pentru a susține cultivarea unui singur tip de celule, cum ar fi Knockout Serum Replacement și Knockout DMEM de la Thermo Fisher Scientific și mediul mTESR de la Stem Cell Technologies [6], pentru celule stem [7].
În plus, aceste medii încorporează cantități definite de factori de creștere purificați, lipoproteine și alte proteine, care sunt furnizate de obicei de ser [8]. Aceste medii sunt adesea denumite "medii culturale definite", deoarece componentele care le alcătuiesc sunt bine cunoscute.
Medii definite chimic
Aceste medii includ componente anorganice și organice ultrapure care nu au fost contaminate de niciun fel de contaminare. Acestea pot include, de asemenea, adaosuri de proteine pure, cum ar fi factorii de creștere.
modificarea genetică a bacteriilor sau a drojdiei, împreună cu adăugarea anumitor acizi grași, vitamine, colesterol și aminoacizi, duce la producerea părților componente ale acestora [9].
Medii fără proteine
Mediile fără proteine sunt cele care nu includ deloc proteine și includ doar elemente neproteice. În comparație cu mediile cu adaos de ser, utilizarea mediilor fără adaos de proteine promovează o mai mare proliferare celulară și expresie proteică și facilitează purificarea oricărui produs generat într-un proces din aval [10-12]. Proteinele nu sunt incluse în formulări precum MEM și RPMI-1640. Cu toate acestea, ar putea fi administrat un supliment de proteine dacă este necesar.
Mediul de cultură și componentele sale de bază
Mediile de cultură comerciale pot fi achiziționate sub formă de pulbere sau lichid și includ adesea o varietate de nutrienți, cum ar fi aminoacizi, glucoză, săruri, vitamine și alte suplimente alimentare.
Necesarul acestor componente este diferit pentru fiecare linie celulară, iar aceste variații sunt responsabile pentru numărul mare de formulări diferite de medii. Fiecare componentă este responsabilă pentru o anumită funcție, care va fi prezentată în paragrafele următoare:
Sisteme tampon
Pentru a menține condiții optime de creștere, pH-ul trebuie controlat, ceea ce se realizează adesea prin unul dintre cele două sisteme tampon:
Sistemul tampon natural
Raportul CO2/H2CO3 din atmosferă este egal cu cel din mediu, creând un mecanism natural de tamponare. Pentru a-și păstra mecanismul tampon natural, culturile trebuie menținute într-un mediu aerian cu 5-10% CO2, ceea ce se realizează adesea prin utilizarea unui incubator cu CO2. Unul dintre cele mai bune aspecte legate de utilizarea unui tampon natural este faptul că este ieftin și sigur.
HEPES
Tamponarea chimică folosind zwitterionul HEPES are o capacitate mai mare de tamponare în intervalul de pH 7,2-7,4 și nu necesită un mediu gazos reglementat. Pentru anumite tipuri de celule, o doză mai mare de HEPES poate fi dăunătoare. Mediile care conțin HEPES sunt, de asemenea, mult mai sensibile la efectele fototoxice ale luminii fluorescente [13].
Fenol roșu
Indicatorul de pH roșu fenol este adesea inclus în mediul de cultură disponibil în comerț, permițând monitorizarea continuă a pH-ului. Prin extinderea celulelor, metaboliții produși de aceste celule determină o modificare a pH-ului și, prin urmare, o schimbare de culoare a mediului. Roșul fenol are un efect dublu asupra culorii unui mediu, făcându-l galben la pH acid și violet la pH alcalin. pH 7,4, valoarea optimă pentru cultura de celule, face ca mediul să apară roșu fluorescent.
Dar roșul fenol are câteva dezavantaje: În primul rând, roșul fenol este capabil să simuleze performanța unui număr de hormoni steroizi, în primul rând estrogenul [14]. Prin urmare, atunci când se studiază celule sensibile la estrogen, cum ar fi țesutul mamar, se recomandă un mediu fără roșu de fenol. Echilibrul sodiu-potasiu este perturbat de prezența roșu de fenol în mai multe formulări fără ser. Adăugarea de ser sau de hormon hipofizar bovin la mediu poate contracara acest efect [15]. În al treilea rând, detectarea în experimentele citometrice în flux este împiedicată de prezența roșu de fenol.
Săruri anorganice
Mediile care conțin săruri anorganice, cum ar fi ionii de sodiu, potasiu și calciu, contribuie la menținerea echilibrului osmotic și la reglarea potențialului membranar.
Aminoacizi
Deoarece aminoacizii sunt componentele fundamentale ale proteinelor, aceștia sunt o componentă esențială a oricărui mediu de creștere celulară care a fost conceput vreodată. Deoarece celulele sunt incapabile să producă singure anumiți aminoacizi, este important ca mediul de cultură să includă aminoacizi esențiali. Aceștia sunt necesari pentru proliferarea celulelor, iar concentrația la care sunt prezenți determină densitatea celulară maximă care poate fi atinsă. În special, L-glutamina, un aminoacid esențial, este deosebit de importantă.
L-glutamina funcționează ca o sursă secundară de energie pentru metabolism și contribuie cu azot la producerea de NAD, NADPH și nucleotide. Datorită faptului că L-glutamina este un aminoacid instabil care, cu timpul, se transformă într-o formă pe care celulele nu o pot utiliza, acesta trebuie să fie administrat mediului.
În plus, aminoacizii neesențiali pot fi introduși în mediu pentru a le reaproviziona pe cele care au fost consumate pe parcursul procesului de creștere. Creșterea celulelor este stimulată și viabilitatea lor este crescută atunci când mediul de creștere este suplimentat cu aminoacizi neesențiali.
Carbohidrați
Glucidele sub formă de zaharuri sunt principala sursă de energie. Multe dintre mediile de cultură includ maltoză și fructoză, pe lângă zaharurile cele mai comune, glucoza și galactoza.
Proteine și peptide
Albumina, transferrina și fibronectina sunt cele mai frecvent utilizate proteine și peptide, care sunt deosebit de importante în mediile care nu includ ser. Albumina, transferrina, aprotinina, fetuina și fibronectina sunt unele dintre proteinele care pot fi găsite în ser, care este o sursă bogată de proteine.
Albumina este principala proteină prezentă în sânge, iar funcția sa este de a lega și transporta diverse substanțe, inclusiv apă, săruri, acizi grași liberi, hormoni și vitamine, între diferite organe și celule. Capacitatea albuminei de a se lega de substanțele chimice o face un candidat eficient pentru eliminarea compușilor nocivi din mediul în care sunt cultivate celulele.
Aprotinina este un agent de protecție în sistemele de cultură celulară, deoarece este stabilă la pH neutru și acid, precum și rezistentă la temperaturi ridicate și la distrugerile care pot fi cauzate de enzimele proteolitice. Este capabilă să inhibe o serie de serine proteaze, inclusiv tripsina, printre altele.
Fetuina este o glicoproteină care poate fi detectată în cantități mai mari în serul animalelor fetale și nou-născute comparativ cu serul adulților. În plus, aceasta acționează ca un inhibitor de serină protează. Proteina fibronectină este o componentă esențială în procesul de adeziune celulară. Transferrina este o proteină care transportă fierul și este responsabilă de livrarea fierului la membranele celulelor.
Acizi grași și lipide
Acestea joacă un rol esențial în mediul fără ser atunci când serul este absent.
Vitamine
Numeroase vitamine sunt necesare pentru dezvoltarea și proliferarea celulară. Vitaminele nu pot fi produse în cantități adecvate de către celule și, prin urmare, sunt esențiale în cultura de țesuturi ca suplimente alimentare.
În cultura celulară, serul este principala sursă de vitamine; cu toate acestea, mediile sunt, de asemenea, tratate cu diverse vitamine pentru a le face adecvate unui anumit tip de celule. Cel mai adesea, vitaminele din grupul B sunt utilizate pentru stimularea creșterii.
Oligoelemente
Elementele chimice precum cuprul, zincul, seleniul și intermediarii acizilor tricarboxilici sunt cunoscute sub denumirea de oligoelemente. Oligoelementele sunt adesea adăugate la medii care nu includ ser pentru a le înlocui pe cele care sunt prezente în mod obișnuit în ser. Aceste elemente sunt componente chimice importante care sunt necesare pentru o dezvoltare celulară sănătoasă. Multe reacții biochimice depind de anumiți micronutrienți, cum ar fi activitatea enzimatică.
Suplimente de mediu
Mediul de creștere completă sugerat pentru anumite linii celulare are nevoie de componente suplimentare care sunt absente din mediul de bază și din ser. Aceste suplimente alimentare susțin creșterea celulară și funcția metabolică adecvată.
Deși hormonii, factorii de creștere și moleculele de semnalizare sunt esențiale pentru proliferarea adecvată a anumitor linii celulare, trebuie luate întotdeauna următoarele precauții: Deoarece adăugarea de suplimente poate modifica osmolalitatea mediului de creștere complet, ceea ce poate inhiba dezvoltarea celulară, este întotdeauna recomandabil să se verifice osmolalitatea după adăugarea de suplimente. Pentru majoritatea liniilor celulare, osmolalitatea optimă variază între 260 și 320 mOSM/kg.
Antibiotice
Antibioticele sunt adesea utilizate pentru a inhiba dezvoltarea poluanților bacterieni și fungici [16], deși acestea nu sunt esențiale pentru creșterea celulară. Deoarece antibioticele pot ascunde contaminarea cu micoplasmă și bacterii rezistente, utilizarea lor de rutină nu este sugerată pentru cultura celulară [17, 18].
În plus, antibioticele pot perturba metabolismul celulelor hipersensibile. Combinațiile penicilină-streptomicină produse de MilliporeSigma și Life Technologies sunt adesea utilizate. Plasmocinul a fost utilizat în cultivarea liniilor celulare de gliom TS603, TS516 și BT260 [19] și s-a dovedit a fi eficient în eliminarea contaminării cu micoplasmă (20).
Serul
Albuminele, factorii de creștere și inhibitorii de creștere sunt toți prezenți în ser. Serul este una dintre cele mai importante componente ale mediului de cultură celulară deoarece furnizează aminoacizi, proteine, vitamine (în special vitamine liposolubile precum A, D, E și K), carbohidrați, lipide, hormoni, factori de creștere, minerale și oligoelemente.
Serul din surse fetale și de vițel bovin este adesea utilizat pentru a promova dezvoltarea celulelor cultivate. Serul fetal este o sursă abundentă de factori de creștere și este potrivit pentru clonarea celulelor și dezvoltarea celulelor sensibile. Datorită capacităților sale reduse de promovare a creșterii, serul de vițel este utilizat în experimentele de inhibare a contactului. Mediile de creștere normale includ adesea între 2% și 10% ser. Adăugarea de ser la mediul de cultură servește următoarelor scopuri [21]:
-
Serul furnizează substanțele nutritive esențiale pentru celule (atât în soluție, cât și atașate la proteine).
-
Mai mulți factori de creștere și hormoni implicați în promovarea creșterii și în activitatea celulară specializată sunt incluși în ser.
-
Acesta oferă multe proteine de legare, precum albumina și transferrina, care transportă alte substanțe chimice în celulă. De exemplu, albumina transportă grăsimile, vitaminele, hormonii etc. în celule.
-
De asemenea, furnizează proteine, precum fibronectina, care sporesc aderența celulelor la substrat. În plus, produce elemente de răspândire care ajută la expansiunea celulară înainte de diviziune.
-
Furnizează inhibitori de protează care previn proteoliza în celule.
-
De asemenea, conține minerale precum Na+, K+, Zn2+ și Fe2+.
-
Mărește vâscozitatea mediului, protejând astfel celulele de leziuni mecanice în timpul agitării culturilor în suspensie.
-
Este, de asemenea, un tampon.
Referințe bibliografice
[1] Morgan J, Morton H, Parker R. Nutrition of animal cells in tissue culture; initial studies on a synthetic medium. Proc Soc Exp Biol Med. 1950;73:1-8
[2] Kerbel R, Blakeslee D. Adsorbția rapidă a unei componente a serului fetal de vițel de către celulele mamiferelor în cultură. O sursă potențială de artefacte în studiile antiserurilor la antigenele specifice celulelor. Imunologie. 1976;31:881-91
[3] Sula K, Draber P, Nouza K. Adăugarea de ser la mediul utilizat pentru prepararea suspensiilor celulare ca o posibilă sursă de artefacte în reacțiile mediate celular studiate prin intermediul testului ganglionului limfatic popliteal. J Immunogenet. 1980;7:483-9
[4] Mariani E, Mariani A, Monaco M, Lalli E, Vitale M, Facchini A. Mediile comerciale fără ser: creșterea hibridomului și producția de anticorpi monoclonali. J Immunol Methods. 1991;145:175-83
[5] Barnes D, Sato G. Metode de creștere a celulelor cultivate în mediu fără ser. Anal Biochem. 1980;102:255-70
[6] Yu H, Lu S, Gasior K, Singh D, Vazquez Sanchez S, Tapia O,et al. HSP70 chaperonează TDP-43 fără ARN în cochilii sferice lichide intranucleare anizotropice. Știință. 2021;371:
[7] Meharena H, Marco A, Dileep V, Lockshin E, Akatsu G, Mullahoo J,et al. Senescența indusă de sindromul Down perturbă arhitectura nucleară a progenitorilor neuronali. Cell Stem Cell. 2022;29:116-130.e7
[8] Iscove N, Melchers F. Înlocuirea completă a serului cu albumină, transferrină și lipide de soia în culturile de limfocite B reactive la lipopolizaharide. J Exp Med. 1978;147:923-33
[9] Stoll T, Muhlethaler K, von Stockar U, Marison I. Îmbunătățirea sistematică a unui mediu fără proteine definit chimic pentru creșterea hibridomilor și producerea de anticorpi monoclonali. J Biotechnol. 1996;45:111-23
[10] Darfler F. A protein-free medium for the growth of hybridomas and other cells of the immune system. In Vitro Cell Dev Biol. 1990;26:769-78
[11] Barnes D, Sato G. Cultura celulară fără ser: o abordare unificatoare. Cell. 1980;22:649-55
[12] Hamilton W, Ham R. Creșterea clonală a liniilor celulare de hamster chinezesc în medii fără proteine. In Vitro. 1977;13:537-47
[13] Zigler J, Lepe Zuniga J, Vistica B, Gery I. Analysis of the cytotoxic effects of light-exposed HEPES-containing culture medium. In Vitro Cell Dev Biol. 1985;21:282-7
[14] Berthois Y, Katzenellenbogen J, Katzenellenbogen B. Fenolul roșu din mediul de cultură a țesuturilor este un estrogen slab: implicații privind studiul celulelor în cultură care răspund la estrogen. Proc Natl Acad Sci U S A. 1986;83:2496-500
[15] Karmiol S. Dezvoltarea mediilor fără ser. În: Master JRW, editor. Animal Cell culture, 3rd ed. Oxford:Oxford University Press; 2000.
[16] Perlman D. Utilizarea antibioticelor în mediile de cultură celulară. Metode Enzymol. 1979;58:110-6
[17] McGarrity G. Răspândirea și controlul infecției micoplasmice a culturilor celulare. In Vitro. 1976;12:643-8
[18] Masters J, Stacey G. Changing medium and passaging cell lines. Nat Protoc. 2007;2:2276-84
[19] Chakraborty A, Laukka T, Myllykoski M, Ringel A, Booker M, Tolstorukov M,et al. Histone demethylase KDM6A detectează direct oxigenul pentru a controla cromatina și destinul celular. Știință. 2019;363:1217-1222
[20] Molla Kazemiha V, Azari S, Amanzadeh A, Bonakdar S, Shojaei Moghadam M, Habibi Anbouhi M,et al. Eficiența Plasmocin™ pe diferite linii de celule de mamifere infectate cu molicute în comparație cu antibioticele utilizate în mod obișnuit în cultura celulară: o experiență locală. Citotehnologie. 2011;63:609-20
[21] Kragh Hansen U. Molecular aspects of ligand binding to serum albumin. Pharmacol Rev. 1981;33:17-53