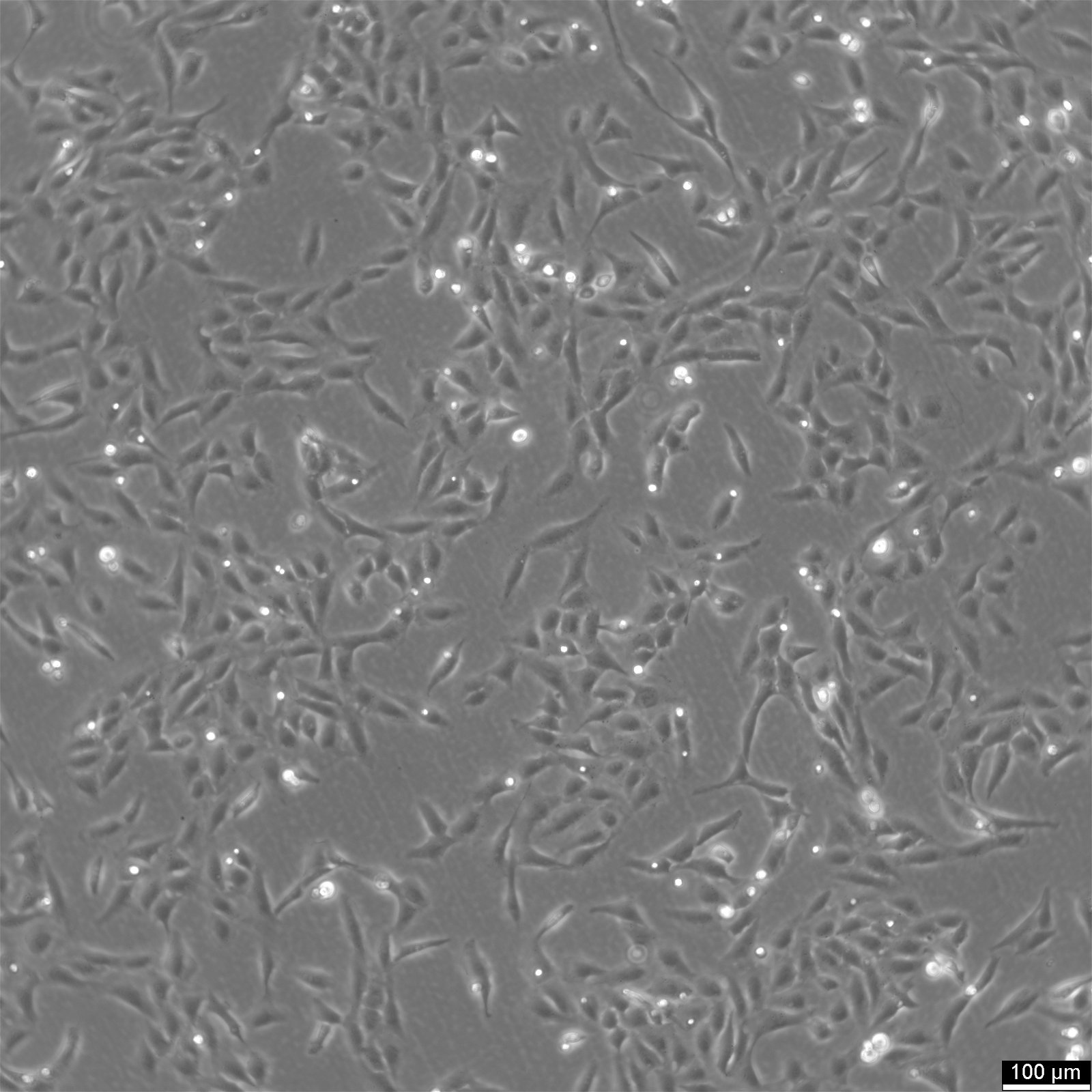
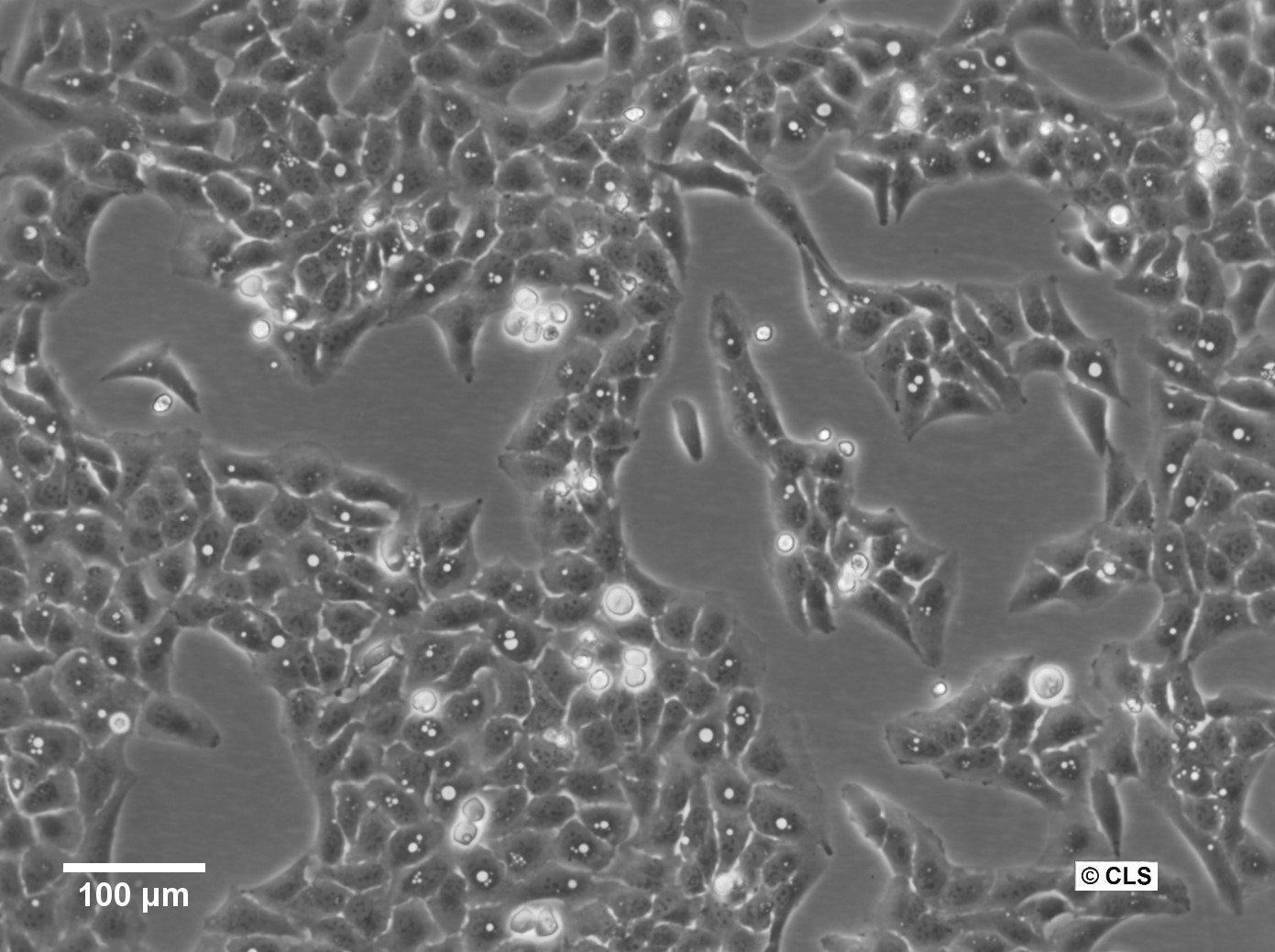
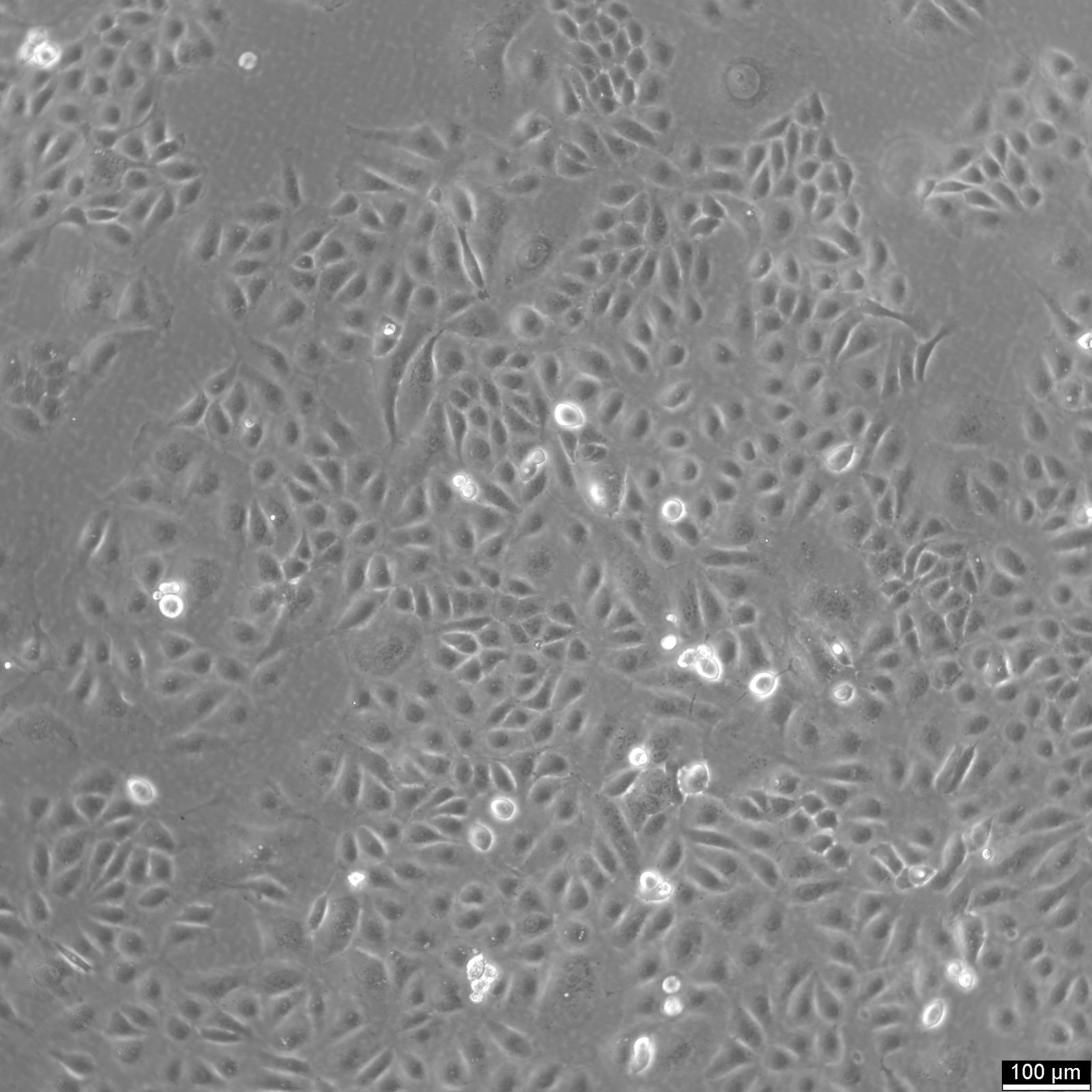
Celule U2OS-CRISPR-SNAPf-Nup358/RanBP2















800,00 EUR*
Produsele sunt expediate congelate în gheață carbonică în criotuburi. Fiecare criotub conține de obicei 3 × 10 6 celule pentru linii aderente sau 5 × 106 celule pentru linii în suspensie (consultați certificatul de analiză al lotului pentru detalii).
Informații generale
| Descriere | U2OS-CRISPR-SNAPf-Nup358/RanBP2 este o linie celulară de osteosarcom uman editată genetic, derivată din celule U2OS, în care locusul endogen RANBP2 (cunoscut și sub denumirea de NUP358) a fost modificat prin CRISPR/Cas9 pentru a codifica o etichetă SNAPf în cadru cu proteina nativă. Nup358/RanBP2 este o nucleoporină mare localizată în filamentele citoplasmatice ale complexului porilor nucleari (NPC) și joacă un rol esențial în transportul nucleocitoplasmatic, SUMOilarea și procesele mitotice. Etichetarea endogenă asigură că SNAPf-Nup358 este exprimat sub controlul promotorului fiziologic, menținând nivelurile native de expresie și minimizând artefactele asociate sistemelor de supraexpresie. Eticheta SNAPf este o variantă de etichetare rapidă a etichetei SNAP, care se leagă covalent de substraturile conjugate cu benzilguanină, permițând etichetarea fluorescentă selectivă și stabilă a Nup358 în celule vii sau fixate. În celulele U2OS-CRISPR-SNAPf-Nup358/RanBP2, proteina de fuziune se localizează în învelișul nuclear într-o distribuție punctiformă caracteristică filamentelor NPC citoplasmatice. Această configurație susține imagistica fluorescentă de înaltă rezoluție, microscopia de super-rezoluție, marcarea pulse-chase și abordările de urmărire a unei singure molecule pentru a studia arhitectura și dinamica NPC. Morfologia plată și nucleele mari ale celulelor U2OS facilitează și mai mult imagistica cantitativă a structurilor membranei nucleare. Acest model permite investigarea rolurilor specifice Nup358 în exportul nuclear dependent de CRM1/exportină, reglarea ciclului Ran GTPază și organizarea spațială a platformelor de transport citoplasmice. Având în vedere implicarea Nup358 în asamblarea fusului mitotic și funcția cinetocorului, linia celulară este, de asemenea, potrivită pentru studierea redistribuirii nucleoporinelor dependente de ciclul celular și a dezasamblării/reasamblării NPC în timpul mitozei. U2OS-CRISPR-SNAPf-Nup358/RanBP2 oferă o platformă relevantă din punct de vedere fiziologic pentru disecarea aspectelor structurale și funcționale ale feței citoplasmatice a complexului porilor nucleari din celulele umane. |
|---|---|
| Organism | Om |
| Țesut | Os |
| Boala | Osteosarcom |
Caracteristici
| Vârsta | 15 ani |
|---|---|
| Gen | Femei |
| Etnicitate | Caucazian |
| Morfologie | De tip epitelial |
| Proprietăți de creștere | Aderent |
Date de reglementare
| Mențiune | U2OS-CRISPR-SNAPf-Nup358/RanBP2 (număr de catalog Cytion 300663) |
|---|---|
| Nivelul de biosecuritate | 1 |
| NCBI_TaxID | 9606 |
| Deponent | Laboratorul Ellenberg (EMBL) |
| Statutul OMG | OMG-S1: Această linie celulară de osteosarcom uman (U2OS-CRISPR-SNAPf-Nup358/RanBP2) conține o fuziune SNAPf-Nup358/RanBP2 modificată prin CRISPR care permite marcarea precisă a fibrilelor citoplasmatice ale porului nuclear. Modificarea este integrată stabil. Această clasificare se aplică numai în Germania și poate diferi în alte țări. |
Date biomoleculare
| Expresia proteinelor | Nup358/RanBP2, SNAPf-tag |
|---|
Manipulare
| Mediu de cultură | McCoys 5a, cu: 3,0 g/L glucoză, cu: glutamină stabilă, cu: 2,0 mM piruvat de sodiu, cu: 2,2 g/L NaHCO3 (numărul articolului Cytion 820200a) |
|---|---|
| Suplimente | Suplimentați mediul cu 10% FBS, 3,0 g/L glucoză, glutamină stabilă, 2,0 mM piruvat de sodiu, 2,2 g/L NaHCO3, 1% NEAA |
| Reactiv de disociere | Accutase |
| Subcultură | Îndepărtați mediul vechi de pe celulele aderente și spălați-le cu PBS care nu conține calciu și magneziu. Pentru flacoanele T25, se utilizează 3-5 ml de PBS, iar pentru flacoanele T75, 5-10 ml. Apoi, se acoperă celulele complet cu Accutase, folosind 1-2 ml pentru flacoanele T25 și 2,5 ml pentru flacoanele T75. Lăsați celulele la incubare la temperatura camerei timp de 8-10 minute pentru a le detașa. După incubare, amestecați ușor celulele cu 10 ml de mediu pentru a le resuspenda, apoi centrifugați la 300xg timp de 3 minute. Aruncați supernatantul, resuspendați celulele în mediu proaspăt și transferați-le în flacoane noi care conțin deja mediu proaspăt. |
| Înghețați mediul | Ca mediu de crioconservare, folosim mediu de creștere complet (inclusiv FBS) + 10% DMSO pentru o viabilitate adecvată după dezghețare sau CM-1 (număr de catalog Cytion 800100), care include osmoprotectanți optimizați și stabilizatori metabolici pentru a spori recuperarea și a reduce stresul indus de criogenie. |
| Decongelarea și cultivarea celulelor |
|
| Atmosfera de incubație | 37°C, 5%CO2, atmosferă umidificată. |
| Acoperirea flaconului | Niciuna |
| Procedura de congelare | Liniile celulare crioconservate sunt expediate pe gheață carbonică în ambalaje izolate, validate, cu suficient agent frigorific pentru a menține aproximativ -78 °C pe toată durata transportului. La primire, se inspectează imediat recipientul și se transferă fără întârziere fiolele în depozitul corespunzător. |
| Condiții de expediere | Liniile celulare crioconservate sunt expediate pe gheață carbonică în ambalaje izolate, validate, cu suficient agent frigorific pentru a menține aproximativ -78 °C pe toată durata transportului. La primire, se inspectează imediat recipientul și se transferă fără întârziere fiolele în depozitul corespunzător. |
| Condiții de depozitare | Pentru conservarea pe termen lung, flacoanele se plasează în azot lichid în fază de vapori la o temperatură cuprinsă între -150 și -196 °C. Păstrarea la -80 °C este acceptabilă doar ca o scurtă etapă intermediară înainte de transferul în azot lichid. |
Controlul calității / Profil genetic / HLA
| Sterilitate | Contaminarea cu micoplasmă este exclusă utilizând atât teste bazate pe PCR, cât și metode de detectare a micoplasmei bazate pe luminescență. Pentru a se asigura că nu există contaminare bacteriană, fungică sau de drojdie, culturile celulare sunt supuse unor inspecții vizuale zilnice. |
|---|
Acordul cu terții
Vă rugăm să rețineți că această linie celulară nu este disponibilă în cadrul unui MTA Cytion standard, deoarece necesită un acord cu o terță parte și/sau face obiectul negocierii cu licențiatorul original.-
Produse necesare
Produse necesare
Mediu de congelare CM-1 - 50 mlVariante de medii de crioconservare: 50 mlMediul de congelare CM-1 de la Cytion este un mediu de crioconservare de ultimă generație, conceput pentru a asigura cel mai înalt nivel de viabilitate și funcționalitate celulară după dezghețare. Acest mediu versatil este potrivit pentru un spectru larg de tipuri de celule, inclusiv celule umane și animale, ceea ce îl face un instrument esențial pentru diverse aplicații de cercetare. Formulat cu o combinație meticulos echilibrată de crioprotectanți și nutrienți esențiali, Freeze Medium CM-1 minimizează formarea cristalelor de gheață și stresul celular în timpul procesului de congelare, păstrând astfel integritatea celulară.
Caracteristicile principale ale Freeze Medium CM-1 includ:
Compatibilitate largă: Eficient pentru o gamă largă de tipuri de celule, inclusiv celule primare, celule stem și linii celulare stabilite.
Viabilitate ridicată: Optimizat pentru a maximiza recuperarea și viabilitatea celulelor după dezghețare, asigurând rezultate experimentale fiabile.
Gata de utilizare: Preparate și sterilizate convenabil pentru aplicare imediată, reducând timpul de preparare și riscul de contaminare.
Stabilitate îmbunătățită: Menține performanța constantă în condiții standard de crioconservare, asigurând rezultate reproductibile.
Durată lungă de valabilitate: CM-1 este un mediu de crioconservare care conține ser, gata de utilizare, care poate fi păstrat în frigider timp de până la un an.
Utilizarea CM-1 pentru congelarea celulelor
Pentru a utiliza CM-1 pentru congelarea celulelor aderente și în suspensie, urmați acești pași
Pentru celulele aderente, spălați-le și disociați-le de substratul de cultură. Pentru celulele în suspensie, treceți direct la pasul următor.
Numărați celulele pentru a vă asigura că sunt la concentrația corespunzătoare.
Centrifugați celulele pentru a le granula, apoi resuspendați-le în mediul de congelare CM-1.
Transferați celulele resuspendate în crioale.
Utilizați o metodă de congelare lentă înainte de a transfera celulele pentru depozitare pe termen lung
Metodă
Descriere
Etape
❄️
Înghețarea manuală
O metodă pas cu pas care implică reducerea treptată a temperaturii pentru a asigura viabilitatea celulelor
1️⃣ Puneți celulele în mediu de congelare într-un congelator la 4°C timp de 40 de minute.
2️⃣ Se transferă la un congelator la -80°C timp de 24 de ore.
3️⃣ Depozitați celulele în azot lichid pentru conservare pe termen lung
❄️
Utilizarea Mr. Frosty
Un dispozitiv convenabil care permite ratele de congelare controlate fără energie electrică
1️⃣ Pregătiți celulele în crioale cu mediu de congelare.
2️⃣ Așezați criovialele în recipientul Mr. Frosty.
3️⃣ Păstrați la -80°C timp de 24 de ore înainte de a transfera în azot lichid
❄️
Congelator cu rată controlată
Un congelator de înaltă precizie de la Thermo Fisher sau de la alți producători conceput pentru reducerea controlată a temperaturii
1️⃣ Programați dispozitivul pentru a reduce treptat temperatura.
2️⃣ Introduceți celulele pregătite în congelator.
3️⃣ După ciclul de congelare, transferați celulele în azot lichid
Depozitați criovialele la temperaturi sub -130°C sau în azot lichid pentru conservare pe termen lung.
Ingrediente
Conține FBS, DMSO, glucoză, săruri
Capacitate de tamponare: pH = 7,2 până la 7,6
Mediul de congelare CM-1 de la Cytion oferă o soluție fiabilă pentru crioconservare, asigurând o viabilitate celulară ridicată și funcționalitate post-dezgheț pentru o gamă largă de aplicații de cercetare.59,00 EUR*Mediu McCoys 5A (modificat), w: 3,0 g/L glucoză, w: glutamină stabilă, w: 2,0 mM piruvat de sodiu, w: 2,2 g/L NaHCO3Mediumul McCoy 5A este un mediu specializat, foarte recomandat, conceput pentru a facilita creșterea și replicarea virusurilor în culturi celulare primare. Acesta a câștigat o recunoaștere semnificativă pentru performanțele sale excepționale în diverse aplicații de cercetare biologică. O aplicație importantă a mediului McCoy's 5A este utilizarea sa în cultivarea liniilor celulare de carcinom colonic uman. Mai precis, a fost utilizat în studiul receptorului cuplat la proteina G bogat în leucină (LGR5) și rolul său în metastazarea cancerului de colon. Acest mediu a fost utilizat în mod eficient în cultivarea mai multor linii celulare de carcinom de colon, inclusiv HCT116, RKO, FET, CBS, HCT116b și TENN, permițând cercetătorilor să aprofundeze mecanismele care stau la baza metastazelor cancerului de colon. Pe lângă aplicarea sa în cercetarea cancerului, mediul McCoy's 5A s-a dovedit a fi indispensabil în studiul osteoblastelor. Cercetătorii care investighează reactivitatea ionică a hidroxiapatitei cu deficit de calciu în mediile standard de cultură celulară au utilizat acest mediu pentru a cultiva osteoblaste. Această aplicație a facilitat o mai bună înțelegere a interacțiunilor dintre osteoblaste și hidroxiapatita cu deficit de calciu, contribuind la progresele în domeniul cercetării osoase. Mediumul McCoy 5A a fost formulat meticulos prin modificarea aminoacizilor din mediumul bazal Eagle pentru a oferi un suport optim celulelor tumorale hepatice. Această formulă îmbogățită îl face potrivit pentru o gamă diversă de linii celulare stabilite, precum și pentru celule primare, sporind și mai mult versatilitatea și aplicabilitatea sa în diverse contexte de cercetare. Mediumul McCoy's 5A extinde efectele sale biochimice și fiziologice dincolo de celulele tumorale hepatice. Acesta a fost utilizat cu succes pentru a susține creșterea în culturi primare de măduvă osoasă, piele, gingie, rinichi, omentum, suprarenală, plămân, splină, embrion de șobolan și alte tipuri de celule. Această gamă largă de aplicații atestă utilitatea extinsă a mediumului McCoy's 5A în susținerea creșterii și menținerii diverselor tipuri de celule pentru cercetarea biologică cuprinzătoare. Formulă Acest mediu McCoy's 5A (modificat) conține 3,0 g/L de glucoză, glutamină stabilă, 2,0 mM de piruvat de sodiu și 2,2 g/L de NaHCO3. Controlul calității pH = 7,2 +/
- 0,02 la 20-25 °C. Fiecare lot a fost testat pentru sterilitate și absența micoplasmei și bacteriilor. Întreținere A se păstra la frigider la +2 °C până la +8 °C, la întuneric. Congelarea și încălzirea până la +37 °C diminuează calitatea produsului. Nu încălziți mediul la peste 37 °C și nu utilizați surse de căldură incontrolabile (de exemplu, aparate cu microunde). Dacă se utilizează doar o parte din mediu, scoateți această cantitate din flacon și încălziți-o la temperatura camerei. Termenul de valabilitate pentru orice mediu, cu excepția mediului de bază, este de 6 până la 8 săptămâni de la data deschiderii. Compoziție Componente mg/L Săruri anorganiceClorură de calciu x 2H2O132,00 Sulfat de magneziu97,67 Clorură de potasiu400 Clorură de sodiu6.460 Hidrogen fosfat disodic (anhidru)504,00 Alte componenteD(+)-Glucoză (anhidră)3.000 Glutation (redus)0,5 Peptone din carne600,00 Sare de sodiu fenol roșu11 AminoaciziL-alanină13,3 L-arginina x HCl42,14 L-asparagină x H2O45,03 Acid L-aspartic19,97 L-Cisteină x HCl x H2O31,75 L-glutamină (stabilă)219,15 Acid L-glutamic22,07 Glicină7,51 L-histidină x HCl x H2O20,96 L-hidroxiprolină19,67 L-izoleucină39,3 L-leucină39,36 L-lizină x HCl36,54 L-metionină14,92 L-fenilalanină16,52 L-Prolină17,27 L-serină26,28 L-treonină17,87 L-triptofan3,06 Sare disodică de L-tirozină26,10 L-valină17,57 VitamineAcid p-aminobenzoic1 Acid ascorbic0,56 D(+)-Biotină0,2 D-pantotenat de calciu0,2 Clorură de colină5 Acid folic10 Mio-inozitol36 Nicotinamidă0,5 Acid nicotinic0,5 Clorhidrat de piridoxal0,5 Clorhidrat de piridoxină0,5 Riboflavină0,2 Tiamină HCl0 Vitamina B122,030,00 EUR*AccutaseVariante: 100 mlReactiv de disociere celulară Accutase
- o alternativă delicată la tripsină
Accutase este o soluție de disociere celulară care revoluționează industria culturilor celulare. Este un amestec de enzime proteolitice și colagenolitice care imită acțiunea tripsinei și a colagenazei. Spre deosebire de tripsină, Accutase nu conține componente de mamifere sau bacteriene și este mult mai blândă cu celulele, ceea ce o face o soluție ideală pentru detașarea de rutină a celulelor de pe materialele plastice standard pentru cultura țesuturilor și de pe materialele plastice acoperite cu aderență. În această postare pe blog, vom explora beneficiile și utilizările Accutase și modul în care acesta schimbă regulile jocului în cultura celulară.
Avantajele Accutase
Accutase are mai multe avantaje față de soluțiile tradiționale de tripsină. În primul rând, poate fi utilizat ori de câte ori este necesară detașarea blândă și eficientă a oricărei linii de celule aderente, ceea ce îl face un înlocuitor direct al tripsinei. În al doilea rând, Accutase funcționează extrem de bine pe celulele stem embrionare și neuronale și s-a demonstrat că menține viabilitatea acestor celule după transfer. În al treilea rând, Accutase păstrează majoritatea epitopilor pentru analiza citometrică în flux ulterioară, ceea ce o face ideală pentru analiza markerilor de suprafață celulară.
În plus, Accutase nu trebuie să fie neutralizat la trecerea celulelor aderente. Adăugarea mai multor medii după divizarea celulelor diluează Accutase astfel încât acesta nu mai este capabil să detașeze celulele. Acest lucru elimină necesitatea unei etape de inactivare și economisește timp pentru tehnicienii de culturi celulare. În cele din urmă, Accutase nu trebuie să fie alicotat, iar un flacon este stabil în frigider timp de 2 luni.
Aplicații ale Accutase
Accutase este un înlocuitor direct pentru soluția de tripsină și poate fi utilizat pentru trecerea liniilor celulare. În plus, Accutase funcționează bine la detașarea celulelor pentru analiza multor markeri de suprafață celulară prin citometrie în flux și pentru sortarea celulelor. Alte aplicații în aval ale tratamentului cu Accutase includ analiza markerilor de suprafață celulară, testul de creștere a virusurilor, proliferarea celulară, testele de migrare a celulelor tumorale, trecerea celulară de rutină, creșterea producției (bioreactor) și citometria în flux.
Compoziția Accutase
Accutase nu conține componente mamifere sau bacteriene și este un amestec enzimatic natural cu activitate enzimatică proteolitică și colagenolitică. Este formulat la o concentrație mult mai mică decât tripsina și colagenaza, ceea ce îl face mai puțin toxic și mai blând, dar la fel de eficient.
Eficiența Accutase
Accutase s-a dovedit a fi eficient în detașarea celulelor primare și stem și menținerea unei viabilități celulare ridicate în comparație cu enzimele de origine animală, cum ar fi tripsina. 100% din celule sunt recuperate după 10 minute și nu există niciun rău în lăsarea celulelor în Accutase timp de până la 45 de minute, datorită autodigestionării Accutase.
În concluzie
În concluzie, Accutase este o soluție puternică care schimbă regulile jocului în cultura celulară. Cu natura sa blândă, eficiența și versatilitatea sa, Accutase este alternativa ideală la tripsină. Dacă sunteți în căutarea unei soluții fiabile și eficiente pentru detașarea celulelor, Accutase este soluția pentru dumneavoastră.75,00 EUR*Soluție antibiotică/antimicotică (100x)Prezentare generală a produsului
Volum: 100 ml Depozitare: ≤-15°C Sterilitate: Steril-filtrat
Antibiotic/Antimicotic Solution (100x) este un concentrat steril, gata de utilizare, conceput pentru a reduce riscurile de contaminare microbiană în culturile celulare și în aplicațiile de laborator conexe. Această soluție 100x conține o combinație bine stabilită de penicilină, streptomicină și amfotericină B
- care asigură o activitate antimicrobiană cu spectru larg împotriva bacteriilor Gram-pozitive și Gram-negative, drojdiilor și ciupercilor filamentoase. Formularea este adecvată pentru utilizarea în culturi de celule eucariote, medii bacteriene și alte sisteme sensibile la contaminare, sprijinind operațiunile de laborator curate și consecvente.
Aplicație și beneficii Optimizată pentru protocoalele de cercetare de rutină, această soluție este utilizată pe scară largă pentru menținerea condițiilor aseptice în fluxurile de lucru din culturile celulare. Aceasta oferă performanțe fiabile în medii sensibile la contaminare, ajutând cercetătorii să reducă riscul de creștere microbiană excesivă fără a compromite sănătatea celulelor sau reproductibilitatea experimentelor. Formularea filtrată steril elimină necesitatea unor etape suplimentare de solubilizare, susținând pregătirea raționalizată a mediilor și reducând variabilitatea procedurilor zilnice de laborator.
Utilizare și compatibilitate Pentru a obține concentrații de lucru standard, diluați soluția 1:100 în mediul de cultură complet. Produsul este compatibil cu o gamă largă de linii celulare de mamifere și medii bazale. Datorită disponibilității constante a stocurilor, cercetătorii beneficiază de o continuitate fiabilă a aprovizionării și de o planificare logistică simplificată. Soluția trebuie depozitată la ≤ -15 °C și protejată de cicluri repetate de îngheț-dezgheț pentru a menține stabilitatea. Numai pentru utilizare în cercetare. A nu se utiliza în proceduri diagnostice sau terapeutice. Nu se utilizează la om sau la animale.45,00 EUR*PBSSoluție salină tamponată cu fosfat (PBS)
Soluția salină tamponată cu fosfat (PBS) este o soluție tampon utilizată pe scară largă în cercetarea biologică și chimică. Aceasta joacă un rol crucial în menținerea echilibrului pH-ului și a osmolarității în timpul diferitelor proceduri experimentale, inclusiv prelucrarea țesuturilor și cultura celulară. Soluția noastră PBS este formulată meticulos cu ingrediente de înaltă puritate pentru a asigura stabilitatea și fiabilitatea în fiecare experiment. Osmolaritatea și concentrațiile de ioni ale soluției noastre PBS le imită îndeaproape pe cele ale corpului uman, făcând-o izotonică și netoxică pentru majoritatea celulelor.
Compoziția soluției noastre PBS
Soluția noastră PBS este un amestec cu pH ajustat de soluții tampon fosfat de calitate ultrapură și soluții saline. La o concentrație de lucru 1X, aceasta conține:
8000 mg/L clorură de sodiu (NaCl)
200 mg/L Clorură de potasiu (KCl)
1150 mg/L Fosfat de sodiu dibazic anhidru (Na2HPO4)
200 mg/L Fosfat de potasiu monobazic anhidru (KH2PO4)
Această compoziție asigură un pH optim și un echilibru ionic, adecvat pentru o gamă largă de aplicații biologice.
Aplicații ale soluției noastre PBS
Soluția noastră PBS este ideală pentru diverse aplicații în cercetarea biologică. Proprietățile sale izotonice și non-toxice o fac potrivită pentru diluarea substanțelor și clătirea recipientelor pentru celule. Soluțiile PBS care conțin EDTA sunt eficiente pentru desprinderea celulelor atașate și grupate. Cu toate acestea, metalele divalente, cum ar fi zincul, nu trebuie adăugate în PBS, deoarece pot provoca precipitații. În astfel de cazuri, sunt recomandate tampoanele Good. În plus, soluția noastră PBS este o alternativă acceptabilă la mediul de transport viral pentru transportul și depozitarea virușilor ARN, inclusiv SARS-CoV-2.
Controlul calității
Steril-filtrat
Depozitare și termen de valabilitate
A se păstra la +2°C până la +25°C, ferit de lumină.
Odată deschis, depozitați la o temperatură cuprinsă între 2°C și 25°C și utilizați în termen de 24 de luni.
Condiții de transport
Temperatură ambiantă
Întreținere
Păstrați la frigider la +2°C până la +8°C, în întuneric. Evitați înghețarea și încălzirea frecventă la +37°C, deoarece reduce calitatea produsului.
Nu încălziți mediul peste 37°C și nu utilizați surse de căldură necontrolate, cum ar fi aparatele cu microunde.
În cazul în care urmează să se utilizeze doar o parte din mediu, se îndepărtează cantitatea necesară și se încălzește la temperatura camerei înainte de utilizare.
Compoziție
Categoria
Componente
Concentrație (mg/L)
Săruri
Clorură de potasiu
200
Fosfat de potasiu monobazic anhidru
200
Clorură de sodiu
8000
Fosfat de sodiu dibazic anhidru
115020,00 EUR* -
Produse conexe
Produse conexe