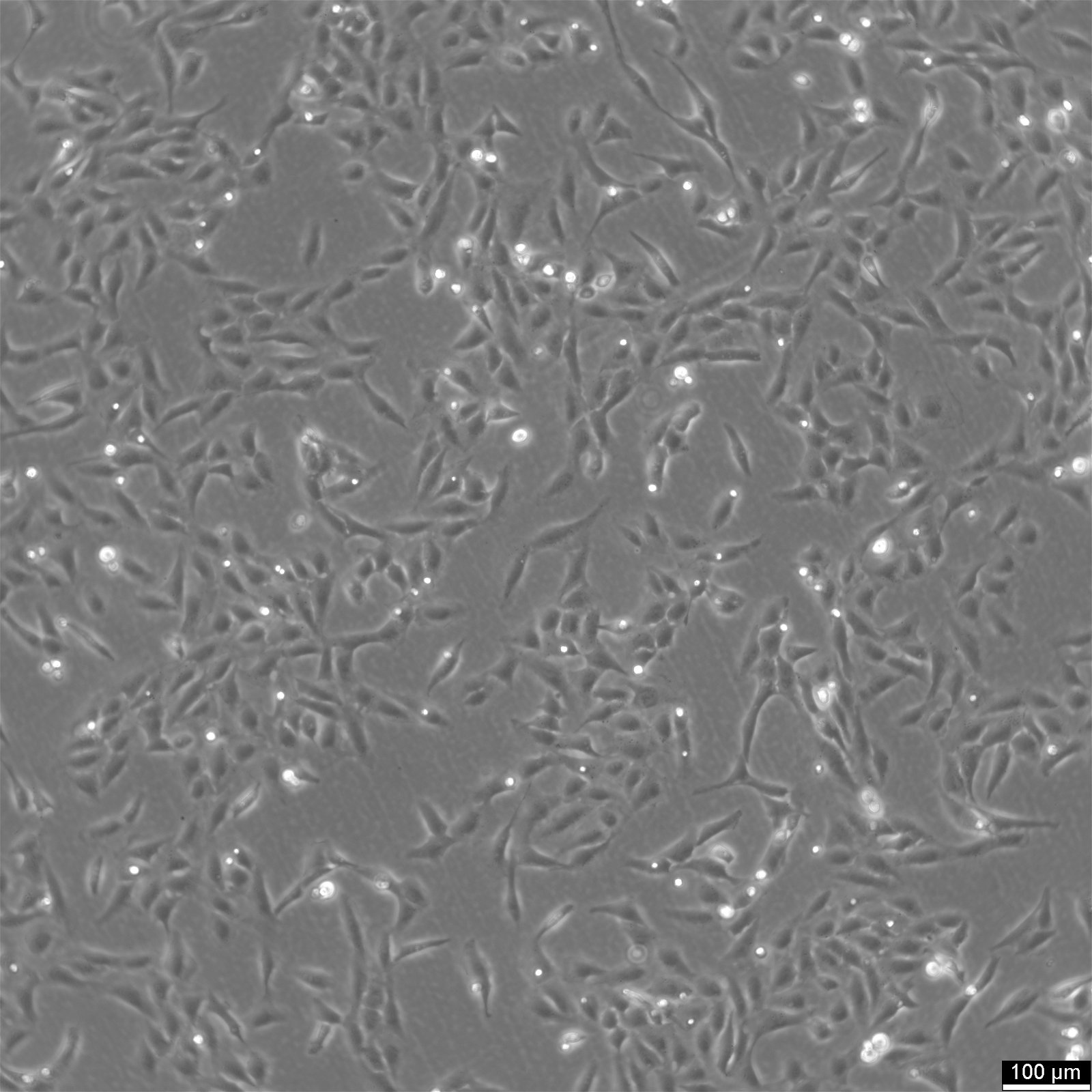
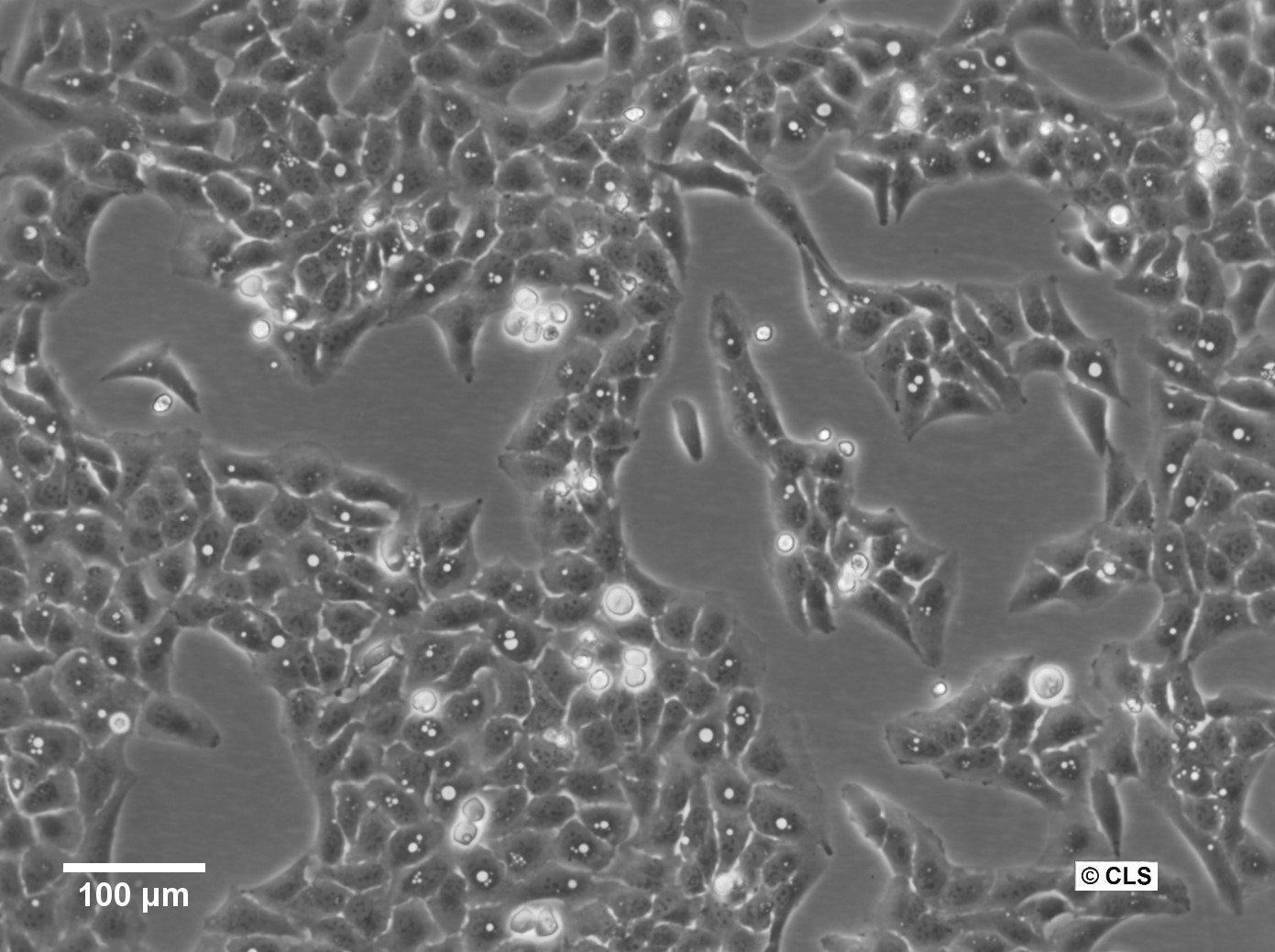
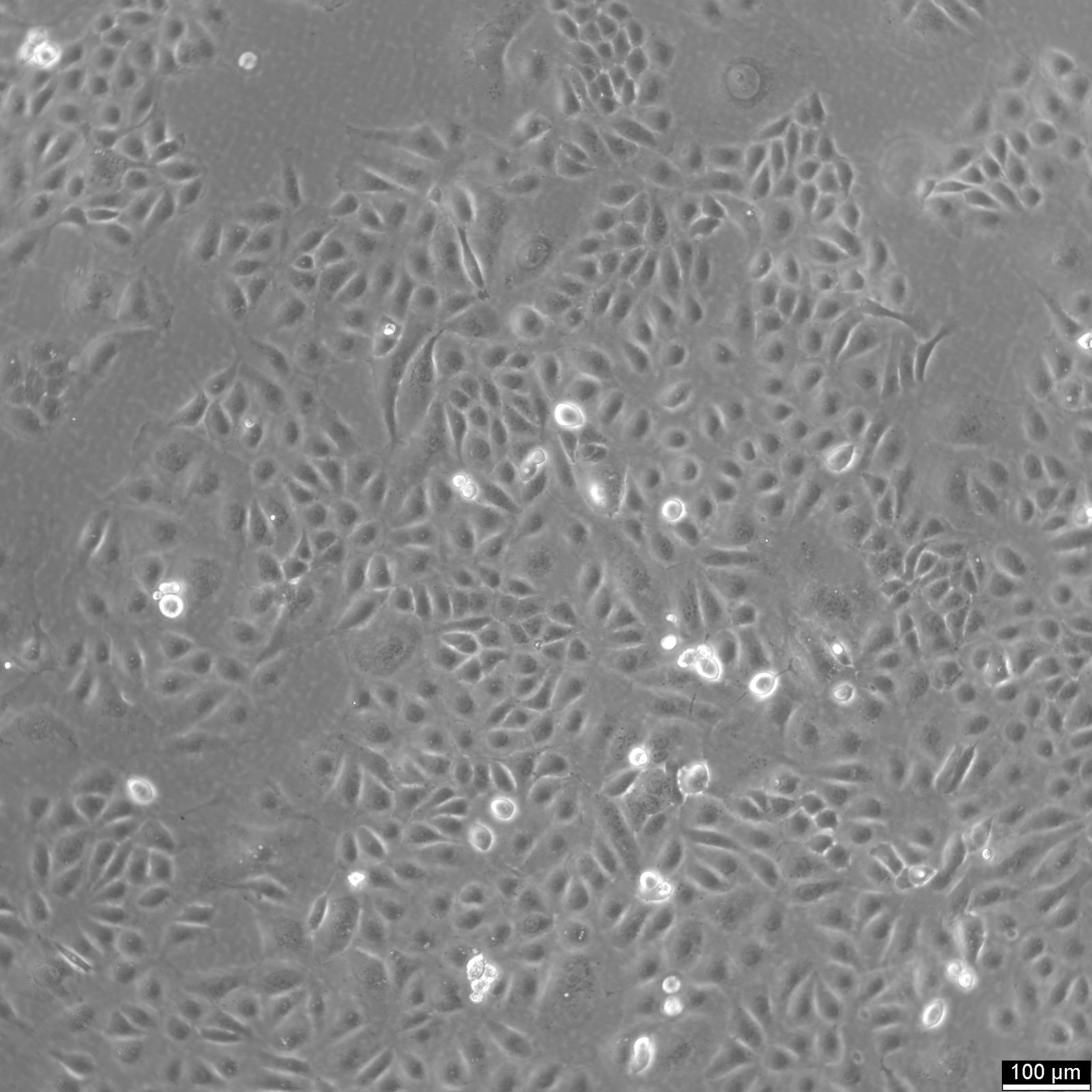
Komórki U2OS-CRISPR-SNAPf-Nup358/RanBP2















800,00 €*
Produkty są wysyłane w stanie zamrożonym w suchym lodzie w probówkach kriogenicznych. Każda probówka kriogeniczna zawiera zazwyczaj 3 × 10 6 komórek dla linii adhezyjnych lub 5 × 106 komórek dla linii zawiesinowych (szczegółowe informacje znajdują się w certyfikacie analizy partii).
Informacje ogólne
| Opis | U2OS-CRISPR-SNAPf-Nup358/RanBP2 to zmodyfikowana genetycznie linia komórek ludzkiego osteosarcoma pochodząca z komórek U2OS, w której endogenny locus RANBP2 (znany również jako NUP358) został zmodyfikowany za pomocą CRISPR/Cas9 w celu kodowania tagu SNAPf w ramce z natywnym białkiem. Nup358/RanBP2 jest dużym nukleoporinem zlokalizowanym w cytoplazmatycznych włóknach kompleksu porów jądrowych (NPC) i odgrywa kluczową rolę w transporcie jądrowo-cytoplazmatycznym, SUMOylacji i procesach mitotycznych. Endogeniczne znakowanie zapewnia, że SNAPf-Nup358 jest wyrażany pod fizjologiczną kontrolą promotora, utrzymując natywne poziomy ekspresji i minimalizując artefakty związane z systemami nadekspresji. Tag SNAPf jest szybko znakującym wariantem tagu SNAP, który kowalencyjnie wiąże substraty sprzężone z benzyloguaniną, umożliwiając selektywne i stabilne znakowanie fluorescencyjne Nup358 w żywych lub utrwalonych komórkach. W komórkach U2OS-CRISPR-SNAPf-Nup358/RanBP2 białko fuzyjne lokalizuje się w otoczce jądra komórkowego w postaci punktowej dystrybucji charakterystycznej dla cytoplazmatycznych włókien NPC. Taka konfiguracja umożliwia obrazowanie fluorescencyjne w wysokiej rozdzielczości, mikroskopię superrozdzielczą, znakowanie metodą pulse-chase oraz śledzenie pojedynczych cząsteczek w celu badania architektury i dynamiki NPC. Płaska morfologia i duże jądra komórek U2OS dodatkowo ułatwiają ilościowe obrazowanie struktur błony jądrowej. Model ten umożliwia badanie specyficznych ról Nup358 w eksporcie jądrowym zależnym od CRM1/eksportyny, regulacji cyklu Ran GTPazy oraz organizacji przestrzennej cytoplazmatycznych platform transportowych. Biorąc pod uwagę udział Nup358 w tworzeniu wrzeciona mitotycznego i funkcji kinetochoru, linia komórkowa nadaje się również do badania zależnej od cyklu komórkowego redystrybucji nukleoporin oraz rozkładu/ponownego składania NPC podczas mitozy. U2OS-CRISPR-SNAPf-Nup358/RanBP2 stanowi fizjologicznie istotną platformę do analizy strukturalnych i funkcjonalnych aspektów cytoplazmatycznej powierzchni kompleksu porów jądrowych w komórkach ludzkich. |
|---|---|
| Organizm | Człowiek |
| Tkanka | Kość |
| Choroba | Mięsak kościopochodny |
Charakterystyka
| Wiek | 15 lat |
|---|---|
| Płeć | Kobieta |
| Pochodzenie etniczne | Kaukaski |
| Morfologia | Podobny do nabłonka |
| Właściwości wzrostu | Adherent |
Dane regulacyjne
| Cytat | U2OS-CRISPR-SNAPf-Nup358/RanBP2 (numer katalogowy Cytion 300663) |
|---|---|
| Poziom bezpieczeństwa biologicznego | 1 |
| NCBI_TaxID | 9606 |
| Deponent | Laboratorium Ellenberg (EMBL) |
| Status GMO | GMO-S1: Ta ludzka linia komórek kostniakomięsaka (U2OS-CRISPR-SNAPf-Nup358/RanBP2) zawiera zmodyfikowaną metodą CRISPR fuzję SNAPf-Nup358/RanBP2 umożliwiającą precyzyjne znakowanie cytoplazmatycznych włókienek porów jądrowych. Modyfikacja jest stabilnie zintegrowana. Ta klasyfikacja ma zastosowanie tylko w Niemczech i może się różnić w innych krajach. |
Dane biomolekularne
| Ekspresja białka | Nup358/RanBP2, tag SNAPf |
|---|
Obsługa
| Podłoże hodowlane | McCoys 5a, w: 3,0 g/l glukozy, w: stabilna glutamina, w: 2,0 mM pirogronianu sodu, w: 2,2 g/l NaHCO3 (numer artykułu Cytion 820200a) |
|---|---|
| Suplementy | Uzupełnić pożywkę o 10% FBS, 3,0 g/l glukozy, stabilną glutaminę, 2,0 mM pirogronianu sodu, 2,2 g/l NaHCO3, 1% NEAA |
| Odczynnik dysocjacyjny | Accutase |
| Subkultury | Usuń starą pożywkę z przylegających komórek i przemyj je PBS, który nie zawiera wapnia i magnezu. W przypadku kolb T25 należy użyć 3-5 ml PBS, a w przypadku kolb T75 5-10 ml. Następnie całkowicie pokryj komórki Accutase, używając 1-2 ml dla kolb T25 i 2,5 ml dla kolb T75. Pozwól komórkom inkubować w temperaturze pokojowej przez 8-10 minut, aby je oddzielić. Po inkubacji delikatnie wymieszaj komórki z 10 ml pożywki, aby ponownie je zawiesić, a następnie odwiruj przy 300xg przez 3 minuty. Odrzucić supernatant, ponownie zawiesić komórki w świeżej pożywce i przenieść je do nowych kolb zawierających już świeżą pożywkę. |
| Środek zamrażający | Jako pożywki do kriokonserwacji używamy kompletnej pożywki wzrostowej (w tym FBS) + 10% DMSO w celu zapewnienia odpowiedniej żywotności po rozmrożeniu lub CM-1 (numer katalogowy Cytion 800100), która zawiera zoptymalizowane osmoprotektanty i stabilizatory metaboliczne w celu zwiększenia regeneracji i zmniejszenia stresu wywołanego kriokonserwacją. |
| Rozmrażanie i hodowla komórek |
|
| Atmosfera inkubacji | 37°C, 5%CO2, nawilżona atmosfera. |
| Powłoka kolby | Brak |
| Procedura zamrażania | Linie komórkowe poddane kriokonserwacji są wysyłane w suchym lodzie w zatwierdzonych, izolowanych opakowaniach z wystarczającą ilością czynnika chłodniczego, aby utrzymać temperaturę około -78°C przez cały czas transportu. Po otrzymaniu przesyłki należy natychmiast sprawdzić pojemnik i bezzwłocznie przenieść fiolki do odpowiedniego miejsca przechowywania. |
| Warunki wysyłki | Linie komórkowe poddane kriokonserwacji są wysyłane w suchym lodzie w zatwierdzonych, izolowanych opakowaniach z wystarczającą ilością czynnika chłodniczego, aby utrzymać temperaturę około -78°C przez cały czas transportu. Po otrzymaniu przesyłki należy natychmiast sprawdzić pojemnik i bezzwłocznie przenieść fiolki do odpowiedniego miejsca przechowywania. |
| Warunki przechowywania | W celu długotrwałego przechowywania należy umieścić fiolki w ciekłym azocie w fazie lotnej w temperaturze od -150 do -196 °C. Przechowywanie w temperaturze -80 °C jest dopuszczalne tylko jako krótki etap przejściowy przed przeniesieniem do ciekłego azotu. |
Kontrola jakości / Profil genetyczny / HLA
| Sterylność | Zanieczyszczenie mykoplazmą jest wykluczane przy użyciu zarówno testów opartych na PCR, jak i metod wykrywania mykoplazmy opartych na luminescencji. Aby upewnić się, że nie ma zanieczyszczenia bakteriami, grzybami lub drożdżami, hodowle komórkowe są poddawane codziennym kontrolom wizualnym. |
|---|
Umowa ze stroną trzecią
Należy pamiętać, że ta linia komórkowa nie jest dostępna w ramach standardowej umowy Cytion MTA, ponieważ wymaga umowy z osobą trzecią i/lub podlega negocjacjom z pierwotnym licencjodawcą.-
Wymagane produkty
Wymagane produkty
Medium zamrażające CM-1 - 50 mlWarianty nośników do kriokonserwacji: 50 mlCytion's Freeze Medium CM-1 to najnowocześniejsza pożywka do kriokonserwacji zaprojektowana w celu zapewnienia najwyższego poziomu żywotności i funkcjonalności komórek po rozmrożeniu. Ta wszechstronna pożywka jest odpowiednia dla szerokiego spektrum typów komórek, w tym zarówno ludzkich, jak i zwierzęcych, co czyni ją niezbędnym narzędziem do różnorodnych zastosowań badawczych. Dzięki starannie zbilansowanej kombinacji krioprotektantów i niezbędnych składników odżywczych, Freeze Medium CM-1 minimalizuje tworzenie się kryształków lodu i stres komórkowy podczas procesu zamrażania, zachowując w ten sposób integralność komórek.
Kluczowe cechy Freeze Medium CM-1 obejmują:
Szeroka kompatybilność: Skuteczny dla szerokiej gamy typów komórek, w tym komórek pierwotnych, komórek macierzystych i ustalonych linii komórkowych.
Wysoka żywotność: Zoptymalizowany w celu maksymalizacji odzysku i żywotności komórek po rozmrożeniu, zapewniając wiarygodne wyniki eksperymentów.
Gotowy do użycia: Wygodnie przygotowany i wysterylizowany do natychmiastowego zastosowania, skracając czas przygotowania i zmniejszając ryzyko zanieczyszczenia.
Zwiększona stabilność: Utrzymuje stałą wydajność w standardowych warunkach kriokonserwacji, zapewniając powtarzalne wyniki.
Długi okres trwałości: CM-1 to zawierająca surowicę, gotowa do użycia pożywka do kriokonserwacji, którą można przechowywać w lodówce przez okres do jednego roku.
Używanie CM-1 do zamrażania komórek
Aby użyć CM-1 do zamrażania zarówno komórek adherentnych, jak i zawiesinowych, należy wykonać następujące kroki
W przypadku komórek przylegających należy je umyć i oddzielić od podłoża hodowlanego. W przypadku komórek w zawiesinie przejdź bezpośrednio do następnego kroku.
Policzyć komórki, aby upewnić się, że mają odpowiednie stężenie.
Odwirować komórki, aby je osuszyć, a następnie ponownie zawiesić w pożywce do zamrażania CM-1.
Przenieś ponownie zawieszone komórki do fiolek.
Użyj metody powolnego zamrażania przed przeniesieniem komórek do długoterminowego przechowywania
Metoda
Opis
Kroki
❄️
Ręczne zamrażanie
Metoda krok po kroku polegająca na stopniowym obniżaniu temperatury w celu zapewnienia żywotności komórek
1️⃣ Umieścić komórki w pożywce do zamrażania w temperaturze 4°C na 40 minut.
2️⃣ Przenieść do zamrażarki o temperaturze -80°C na 24 godziny.
3️⃣ Przechowywać komórki w ciekłym azocie w celu długotrwałego przechowywania
❄️
Korzystanie z Mr. Frosty
Wygodne urządzenie umożliwiające kontrolowane zamrażanie bez zasilania elektrycznego
1️⃣ Przygotować komórki w kriofiolach z pożywką do zamrażania.
2️⃣ Umieścić kriofiole w pojemniku Mr. Frosty.
3️⃣ Przechowywać w temperaturze -80°C przez 24 godziny przed przeniesieniem do ciekłego azotu
❄️
Zamrażarka o kontrolowanej prędkości
Precyzyjna zamrażarka firmy Thermo Fisher lub innych producentów przeznaczona do kontrolowanego obniżania temperatury
1️⃣ Zaprogramuj urządzenie tak, aby stopniowo obniżało temperaturę.
2️⃣ Umieść przygotowane komórki w zamrażarce.
3️⃣ Po cyklu zamrażania przenieś komórki do ciekłego azotu
Przechowywać kriofiole w temperaturze poniżej -130°C lub w ciekłym azocie w celu długotrwałego przechowywania.
Składniki
Zawiera FBS, DMSO, glukozę, sole
Zdolność buforowania: pH = 7,2 do 7,6
Cytion's Freeze Medium CM-1 oferuje niezawodne rozwiązanie do kriokonserwacji, zapewniając wysoką żywotność komórek i funkcjonalność po rozmrożeniu w szerokim zakresie zastosowań badawczych.59,00 €*Podłoże McCoys 5A (zmodyfikowane), w: 3,0 g/l glukozy, w: stabilna glutamina, w: 2,0 mM pirogronianu sodu, w: 2,2 g/l NaHCO3Pożywka McCoy's 5A Medium jest wysoce zalecaną i wyspecjalizowaną pożywką przeznaczoną do ułatwiania wzrostu i replikacji wirusów w pierwotnych hodowlach komórkowych. Zyskała ona znaczące uznanie dzięki swojej wyjątkowej skuteczności w różnych zastosowaniach badawczych w dziedzinie biologii. Jednym z najważniejszych zastosowań pożywki McCoy's 5A jest hodowla ludzkich linii komórkowych raka jelita grubego. W szczególności została ona wykorzystana w badaniach nad receptorem sprzężonym z białkiem G zawierającym powtórzenia bogate w leucynę (LGR5) i jego rolą w przerzutach raka jelita grubego. Pożywka ta została skutecznie wykorzystana w hodowli kilku linii komórek raka jelita grubego, w tym HCT116, RKO, FET, CBS, HCT116b i TENN, umożliwiając badaczom głębsze zgłębienie mechanizmów leżących u podstaw przerzutów raka jelita grubego. Oprócz zastosowania w badaniach nad rakiem, pożywka McCoy's 5A okazała się nieodzowna w badaniach nad osteoblastami. Naukowcy badający reaktywność jonową hydroksyapatytu z niedoborem wapnia w standardowych pożywkach do hodowli komórek wykorzystali tę pożywkę do hodowli osteoblastów. Zastosowanie to ułatwiło lepsze zrozumienie interakcji między osteoblastami a hydroksyapatytem z niedoborem wapnia, przyczyniając się do postępów w dziedzinie badań nad kościami. Pożywka McCoy's 5A została starannie opracowana poprzez modyfikację aminokwasów występujących w pożywce Basal Medium Eagle, aby zapewnić optymalne wsparcie dla komórek nowotworowych wątroby. Ta wzbogacona formuła sprawia, że pożywka nadaje się do stosowania w różnych ustalonych liniach komórkowych, a także w komórkach pierwotnych, co dodatkowo zwiększa jej wszechstronność i przydatność w różnych warunkach badawczych. McCoy's 5A Medium rozszerza swoje działanie biochemiczne i fizjologiczne poza komórki nowotworowe wątroby. Zostało z powodzeniem zastosowane do wspierania wzrostu w pierwotnych hodowlach szpiku kostnego, skóry, dziąseł, nerek, sieci, nadnerczy, płuc, śledziony, embrionów szczurów i innych typów komórek. Tak szeroki zakres zastosowań świadczy o dużej użyteczności McCoy's 5A Medium we wspieraniu wzrostu i utrzymania różnych typów komórek w kompleksowych badaniach biologicznych. Skład Pożywka McCoy's 5A (zmodyfikowana) zawiera 3,0 g/l glukozy, stabilną glutaminę, 2,0 mM pirogronianu sodu i 2,2 g/l NaHCO3. Kontrola jakości pH = 7,2 +/
- 0,02 w temperaturze 20-25°C. Każda partia została przetestowana pod kątem sterylności oraz braku mykoplazmy i bakterii. Przechowywanie Przechowywać w lodówce w temperaturze od +2°C do +8°C, w ciemnym miejscu. Zamrażanie i ogrzewanie do temperatury +37°C obniża jakość produktu. Nie należy podgrzewać pożywki do temperatury powyżej 37°C ani stosować niekontrolowanych źródeł ciepła (np. kuchenek mikrofalowych). Jeśli ma być użyta tylko część pożywki, należy wyjąć tę ilość z butelki i ogrzać ją w temperaturze pokojowej. Okres przydatności do użycia dla wszystkich pożywek z wyjątkiem pożywki podstawowej wynosi od 6 do 8 tygodni od daty otwarcia. Skład Składniki mg/l Sole nieorganiczneChlorek wapnia x 2H2O132,00 Siarczan magnezu97,67 Chlorek potasu400,00 Chlorek sodu6460 Wodorofosforan disodowy (bezwodny)504,00 Inne składnikiD(+)-glukoza (bezwodna)3000 Glutation (zredukowany)0,5 Pepton mięsny600,00 Sól sodowa fenoloftaleiny11 AminokwasyL-alanina13,36 L-arginina x HCl42,14 L-asparagina x H2O45,03 Kwas L-asparaginowy19,97 L-cysteina x HCl x H2O31,75 L-glutamina (stabilna)219,15 Kwas L-glutaminowy22,07 Glicyna7,51 L-histydyna x HCl x H2O20,96 L-hydroksyprolina19,67 L-izoleucyna39,36 L-leucyna39,36 L-lizyna x HCl36,54 L-metionina14,92 L-fenyloalanina16,52 L-prolina17,27 L-seryna26,28 L-treonina17,87 L-tryptofan3,06 Sól disodowa L-tyrozyny26,10 L-walina17,57 WitaminyKwas p-aminobenzoesowy1,0 Kwas askorbinowy0,56 D(+)-biotyna0,20 D-pantotenian wapnia0,2 Chlorek choliny5,0 Kwas foliowy10 Mio-inozytol36,00 Nikotynamid0,5 Kwas nikotynowy0,5 Chlorowodorek pirydoksalu0,50 Chlorowodorek pirydoksyny0,50 Ryboflawina0,2 Chlorowodorek tiaminy0,2 Witamina B122,0030,00 €*AccutaseWarianty: 100 mlOdczynnik do dysocjacji komórek Accutase
- delikatna alternatywa dla trypsyny
Accutase to roztwór do odłączania komórek, który rewolucjonizuje przemysł hodowli komórkowych. Jest to mieszanka enzymów proteolitycznych i kolagenolitycznych, która naśladuje działanie trypsyny i kolagenazy. W przeciwieństwie do trypsyny, Accutase nie zawiera żadnych składników pochodzących od ssaków lub bakterii i jest znacznie łagodniejszy dla komórek, co czyni go idealnym rozwiązaniem do rutynowego odłączania komórek od standardowych naczyń plastikowych do hodowli tkankowych i naczyń plastikowych pokrytych powłoką adhezyjną. W tym wpisie na blogu omówimy zalety i zastosowania Accutase oraz sposób, w jaki zmienia ona zasady gry w hodowli komórkowej.
Zalety Accutase
Accutase ma kilka zalet w porównaniu z tradycyjnymi roztworami trypsyny. Po pierwsze, może być stosowana wszędzie tam, gdzie potrzebne jest delikatne i skuteczne oderwanie dowolnej przylegającej linii komórkowej, co czyni ją bezpośrednim zamiennikiem trypsyny. Po drugie, Accutase działa wyjątkowo dobrze na embrionalnych i neuronalnych komórkach macierzystych i wykazano, że utrzymuje żywotność tych komórek po pasażowaniu. Po trzecie, Accutase zachowuje większość epitopów do późniejszej analizy cytometrii przepływowej, co czyni ją idealną do analizy markerów powierzchniowych komórek.
Dodatkowo, Accutase nie musi być neutralizowana podczas pasażowania przylegających komórek. Dodanie większej ilości pożywki po rozdzieleniu komórek rozcieńcza Accutase tak, że nie jest już w stanie oddzielić komórek. Eliminuje to potrzebę etapu inaktywacji i oszczędza czas techników zajmujących się hodowlą komórek. Wreszcie, Accutase nie musi być dzielona na porcje, a butelka jest stabilna w lodówce przez 2 miesiące.
Zastosowania Accutazy
Accutase jest bezpośrednim zamiennikiem roztworu trypsyny i może być stosowany do pasażowania linii komórkowych. Ponadto, Accutase dobrze sprawdza się podczas odłączania komórek w celu analizy wielu markerów powierzchniowych komórek za pomocą cytometrii przepływowej i sortowania komórek. Inne zastosowania Accutase obejmują analizę markerów powierzchniowych komórek, test wzrostu wirusa, proliferację komórek, testy migracji komórek nowotworowych, rutynowe pasażowanie komórek, zwiększanie skali produkcji (bioreaktor) i cytometrię przepływową.
Skład Accutazy
Accutase nie zawiera składników pochodzących od ssaków lub bakterii i jest naturalną mieszaniną enzymów o aktywności proteolitycznej i kolagenolitycznej. Jest formułowany w znacznie niższym stężeniu niż trypsyna i kolagenaza, dzięki czemu jest mniej toksyczny i łagodniejszy, ale równie skuteczny.
Skuteczność Accutase
Wykazano, że Accutase jest skuteczny w odłączaniu komórek pierwotnych i macierzystych oraz utrzymuje wysoką żywotność komórek w porównaniu z enzymami pochodzenia zwierzęcego, takimi jak trypsyna. 100% komórek jest odzyskiwanych po 10 minutach, a pozostawienie komórek w Accutase do 45 minut nie jest szkodliwe, dzięki automatycznemu trawieniu Accutase.
Podsumowanie
Podsumowując, Accutase to potężne rozwiązanie, które zmienia zasady gry w hodowli komórkowej. Dzięki swojej łagodności, wydajności i wszechstronności, Accutase jest idealną alternatywą dla trypsyny. Jeśli szukasz niezawodnego i wydajnego rozwiązania do odłączania komórek, Accutase jest rozwiązaniem dla Ciebie.75,00 €*Roztwór antybiotyku/przeciwgrzybiczy (100x)Przegląd produktów
Pojemność: 100 ml Przechowywanie: ≤-15°C Sterylność: Sterylnie filtrowany
Antibiotic/Antimycotic Solution (100x) to sterylny, gotowy do użycia koncentrat zaprojektowany w celu zmniejszenia ryzyka skażenia mikrobiologicznego w hodowli komórkowej i powiązanych zastosowaniach laboratoryjnych. Roztwór 100x zawiera dobrze znane połączenie penicyliny, streptomycyny i amfoterycyny B, zapewniając szerokie spektrum działania przeciwdrobnoustrojowego przeciwko bakteriom Gram-dodatnim i Gram-ujemnym, drożdżom i grzybom nitkowatym. Preparat nadaje się do stosowania w hodowlach komórek eukariotycznych, pożywkach bakteryjnych i innych systemach wrażliwych na zanieczyszczenia, wspierając czyste i spójne operacje laboratoryjne.
Zastosowanie i korzyści Rozwiązanie to, zoptymalizowane pod kątem rutynowych protokołów badawczych, jest szeroko stosowane do utrzymywania aseptycznych warunków w procesach hodowli komórkowych. Zapewnia niezawodne działanie w środowiskach wrażliwych na zanieczyszczenia, pomagając naukowcom zmniejszyć ryzyko przerostu drobnoustrojów bez uszczerbku dla zdrowia komórek lub powtarzalności eksperymentów. Sterylnie filtrowana formuła eliminuje potrzebę dodatkowych etapów solubilizacji, wspierając usprawnione przygotowanie mediów i zmniejszając zmienność w codziennych procedurach laboratoryjnych.
Zastosowanie i kompatybilność Aby uzyskać standardowe stężenia robocze, należy rozcieńczyć roztwór w stosunku 1:100 w pełnym podłożu hodowlanym. Produkt jest kompatybilny z szeroką gamą linii komórkowych ssaków i pożywek podstawowych. Dzięki stałej dostępności produktu, badacze mogą korzystać z niezawodnej ciągłości dostaw i uproszczonego planowania logistycznego. Roztwór należy przechowywać w temperaturze ≤ -15 °C i chronić przed powtarzającymi się cyklami zamrażania i rozmrażania w celu zachowania stabilności. Wyłącznie do użytku badawczego. Nie stosować w procedurach diagnostycznych lub terapeutycznych. Nie stosować u ludzi ani zwierząt.45,00 €*PBSRoztwór soli fizjologicznej buforowanej fosforanami (PBS)
Sól fizjologiczna buforowana fosforanami (PBS) jest szeroko stosowanym roztworem buforowym w badaniach biologicznych i chemicznych. Odgrywa kluczową rolę w utrzymywaniu równowagi pH i osmolarności podczas różnych procedur eksperymentalnych, w tym przetwarzania tkanek i hodowli komórkowej. Nasz roztwór PBS jest starannie opracowany ze składników o wysokiej czystości, aby zapewnić stabilność i niezawodność w każdym eksperymencie. Osmolarność i stężenia jonów naszego PBS ściśle naśladują te występujące w ludzkim organizmie, dzięki czemu jest on izotoniczny i nietoksyczny dla większości komórek.
Skład naszego roztworu PBS
Nasz roztwór PBS to dostosowana pod względem pH mieszanka ultraczystych buforów fosforanowych i roztworów soli fizjologicznej. W stężeniu roboczym 1X zawiera:
8000 mg/l chlorku sodu (NaCl)
200 mg/l chlorku potasu (KCl)
1150 mg/L Bezwodny dwuzasadowy fosforan sodu (Na2HPO4)
200 mg/L Fosforan potasu jednozasadowy bezwodny (KH2PO4)
Taki skład zapewnia optymalne pH i równowagę jonową, odpowiednie do szerokiego zakresu zastosowań biologicznych.
Zastosowania naszego roztworu PBS
Nasz roztwór PBS jest idealny do różnych zastosowań w badaniach biologicznych. Jego izotoniczne i nietoksyczne właściwości sprawiają, że nadaje się do rozcieńczania substancji i płukania pojemników z komórkami. Roztwory PBS zawierające EDTA są skuteczne w odłączaniu przyczepionych i zbrylonych komórek. Do PBS nie należy jednak dodawać metali dwuwartościowych, takich jak cynk, ponieważ może to spowodować wytrącanie się osadów. W takich przypadkach zalecane są bufory Good's. Ponadto nasz roztwór PBS jest akceptowalną alternatywą dla wirusowego podłoża transportowego do transportu i przechowywania wirusów RNA, w tym SARS-CoV-2.
Kontrola jakości
Sterylnie filtrowany
Przechowywanie i okres trwałości
Przechowywać w temperaturze od +2°C do +25°C, chronić przed światłem.
Po otwarciu przechowywać w temperaturze od 2°C do 25°C i zużyć w ciągu 24 miesięcy.
Warunki wysyłki
Temperatura otoczenia
Konserwacja
Przechowywać w lodówce w temperaturze od +2°C do +8°C w ciemności. Unikać zamrażania i częstego podgrzewania do temperatury +37°C, ponieważ obniża to jakość produktu.
Nie podgrzewać nośnika powyżej 37°C ani nie używać niekontrolowanych źródeł ciepła, takich jak urządzenia mikrofalowe.
Jeśli ma być użyta tylko część pożywki, należy usunąć wymaganą ilość i ogrzać ją do temperatury pokojowej przed użyciem.
Skład
Kategoria
Składniki
Stężenie (mg/L)
Sole
Chlorek potasu
200
Fosforan potasu jednozasadowy bezwodny
200
Chlorek sodu
8000
Bezwodny dwuzasadowy fosforan sodu
115020,00 €* -
Powiązane produkty
Powiązane produkty
Komórki U2OS-CRISPR-NUP96-mEGFPOrganizm Człowiek Tkanka Kość Choroba Mięsak kościopochodny 800,00 €*Komórki U2OS-CRISPR-NUP96-SNAPOrganizm Człowiek Tkanka Kość Choroba Mięsak kościopochodny 800,00 €*Komórki U2OS-CRISPR-NUP96-HaloOrganizm Człowiek Tkanka Kość Choroba Mięsak kościopochodny 800,00 €*Komórki U2OS-CRISPR-NUP96-mMapleOrganizm Człowiek Tkanka Kość Choroba Mięsak kościopochodny 800,00 €*Komórki U2OS-CRISPR-SNAPf-SEH1Organizm Człowiek Tkanka Kość Choroba Mięsak kościopochodny 800,00 €*Komórki U2OS-CRISPR-SNAPf-Nup133Organizm Człowiek Tkanka Kość Choroba Mięsak kościopochodny 800,00 €*