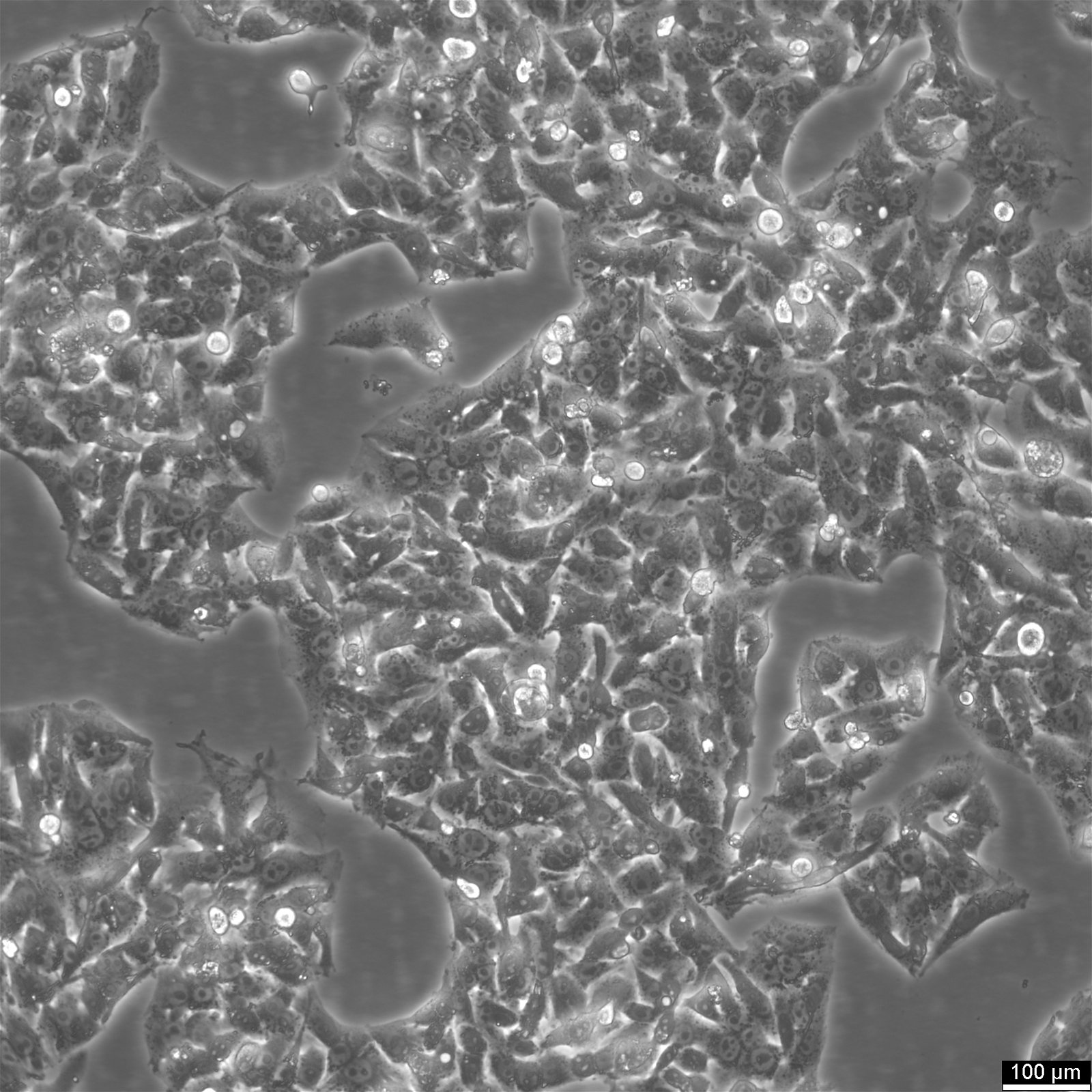
HepG2-cellen - een bron voor onderzoek naar leverkanker
Hep-G2 is een menselijke leverkankercellijn afkomstig van het leverweefsel van een 15-jarige blanke man met hepatocellulair carcinoom. Deze cellen worden vaak gebruikt in onderzoeken naar medicijnmetabolisme en hepatotoxiciteit. Hoewel HepG2-cellen een hoge proliferatiesnelheid hebben en er epitheelachtig uitzien, zijn ze niet tumorigeen en vervullen ze verschillende gedifferentieerde leverfuncties. In 1975 leidden onderzoekers HepG2-cellen af van hepatocellulair carcinoom, waardoor het de eerste levercellijn werd die de kritieke kenmerken van hepatocyten vertoonde. In tegenstelling tot de eerder ontwikkelde SK-Hep1 cellijn, die essentiële levercelmarkers mist, kunnen HepG2 cellen verschillende plasma-eiwitten afscheiden en vormen ze een waardevol model voor het bestuderen van de intracellulaire dynamica van celoppervlaktedomeinen in menselijke hepatocyten. Deze cellen vertonen een epitheliale morfologie, hebben een modaal chromosoomnummer van 55 en kunnen worden gestimuleerd met menselijk groeihormoon
HepG2 Kenmerken
Primaire hepatocyten hebben een typische kubusvorm en bevatten meestal twee kernen. HepG2-cellen daarentegen hebben een epitheelachtige morfologie met een enkele kern en een aantal chromosomen variërend van 48 tot 54 per cel. Hoewel HepG2-cellen tot 25% van het totale cellulaire eiwit kunnen bevatten, zijn ze groter dan normale hepatocyten en bevatten ze ongeveer 10% van het complete eiwit in de cel. Celproteïnen zijn cruciale actoren in de cel die de functies uitvoeren die door genen zijn gespecificeerd.
Tumorcellen, inclusief cellen met een abnormaal aantal chromosomen, vertonen vaak een toename van het aantal kernen, tot wel zeven per cel. Door hun hoge mate van differentiatie in vitro vormen HepG2-cellen een ideaal model voor het bestuderen van de intracellulaire handel en dynamica van galkanaal- en sinusoïdale membraaneiwitten en lipiden in menselijke hepatocyten.
De gemiddelde diameter van een HepG2-cel is ongeveer 10-20 µm, wat kleiner is dan een hepatocyt met een diameter van 15 µm, maar vergelijkbaar met tumorcellen van Hepatoblastoma (HB), die variëren van 10-20 µm.
HepG2 genetica
De Hep-G2 cellijn vertoont verschillende translocaties, waaronder die tussen de korte armen van chromosomen 1 en 21, trisomieën van chromosomen 2, 16 en 17, en tetrasomieën van chromosoom 20. Het verlies van de chromosoom 4q3 regio wordt ook waargenomen, geassocieerd met translocatie t(1;4) vaak gezien in hepatoblastoom (HB) en andere chromosomale afwijkingen, zoals trisomieën 2 en 20. Het aantal chromosomen in HepG2-cellen varieert van 50 tot 60, wat duidt op een hyperdiploïd karyotype, terwijl sommige gevallen meer dan 100 chromosomen vertonen en gekenmerkt worden door een tetraploïde vergroting. HepG2-cellen bevatten ongeveer 7,5 pg DNA, 15% meer dan een gemiddelde somatische cel. Ter vergelijking: primaire hepatocyten hebben een kubusvormige celvorm en bevatten meestal twee kernen [1].
Mutatieprofiel van HepG2-cellen
De HepG2-cellijn draagt de TERT-promoterregio-mutatie C228T, die ook voorkomt in hepatocellulair carcinoom (HCC) en hepatoblastoom (HB). Deze mutatie draagt bij aan immortalisatie door telomeren in kankercellen te beschermen. Daarnaast vertonen HepG2-cellen wild-type TP53, een cruciaal gen voor het onderdrukken van kanker bij de mens, omdat het een rol speelt bij celcyclusstilstand, apoptose en veroudering. Mutaties in dit gen kunnen de celdeling bevorderen.
HepG2 cellen nemen deel aan verschillende pathways, waaronder ontregeling van celgroei, overlevingspathways zoals foetaal en embryonaal HB, en de Wnt/β-catenine pathway. Bovendien heeft de cellijn een karakteristieke deletie van het derde exon van het CTNNB1-gen, die identiek is aan die in epitheliaal type HB [2,3].
Overzicht van HepG2 hepatocellulaire carcinoomcellen in leveronderzoek
HepG2-cellen, afkomstig van humaan hepatoma, zijn van onschatbare waarde geworden voor onderzoek naar leverfuncties en -ziekten, waaronder hepatocellulair carcinoom. Deze levercellijnen geven inzicht in de cellulaire reacties van menselijke hepatocyten onder verschillende experimentele omstandigheden. Het gebruik van luciferase reporterplasmiden in HepG2-cellen is bijzonder effectief gebleken voor het volgen van genexpressie en cellulaire transfecties, die fundamenteel zijn voor metabolisch onderzoek, zoals het onderzoek naar de effecten van ethanol op levercellen
Studies naar virale infecties en leverziekten met HepG2-cellen
Geïmmortaliseerde levertumorcellijnen zoals HepG2 en Huh7 zijn essentieel voor het bestuderen van virale infecties, omdat ze volledige celcyclusreplicatie van hepatitis D (HDV) en expressie van hepatitis B (HBV) aantonen [5,6]. Daarnaast spelen HepaRG-cellijnen een cruciale rol bij het ophelderen van HBV-invoermechanismen [7]. HepG2-cellen worden ook gebruikt om een verscheidenheid aan menselijke leverziekten te onderzoeken, van genetische aandoeningen zoals progressieve familiaire intrahepatische cholestase (PFIC) en het Dubin-Johnson-syndroom tot milieu- en voedingsstudies met betrekking tot cytotoxische en genotoxische agentia, en bij onderzoek naar de doelgerichtheid van geneesmiddelen en hepatocarcinogenese [8,9]. Het gebruik ervan strekt zich uit tot proeven met bio-kunstmatige leverapparaten
Interacties van HepG2-cellen met biomaterialen in weefselmanipulatie
De interactie van HepG2-cellen met verschillende biomaterialen is van cruciaal belang bij tissue engineering. Technieken zoals de colloïdale sondetechniek helpen deze interacties te begrijpen door het meten van celadhesie-eigenschappen, die van vitaal belang zijn bij het bepalen van de levensvatbaarheid van cellen voor de ontwikkeling van scaffolds en nauwkeurige leverweefselmodellen
Celgedrag en innovaties in op HepG2 gebaseerde modellen
Het bestuderen van celgedrag in HepG2-gebaseerde modellen is cruciaal voor onderzoek naar leverziekten. Vooruitgang in driedimensionale sferoïde celculturen heeft geleid tot de creatie van HepG2-celsferoïden, die een fysiologisch relevanter model bieden dat normale hepatocyten goed benadert. Deze 3D-modellen, met verhoogde metabolische activiteit, wijzen op het potentieel van HepG2-cellen om te dienen als model voor hepatoblastoom en zijn belangrijk voor kankerbehandelingsonderzoek, vooral voor het simuleren van levertumoren en het testen van nieuwe therapeutische benaderingen [10-12]
Vergelijking en kenmerken van HepG2 onder andere tumorcellijnen
HepG2 is een van de meest gebruikte levertumor cellijnen, geselecteerd voor zijn brede toepassingen in wetenschappelijk onderzoek onder de ongeveer 40 beschikbare levertumor cellijnen [13]. Ondanks de zwakke of afwezige expressie van bepaalde cytochroom P450-enzymen in vergelijking met normale hepatocyten, heeft het metabole profiel van HepG2 de inspanningen gestimuleerd om de cellijn aan te passen voor betere studies naar het metabolisme van geneesmiddelen [13]. Vergeleken met tumorcellijnen als MCF7, PC3, 143B en HEK293 vertonen HepG2-cellen unieke aminozuurprofielen die de eiwitsynthese en secretie aanzienlijk beïnvloeden, wat hun unieke metabolische routes benadrukt [14]
Onderzoek naar leverziekten met HepG2
Subculturen van HepG2-cellen
Hier volgen vijf stappen voor het verwijderen van adherente cellen uit celkweekflessen met Accutase:
- Verwijder het medium uit de celkweekfles en spoel de aanhangende cellen met PBS zonder calcium en magnesium. Gebruik 3-5 ml PBS voor T25-flesjes en 5-10 ml voor T75-flesjes.
- Voeg Accutase toe aan de celkweekkolf, met 1-2 ml per T25-kolf en 2,5 ml per T75-kolf. Zorg ervoor dat de Accutase het hele celblad bedekt.
- Incubeer de kolf gedurende 8-10 minuten bij kamertemperatuur.
- Resuspendeer de cellen voorzichtig met medium met behulp van 10 ml vers medium.
- Centrifugeer de geresuspendeerde cellen 5 minuten bij 300xg, resuspendeer ze in vers medium en breng ze over in nieuwe kolven met vers medium.
Toekomstperspectieven voor HepG2-cellen
De zoektocht naar het ontsluiten van het volledige potentieel van de HepG2 cellijn gaat verder met baanbrekende vooruitgang in het verhogen van de expressie van cytochromen. Onderzoekers onderzoeken ook de mogelijkheid van driedimensionale sferoïde celculturen, die een fysiologisch relevanter systeem bieden. De metabolische activiteit, inclusief cytochromen, is opmerkelijk hoger in 3D sferoïdale HepG2-modellen dan in 2D-cellen, wat ons dichter bij het creëren van een model brengt dat normale hepatocyten weerspiegelt. Daarnaast kan het onderzoeken van de dynamische processen die ten grondslag liggen aan de onjuiste distributie van celoppervlakteleiwitten de weg vrijmaken voor een beter begrip van leverziekten
HepG2-cellen: Hun rol en verschillen in biomedisch onderzoek begrijpen - FAQs
Referenties
- Vyas, R.C., Darroudi, F., Natarajan, A.T. Radiation-induced chromosomal breakage and rejoining in interphase-metaphase chromosomes of human lymphocytes, Mutat Res, 1991; 249(1):29-35.
- Woodfield, S.E., Shi, Y., Patel, R.H., Chen, Z., Shah, A.P., Srivastava, R.K., Whitlock, R.S., Ibarra, A.M., Larson, S.R., Sarabia, S.F., et al. MDM4 Inhibition: A Novel Therapeutic Strategy to Reactivate P53 in Hepatoblastoma. Sci. Rep. 2021, 11, 2967.
- Hussain, S.P., Schwank, J., Staib, F., Wang, X.W., Harris, C.C. TP53 Mutations and hepatocellular Carcinoma: Insights into the Etiology and Pathogenesis of Liver Cancer. Oncogene 2004.
- Schicht, G., Seidemann, L., Haensel, R., Seehofer, D., Damm, G. Critical Investigation of the Usability of Hepatoma Cell Lines HepG2 and Huh7 as Models for the Metabolic Representation of Resectable Hepatocellular Carcinoma. Cancers 2022, 14(17), 4227.
- Verrier, E.R., Colpitts, C.C., Schuster, C., Zeisel, M.B., Baumert, T.F. Cell Culture Models for the Investigation of Hepatitis B and D Virus Infection. Virussen 2016, 8, 261.
- Verrier, E.R., Colpitts, C.C., Bach, C., Heydmann, L., Weiss, A., Renaud, M., Durand, S.C., Habersetzer, F., Durantel, D., AbouJaoudé, G., et al. A Targeted Functional RNA Interference screen Uncovers Glypican 5 as an Entry Factor for Hepatitis B and D Viruses. Hepatology 2016, 63, 35-48.
- Gripon, P., Rumin, S., Urban, S., Le Seyec, J., Glaise, D., Cannie, I., Guyomard, C., Lucas, J., Trepo, C., Guguen-Guillouzo, C. Infection of a Human Hepatoma Cell Line by Hepatitis B Virus. Proc. Natl. Acad. Sci. USA 2002, 99, 15655-15660.
- Mersch-Sundermann, V., Knasmüller, S., Wu, X.J., Darroudi, F., Kassie, F. Use of a human-derived liver cell line for the detection of cytoprotective, antigenotoxic and cogenotoxic agents. Toxicology. 2004; 198(1-3): 329-340.
- Fanelli, A. HepG2 (leverhepatocellulair carcinoom): celkweek. HepG2. Op 3 december 2017 ontsloten.
- Xuan, J., Chen, S., Ning, B., Tolleson, W.H., Guo, L. Development of HepG2-Derived Cells Expressing Cytochrome P450s for Assessing Metabolism-Associated Drug-Induced Liver Toxicity. Physiol. Behav. 2017, 176, 139-148.
- Ooka, M., Lynch, C., Xia, M. Application of in Vitro Metabolism Activation in High-Throughput Screening. Int. J. Mol. Sci. 2020, 21, 8182.
- Huang, L., Coughtrie, M.W.H., Hsu, H. Down-Regulation of Dehydroepiandrosterone Sulfotransferase Gene in Human Hepatocellular Carcinoma. Mol. Cell. Endocrinol.
- Zhu, Z., Hao, X., Yan, M., et al. Cancer stem/progenitor cells are highly enriched in CD133 + CD44 + population in hepatocellular carcinoma. Int J Cancer. 2010; 126:2067-2078.
- Arbus, C., Benyamina, A., Llorca, P.-M., Baylé, F., Bromet, N., Massiere, F., Garay, R.P., Hameg, A. Characterization of human cytochrome P450 enzymes involved in the metabolism of cyamemazine. Eur J Pharm Sci. 2007 Dec;32(4-5):357-66.