HepG2-solut - maksasyövän tutkimusresurssi
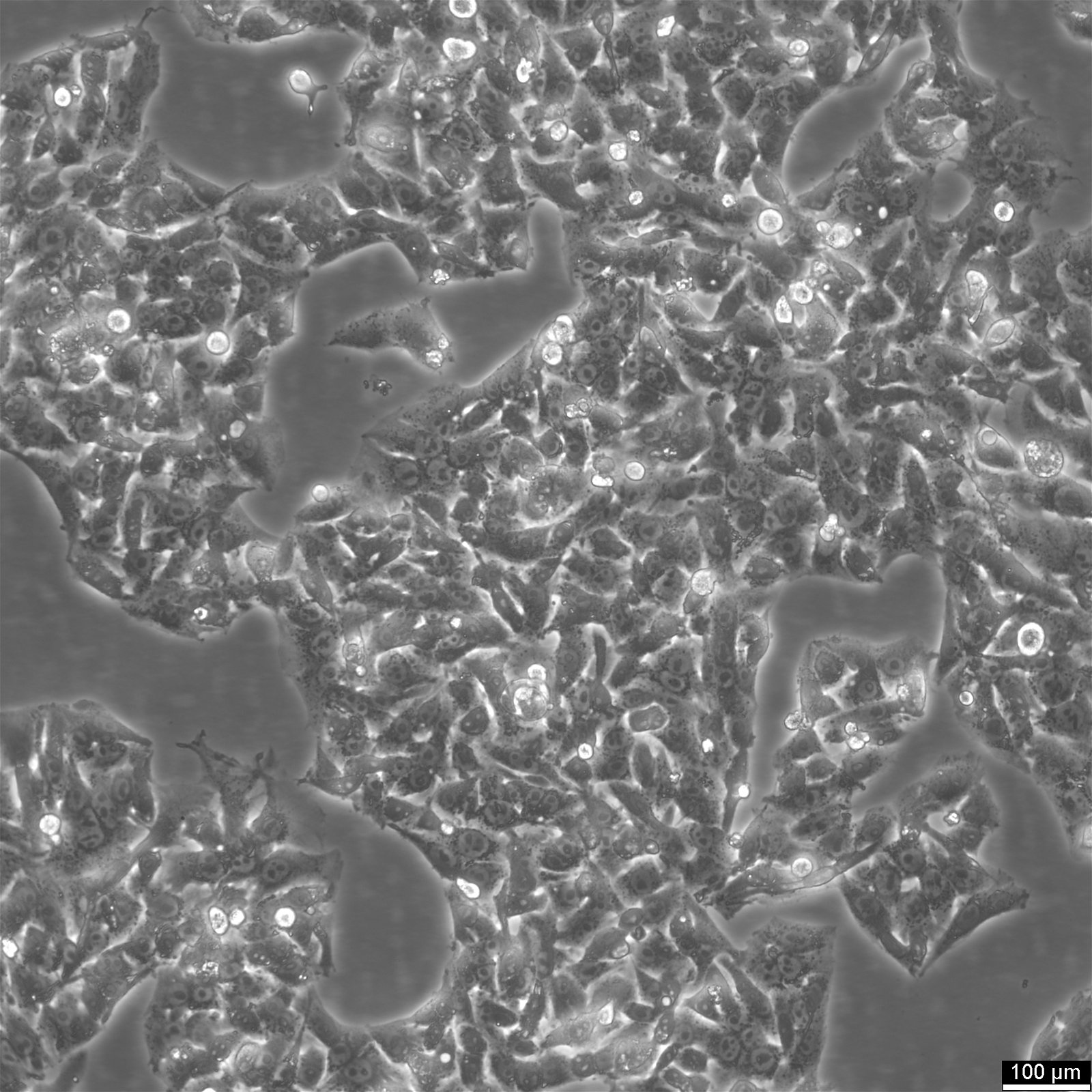
Hep-G2 on ihmisen maksasyöpäsolulinja, joka on peräisin 15-vuotiaan valkoihoisen miehen maksakudoksesta, jolla oli maksasolusyöpä. Näitä soluja käytetään usein lääkkeiden metaboliaa ja maksatoksisuutta koskevissa tutkimuksissa. Vaikka HepG2-soluilla on korkea proliferaatiovauhti ja epiteelin kaltainen ulkonäkö, ne eivät ole kasvainvaarallisia ja suorittavat erilaisia erilaistuneita maksan toimintoja. Vuonna 1975 tutkijat saivat HepG2-soluja hepatosellulaarisesta karsinoomasta, mikä teki siitä ensimmäisen maksasolulinjan, jolla oli hepatosyyttien kriittiset ominaisuudet. Toisin kuin aiemmin vakiintunut SK-Hep1-solulinja, josta puuttuvat olennaiset maksasolujen merkkiaineet, HepG2-solut pystyvät erittämään erilaisia plasmaproteiineja ja tarjoavat arvokkaan mallin solunsisäisten solupintadomeenien dynamiikan tutkimiseen ihmisen hepatosyyteissä. Näillä soluilla on epiteelin kaltainen morfologia, niiden modaalinen kromosomimäärä on 55 ja niitä voidaan stimuloida ihmisen kasvuhormonilla.
HepG2 Ominaisuudet
Primaaristen hepatosyyttien tyypillinen muoto on kuutiomainen, ja niissä on yleensä kaksi ydintä. Sen sijaan HepG2-soluilla on epiteelin kaltainen morfologia, yksi tuma ja kromosomimäärä 48-54 solua kohti. Vaikka HepG2-solujen osuus solun kokonaisproteiinista voi olla jopa 25 %, niiden koko on suurempi kuin normaalien hepatosyyttien, ja niiden osuus on noin 10 % solun koko proteiinista. Soluproteiinit ovat solun kriittisiä toimijoita, jotka suorittavat geenien määrittelemiä toimintoja.
Kasvainsoluissa, mukaan lukien solut, joissa on epänormaali määrä kromosomeja, on usein enemmän tumia, jopa seitsemän solua kohti. Koska HepG2-solut ovat hyvin erilaistuneita in vitro, ne ovat ihanteellinen malli ihmisen hepatosyyttien sappitiehyiden, sinusoidaalisten kalvoproteiinien ja lipidien solunsisäisen liikkumisen ja dynamiikan tutkimiseen.
HepG2-solun keskimääräinen läpimitta on noin 10-20 µm, mikä on pienempi kuin hepatosyytin, jonka läpimitta on 15 µm, mutta samanlainen kuin hepatoblastooman (HB) kasvainsolujen, joiden läpimitta on 10-20 µm.
HepG2:n genetiikka
Hep-G2-solulinjalla on useita translokaatioita, mukaan lukien kromosomien 1 ja 21 lyhyiden varsien väliset translokaatiot, kromosomien 2, 16 ja 17 trisomiat ja kromosomin 20 tetrasomia. Havaitaan myös kromosomin 4q3 alueen häviämistä, mikä liittyy translokaatioon t(1;4), joka esiintyy usein hepatoblastoomassa (HB), ja muihin kromosomipoikkeavuuksiin, kuten trisomioihin 2 ja 20. Kromosomien lukumäärä HepG2-soluissa vaihtelee 50-60 välillä, mikä viittaa hyperdiploidiseen karyotyyppiin, kun taas joissakin tapauksissa kromosomeja on yli 100, ja niille on ominaista tetraploidinen laajentuminen. HepG2-solut sisältävät noin 7,5 pg DNA:ta, mikä on 15 prosenttia enemmän kuin keskimääräinen somaattinen solu. Vertailun vuoksi primaariset hepatosyytit ovat kuutiomaisia ja sisältävät tyypillisesti kaksi ydintä [1].
HepG2-solujen mutaatioprofiili
HepG2-solulinjassa on TERT-promoottorin alueen mutaatio C228T, jota esiintyy myös hepatosellulaarisessa karsinoomassa (HCC) ja hepatoblastoomassa (HB). Tämä mutaatio edistää kuolemattomuutta suojaamalla telomeerejä syöpäsoluissa. Lisäksi HepG2-soluissa esiintyy villiä TP53-tyyppiä, joka on kriittinen geeni ihmisen syövän tukahduttamisen kannalta, koska sillä on rooli solusyklin pysähtymisessä, apoptoosissa ja ikääntymisessä. Tämän geenin mutaatiot voivat edistää solujen lisääntymistä.
HepG2-solut osallistuvat useisiin polkuihin, kuten solukasvun säätelyhäiriöihin, eloonjäämispolkuihin, kuten sikiön ja alkion HB:hen, ja Wnt/β-kateniinipolkuun. Lisäksi solulinjalla on tyypillinen CTNNB1-geenin kolmannen eksonin deleetio, joka on identtinen epiteelityyppisessä HB:ssä esiintyvän deleetion kanssa [2,3].
Yleiskatsaus HepG2-hepatosellulaarisista karsinoomasoluista maksatutkimuksessa
Ihmisen hepatoomasta peräisin olevista HepG2-soluista on tullut korvaamaton väline maksan toimintojen ja sairauksien, kuten hepatosellulaarisen karsinooman, tutkimiseen. Nämä maksasolulinjat tarjoavat tietoa ihmisen hepatosyyttien soluvasteista erilaisissa koeolosuhteissa. Luciferaasi-reporttiplasmidien käyttö HepG2-soluissa on ollut erityisen tehokasta geeniekspression ja solutransfektioiden seurannassa, jotka ovat keskeisiä aineenvaihduntatutkimuksessa, kuten etanolin vaikutusten tutkimisessa maksasoluihin
Virusinfektioita ja maksasairauksia koskevat tutkimukset HepG2-soluja käyttäen
Immortalisoidut maksan kasvainsolulinjat, kuten HepG2 ja Huh7, ovat olennaisia virusinfektioiden tutkimisessa, sillä ne osoittavat hepatiitti D:n (HDV) täydellisen solusyklin replikaation ja hepatiitti B:n (HBV) ilmentymisen [5,6]. Samanaikaisesti HepaRG-solulinjoilla on ratkaiseva rooli HBV:n sisäänpääsymekanismien selvittämisessä [7]. HepG2-soluja käytetään myös erilaisten ihmisen maksasairauksien tutkimiseen, alkaen geneettisistä tiloista, kuten progressiivisesta familiaalisesta intrahepaattisesta kolestaasista (PFIC) ja Dubin-Johnsonin oireyhtymästä, sytotoksisiin ja genotoksisiin aineisiin liittyviin ympäristö- ja ravintotutkimuksiin sekä lääkkeiden kohdentamiseen ja hepatokarsinogeneesin tutkimiseen [8,9]. Niiden käyttö ulottuu myös bioteknisillä maksalaitteilla tehtäviin kokeisiin
HepG2-solujen ja biomateriaalien vuorovaikutukset kudostekniikassa
HepG2-solujen vuorovaikutus erilaisten biomateriaalien kanssa on keskeistä kudostekniikassa. Tekniikat, kuten kolloidinen anturitekniikka, auttavat ymmärtämään näitä vuorovaikutuksia mittaamalla solujen tarttumisominaisuuksia, jotka ovat elintärkeitä solujen elinkelpoisuuden määrittämisessä telineiden ja tarkkojen maksakudosmallien kehittämiseksi
Solujen käyttäytyminen ja innovaatiot HepG2-pohjaisissa malleissa
Solujen käyttäytymisen tutkiminen HepG2-pohjaisissa malleissa on ratkaisevan tärkeää maksasairauksien tutkimuksessa. Kolmiulotteisten sferoidisoluviljelmien kehittyminen on johtanut HepG2-solujen sferoidien luomiseen, mikä tarjoaa fysiologisesti relevantin mallin, joka heijastaa tarkasti normaaleja hepatosyyttejä. Nämä 3D-mallit, joissa on lisääntynyt metabolinen aktiivisuus, osoittavat, että HepG2-solut voivat toimia hepatoblastooman mallina, ja niillä on merkitystä syövän hoitotutkimuksessa, erityisesti maksakasvainten simuloinnissa ja uusien terapeuttisten lähestymistapojen testaamisessa [10-12]
HepG2:n vertailu ja ominaisuudet muiden kasvainsolulinjojen joukossa
HepG2 on yksi yleisimmin käytetyistä maksan kasvainsolulinjoista, joka on valittu sen laajojen sovellusten vuoksi tieteellisessä tutkimuksessa noin 40 saatavilla olevan maksan kasvainsolulinjan joukosta [13]. Huolimatta tiettyjen sytokromi P450 -entsyymien heikosta tai puuttuvasta ilmentymisestä verrattuna normaaleihin hepatosyytteihin, HepG2:n metabolinen profiili on johtanut pyrkimyksiin muokata solulinjaa parempien lääkeaineenvaihduntatutkimusten tekemiseksi [13]. Verrattuna kasvainsolulinjoihin, kuten MCF7, PC3, 143B ja HEK293, HepG2-soluilla on ainutlaatuiset aminohappopitoisuusprofiilit, jotka vaikuttavat merkittävästi proteiinisynteesiin ja eritykseen, mikä korostaa niiden ainutlaatuisia metaboliareittejä [14]
Maksasairauksien tutkimus HepG2:n avulla
HepG2-solujen subkultivointi
Seuraavassa on viisi vaihetta tarttuvien solujen poistamiseksi soluviljelypulloista Accutasea käyttäen:
- Poista väliaine soluviljelypullosta ja huuhtele tarttuneet solut PBS:llä, jossa ei ole kalsiumia ja magnesiumia. Käytä 3-5 ml PBS:ää T25-pulloihin ja 5-10 ml T75-pulloihin.
- Lisää Accutaasia soluviljelypulloon 1-2 ml T25-pulloa ja 2,5 ml T75-pulloa kohti. Varmista, että Accutase peittää koko solulevyn.
- Inkuboi pulloa huoneenlämmössä 8-10 minuuttia.
- Resuspendoi solut varovasti elatusaineella käyttäen 10 ml tuoretta elatusainetta.
- Sentrifugoi resuspendoituja soluja 5 minuuttia 300xg:n kierrosluvulla, suspendoi ne uudelleen tuoreeseen väliaineeseen ja annostele ne uusiin pulloihin, jotka sisältävät tuoretta väliaineita.
HepG2-solujen tulevaisuuden näkymät
HepG2-solulinjan koko potentiaalin hyödyntäminen jatkuu, sillä sytokromien ilmentymisen lisäämisessä on tapahtunut uraauurtavaa edistystä. Tutkijat tutkivat myös mahdollisuutta käyttää kolmiulotteisia pallosoluviljelmiä, jotka tarjoavat fysiologisesti relevantin järjestelmän. Metabolinen aktiivisuus, mukaan lukien sytokromit, on huomattavasti korkeampi 3D-sferoidisissa HepG2-malleissa kuin 2D-soluissa, mikä tuo meidät lähemmäksi sellaisen mallin luomista, joka heijastaa normaaleja hepatosyyttejä. Lisäksi solun pintaproteiinien virheellisen jakautumisen taustalla olevien dynaamisten prosessien tutkiminen voi tasoittaa tietä maksasairauksien paremmalle ymmärtämiselle
HepG2-solut: Hepa Hepa Hepa Hepa: Ymmärrys niiden roolista ja eroista biolääketieteellisessä tutkimuksessa - FAQ
Viitteet
- Vyas, R.C., Darroudi, F., Natarajan, A.T. Radiation-induced chromosomal breakage and rejoining in interphase-metaphase chromosomes of human lymphocytes, Mutat Res, 1991; 249(1):29-35.
- Woodfield, S.E., Shi, Y., Patel, R.H., Chen, Z., Shah, A.P., Srivastava, R.K., Whitlock, R.S., Ibarra, A.M., Larson, S.R., Sarabia, S.F., et al. MDM4:n esto: Uusi terapeuttinen strategia P53:n uudelleenaktivoimiseksi hepatoblastoomassa. Sci. Rep. 2021, 11, 2967.
- Hussain, S.P., Schwank, J., Staib, F., Wang, X.W., Harris, C.C. TP53-mutaatiot ja hepatosellulaarinen karsinooma: Insights into the Etiology and Pathogenesis of Liver Cancer. Oncogene 2004.
- Schicht, G., Seidemann, L., Haensel, R., Seehofer, D., Damm, G. Critical Investigation of the Usability of Hepatoma Cell Lines HepG2 and Huh7 as Models for the Metabolic Representation of Resectable Hepatocellular Carcinoma. Cancers 2022, 14(17), 4227.
- Verrier, E.R., Colpitts, C.C., Schuster, C., Zeisel, M.B., Baumert, T.F. Soluviljelymallit hepatiitti B- ja D-virusinfektion tutkimiseen. Viruses 2016, 8, 261.
- Verrier, E.R., Colpitts, C.C., Bach, C., Heydmann, L., Weiss, A., Renaud, M., Durand, S.C., Habersetzer, F., Durantel, D., AbouJaoudé, G., et al. A Targeted Functional RNA Interference screen Uncovers Glypican 5 as an Entry Factor for Hepatitis B and D Viruses. Hepatology 2016, 63, 35-48.
- Gripon, P., Rumin, S., Urban, S., Le Seyec, J., Glaise, D., Cannie, I., Guyomard, C., Lucas, J., Trepo, C., Guguen-Guillouzo, C. Infection of a Human Hepatoma Cell Line by Hepatitis B Virus. Proc. Natl. Acad. Sci. USA 2002, 99, 15655-15660.
- Mersch-Sundermann, V., Knasmüller, S., Wu, X.J., Darroudi, F., Kassie, F. Ihmisestä peräisin olevan maksasolulinjan käyttö sytoprotektiivisten, antigenotoksisten ja kogenotoksisten aineiden havaitsemiseen. Toxicology. 2004; 198(1-3): 329-340.
- Fanelli, A. HepG2 (maksan hepatosellulaarinen karsinooma): soluviljely. HepG2. Haettu 3. joulukuuta 2017.
- Xuan, J., Chen, S., Ning, B., Tolleson, W.H., Guo, L. Development of HepG2-Derived Cytochrome P450s Expressing Cells for Assessing Metabolism-Associated Drug-Induced Liver Toxicity. Physiol. Behav. 2017, 176, 139-148.
- Ooka, M., Lynch, C., Xia, M. Application of in vitro Metabolism Activation in High-Throughput Screening. Int. J. Mol. Sci. 2020, 21, 8182.
- Huang, L., Coughtrie, M.W.H., Hsu, H. Dehydroepiandrosteronisulfotransferaasigeenin alaspäin säätely ihmisen hepatosellulaarisessa karsinoomassa. Mol. Cell. Endocrinol.
- Zhu, Z., Hao, X., Yan, M., et al. Cancer stem/progenitor cells are highly enriched in CD133 + CD44 + population in hepatocellular carcinoma. Int J Cancer. 2010; 126:2067-2078.
- Arbus, C., Benyamina, A., Llorca, P.-M., Baylé, F., Bromet, N., Massiere, F., Garay, R.P., Hameg, A. Syamematsiinin metaboliaan osallistuvien ihmisen sytokromi P450 -entsyymien karakterisointi. Eur J Pharm Sci. 2007 Dec;32(4-5):357-66.