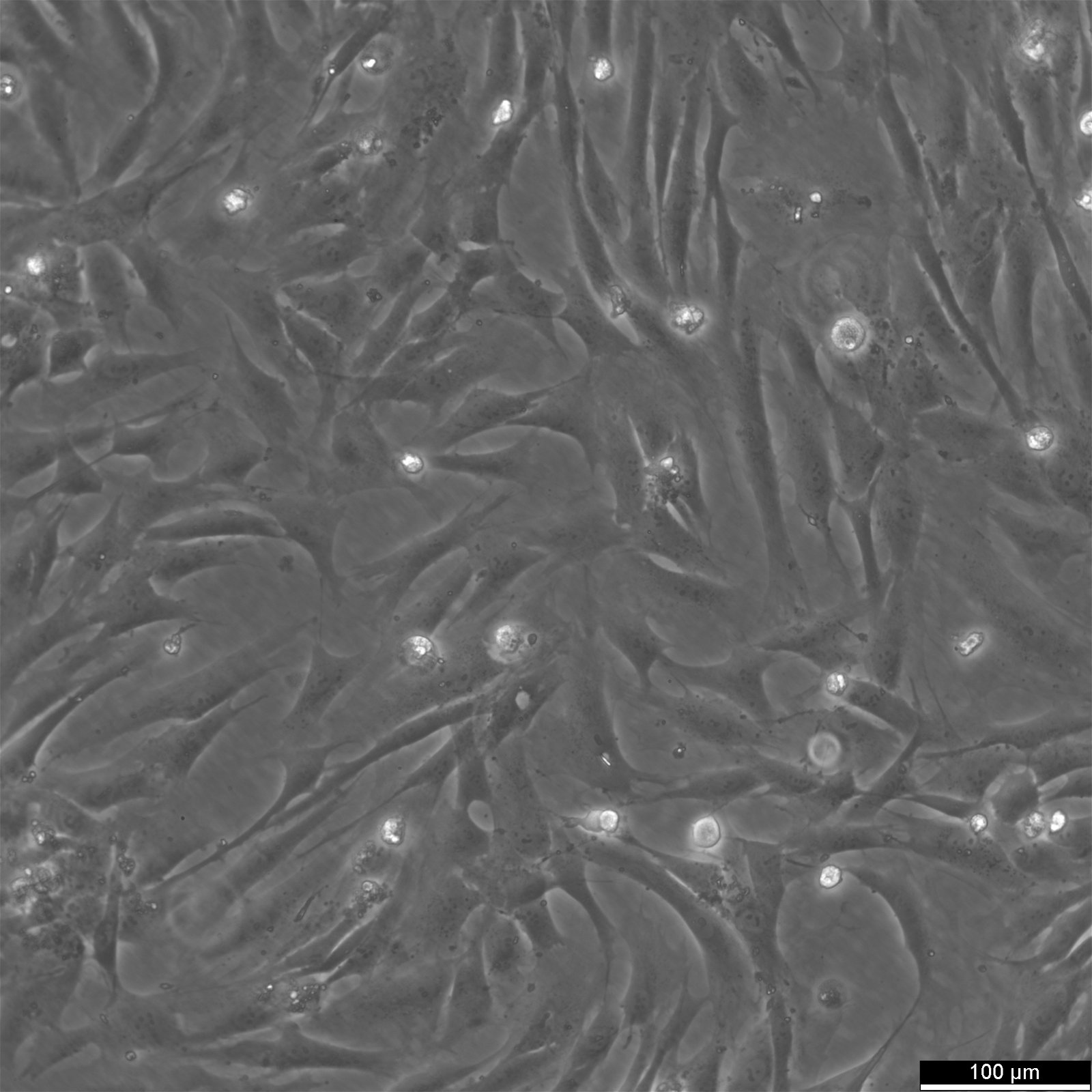
Ihmisen primaarisolut
Cytion tarjoaa valikoiman ihmisen primaarisoluja, jotka on saatu erilaisista kudoksista ja luovuttajilta. Nämä fysiologisesti merkitykselliset mallit on suunniteltu tukemaan translaatiotutkimusta, toksisuustestausta, regeneratiivista lääketiedettä ja edistyneitä in vitro -tutkimuksia. Jokainen viljelmä valmistetaan kontrolloiduissa olosuhteissa ja se käy läpi tiukan laadunvalvonnan, jolla varmistetaan sen identiteetti, steriiliys ja tasainen suorituskyky.
Fysiologisesti merkitykselliset mallit edistyneeseen tutkimukseen
Primaarisolujen valikoimaamme kuuluu endoteeli-, epiteeli-, fibroblasti- ja kantasolupopulaatioita useista ihmisen kudoksista. Nämä mallit säilyttävät alkuperäisen kudoksen keskeiset toiminnalliset ominaisuudet ja tarjoavat luotettavia järjestelmiä tautien mallintamiseen, lääkeaineiden seulontaan ja kudostekniikan sovelluksiin.
Mitä ovat ihmisen primaarisolut?
Primäärisolut ovat omien kudostensa puhtaimpia edustajia. Ne eristetään kudoksesta ja käsitellään niin, että ne voivat vakiintua viljelyyn ihanteellisissa olosuhteissa. Ne jäljittelevät paremmin in vivo -tilaa ja osoittavat normaalia fysiologiaa, koska ne on johdettu kudoksesta eikä niitä ole muokattu. Tämän vuoksi ne voivat toimia hyödyllisinä malleina solufarmakologian, toksikologian ja fysiologian tutkimuksessa (mukaan lukien aineenvaihdunnan, ikääntymisen ja signaalinsiirron tutkimukset). Muista, että primaarisoluja on haastavampi viljellä ja ylläpitää kuin jatkuvaa solulinjaa, koska niiden elinikä on lyhyempi ja ne lakkaavat jakautumasta (tai vanhenemasta) tietyn solunjakautumismäärän jälkeen. Solujen signaalireittien tutkimista hankaloittaa luovuttajilta hankittujen primaarisolujen luontainen vaihtelevuus ja aliviljelykäytännöt. Ennen signalointitutkimusten aloittamista tutkijat suorittavat usein seulonnan selvittääkseen, reagoivatko solut yleisesti käytettyihin ärsykkeisiin. Ajan ja rahan tuhlaamisen välttämiseksi primaarisoluja voidaan stimuloida aktivoimaan tärkeimpiä signaalireittejä ennen seulontaa.
Miksi käyttää ihmisen primaarisoluja?
Kuolemattomaksi tehtyjä solulinjoja käytetään yleisesti solumäärityksinä. Vaikka tutkijat ovatkin myöntäneet, että solulinjojen aiheuttamat biologiset muutokset voivat olla haitallisia niiden fysiologisen merkityksen tutkimisessa. Ihmisen primaarisolujen käyttö parantaa soluviljelmillä saatujen tietojen fysiologista arvoa, ja niitä pidetään yhä tärkeämpinä biologisten prosessien, sairauksien etenemisen ja lääkekehityksen tutkimisessa.
Ihmisen primaarisoluja käytetään laajalti in vitro -tutkimuksissa, joissa tutkitaan muun muassa solujen välistä ja solunsisäistä viestintää, kehitysbiologiaa sekä syövän, Parkinsonin taudin ja diabeteksen taustalla olevia mekanismeja, ja monilla muilla prekliinisillä ja tutkivilla biologisilla tutkimusalueilla. Tutkijat ovat jo pitkään käyttäneet kuolemattomia solulinjoja kudosten toiminnan tutkimiseen; solulinjat, joissa on selviä mutaatioita ja kromosomipoikkeavuuksia, eivät kuitenkaan välttämättä ole hyviä korvikkeita normaaleille soluille ja sairauden kehittymiselle sen alkuvaiheessa. Tarkempi malli tietystä kudoksen solutyypistä voidaan nyt saada käyttämällä kyseisestä kudoksesta eristettyjä ihmisen primaarisoluja, joita ylläpidetään primaarisoluviljelyaineissa ja -lisäaineissa.
Mitä on primaarinen soluviljely?
Kuolemattomien solulinjojen käytön sijaan primaarisessa soluviljelyssä kasvatetaan soluja suoraan monisoluisesta organismista kehon ulkopuolella. Joissakin maissa, kuten Yhdistyneessä kuningaskunnassa, on oikeudellisesti tunnustettu, että primaariset soluviljelmät edustavat paremmin in vivo -kudoksia kuin solulinjat. Primäärisolut tarvitsevat kuitenkin kasvuunsa oikean substraatin ja ravintoaineet, ja tietyn määrän jakautumisia jälkeen ne kehittävät senesenssifenotyypin, joka saa ne lopettamaan jakautumisen pysyvästi. Nämä kaksi tekijää motivoivat solulinjojen luomista. Sekä luonnollisesti kuolemattomiksi tehtyjä primaarisoluja (esim. HeLa-solut) että keinotekoisesti kuolemattomiksi tehtyjä primaarisoluja (esim. HEK-solut) voidaan kasvattaa soluviljelmissä loputtomiin.
Ihmisen primaarisolut kudostyypeittäin
Epiteelisolut, fibroblastit, keratinosyytit, melanosyytit, endoteelisolut, lihassolut, immuunisolut ja kantasolut, kuten mesenkymaaliset kantasolut, ovat yleisimmin tieteellisessä tutkimuksessa käytettyjä ihmisen primaarisoluja. Aluksi viljelmät ovat heterogeenisiä (edustavat kudoksessa olevien solutyyppien sekoitusta), ja niitä voidaan pitää elossa in vitro vain tietyn ajan. Transformaatio on in vitro -prosessi, jonka avulla ihmisen primaarisoluja voidaan manipuloida rajattomasti alaviljelmiä varten. Transformaatio voi tapahtua luonnollisesti tai se voidaan indusoida kemikaaleilla tai viruksilla. Geneettisen transformaation jälkeen primaariviljelmä voi jakautua loputtomiin kuolemattomaksi sekundaariseksi solulinjaksi, jos sille annetaan riittävästi ravinteita ja tilaa.
Endoteelisolut
Syöpähoito, haavojen paraneminen, solusignaalien tutkimus, korkean läpimenon ja suuren sisällön seulonta sekä toksikologinen seulonta ovat vain joitakin aloja, joilla primaaristen endoteelisolujen käytöstä tutkimusvälineenä voidaan hyötyä.
Keratinosyytit
Keratinosyytit, jotka ovat peräisin joko aikuisen ihmisen ihon tai vastasyntyneen esinahan epidermiksestä, ovat ratkaisevassa asemassa psoriaasin ja syövän kaltaisten ihosairauksien tutkimuksessa.
Epiteelisolut
Primaariset epiteelisolut ovat osoittautuneet korvaamattomiksi resursseiksi elimistön luonnollisen puolustuskyvyn mallintamisessa syöpätutkimuksista toksikologisiin tutkimuksiin.
Fibroblastit
Pluripotenttien kantasolujen (iPS-solujen) indusoiminen ja haavojen paranemisen tutkiminen ovat vain muutama primaaristen fibroblastien monista käyttötarkoituksista.
Immuunisolut
Perifeerisen veren mononukleaariset solut, lyhyesti PBMC, ovat veren mononukleaarisia soluja, joilla on pyöreä solutydin. Niihin kuuluvat pääasiassa lymfosyytit ja monosyytit, jotka omaksuvat tärkeitä tehtäviä immuunivasteen aikana. Perifeerisen veren mononukleaarisia soluja käytetään usein infektioiden diagnosointiin tai mahdollisen rokotussuojan havaitsemiseen. T-solujen välittämän soluvälitteisen immuunivasteen ymmärtäminen on usein ratkaisevan tärkeää.
Melanosyytit
Melanosyytit ovat erikoistuneita ihosoluja, jotka tuottavat melaniinipigmenttiä, ja ne ovat hyödyllisiä malleja esimerkiksi haavan paranemista, toksisuutta, melanoomaa, ihon vastetta ultraviolettisäteilylle (UV-säteilylle), ihosairauksia ja kosmetiikkaa koskevissa tutkimuksissa.
Kantasolut
Kantasoluilla on mahdollisuus erilaistua moniksi erilaisiksi solutyypeiksi. Erilaistumiskykynsä ansiosta ne tarjoavat uusia mahdollisuuksia ihmisen kudosten ja terveystilojen mallintamiseen.
Mesenkymaaliset kantasolut
Mesenkymaalisia kantasoluja, jotka tunnetaan myös nimellä MSC, voidaan saada eri ihmislähteistä, kuten luuytimestä, rasvasta (rasvakudoksesta), napanuorakudoksesta (Whartonin hyytelöstä) ja lapsivedestä (sikiötä ympäröivä neste), ja niitä voidaan laajentaa in vitro. Näillä aikuisten stroomaalisilla kantasoluilla on kyky kehittyä monenlaisiksi solutyypeiksi. Joitakin näistä solutyypeistä ovat luusolut, rustosolut, lihassolut, hermosolut, ihosolut ja sarveiskalvosolut.
Sileät lihassolut
Onttojen elinten sisällä primaariset sileät lihassolut (SMC) vuorailevat sisätiloja ja välittävät supistumiskykyä. Syövän ja muiden sairauksien lisäksi SMC-soluja voidaan käyttää verenpaineen fibroosin mallintamiseen.
Primäärisolut ja solulinjat
Joko spontaanin mutaation kautta, kuten muunnetuissa syöpäsolulinjoissa, tai tarkoituksellisen muutoksen kautta, kuten syöpägeenien keinotekoisessa tuottamisessa, jatkuvat solulinjat ovat saaneet mahdollisuuden lisääntyä loputtomasti (kuolemattomiksi). Jatkuvat solulinjat ovat yleensä luotettavampia ja helpompia käsitellä kuin primaarisolut. Ne voivat laajentua loputtomiin ja tarjoavat nopean pääsyn olennaisiin tietoihin. Jatkuvien solulinjojen käyttöön liittyy tiettyjä rajoituksia, muun muassa se, että ne ovat geneettisesti muunnettuja/muuntuneita, mikä saattaa muuttaa fysiologisia ominaisuuksia eikä vastaa in vivo -olosuhteita, ja että tämä voi muuttua edelleen ajan mittaan, kun soluja passagoidaan merkittävästi.
Primäärisoluviljelyn edistysaskeleet
Primäärisoluilla on huonomaineinen maine siitä, että niiden kanssa on vaikea työskennellä. Prosessi on kuitenkin muuttumassa helpommaksi kuin koskaan aiemmin, koska primaarisoluviljelyä on kehitetty, kaupallisia primaarisoluja on saatavilla täysin optimoiduilla protokollilla ja uusia analyysitekniikoita, jotka vaativat vähemmän työpanosta.
Siirtymistä kaksiulotteisesta soluviljelystä kolmiulotteiseen soluviljelyyn pidetään merkittävänä virstanpylväänä alalla. Kudospesifinen arkkitehtuuri, solujen ja solujen väliset vuorovaikutukset sekä mekaaninen/biokemiallinen signalointi voivat heikentyä 2D-viljelmässä. Näin ollen näiden viljelmien biologiselle arvolle on asetettu yläraja.
Toisaalta 3D-soluviljely antaa soluille mahdollisuuden laajentua ja olla vuorovaikutuksessa solunulkoisen 3D-kehyksen kanssa. Näin solut voivat olla vuorovaikutuksessa toistensa ja solunulkoisen matriisin kanssa, mikä tekee 3D-viljelmistä fysiologisesti merkityksellisempiä. Menetelmän tarkkuus in vivo -reaktioiden ennustamisessa on tehnyt siitä vallankumouksellisen esimerkiksi lääkkeiden löytämisen ja kehittämisen alalla. Tämän vuoksi nykyaikaiset teknologiat, kuten potilaista peräisin olevat organoidit ja organs-on-a-chip-menetelmät, tarjoavat erittäin kontekstisidonnaisia malleja lääkkeiden seulontaan ja kehittämiseen.
Primäärisolujen tuottaminen on pullonkaula primaariviljelyssä. Tämän ongelman ratkaisemiseksi tarvitaan yleensä suurempi kudosmäärä, ja sen saavuttaminen voi olla haastavaa. Analyyttisen herkkyyden parantaminen tarjoaa kuitenkin keinon päästä eteenpäin. Esimerkiksi tarve kasvattaa suuria määriä primaarisoluja vähenee, kun käytetään yksittäissoluteknologiaa, johon kuuluvat sekvensointi, western blotting ja massasytometria.
Primäärisoluviljelyn lupaavat näkymät
Teknologinen kehitys lieventää primaarisoluviljelyn yleisiä vaikeuksia. Tämä menetelmä on puolestaan nopeasti syrjäyttämässä muita menetelmiä solu- ja molekyylibiologian tutkimuksen ja käytännön kultaisena standardina. Rokotteiden valmistus, elinten korvaaminen, kantasoluhoidot, syöpätutkimus ja monet muut alat hyötyvät suuresti primäärisoluviljelyn jatkuvasta kehityksestä.
Primäärisoluviljelyn vinkkejä ja niksejä
Solujen laajentamisen tarpeet
Kaksi yleisintä primäärisolujen viljelymenetelmää ovat suspensiossa tai pinnalla (2D). Jotkin solut voivat kellua vapaasti verenkierrossa kiinnittymättä koskaan pintaan (esimerkiksi perifeerisestä verestä peräisin olevat solut). Erilaisia solulinjoja on kehitetty menestymään suspensioviljelmissä, joissa ne voivat saavuttaa tiheyksiä, joita ei voida saavuttaa 2D-kasvatusolosuhteissa. Primäärisoluja, jotka tarvitsevat kiinnittymistä kasvaakseen in vitro, kutsutaan adherenttisoluiksi, ja niihin kuuluvat myös kiinteissä kudoksissa olevat solut. Adheesio-ominaisuuksien parantamiseksi ja muiden kasvun ja erilaistumisen edellyttämien signaalien syöttämiseksi näitä soluja viljellään tavallisesti litteässä päällystämättömässä muoviastiassa, mutta toisinaan myös mikrokannattimessa. Jälkimmäinen vaihtoehto voidaan päällystää solunulkoisella matriisiproteiinilla (kuten kollageenilla ja laminiinilla). Soluviljelyssä käytettävä elatusaine koostuu perusväliaineesta, jota on täydennetty asianmukaisilla kasvutekijöillä ja sytokiineillä. Soluinkubaattori on erityyppinen laboratorioinkubaattori, jota käytetään solujen viljelyyn ja ylläpitoon tietyssä lämpötilassa ja kaasuseoksessa (tyypillisesti 37 °C, 5 % CO2 nisäkässoluille). Optimaaliset olosuhteet voivat olla hyvin erilaiset viljeltävän solutyypin mukaan. Kasvatettavista solutyypeistä riippuen optimaalinen kasvualusta sisältää ainutlaatuisen yhdistelmän tekijöitä, kuten pH, glukoosipitoisuus, kasvutekijät ja muiden ravintoaineiden läsnäolo.
Antibiootit kasvualustassa ovat ratkaisevan tärkeitä primaariviljelyn perustamisen aikana, jotta estetään isäntäkudoksesta peräisin oleva kontaminaatio. Joissakin antibioottiohjelmissa käytetään gentamysiinin, penisilliinin, streptomysiinin ja amfoterisiini B:n yhdistelmää. Antibioottien pitkäaikaista käyttöä ei kuitenkaan suositella, koska jotkin reagenssit (kuten amfoterisiini B) voivat olla pitkällä aikavälillä myrkyllisiä soluille.
Useimmat primaarisolut vanhenevat ja lakkaavat jakautumasta tietyn määrän populaatiokaksinkertaistumisia jälkeen, joten on ratkaisevan tärkeää pitää ne elossa eristämisen jälkeen. Solujen pitkäaikainen elinkelpoisuus edellyttää asiantuntevia soluviljelytekniikoita ja ihanteellisia viljelyolosuhteita (kuten oikeaa elatusainetta, oikeaa lämpötilaa, oikeaa kaasuseosta, oikeaa pH:ta, oikeaa kasvutekijöiden pitoisuutta, ravinteiden läsnäoloa ja glukoosin läsnäoloa). Koska monet kasvutekijät, joita käytetään elatusaineiden täydentämiseen, saadaan eläinten verestä (verestä peräisin olevissa ainesosissa on kontaminaatiopotentiaali), on suositeltavaa, että niiden käyttö minimoidaan tai sitä vältetään kokonaan. On myös tärkeää käyttää aseptista tekniikkaa.
Subkulttuuri ja ylläpito
Kun eristetyt solut tarttuvat viljelymaljan pintaan, alkaa ylläpitovaihe. Kiinnittyminen tapahtuu tyypillisesti 24 tunnin kuluttua viljelyn aloittamisesta. Solut olisi subkulturoitava, kun ne ovat saavuttaneet tietyn konfluenssiprosentin ja lisääntyvät aktiivisesti. Koska konfluenssin jälkeiset solut saattavat erilaistua ja niiden proliferaatio hidastua kulkeutumisen jälkeen, primaariset soluviljelmät on parasta subkulturoida ennen kuin ne saavuttavat 100 prosentin konfluenssin.
Alikultivointi tuoreessa väliaineessa ylläpitää ankkurointiin riippuvaisten solujen eksponentiaalista kasvua. Monolayerien subkultivointi häiritsee solujen välisiä ja solunsisäisiä solupinnan vuorovaikutuksia. Alhaisia proteolyyttisten entsyymien, kuten trypsiinin/EDTA:n, pitoisuuksia käytetään tarttuvien primaarisolujen irrottamiseen monolayereistä tai kudoksista. Kun solut on dissosioitu ja laimennettu yksisoluliuokseksi, ne lasketaan ja siirretään tuoreisiin viljelyastioihin kiinnittymään ja lisääntymään uudelleen.
Kryosäilytys ja talteenotto
Kryosäilytys säilyttää elävät solut pakastamalla ne alhaisissa lämpötiloissa. Ihmisen primaarisolujen kryosäilytys ja sulatus estää solukuoleman ja -vaurion varastoinnin ja käytön aikana. Ihmisen primaarisolut kryosuojataan käyttämällä DMSO:ta tai glyserolia (oikeassa lämpötilassa ja hallitulla jäädytysnopeudella). Jäädytysprosessin on tapahduttava asteittain -1 °C:n lämpötilassa joka minuutti jääkiteiden muodostumisen estämiseksi. Pitkäaikainen varastointi edellyttää nestemäistä typpeä (-196 °C) tai alle -130 °C:n lämpötilaa.
Pakastettujen solujen sulattaminen 37 °C:n vesihauteessa noin 1-2 minuutin ajan riittää kryosäilöttyjen solujen sulattamiseen. Ihmisen primaarisoluja ei pidä sentrifugoida sen jälkeen, kun ne on sulatettu pakastimesta (koska ne ovat erittäin herkkiä vaurioitumaan kryosäilytyksestä palautumisen aikana). Se soveltuu solujen levittämiseen välittömästi sulatuksen jälkeen, ja se edistää viljelmien kiinnittymistä ensimmäisten 24 tunnin aikana levittämisen jälkeen. 1 Kun kryosäilytetyt primaarisolut ovat kiinnittyneet, käytetty elatusaine on poistettava (koska DMSO on haitallista primaarisoluille ja voi aiheuttaa sulatuksen jälkeisen elinkelpoisuuden laskua).