HCT116-solulinja: Colorektaalisyöpätutkimuksen tukipilari
HCT116-solulinja on kolorektaalisyövän tutkimuksen kulmakivi, joka tarjoaa korvaamatonta tietoa taudin patogeneesistä ja mahdollisista hoitokeinoista. HCT116 on tunnettu hyödyllisyydestään syöpätutkimuksessa ja farmakologisissa arvioinneissa, ja se helpottaa keskeisiä tutkimuksia kasvaimen käyttäytymisestä ja lääkkeiden tehosta.
HCT116-solujen alkuperä ja perusominaisuudet
HCT116-solujen juurien ja perusominaisuuksien, kuten niiden morfologisten ominaisuuksien, geneettisen rakenteen ja solumittojen, ymmärtäminen on olennaista tutkijoille, jotka aloittavat tutkimukset tällä solulinjalla.
Alkuperä ja geneettinen maisema: HCT116-solut ovat peräisin 48-vuotiaan valkoihoisen miehen paksusuolensyöpädiagnoosin saaneesta paksusuolesta, ja niissä on mutaatio RAS/RAF/MEK/ERK-signalointireittiin kuuluvan KRAS-geenin kodonissa 13 (G13D). Tämä mutaatio on ratkaiseva näiden solujen onkogeenisen muutoksen kannalta, mikä korostaa niiden merkitystä syöpätutkimuksessa.
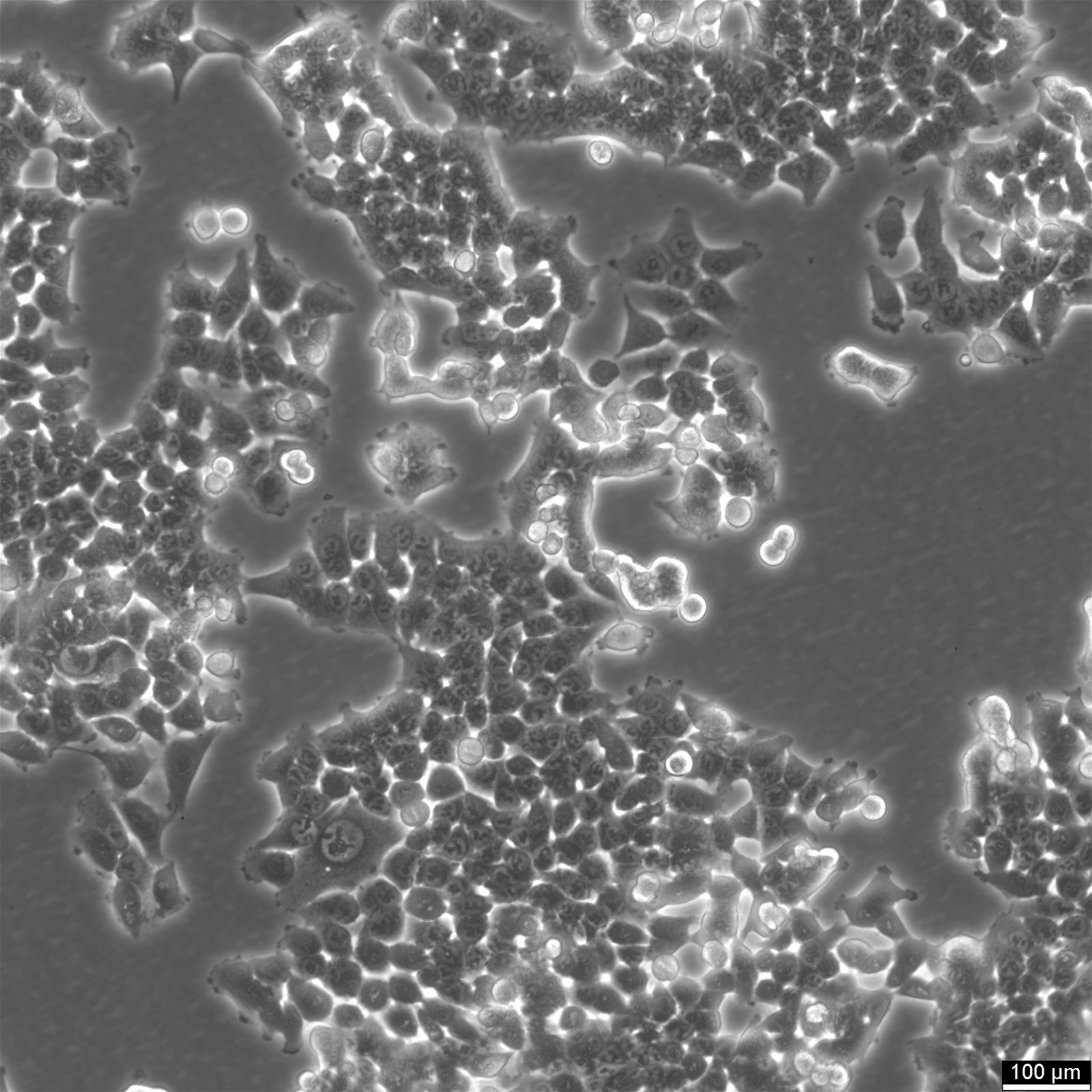
Morfologia ja kasvuominaisuudet: HCT116-solut, joilla on epiteelin kaltainen morfologia, kasvavat tyypillisesti yksikerrosviljelmissä, mutta ne voivat myös muodostaa sferoideja, joiden halkaisija on 150-400 µm. Tämä kasvumallien sopeutumiskyky korostaa niiden monipuolisuutta erilaisissa koejärjestelyissä.
Kromosomiprofiili: HCT116-solujen kromosomikoostumus on lähes diploidi, ja noin 70 prosentilla solupopulaatiosta on 45 kromosomia. Kromosomien 8, 10, 16 ja 17 pitkissä haaroissa on toistuvaa monistumista, kun taas kromosomi Y puuttuu, mikä osaltaan vaikuttaa niiden ainutlaatuiseen genomiseen ominaisuuteen.
Vertaileva analyysi: HCT116 vs. HT29-solulinjat
Kun HCT116:n ja HT29:n, toisen ihmisen kolorektaalikarsinooman solulinjan, rinnakkain asettaminen osoittaa selviä eroja niiden onkogeenisessa potentiaalissa ja erilaistumiskyvyssä:
Onkogeeninen aggressiivisuus ja erilaistuminen: HCT116-soluille on ominaista korkea onkogeeninen aggressiivisuus ja rajallinen erilaistumispotentiaali, mikä tekee niistä mallin aggressiivisten kasvainfenotyyppien tutkimiseen. Sitä vastoin HT29-soluilla on kyky erilaistua enterosyyttien kaltaisiksi ja musiinia tuottaviksi sukulinjoiksi, mikä tarjoaa kontrastiivisen mallin, joka jäljittelee kolorektaalisen syövän biologian eri näkökohtia.
HCT116- ja HT29-solulinjojen vertaileva ymmärtäminen rikastuttaa tutkijoiden käytettävissä olevaa työkalupakkia, mikä mahdollistaa hienovaraisemmat tutkimukset paksusuolisyövän monitahoisesta luonteesta.
HCT116-solujen käsittely
|
Kaksinkertaistumisaika: |
HCT116-syöpäsolujen kaksinkertaistumisaika on 25-35 tuntia. |
|
Adheesiossa tai suspensiossa: |
HCT116-paksusuolen syöpäsolulinja on tarttuva, ja solut kasvavat monolayereinä. |
|
Kylvötiheys: |
HCT116-soluviljelmälle suositellaan kylvötiheyttä 2 x104 solua/cm2. Subkultivointia varten solut on irrotettava Accutase-liuoksella 1x PBS-pesun jälkeen. Sentrifugoinnin jälkeen solupelletti suspendoidaan uudelleen tuoreeseen kasvualustaan ja siirretään uuteen pulloon. |
|
Kasvualusta: |
McCoys 5a -ympäristö, jota on täydennetty 3,0 g/l L-glukoosilla, 1,5 mM L-glutamiinilla, 3,0 g/l NaHCO3:lla ja 10 %:lla naudan sikiöseerumilla, on optimaalinen HCT116-solujen viljelyyn. On suositeltavaa uusia väliaine 1-2 kertaa viikossa. |
|
Kasvuolosuhteet (lämpötila,CO2): |
Viljely tapahtuu kostutetussa inkubaattorissa 37 °C:n lämpötilassa ja 5 %CO2-ilmakehässä. |
|
Varastointi: |
HCT116-soluja voidaan säilyttää alle -150 °C:n lämpötiloissa joko nestemäisen typen höyry- tai nestefaasissa. |
|
Pakastusprosessi ja väliaine: |
Käytä CM-1- tai CM-ACF-mediaa kryosäilytykseen. Suositellaan säädellyn nopeuden pakastusmenetelmää, joka mahdollistaa asteittaisen lämpötilan laskun 1 °C minuutissa, mikä auttaa säilyttämään solujen elinkelpoisuuden. |
|
Sulatusprosessi: |
Sulata HCT116-solut 37 °C:n vesihauteessa. Kasvualustan lisäämisen jälkeen sentrifugoidaan jäädytysalustajäämien poistamiseksi. Resuspendoi solupelletti tuoreeseen väliaineeseen ja viljele uusissa pulloissa. |
|
Bioturvallisuustaso: |
Taso 1 |
HCT116-solulinjan edut
Tässä jaksossa perehdytään HCT116-solulinjaan, korostetaan sen keskeistä asemaa syöpätutkimuksessa, erityisesti paksu- ja peräsuolisyövän tutkimuksessa, ja käsitellään sen luontaisia etuja.
HCT116-solulinja erottuu syöpätutkimuksessa useiden keskeisten etujensa ansiosta:
Kolorektaalisyöpämalli: Se toimii laajalti tunnustettuna in vitro -mallina paksu- ja peräsuolisyövälle, joka on kolmanneksi yleisin syöpä maailmanlaajuisesti. Koska se jäljittelee ihmisen paksusuolen ja peräsuolen syöpää, se on korvaamaton syövän biologian ymmärtämisessä ja hoitostrategioiden testaamisessa.
Homogeenisuus: Huomionarvoista on, että noin 70 prosentilla HCT116-soluista on yhtenäiset geneettiset profiilit, joten kyseessä on suhteellisen homogeeninen populaatio. Tämä yhdenmukaisuus on ratkaisevan tärkeää tutkimuksissa, joissa keskitytään geeniekspressioon, solujen signaalireitteihin ja lääkehoitojen tehokkuuden arviointiin, sillä se takaa kokeellisten tulosten johdonmukaisuuden ja luotettavuuden.
Transfektion tehokkuus: Yksi HCT116-solujen erityispiirteistä on niiden hyvä transfektiokyky, erityisesti virusvektoreilla. Tämä ominaisuus on erityisen hyödyllinen geeniterapiatutkimuksessa, sillä se mahdollistaa geneettisen materiaalin tehokkaan ja täsmällisen lisäämisen, mikä helpottaa kehittyneitä geneettisiä manipulaatioita ja toiminnallisia tutkimuksia.
Edistä tutkimustuloksiasi autenttisen HCT116-solulinjamme avulla
HCT116-solulinjan tutkimussovellukset
HCT116-solulinjalla on monenlaisia sovelluksia syöpätutkimuksessa. Joitakin merkittäviä sovelluksia ovat:
Syöpäbiologia
HCT116-paksusuolisyövän solulinjaa käytetään paksusuolisyövän etenemisen ja kehittymisen tutkimiseen. Lisäksi se auttaa valaisemaan syövän proliferaatioon, migraatioon ja invaasioon liittyviä mekanismeja ja signaalireittejä. Eräässä tutkimuksessa HCT116-soluja käytettiin lääkeresistenssin kehittymiseen osallistuvien geenien tutkimiseen. Tutkijat yliekspressoivat MDR1-geeniä paksusuolen syöpäsoluissa ja havaitsivat NOX (NADPH-oksidi) -isoformien ja Nrf2:n ilmentymistä. Tutkimus osoitti, että NOX2:n ja Nrf2:n regulaatio aiheuttaa syöpäsolujen kemoresistenssiä; näin ollen näihin geeneihin voidaan kohdistaa vastustuskyvyn kehittymisen voittamiseksi syöpähoidon aikana [1]. Samoin vuonna 2021 tehdyssä tutkimuksessa raportoitiin, että NF-κB-signalointireitti osallistuu paksusuolen syövän proliferaation ja migraation säätelyyn. Siten siihen voidaan kohdistaa uusien ja tehokkaiden terapioiden kehittäminen paksusuolen karsinoomaa vastaan [2].
Onkologian alalla solusyklin, proliferaation ja kasvun sekä apoptoosin monimutkaisten prosessien ymmärtäminen on perustavanlaatuista. Nämä biologiset toiminnot ovat keskeisiä tutkittaessa ihmisen solulinjoja, erityisesti niitä, jotka on johdettu pahanlaatuisista soluista, kuten ihmisen paksusuolen syöpäsoluista ja haimasyöpämalleista. Esimerkiksi HCT116- ja SW620-solulinjat ovat tärkeitä paksusuolen syövän ja haimasyövän taustalla olevien mekanismien tutkimisessa. Virtaussytometrian ja klonogeneettisten määritysten kaltaisten tekniikoiden avulla tutkijat voivat selvittää geeniekspressioprofiileja ja riippumattomien solujen käyttäytymistä kasvaimissa ja valottaa sitä, miten syöpä kommunikoi solunulkoisessa matriisissa.
Apoptoosin rooli syövän etenemisessä
Apoptoosilla eli ohjelmoidulla solukuolemalla on ratkaiseva merkitys solujen homeostaasin ylläpitämisessä, ja se on keskeinen tutkimusalue syöpätutkimuksessa. On ratkaisevan tärkeää erottaa toisistaan apoptoosi, joka ei liity syöpään, ja apoptoosi, joka on erityisesti syövän yhteydessä indusoitu, kuten paksusuolisyövän solukuolema. Tässä prosessissa ei ole kyse pelkästään solujen eliminoinnista, vaan siihen liittyy monimutkainen signaalien vuorovaikutus, joka voi vaikuttaa kasvaimen kasvuun ja etäpesäkkeiden muodostumiseen. Tarkastelemalla apoptoosia ja solukuolemaa yhdessä metastaasin suppressorien ja kasvainsuppressorien aktiivisuuden kanssa tutkijat voivat saada käsityksen niistä reiteistä, jotka säätelevät syövän etenemistä ja metastaasipotentiaalia.
Metastaasi ja molekyylimarkkerit syövässä
Metastaasit ovat edelleen yksi syövän pelottavimmista näkökohdista, ja hematogeeninen etäpesäke on merkittävä huolenaihe pahanlaatuisten solujen leviämisessä. Metastaasin tutkimiseen kuuluu syöpäsolujen liikkumis- ja invaasiokyvyn eli solujen liikkumisen tutkiminen sekä solujen vuorovaikutus ympäristönsä, myös solunulkoisen matriisin, kanssa. Molekyylimarkkerit, kuten CD133:n ilmentyminen ja epidermisen kasvutekijän reseptori, ovat ratkaisevassa asemassa tunnistettaessa ja ymmärrettäessä positiivisten paksusuolen karsinoomasolujen ja muiden syöpätyyppien käyttäytymistä. Esimerkiksi SIRT6-reitti on noussut kiinnostuksen kohteeksi sen mahdollisen roolin vuoksi, joka sillä on kasvaimen kasvun ja metastaattisen paksusuolisyövän moduloinnissa.
Toksikologia/lääkekehitys
HCT116-solulinjaa käytetään uusien syöpälääkkeiden seulontamallina. Useita tutkimuksia on tehty syöpälääkkeiden, myös luonnontuotteiden ja kemiallisesti syntetisoitujen nanohiukkasten, tehon ja toksisuuden arvioimiseksi. Sellaisenaan tutkimuksessa arvioitiin kasviperäisen lääkeaineen, Caesalpinia pulcherrima , uutteista syntetisoitujen hopean nanohiukkasten sytotoksisuutta HCT116-soluissa [3]. Tutkimuksessa tutkijat käyttivät HCT116-syöpäsolulinjaa arvioidakseen kaakaotee-vesiuutteen syöpää ehkäisevää potentiaalia. He havaitsivat, että kaakaoteeuute vähentää paksusuolen syövän proliferaatiota ja indusoi solukuolemaa [4]. Toisessa tutkimuksessa käytettiin HCT116-syöpäsoluja ja havaittiin, että ilmaperunan, Dioscorea bulbifera, uutteilla on pro-apoptoottista aktiivisuutta paksusuolen karsinoomasoluissa aktivoimalla JNK-signalointikaskadia ja tukahduttamalla ERK1/2-geeniä [5].
Metformiinin vaikutukset syöpäsoluihin, erityisesti paksusuolen ja haimasyövän yhteydessä, ovat esimerkki siitä, miten syöpäsolujen biologisten toimintojen ymmärtäminen voi johtaa mahdollisiin hoitostrategioihin. Syöpäsolujen klonogeenisen selviytymisen eli kyvyn muodostaa klooneja, kun niitä hoidetaan metformiinin kaltaisilla aineilla tai kun ne kohdistuvat tiettyihin reitteihin, kuten epidermisen kasvutekijän reseptoriin, tutkiminen voi antaa arvokasta tietoa tehokkaista syöpähoidoista. Lisäksi HCT116-kloonien ja HCT116-solupopulaatioiden käyttö näissä tutkimuksissa antaa mahdollisuuden ymmärtää paremmin, miten syöpäsolut reagoivat erilaisiin terapeuttisiin toimenpiteisiin, mikä tasoittaa tietä yksilöllisemmille lähestymistavoille syövän hoidossa.
HCT116-solut: 116T116T: Tutkimusjulkaisut
Tässä jaksossa käydään läpi muutamia merkittäviä ja eniten siteerattuja viimeaikaisia julkaisuja, joissa käytetään HCT116-solulinjaa.
Tämä tutkimus julkaistiin Journal of Photochemistry and Photobiology B: Biology -lehdessä (2017). Tutkijat käyttivät HCT116-paksusuolen syöpä- ja A549-keuhkosyöpäsolulinjoja arvioidakseen piper nigrumin siemenistä syntetisoitujen tinaoksidinanohiukkasten sytotoksisia vaikutuksia.
Tässä Cancer Letters -lehdessä (2018) julkaistussa tutkimuksessa ehdotetaan, että lncRNA SNHG15 edistää paksusuolen syöpäsolujen migraatiota paksusuolen syöpäsolulinjoissa, mukaan lukien HCT116.
Pitkän ei-koodaavan RNA:n TUG1:n yliekspressio edistää paksusuolen syövän etenemistä
Tämä artikkeli julkaistiin Medical Science Monitor -lehdessä vuonna 2016. Tutkimuksessa havaittiin, että onkogeeninen LncRNA TUG1 edistää HCT116-paksusuolen syöpäsolujen proliferaatiota ja migraatiota.
Lääkeresistenssi indusoi H2S:ää tuottavien entsyymien ylössäätelyä HCT116-paksusuolen syöpäsoluissa
Tässä Biochemical Pharmacology -lehdessä (2018) julkaistussa tutkimuksessa ehdotetaan, että lääkeresistenssin kehittyminen kohottaa H2S:ää tuottavien entsyymien tasoja HCT116-paksusuolen syöpäsoluissa.
Tässä International Journal of Environmental Health Research -lehdessä (2023) julkaistussa tutkimusartikkelissa ehdotetaan, että Inula viscosa L. - uute vaikuttaa HCT116-paksusuolen syöpäsoluihin syövän vastaisesti mikroRNA:iden säätelyn kautta.
HCT116-soluja koskevat resurssit
Alla on muutamia HCT116-soluja koskevia resursseja.
- HCT116-solujen transfektointi: Tämä video on vaiheittainen opas HCT116-syöpäsolujen transfektointiin.
- HCT116-solulinjan viljely: Tässä videossa näytetään HCT116-paksusuolen syöpäsolulinjan subkulturointiprotokolla.
- HCT116-solulinjan subkultivointi: Tällä verkkosivustolla on paljon hyödyllistä tietoa HCT116-kasvatusalustasta. Lisäksi se tarjoaa menettelyjä solujen jäädyttämistä, sulattamista ja subkulturointia varten.
Usein kysyttyjä kysymyksiä HCT116-soluista
viitteet
- Waghela, B.N., F.U. Vaidya ja C. Pathak: NOX-2:n ja Nrf-2: NOX-2:n ja Nrf-2:n pregulaatio edistää 5-fluorourasiiliresistenssiä ihmisen paksusuolen karsinooman (HCT-116) soluissa. Biokemia (Moskova), 2021, 86, s. 262-274.
- Yang, M., et al., Astragaliini estää ihmisen paksusuolisyövän HCT116-solujen proliferaatiota ja migraatiota säätelemällä NF-κB-signalointireittiä. Frontiers in Pharmacology, 2021, 12: s. 639256.
- Deepika, S., C.I. Selvaraj ja S.M. Roopan, Caesalpinia pulcherrima L. swartzin bioaktiivisuuksien seulonta ja uutteen syntetisoitujen hopean nanohiukkasten sytotoksisuus HCT116-solulinjassa. Materials Science and Engineering, C, 2020, 106, s. 110279.
- Gao, X., et al., Kaakaotee (Camellia ptilophylla) indusoi mitokondrioista riippuvaista apoptoosia HCT116-soluissa ROS:n tuottamisen ja PI3K/Akt-signalointireitin kautta. Food Research International, 2020, 129, s. 108854.
- Hidayat, A.F.A., et al., Dioscorea bulbifera indusoi apoptoosia ERK 1/2:n estämisen ja JNK-signalointireittien aktivoinnin kautta HCT116-ihmisen kolorektaalikarsinoomasoluissa. Biomedicine & Pharmacotherapy, 2018. 104: p. 806-816.