
Johdanto
Biolääketieteellisen tutkimuksen laajassa kentässä solulinjat ovat nousseet laulamattomiksi sankareiksi, jotka ovat hiljaa mullistaneet ymmärryksemme ihmisen terveydestä ja sairauksista. Nämä pienet, elävät laboratoriot ovat avanneet ovet lukemattomiin keksintöihin, jotka ovat ulottuneet solumekanismien monimutkaisuuden selvittämisestä elämää pelastavien hoitomuotojen kehittämiseen. Solulinjojen merkitys tieteellisessä tutkimuksessa kasvaa vuosi vuodelta, sillä ne tarjoavat vertaansa vailla olevan ikkunan biologian monimutkaiseen maailmaan.
Mutta lukemattomien saatavilla olevien solulinjojen joukosta vain muutamat valitut solulinjat ovat nousseet merkittäviksi ja ansainneet paikkansa nykyaikaisen biolääketieteen työvälineinä. Nämä solulinjat ovat osoittaneet arvonsa kerta toisensa jälkeen, ja ne ovat tarjonneet tutkijoille välineet, joita he tarvitsevat tieteellisen tiedon rajojen laajentamiseen. Tässä artikkelissa lähdemme mukaansatempaavalle matkalle viiden tärkeimmän solulinjan läpi, jotka ovat jättäneet lähtemättömän jäljen biolääketieteellisen tutkimuksen maailmaan. Tutustumme näiden solujen voimanpesien kiehtoviin tarinoihin HeLa-solujen vaatimattomista alkuajoista HEK293-solujen mahdollistamiin huippuluokan innovaatioihin ja niiden syvälliseen vaikutukseen ymmärrykseemme elämästä itsestään. Liity siis seuraamme, kun syvennymme näiden poikkeuksellisten solulinjojen salaisuuksiin ja selvitämme, miten ne edistävät huomisen biolääketieteellisiä läpimurtoja.
Top 5 solulinjaa biolääketieteellisen tutkimuksen polttoaineena
HeLa-solut
Ensimmäinen kuolematon ihmisen solulinja, joka perustettiin vuonna 1951 Henrietta Lacksin kohdunkaulan syöpäsoluista. HeLa-solut ovat olleet keskeisessä asemassa lukuisissa tieteellisissä läpimurroissa, kuten poliorokotteen kehittämisessä.
HEK293-solut
Ihmisen alkiomunuaisperäiset epiteelisolut, joita käytetään laajalti ohimeneviin ja stabiileihin transformaatiokokeisiin, proteiinien ilmentämiseen ja tuottamiseen sekä elektrofysiologisiin kokeisiin.
MCF-7-solut
Rintasyöpäsolulinja, jota käytetään yleisesti hormonaalisen säätelyn tutkimuksessa, lääkekehityksessä ja rintasyövän biologian tutkimuksessa.
CHO-solut
Kiinalaisen hamsterin munasarjasolut, joita käytetään laajasti biologisissa, lääketieteellisissä ja farmaseuttisissa tutkimussovelluksissa, kuten rekombinanttiproteiinien tuotannossa ja epidermisen kasvutekijän reseptorin tutkimuksissa.
PC-12-solut
Rotan lisämunuaisydinytimestä peräisin oleva solulinja, jota käytetään laajalti neurotieteellisessä tutkimuksessa, erityisesti hermosolujen erilaistumisen, välittäjäaineiden synteesin ja neurotoksisuuden tutkimuksessa.
Numero 5: Sf9-solut

Sf9-soluista, jotka on saatu syyspistiäisen(Spodoptera frugiperda) munasarjakudoksesta, on tullut hyönteisten soluviljelyn ja proteiinien ilmentymistutkimusten kulmakivi. Näillä monipuolisilla soluilla on ainutlaatuinen kyky kasvaa adheesioviljelminä tai suspensioviljelminä, joten ne soveltuvat hyvin monenlaisiin sovelluksiin pienimuotoisesta laboratoriotutkimuksesta laajamittaiseen teolliseen tuotantoon.
Yksi Sf9-solujen tärkeimmistä eduista on niiden yhteensopivuus bakulovirus-ekspressiovektorijärjestelmän (BEVS) kanssa. Tämän tehokkaan välineen avulla tutkijat voivat tuoda soluihin vieraita geenejä muokattujen bakulovirusten avulla, jolloin voidaan tuottaa suuria määriä rekombinanttiproteiineja. Sf9/BEVS-yhdistelmä on osoittautunut erityisen tehokkaaksi sellaisten monimutkaisten nisäkäsproteiinien ilmentämisessä, jotka vaativat niiden biologisen aktiivisuuden kannalta välttämättömiä posttranslationaalisia modifikaatioita, kuten glykosylaatiota ja asianmukaista taittumista.
Sf9-solujen menestys proteiinituotannossa on johtanut niiden laajaan käyttöön rokotteiden, terapeuttisten proteiinien ja diagnostisten reagenssien valmistuksessa. Yksi merkittävä esimerkki on HPV-rokotteen CERVARIX® tuotanto, jossa käytetään Sf9-soluja rokotteen avainkomponentin, ihmisen papilloomaviruksen L1-proteiinin, ilmentämiseen. Kyky tuottaa tätä proteiinia suuria määriä ja erittäin puhtaana on ollut ratkaisevan tärkeää tämän hengenpelastavan rokotteen kehittämisessä ja jakelussa.
Bioteknologian sovellusten lisäksi Sf9-solut ovat osoittautuneet korvaamattomiksi myös perustutkimuksessa, erityisesti hyönteisten biologian ja isännän ja taudinaiheuttajan vuorovaikutuksen tutkimuksessa. Koska hyönteiset ovat tärkeitä vektoreita lukuisille ihmis- ja eläintaudeille, niiden biologian taustalla olevien solu- ja molekyylimekanismien ymmärtäminen voi tarjota ratkaisevan tärkeää tietoa tautien leviämisestä ja torjuntastrategioista.
Yhteenvetona voidaan todeta, että Sf9-solut ovat ansainneet paikkansa viiden tärkeimmän solulinjan joukossa biolääketieteellisessä tutkimuksessa monipuolisuutensa, kestävyytensä ja vertaansa vailla olevan menestyksensä proteiinien ilmentämisessä. Kun tutkijat jatkavat tieteellisen tiedon rajojen laajentamista, Sf9-solut ovat epäilemättä jatkossakin olennainen väline heidän arsenaalissaan, joka edistää läpimurtoja sekä perus- että soveltavassa tutkimuksessa.
Numero 4: CHO-solut
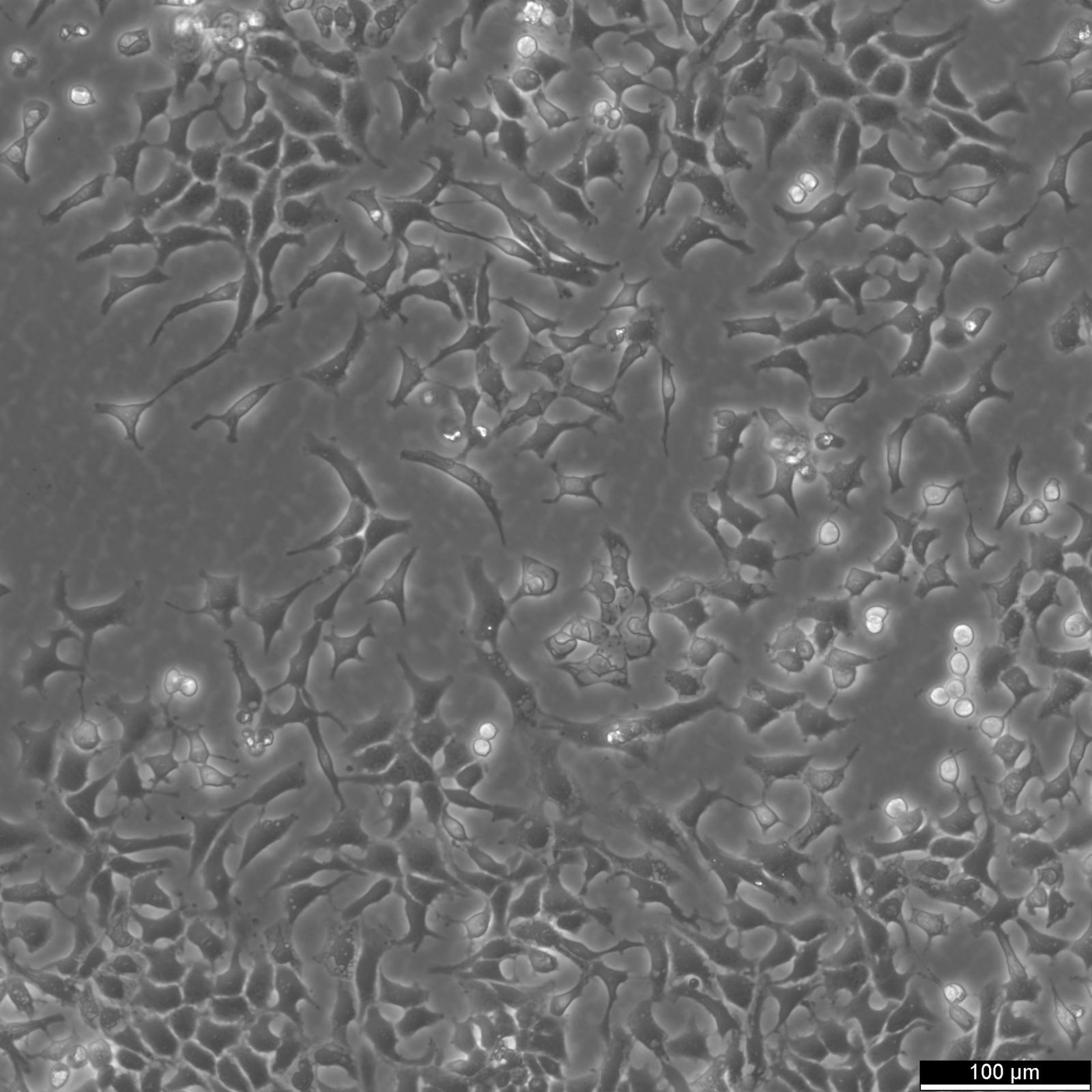
CHO-soluista eli kiinalaisen hamsterin munasarjasoluista on tullut biolääketieteellisen tutkimuksen ja biotekniikan tukipilari. Nämä nisäkässolut, jotka Theodore Puck eristi ensimmäisen kerran vuonna 1957, ovat osoittautuneet huomattavan monipuoliseksi ja kestäväksi välineeksi monenlaisiin sovelluksiin perustutkimuksesta elintärkeiden terapeuttisten lääkkeiden tuotantoon.
Yksi CHO-solujen menestyksen avaintekijöistä on niiden sopeutumiskyky erilaisiin viljelyolosuhteisiin. Niitä voidaan kasvattaa adheesioviljelminä tai suspensioviljelminä, jolloin tutkijat voivat skaalata tuotantoa tarpeen mukaan. Lisäksi CHO-solut kykenevät suorittamaan monimutkaisia posttranslationaalisia modifikaatioita, kuten glykosylaatiota, jotka ovat välttämättömiä monien nisäkäsproteiinien asianmukaisen toiminnan kannalta.
CHO-solujen kyky tuottaa biologisesti aktiivisia proteiineja on tehnyt niistä biolääketeollisuuden työhevosen. Nykyään CHO-soluja käytetään monenlaisten terapeuttisten proteiinien, kuten monoklonaalisten vasta-aineiden, hormonien ja entsyymien valmistukseen. Itse asiassa CHO-soluilla tuotetaan noin 70 prosenttia kaikista markkinoilla olevista rekombinanttiproteiiniterapeuteista, joiden maailmanlaajuinen markkina-arvo on arviolta yli 100 miljardia dollaria.
Bioteknologian sovellusten lisäksi CHO-solut ovat myös edistäneet biologisten perusprosessien ymmärtämistä. Niitä on esimerkiksi käytetty epidermisen kasvutekijän reseptorin (EGFR) tutkimiseen. EGFR on solujen kasvun ja eloonjäämisen kannalta keskeinen tekijä, joka on usein häiriintynyt syövässä. Ekspressoimalla EGFR:ää CHO-soluissa tutkijat ovat voineet selvittää sen signaalireittejä ja kehittää kohdennettuja hoitoja, joilla estetään sen toimintaa kasvaimissa.
Biolääkkeiden kysynnän kasvaessa CHO-solujen merkitys tutkimuksessa ja tuotannossa kasvaa. Jatkuvat pyrkimykset optimoida CHO-solulinjoja, kuten proteiinien saannon lisääminen, glykosylaatiomallien parantaminen ja viruskontaminaation riskin vähentäminen, vahvistavat entisestään niiden asemaa kriittisenä välineenä tautien torjunnassa.
Yhteenvetona voidaan todeta, että CHO-solut ovat ansainneet paikkansa biolääketieteellisen tutkimuksen tärkeimpien solulinjojen joukossa, koska ne ovat sopeutumiskykyisiä, kykenevät tuottamaan monimutkaisia nisäkäsproteiineja ja niillä on laaja kokemus biolääketeollisuudessa. Kun jatkamme biologian salaisuuksien selvittämistä ja uusien hoitomuotojen kehittämistä, CHO-solut ovat epäilemättä jatkossakin elintärkeä resurssi sekä tutkijoille että valmistajille.
Numero 3: Kuolemattomat ihmisen solulinjat
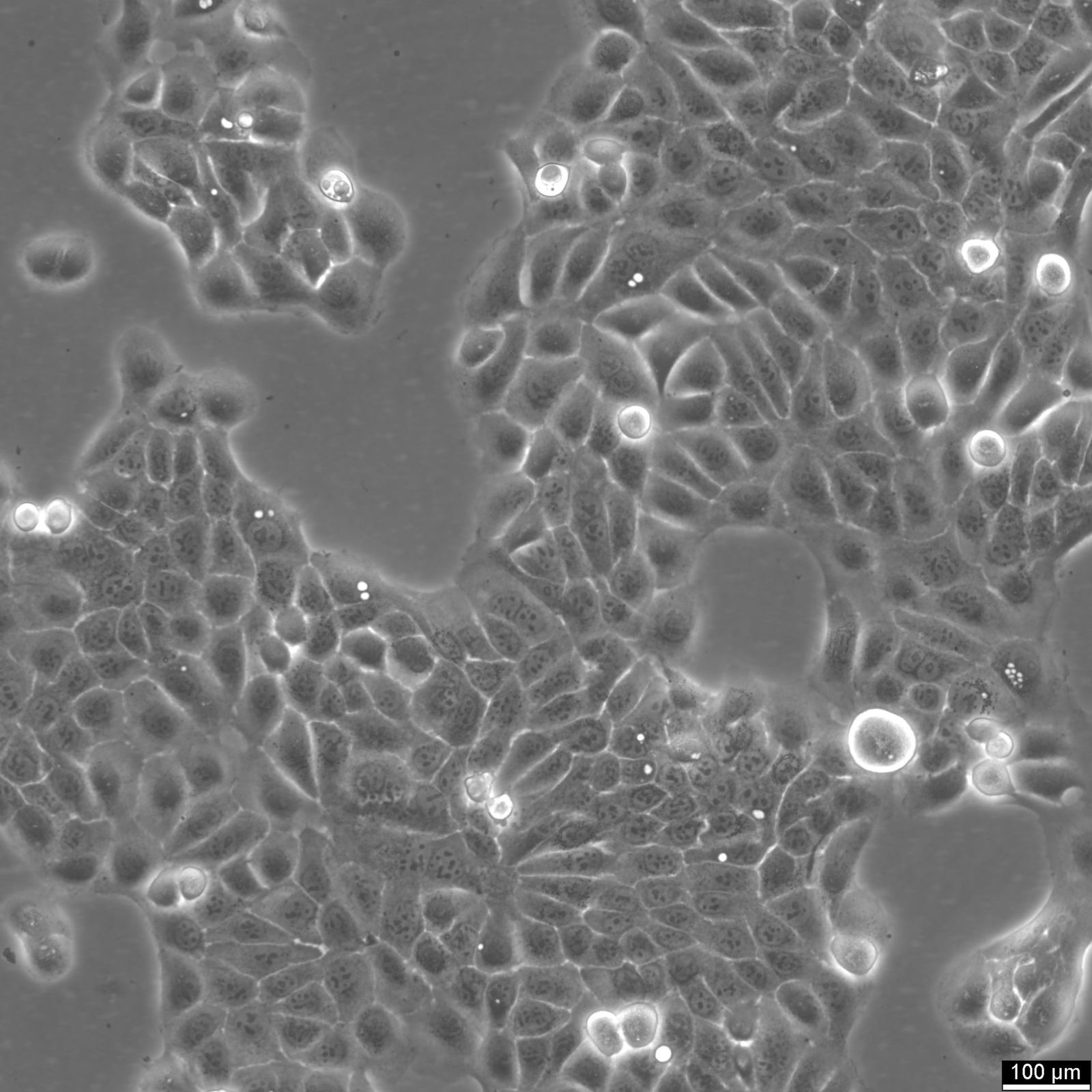
Kuolemattomista ihmissolulinjoista on tullut välttämätön väline biolääketieteellisessä tutkimuksessa, sillä ne tarjoavat tutkijoille käytännöllisesti katsoen loputtoman määrän geneettisesti yhtenäisiä soluja ihmisen biologian ja sairauksien tutkimiseen. Nämä solulinjat ovat peräisin erilaisista kudoksista, ja niitä on geneettisesti muunneltu tai ne on valittu luonnollisesti siten, että ne ovat voittaneet solujen jakautumisen normaalit rajoitukset, minkä ansiosta ne voivat lisääntyä loputtomasti viljelyssä.
Yksi kuolemattomien ihmissolulinjojen merkittävimmistä eduista on niiden kyky tarjota johdonmukainen ja toistettavissa oleva malli ihmisen biologian tutkimiseen. Poistamalla primäärisoluihin liittyvät vaihtelut, joiden elinikä on rajallinen ja jotka voivat vaihdella luovuttajasta toiseen, kuolematon solulinja antaa tutkijoille mahdollisuuden tehdä kokeita entistä tarkemmin ja luotettavammin.
Nykyisin saatavilla on laaja valikoima kuolemattomaksi tehtyjä ihmisen solulinjoja, ja jokainen solulinja tarjoaa ainutlaatuista tietoa ihmisen biologian tai sairauksien erityispiirteistä. Esimerkiksi ihmisen T-soluleukemiasta peräisin olevat Jurkat-solut ovat olleet tärkeitä T-solujen signaloinnin ja immuunivasteen tutkimisessa. Vastaavasti MCF-7-soluja, rintasyöpäsolulinjaa, on käytetty laajalti rintasyövän molekyylimekanismien tutkimiseen ja mahdollisten terapeuttisten aineiden seulontaan.
NCI-60 Human Tumor Cell Lines Screen, joka on kokoelma 60:tä kuolematon ihmisen syöpäsolulinjaa, jotka edustavat yhdeksää erilaista kasvaintyyppiä, on ollut arvokas resurssi syöpätutkimukselle siitä lähtien, kun se perustettiin 1980-luvun lopulla. Tätä paneelia on käytetty satojentuhansien yhdisteiden seulontaan syöpää vastaan, mikä on johtanut lukuisten lupaavien lääkeaihioiden tunnistamiseen ja edistänyt ymmärrystä syövän biologiasta.
Monista eduistaan huolimatta on tärkeää tunnustaa kuolemattomien ihmissolulinjojen rajoitukset. Näihin soluihin on tehty huomattavia geneettisiä muutoksia kuolemattomuuden saavuttamiseksi, mikä ei välttämättä vastaa tarkasti normaalien ihmissolujen käyttäytymistä in vivo. Lisäksi näiden solujen pitkäaikainen viljely voi johtaa uusiin geneettisiin ja fenotyyppisiin muutoksiin, mikä korostaa säännöllisten solulinjojen todentamisen ja laadunvalvontatoimenpiteiden merkitystä.
Yhteenvetona voidaan todeta, että kuolemattomat ihmisen solulinjat ovat mullistaneet biolääketieteellisen tutkimuksen tarjoamalla standardoidun ja ehtymättömän lähteen ihmissoluille monien biologisten prosessien ja sairauksien tutkimiseen. Kun tutkijat jatkavat uusien solulinjojen kehittämistä ja nykyisten jalostamista, näillä tehokkailla välineillä on epäilemättä keskeinen rooli ihmisen biologian ymmärtämisessä ja uusien hoitomuotojen kehittämisessä tulevina vuosina.
Numero 2: HEK293-solut
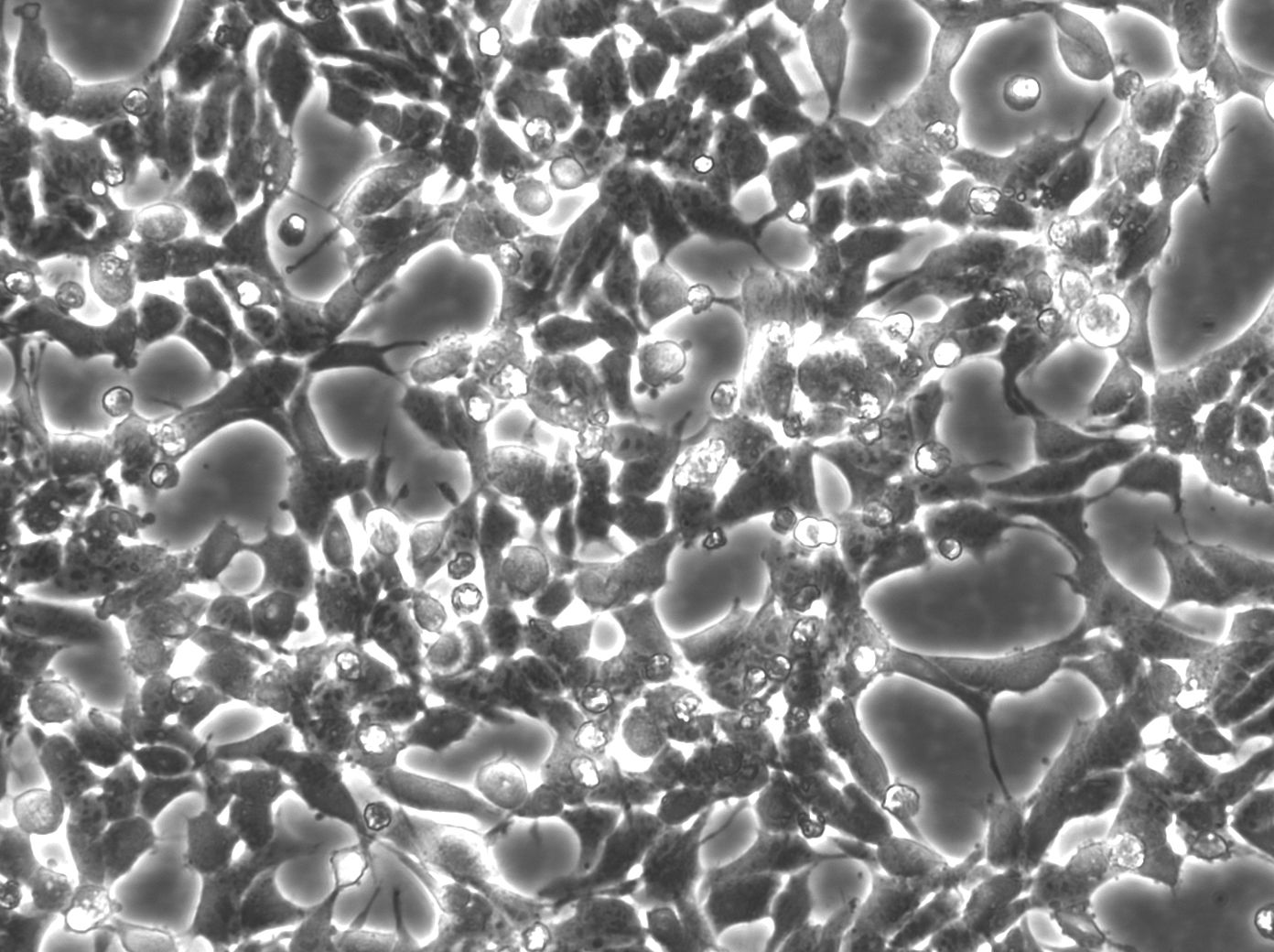
HEK293-soluista eli ihmisen alkiomunuaisen 293-soluista on tullut yksi biolääketieteellisessä tutkimuksessa yleisimmin käytetyistä solulinjoista niiden monipuolisuuden, viljelyn helppouden ja hyvän transfeekoitavuuden vuoksi. Nämä solut johdettiin alun perin ihmisen alkion munuaissoluista vuonna 1973 muuntamalla niitä adenoviruksen DNA:lla, ja niitä on sittemmin mukautettu monenlaisiin sovelluksiin.
Yksi HEK293-solujen tärkeimmistä vahvuuksista on niiden kyky ilmentää suuria määriä rekombinanttiproteiineja, kun ne transfektoidaan sopivilla ekspressiovektoreilla. Tämä on tehnyt niistä korvaamattoman arvokkaan välineen proteiinien toiminnan, signaalinsiirtoreittien ja lääkeaineiden ja proteiinien vuorovaikutusten tutkimiseen. Lisäksi HEK293-solut kykenevät suorittamaan monia proteiinien asianmukaisen toiminnan edellyttämiä translaation jälkeisiä modifikaatioita, mikä varmistaa, että näissä soluissa tuotetut rekombinanttiproteiinit muistuttavat läheisesti niiden natiivia vastinetta.
Sen lisäksi, että HEK293-soluja käytetään proteiinien ilmentymistutkimuksissa, niitä on käytetty laajalti myös geeniterapian alalla. Nämä solut ovat erittäin alttiita virusinfektiolle ja -replikaatiolle, mikä tekee niistä ihanteellisen alustan geenien levittämisessä käytettävien virusvektoreiden tuottamiseen. HEK293-soluja on itse asiassa käytetty useiden FDA:n hyväksymien geeniterapiatuotteiden, kuten selkäydinlihasatrofian hoitoon tarkoitetun Zolgensma®:n, tuottamiseen.
Viime vuosina HEK293-solut ovat myös osoittautuneet arvokkaaksi välineeksi ionikanavien ja G-proteiinikytkentäisten reseptorien (GPCR) tutkimuksessa. Ilmentämällä näitä proteiineja HEK293-soluissa ja käyttämällä kehittyneitä elektrofysiologisia tekniikoita tutkijat ovat voineet saada uutta tietoa niiden rakenteesta, toiminnasta ja farmakologiasta. Tämä on johtanut uusien lääkekohteiden tunnistamiseen ja entistä valikoivampien ja tehokkaampien terapeuttisten aineiden kehittämiseen.
Monista eduistaan huolimatta on tärkeää tunnustaa, että HEK293-solut eivät ole rajoittamattomia. Kuolemattomana solulinjana ne eivät välttämättä aina vastaa tarkasti normaalien ihmissolujen käyttäytymistä in vivo. Lisäksi näiden solujen luomisessa käytetty adenovirustransformaatio on johtanut merkittäviin genomisiin uudelleenjärjestelyihin ja muutoksiin geeniekspressiossa, mikä voi vaikuttaa niiden biologisiin ominaisuuksiin.
Yhteenvetona voidaan todeta, että HEK293-solut ovat ansainneet paikkansa yhtenä biolääketieteellisen tutkimuksen tärkeimmistä solulinjoista, koska ne ovat monipuolisia, hyvin siirrettäviä ja niillä on laaja kokemus proteiinien ilmentymisestä, geeniterapiasta ja ionikanavien/GPCR-tutkimuksista. Kun tutkijat jatkavat tieteellisen tiedon rajojen laajentamista, HEK293-solut ovat epäilemättä jatkossakin ensisijainen väline ihmisen biologian ja sairauksien monimutkaisuuden selvittämisessä.
Numero 1: HeLa-solut

HeLa-soluilla, ensimmäisellä kuolemattomalla ihmisen solulinjalla, on kiehtova ja kiistanalainen historia, joka on jättänyt lähtemättömän jäljen biolääketieteelliseen tutkimukseen. Henrietta Lacksilta vuonna 1951 otetuista kohdunkaulan syöpäsoluista peräisin olevat HeLa-solut ovat olleet tieteellisten keksintöjen eturintamassa yli puolen vuosisadan ajan, ja ne ovat myötävaikuttaneet lukuisiin läpimurtoihin syöpätutkimuksesta rokotteiden kehittämiseen.
Yksi HeLa-solujen merkittävimmistä ominaisuuksista on niiden poikkeuksellinen kestävyys ja sopeutumiskyky. Nämä solut voivat selviytyä ja lisääntyä monenlaisissa olosuhteissa, mikä tekee niistä ihanteellisen mallin lääkkeiden, toksiinien ja muiden ympäristötekijöiden vaikutusten tutkimiseen ihmissoluihin. Lisäksi HeLa-soluilla on epätavallisen korkea telomeraasiaktiivisuus, jonka ansiosta ne pystyvät säilyttämään telomeerinsa ja välttämään solujen vanhenemista, mikä osaltaan edistää niiden kuolemattomuutta.
HeLa-solujen vaikutusta biolääketieteelliseen tutkimukseen ei voi liioitella. Niitä on käytetty solubiologian lähes kaikkien osa-alueiden tutkimiseen, aina solujen perusprosesseista, kuten DNA:n replikaatiosta ja proteiinisynteesistä, monimutkaisiin tautimekanismeihin, kuten virusinfektioihin ja syövän etenemiseen. Itse asiassa HeLa-solut olivat keskeisessä asemassa poliorokotteen kehittämisessä 1950-luvulla, ja sittemmin niitä on käytetty monien eri virusten, kuten HIV:n, Zikan ja SARS-CoV-2:n, tutkimiseen.
HeLa-solujen tarina ei kuitenkaan ole kiistaton. Yleisö ei vuosikymmeniin tiennyt näiden solujen alkuperää, eikä Henrietta Lacksin perhe tiennyt, että hänen solujaan oli otettu ja käytetty tutkimukseen ilman hänen suostumustaan. Tämä herättää tärkeitä eettisiä kysymyksiä tietoon perustuvasta suostumuksesta, potilaiden yksityisyydestä ja ihmiskudosten kaupallistamisesta.
Viime vuosina on pyritty tunnustamaan Henrietta Lacksin panos tieteelle ja ottamaan hänen perheensä mukaan keskusteluihin HeLa-solujen käytöstä. Vuonna 2013 National Institutes of Health pääsi Lacksin perheen kanssa sopimukseen HeLa Genome Data Access Working Group -työryhmän perustamisesta, mikä antaa perheelle jonkin verran valtaa siihen, miten HeLa-genomitietoja käytetään tutkimuksessa.
HeLa-solut ovat niiden alkuperään liittyvistä eettisistä huolenaiheista huolimatta edelleen tärkeä väline biolääketieteellisessä tutkimuksessa. Niiden ainutlaatuiset ominaisuudet ja historiallinen merkitys ovat vakiinnuttaneet niiden aseman maailman käytetyimpänä ja vaikutusvaltaisimpana solulinjana. Kun jatkamme pohdintaa HeLa-solujen tieteellisistä ja eettisistä vaikutuksista, on selvää, että niiden vaikutus tieteeseen ja yhteiskuntaan säilyy vielä sukupolvien ajan.
Päätelmät
Tässä artikkelissa tarkastellut viisi tärkeintä solulinjaa - Sf9, CHO, kuolemattomat ihmisen solulinjat, HEK293 ja HeLa - ovat kaikki olleet keskeisessä asemassa biologian ja sairauksien ymmärtämisen edistämisessä. Nämä solulinjat ovat olleet tutkijoiden korvaamattomia työkaluja, jotka ovat mahdollistaneet uraauurtavia löytöjä ja tasoittaneet tietä uusille hoitomuodoille ja hoidoille.
Kun katsomme biolääketieteellisen tutkimuksen tulevaisuuteen, on selvää, että solulinjat ovat jatkossakin tieteellisen edistyksen kantava voima. Tarjoamalla standardoidun ja helposti saatavilla olevan mallin monimutkaisten biologisten prosessien tutkimiseen solulinjat antavat tutkijoille mahdollisuuden esittää uusia kysymyksiä, testata rohkeita hypoteeseja ja pidentää mahdollisen rajoja.
Kuten HeLa-solujen tarina kuitenkin muistuttaa, solulinjojen käyttö tutkimuksessa ei ole täysin vailla eettisiä ja sosiaalisia vaikutuksia. Tutkijoina meillä on velvollisuus paneutua näihin kysymyksiin ja varmistaa, että työmme tehdään potilaan autonomiaa, yksityisyyttä ja ihmisarvoa kunnioittaen.
Viime kädessä biolääketieteellisen tutkimuksen onnistuminen riippuu paitsi tieteellisten välineiden voimasta myös siitä, kuinka rehellisesti ja myötätuntoisesti niitä käytämme. Hyväksymällä solulinjatutkimuksen tieteelliset mahdollisuudet ja eettiset haasteet voimme jatkaa elämän mysteerien selvittämistä ja pyrkiä kohti tulevaisuutta, jossa tieteellisen edistyksen hyödyt ovat kaikkien ulottuvilla.
