8305C Kennot













430,00 €*
Tuotteet toimitetaan jäädytettyinä kuivajäässä kryoputkissa. Jokainen kryoputki sisältää tyypillisesti 3 × 10 6 solua adheesiivisille soluille tai 5 × 106 solua suspensiosoluille (katso lisätietoja erän CoA-todistuksesta).
Yleisiä tietoja
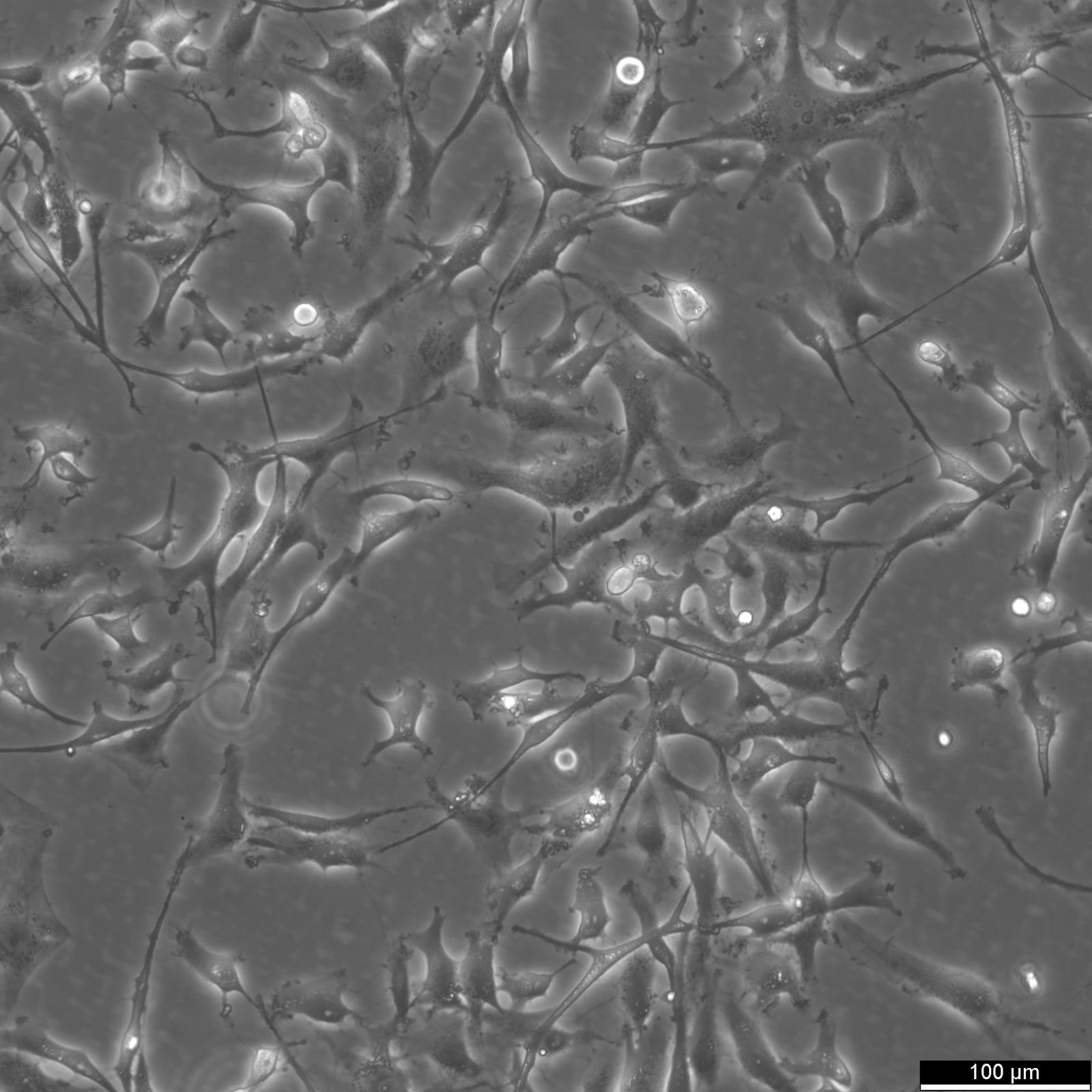
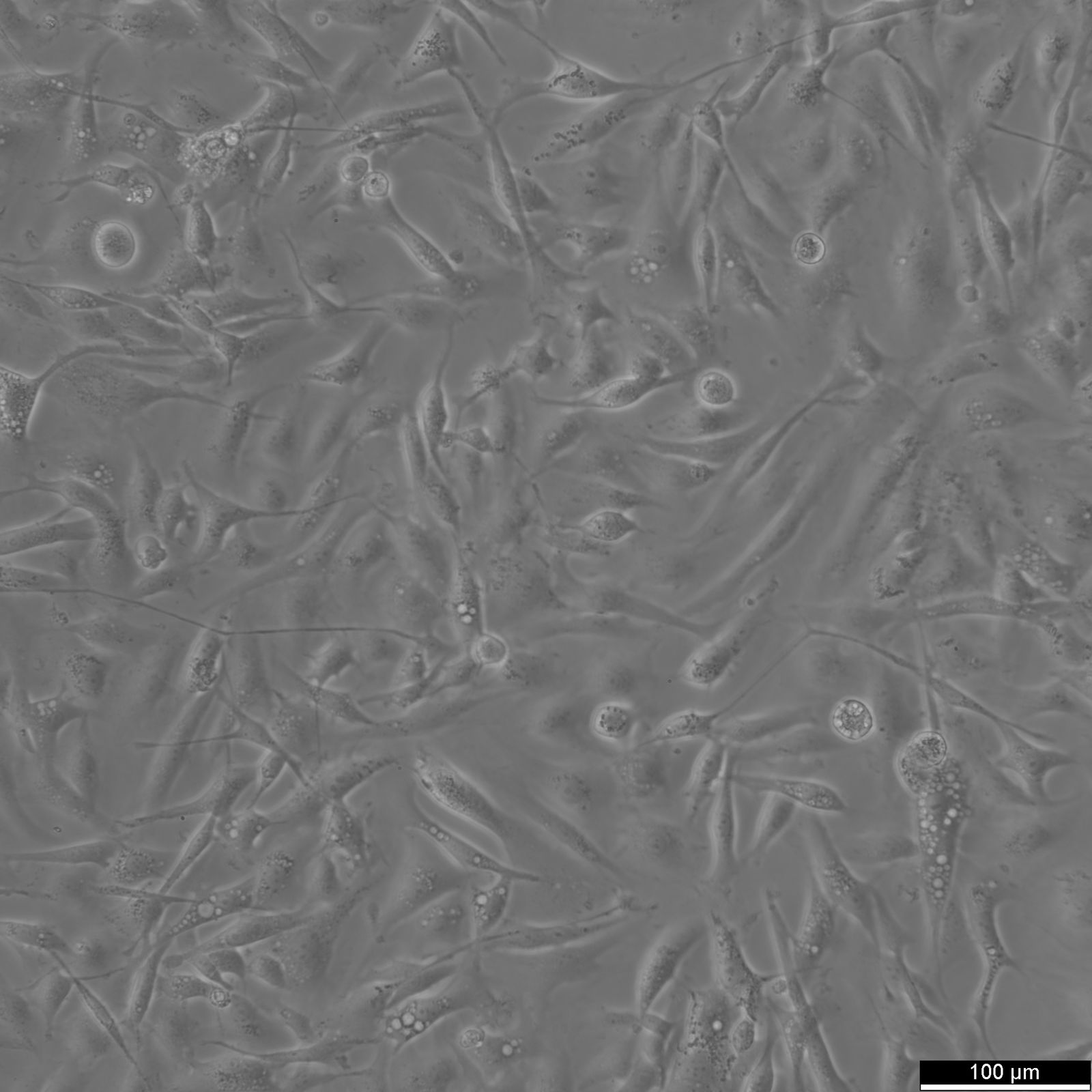
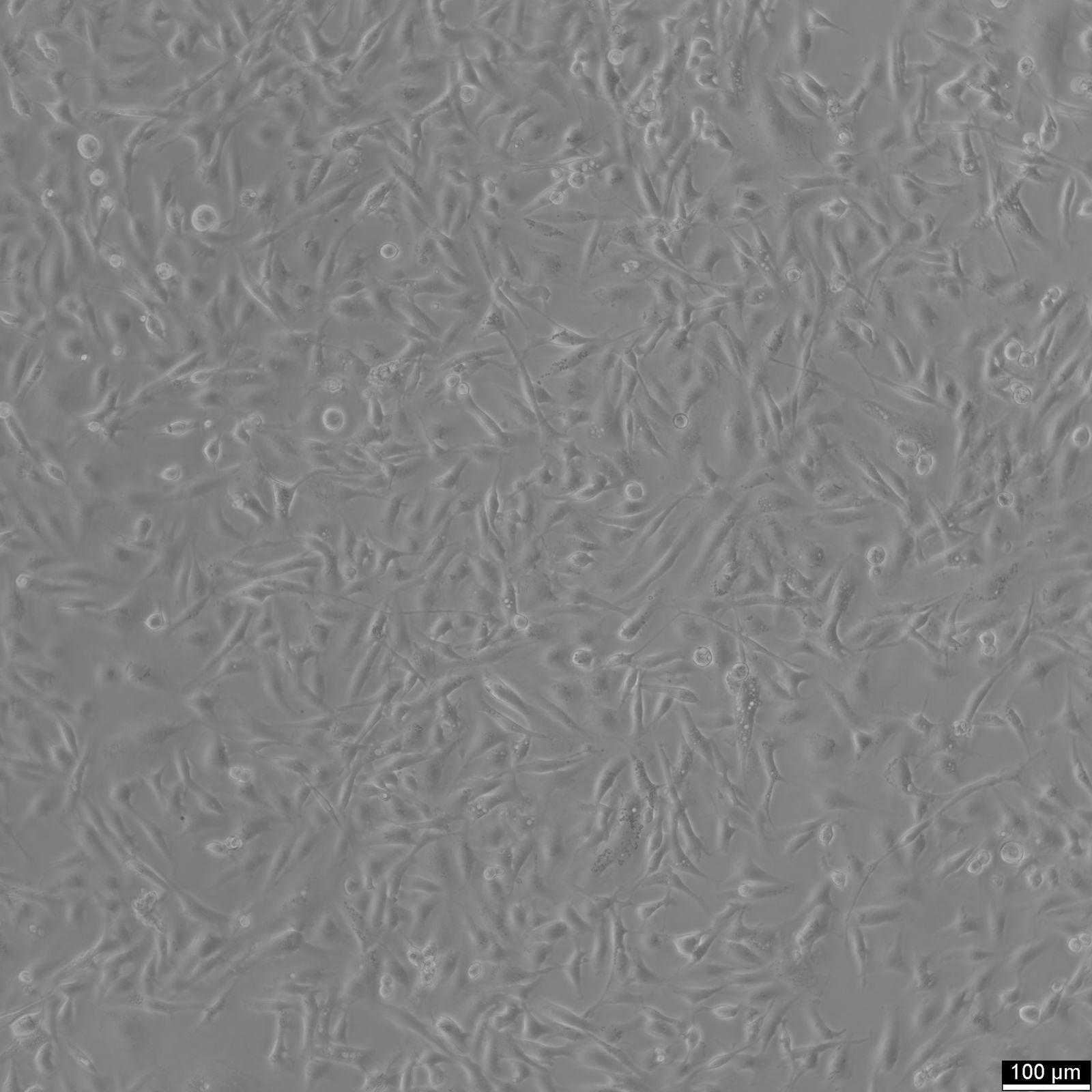
| Kuvaus | 8305C-solulinja on ihmisen kilpirauhaskarsinooman solulinja, joka on peräisin erilaistumattomasta anaplastisesta kilpirauhaskarsinoomasta. Näille soluille on ominaista aggressiivinen kasvukäyttäytyminen ja huono erilaistuminen, jotka ovat anaplastisten kilpirauhaskarsinoomien tunnusmerkkejä. Tässä solulinjassa on useita keskeisiä ominaisuuksia, jotka ovat merkityksellisiä kilpirauhassyövän patofysiologian tutkimisen kannalta, mukaan lukien muutokset geeniekspressioprofiileissa ja signaalireiteissä, jotka ovat keskeisiä kilpirauhaskarsinogeneesissä. 8305C-solulinjaa hyödyntävät tutkimukset ovat osoittaneet sen hyödyllisyyden kilpirauhassyövän etenemisen, hoitoresistenssin ja etäpesäkkeiden taustalla olevien molekyylimekanismien tutkimisessa. Erityisesti tätä solulinjaa on käytetty erilaisten kemoterapeuttisten aineiden ja kohdennettujen hoitojen tehokkuuden tutkimiseen, mikä tekee siitä arvokkaan mallin prekliiniseen lääketestaukseen. Lisäksi 8305C:tä on käytetty tutkimuksessa, jossa on keskitytty geneettisten ja epigeneettisten muutosten rooliin kilpirauhassyövässä, mikä tarjoaa tietoa tämän aggressiivisen syöpätyypin mahdollisista hoitokohteista ja biomarkkereista. Koska 8305C-solulinja on peräisin korkea-asteisesta pahanlaatuisesta kasvaimesta, se on tärkeä väline kilpirauhassyöpätutkimuksessa, erityisesti tutkimuksissa, joilla pyritään ymmärtämään anaplastisen kilpirauhaskarsinooman aggressiivista käyttäytymistä ja kehittämään strategioita sen tehokasta hoitoa varten. |
|---|---|
| Organismi | Ihminen |
| Kudos | Kilpirauhanen |
| Tauti | Kilpirauhasen anaplastinen karsinooma |
| Synonyymit | 8305c, 8305-C, 8305C_1 |
Ominaisuudet
| Ikä | 67 vuotta |
|---|---|
| Sukupuoli | Nainen |
| Etnisyys | Aasialainen |
| Morfologia | Epiteeli |
| Kasvuominaisuudet | Tarttuva |
Sääntelytiedot
| Viittaus | 8305C (Cytionin luettelonumero 305101) |
|---|---|
| Bioturvallisuustaso | 1 |
| NCBI_TaxID | 9606 |
| CellosaurusLiittyminen | CVCL_1053 |
Biomolekyylitiedot
Käsittely
| Viljelyalusta | EMEM (MEM Eagle), w: 2 mM L-Glutamiini, w: 2,2 g/L NaHCO3, w: EBSS (Cytionin artikkelinumero 820100a) |
|---|---|
| Lisäravinteet | Täydennetään elatusainetta 10 % FBS:llä ja 1 % NEAA:lla |
| Dissosiaatioreagenssi | Accutase |
| Kaksinkertaistumisaika | 54 tuntia |
| Alakulttuuri | Poista vanha väliaine tarttuneista soluista ja pese ne PBS:llä, josta puuttuu kalsiumia ja magnesiumia. Käytä T25-pulloissa 3-5 ml PBS:ää ja T75-pulloissa 5-10 ml. Peitä sitten solut kokonaan Accutase-valmisteella, käyttäen 1-2 ml T25-pulloissa ja 2,5 ml T75-pulloissa. Anna solujen inkuboitua huoneenlämmössä 8-10 minuuttia solujen irtoamiseksi. Inkuboinnin jälkeen solut sekoitetaan varovasti 10 ml:n väliaineella niiden resuspendoimiseksi ja sentrifugoidaan sitten 300xg:n nopeudella 3 minuutin ajan. Hävitä supernatantti, suspendoi solut uudelleen tuoreessa väliaineessa ja siirrä ne uusiin pulloihin, jotka sisältävät jo tuoretta väliaineita. |
| Nesteen uusiminen | 2-3 kertaa viikossa |
| Jäädytä väliaine | Kryosäilytysmediana käytämme täydellistä kasvualustaa (mukaan lukien FBS) + 10 % DMSO:ta riittävän sulatuksen jälkeisen elinkelpoisuuden varmistamiseksi tai CM-1:tä (Cytionin luettelonumero 800100), joka sisältää optimoituja osmoprotectantteja ja metabolisia stabilisaattoreita, jotka parantavat elpymistä ja vähentävät kryosäilytyksen aiheuttamaa stressiä. |
| Solujen sulattaminen ja viljely |
|
| Inkubaatioilmapiiri | 37 °C, 5 %CO2, kostutettu ilmakehä. |
| Pullon pinnoite | Ei mitään |
| Jäädytysmenettely | Kryosäilytetyt solulinjat kuljetetaan kuivajäässä validoidussa, eristetyssä pakkauksessa, jossa on riittävästi kylmäainetta, jotta lämpötila pysyy noin -78 °C:ssa koko kuljetuksen ajan. Pakkaus on tarkastettava välittömästi sen vastaanottamisen jälkeen ja injektiopullot on siirrettävä viipymättä asianmukaiseen varastoon. |
| Toimitusehdot | Kryosäilytetyt solulinjat kuljetetaan kuivajäässä validoidussa, eristetyssä pakkauksessa, jossa on riittävästi kylmäainetta, jotta lämpötila pysyy noin -78 °C:ssa koko kuljetuksen ajan. Pakkaus on tarkastettava välittömästi sen vastaanottamisen jälkeen ja injektiopullot on siirrettävä viipymättä asianmukaiseen varastoon. |
| Varastointiolosuhteet | Pitkäaikaissäilytystä varten injektiopullot asetetaan höyryfaasissa olevaan nestemäiseen typpeen noin -150 - -196 °C:een. Säilytys -80 °C:ssa on hyväksyttävää vain lyhyenä välivaiheena ennen siirtoa nestemäiseen typpeen. |
Laadunvalvonta / Geneettinen profiili / HLA
| Steriliteetti | Mykoplasmakontaminaatio suljetaan pois sekä PCR-pohjaisilla määrityksillä että luminesenssiin perustuvilla mykoplasman osoitusmenetelmillä. Bakteeri-, sieni- tai hiivakontaminaation välttämiseksi soluviljelmät tarkastetaan päivittäin silmämääräisesti. |
|---|
Analyysitodistus (CoA)
| Erän numero | Todistuksen tyyppi | Päivämäärä | Luettelonumero |
|---|---|---|---|
| 305101-130326 | Analyysitodistus | 14. Apr. 2026 | 305101 |
| 305101-030225 | Analyysitodistus | 23. May. 2025 | 305101 |
Materiaalin siirtosopimus
Jos aiot käyttää Cytion-solulinjoja yksinomaan sisäiseen tutkimukseen yhdellä tutkimuspaikalla, täytä ja allekirjoita materiaalinsiirtosopimus (MTA) ja lähetä se tilauksesi mukana.
Kaikissa kaupallisissa sovelluksissa – mukaan lukien mutta ei rajoittuen maksullisiin palveluihin, laadunvalvontatestaukseen, tuotteiden julkaisemiseen, diagnostiseen käyttöön tai sääntelytutkimuksiin – täytä käyttötarkoituksen lomake, jotta voimme laatia projektiisi sopivan sopimuksen.
Huomaa: MTA koskee vain tiettyjä solulinjoja. Jos tämä ilmoitus ja MTA-asiakirja näkyvät tuotesivulla, sopimus on voimassa. Solulinjoille, joita MTA ei koske, sopimusta ei mainita. MTA ei ole voimassa asiakkaille Amerikassa, Kiinassa tai Taiwanissa. Ota yhteyttä Yhdysvaltain yksikköömme saadaksesi sopivan sopimuksen.
-
Tarvittavat tuotteet
Tarvittavat tuotteet
Jäädytysmedium CM-1 - 50 mlKryosäilytysmediavaihtoehdot: 50 mlCytionin Freeze Medium CM-1 on huipputekninen kryosäilytysmedium, joka on suunniteltu varmistamaan solujen elinkelpoisuuden ja toimivuuden korkein mahdollinen taso sulatuksen jälkeen. Tämä monipuolinen väliaine soveltuu monille eri solutyypeille, mukaan lukien ihmis
- ja eläinsolut, mikä tekee siitä välttämättömän työkalun erilaisiin tutkimussovelluksiin. Freeze Medium CM-1 on koostettu huolellisesti tasapainotetusta yhdistelmästä kryosuojakemikaaleja ja välttämättömiä ravintoaineita, ja se minimoi jääkiteiden muodostumisen ja solustressin jäädytysprosessin aikana, jolloin solujen eheys säilyy.
Freeze Medium CM-1:n tärkeimpiä ominaisuuksia ovat mm:
Laaja yhteensopivuus: Tehokas monenlaisille solutyypeille, mukaan lukien primaarisolut, kantasolut ja vakiintuneet solulinjat.
Korkea elinkelpoisuus: Optimoitu maksimoimaan solujen palautuminen ja elinkelpoisuus sulatuksen jälkeen, mikä takaa luotettavat koetulokset.
Käyttövalmis: Kätevästi valmisteltu ja steriloitu välitöntä käyttöä varten, mikä vähentää valmisteluaikaa ja kontaminaatioriskiä.
Parannettu stabiilisuus: Säilyttää tasaisen suorituskyvyn tavanomaisissa kryosäilytysolosuhteissa, mikä takaa toistettavat tulokset.
Pitkä säilyvyysaika: CM-1 on seerumia sisältävä, käyttövalmis kryosäilytysmedia, jota voidaan säilyttää jääkaapissa jopa vuoden ajan.
CM-1:n käyttö solujen pakastamiseen
Jos haluat käyttää CM-1:tä sekä adheesiosolujen että suspensiosolujen jäädyttämiseen, toimi seuraavasti
Adheesiosolut pestään ja irrotetaan viljelyalustasta. Jos kyseessä ovat suspensiosolut, siirry suoraan seuraavaan vaiheeseen.
Laske solut varmistaaksesi, että niiden pitoisuus on oikea.
Sentrifugoi solut pelletiksi ja suspendoi ne uudelleen CM-1-pakastusmediumiin.
Siirretään resuspendoidut solut kryopulloihin.
Käytä hidasta pakastusmenetelmää ennen solujen siirtämistä pitkäaikaissäilytykseen
Menetelmä
Kuvaus
Vaiheet
❄️
Manuaalinen jäädytys
Vaiheittainen menetelmä, jossa lämpötilaa alennetaan asteittain solujen elinkelpoisuuden varmistamiseksi
1️⃣ Aseta solut pakastusmediumiin 4 °C:n pakastimeen 40 minuutiksi.
2️⃣ Siirretään -80 °C:n pakastimeen 24 tunniksi.
3️⃣ Säilytä solut nestemäisessä typessä pitkäaikaissäilytystä varten
❄️
Mr. Frostyn käyttäminen
Kätevä laite, joka mahdollistaa hallitun pakastusnopeuden ilman sähkövirtaa
1️⃣ Valmistele solut kryopulloihin pakastusmediumilla.
2️⃣ Aseta kryopullot Mr. Frosty -astiaan.
3️⃣ Säilytä -80 °C:ssa 24 tuntia ennen siirtämistä nestemäiseen typpeen
❄️
Pakastin, jonka nopeus on säädetty
Thermo Fisherin tai muiden valmistajien korkean tarkkuuden pakastin, joka on suunniteltu lämpötilan hallittuun alentamiseen
1️⃣ Ohjelmoi laite alentamaan lämpötilaa asteittain.
2️⃣ Aseta valmistetut solut pakastimeen.
3️⃣ Siirrä solut pakastussyklin jälkeen nestemäiseen typpeen
Säilytä kryopullot alle -130 °C:n lämpötilassa tai nestemäisessä typessä pitkäaikaissäilytystä varten.
Ainesosat
Sisältää FBS:ää, DMSO:ta, glukoosia, suoloja
Puskurikyky: pH = 7,2-7,6
Cytionin Freeze Medium CM-1 tarjoaa luotettavan ratkaisun kryosäilytykseen, joka takaa solujen korkean elinkelpoisuuden ja toimivuuden sulatuksen jälkeen monenlaisissa tutkimussovelluksissa.59,00 €*EMEM (MEM Eagle), w: 2 mM L-Glutamiinia, w: 2,2 g/L NaHCO3, w: EBSSYksi yleisimmin käytetyistä synteettisistä soluviljelyaineista on Minimum Essential Medium Eagle (MEM). Tämä Harry Eaglen kehittämä väliaine otettiin käyttöön ensimmäisen kerran vuonna 1959, ja siitä on sittemmin tullut suosittu valinta erilaisille solutyypeille, joita kasvatetaan monolayereissä ja tarttuvissa solulinjoissa.
Mitä EMEM:ssä on?
EMEM on modifioitu versio Eaglen minimaalisesta välttämättömästä elatusaineesta, joka sisältää Earlen tasapainotettua suolaliuosta, muita kuin välttämättömiä aminohappoja, L-glutamiinia, natriumpyruvaattia ja natriumbikarbonaattia. On tärkeää huomata, että tämä natriumbikarbonaattitaso on tarkoitettu käytettäväksi 5 %:n hiilidioksidipitoisessa ilmassa. Tehokkuuden säilyttämiseksi suositellaan väliaineen säilyttämistä pimeässä 2°C-8°C:ssa, kun sitä ei käytetä.
Mihin EMEM:ää käytetään?
Eagle's minimal essential medium (EMEM) on soluviljelyalusta, jolla voidaan ylläpitää soluja kudosviljelyssä. Väliaine sisältää korkeampia pitoisuuksia aminohappoja, mikä mahdollistaa viljeltyjen nisäkässolujen proteiinikoostumuksen tarkemman lähentämisen. EMEM:ää voidaan käyttää erilaisten solujen, kuten fibroblastien, ihmisen maksasyöpäsolulinjan (HepG2) solujen ja ihmisen sikiöaivojen progenitaattorista peräisin olevien astrosyyttisolujen (PDA) viljelyyn. Sitä käytetään tyypillisesti naudan sikiöseerumin (FBS), vasikan
- tai hevosen seerumin läsnä ollessa.
Miten EMEM eroaa muista soluviljelymedioista?
Vaikka EMEM:llä ja Dulbecco's modified Eagle's mediumilla (DMEM) on joitakin yhtäläisyyksiä, ne myös eroavat toisistaan. Molemmista väliaineista puuttuu proteiinia, ja ne sisältävät aminohappoja, suoloja, glukoosia ja vitamiineja, joita tarvitaan solun energiansaantiin ja sen ylläpitämiseen kudosviljelyssä. DMEM on kuitenkin muunnettu siten, että se sisältää jopa neljä kertaa enemmän vitamiineja ja aminohappoja ja kahdesta neljään kertaa enemmän glukoosia kuin EMEM. On syytä huomata, että EMEM eroaa myös alkuperäisestä MEM-formulaatiosta.
Laadunvalvonta
Steriilisuodatettu
Varastointi ja säilyvyys
Säilytetään +2°C
- +8°C:ssa, valolta suojattuna.
Kun se on avattu, säilytä 4°C:ssa ja käytä 6-8 viikon kuluessa.
Toimitusolosuhteet
Ympäristön lämpötila
Huolto
Säilytettävä jääkaapissa +2°C
- +8°C:ssa pimeässä. Vältä pakastamista ja usein tapahtuvaa lämmittämistä +37°C:seen, koska se heikentää tuotteen laatua.
Älä lämmitä väliaineen lämpötilaa yli 37°C äläkä käytä kontrolloimattomia lämmönlähteitä, kuten mikroaaltolaitteita.
Jos väliaineesta käytetään vain osa, poista tarvittava määrä ja lämmitä se huoneenlämpöiseksi ennen käyttöä.
Koostumus
Luokka
Ainesosat
Pitoisuus (mg/l)
Aminohapot
L-arginiini HCl
126.00
L-kystiini 2 HCl
31.30
L-Glutamiini
292.00
L-histidiini HClH2O
42.00
L-isoleusiini
52.00
L-leusiini
52.00
L-lysiini HCl
72.50
L-metioniini
15.00
L-Fenyylialaniini
32.00
L-treoniini
48.00
L-tryptofaani
10.00
L-tyrosiini 2 Na 2H2O
51.90
L-valiini
46.00
Vitamiinit
Koliinikloridi
1.00
Vitamiinit
D-kalsiumpantotenaatti
1.00
Foolihappo
1.00
myo-Inositoli
2.00
Nikotiiniamidi
1.00
Pyridoksaali-HCl
1.00
Riboflaviini
0.10
Tiamiini HCl
1.00
Epäorgaaniset suolat
CaCl2 2H2O
265.00
Epäorgaaniset suolat
KCl
400.00
MgSO4
97.67
NaCl
6800.00
NaHCO3
2200.00
NaH2PO4
122.00
Muut komponentit
D-glukoosi
1000.00
Muut aineosat
Fenolipunainen natriumsuola
11.0025,00 €*AccutaseVaihtoehdot: 100 mlAccutase Cell Dissociation Reagent
- hellävarainen vaihtoehto trypsiinille
Accutase on solujen irrotusliuos, joka mullistaa soluviljelyteollisuuden. Se on proteolyyttisten ja kollagenolyyttisten entsyymien seos, joka jäljittelee trypsiinin ja kollagenaasin toimintaa. Toisin kuin trypsiini, Accutase ei sisällä nisäkäs
- tai bakteerikomponentteja, ja se on paljon hellävaraisempi soluille, mikä tekee siitä ihanteellisen ratkaisun solujen rutiininomaiseen irrottamiseen tavanomaisista kudosviljelymuovitavaroista ja adheesiopinnoitetuista muovitavaroista. Tässä blogikirjoituksessa tarkastelemme Accutaasin hyötyjä ja käyttötapoja sekä sitä, miten se muuttaa soluviljelyä.
Accutasen edut
Accutaasilla on useita etuja perinteisiin trypsiiniliuoksiin verrattuna. Ensinnäkin sitä voidaan käyttää aina, kun tarvitaan minkä tahansa tarttuvan solulinjan hellävaraista ja tehokasta irrottamista, joten se korvaa suoraan trypsiinin. Toiseksi Accutase toimii erittäin hyvin alkion ja hermoston kantasoluissa, ja sen on osoitettu säilyttävän näiden solujen elinkelpoisuuden passageauksen jälkeen. Kolmanneksi Accutase säilyttää useimmat epitoopit myöhempää virtaussytometria-analyysia varten, joten se on ihanteellinen solupintamarkkerien analysointiin.
Lisäksi Accutasea ei tarvitse neutraloida, kun soluja passageerataan adherenttien solujen kanssa. Lisää väliaineen lisääminen solujen jakamisen jälkeen laimentaa Accutaasia niin, että se ei enää kykene irrottamaan soluja. Tämä poistaa inaktivointivaiheen tarpeen ja säästää soluviljelyteknikoiden aikaa. Accutasea ei myöskään tarvitse annostella, ja pullo säilyy jääkaapissa 2 kuukautta.
Accutaasin sovellukset
Accutase korvaa suoraan trypsiiniliuoksen, ja sitä voidaan käyttää solulinjojen passagointiin. Lisäksi Accutase toimii hyvin, kun soluja irrotetaan monien solujen pintamerkkiaineiden analysoimiseksi virtaussytometrialla ja solujen lajittelussa. Muita Accutase-käsittelyn jatkokäyttösovelluksia ovat solujen pintamarkkereiden analysointi, virusten kasvun määritys, solujen proliferaatio, kasvainsolujen migraatiomääritykset, rutiinisolupassagointi, tuotannon skaalaaminen (bioreaktori) ja virtaussytometria.
Accutaasin koostumus
Accutase ei sisällä nisäkäs
- tai bakteerikomponentteja, ja se on luonnollinen entsyymiseos, jolla on proteolyyttinen ja kollageenilyyttinen entsyymiaktiivisuus. Se on muotoiltu paljon pienemmällä pitoisuudella kuin trypsiini ja kollagenaasi, mikä tekee siitä vähemmän myrkyllisen ja hellävaraisemman, mutta yhtä tehokkaan.
Accutasen tehokkuus
Accutaasin on osoitettu olevan tehokas primääri
- ja kantasolujen irrottamisessa ja solujen korkean elinkelpoisuuden säilyttämisessä verrattuna eläinperäisiin entsyymeihin, kuten trypsiiniin. solut saadaan talteen 100-prosenttisesti 10 minuutin kuluttua, eikä solujen jättämisestä Accutaseen jopa 45 minuutiksi ole haittaa Accutasen automaattisen sulatuksen ansiosta.
Yhteenvetona
Yhteenvetona voidaan todeta, että Accutase on tehokas ratkaisu, joka on muuttamassa soluviljelyä. Hellävaraisen luonteensa, tehokkuutensa ja monipuolisuutensa ansiosta Accutase on ihanteellinen vaihtoehto trypsiinille. Jos etsit luotettavaa ja tehokasta ratkaisua solujen irrottamiseen, Accutase on ratkaisu sinulle.75,00 €*Antibiootti-/antimykoottiliuos (100x)Tuotteen yleiskatsaus
Tilavuus: 100 ml Säilytys: ≤-15°C Steriliteetti: Steriili suodatettu
Antibiootti-/antimykoottiliuos (100x) on steriili, käyttövalmis konsentraatti, joka on suunniteltu vähentämään mikrobikontaminaatioriskiä soluviljelyssä ja siihen liittyvissä laboratoriosovelluksissa. Tämä 100x-liuos sisältää vakiintuneen yhdistelmän penisilliiniä, streptomysiiniä ja amfoterisiini B:tä, joka tarjoaa laajakirjoisen antimikrobisen aktiivisuuden grampositiivisia ja gramnegatiivisia bakteereja, hiivoja ja säikeisiä sieniä vastaan. Valmiste soveltuu käytettäväksi eukaryoottisissa soluviljelmissä, bakteerialustoissa ja muissa kontaminaatioherkissä järjestelmissä, mikä tukee puhtaita ja johdonmukaisia laboratoriotoimintoja.
Käyttö ja hyödyt Rutiininomaisiin tutkimusprotokolliin optimoitua liuosta käytetään laajalti aseptisten olosuhteiden ylläpitämiseen soluviljelytyöprosesseissa. Se tarjoaa luotettavan suorituskyvyn kontaminaatioherkissä ympäristöissä ja auttaa tutkijoita vähentämään mikrobien liikakasvun riskiä vaarantamatta solujen terveyttä tai kokeiden toistettavuutta. Steriilisuodatettu koostumus poistaa tarpeen ylimääräisille liuotusvaiheille, mikä tukee virtaviivaista väliaineen valmistusta ja vähentää vaihtelua päivittäisissä laboratoriomenetelmissä.
Käyttö ja yhteensopivuus Saavuttaaksesi vakiotyöpitoisuudet laimenna liuos 1:100 täydelliseen kasvatusalustaan. Tuote on yhteensopiva monenlaisten nisäkässolulinjojen ja perusmedioiden kanssa. Jatkuvan varastosaatavuuden ansiosta tutkijat hyötyvät toimitusten luotettavasta jatkuvuudesta ja logistiikkasuunnittelun yksinkertaistamisesta. Liuos on säilytettävä ≤ -15 °C:ssa ja suojattava toistuvilta jäädytys-sulatussykleiltä stabiilisuuden säilyttämiseksi. Vain tutkimuskäyttöön. Ei käytettäväksi diagnostisissa tai terapeuttisissa toimenpiteissä. Ei käytettäväksi ihmisillä tai eläimillä.45,00 €*PBSFosfaattipuskuroitu keittosuolaliuos (PBS-liuos)
Fosfaattipuskuroitu suolaliuos (PBS) on laajalti käytetty puskuriliuos biologisessa ja kemiallisessa tutkimuksessa. Sillä on ratkaiseva merkitys pH-tasapainon ja osmolaarisuuden ylläpitämisessä erilaisten kokeellisten toimenpiteiden aikana, mukaan lukien kudosten käsittely ja soluviljely. PBS-liuoksemme on valmistettu huolellisesti erittäin puhtaista ainesosista vakauden ja luotettavuuden varmistamiseksi jokaisessa kokeessa. PBS-liuoksemme osmolaarisuus ja ionipitoisuudet jäljittelevät läheisesti ihmiskehon osmolaarisuutta ja ionipitoisuuksia, joten se on isotoninen ja myrkytön useimmille soluille.
PBS-liuoksemme koostumus
PBS-liuoksemme on pH-säädetty sekoitus erittäin puhdasta laatua olevia fosfaattipuskureita ja suolaliuoksia. Se sisältää 1-kertaisena käyttökonsentraationa:
8000 mg/l natriumkloridia (NaCl)
200 mg/l kaliumkloridia (KCl)
1150 mg/L natriumfosfaattidibasinen vedetön (Na2HPO4)
200 mg/L Kaliumfosfaatti, monobasinen, vedetön (KH2PO4)
Tämä koostumus takaa optimaalisen pH
- ja ionitasapainon, joka soveltuu monenlaisiin biologisiin sovelluksiin.
PBS-liuoksemme käyttökohteet
PBS-liuoksemme soveltuu erinomaisesti erilaisiin biologisen tutkimuksen sovelluksiin. Sen isotonisten ja myrkyttömien ominaisuuksien ansiosta se soveltuu aineiden laimentamiseen ja solusäiliöiden huuhteluun. EDTA:ta sisältävät PBS-liuokset irrottavat tehokkaasti kiinnittyneet ja kyhmyiset solut. PBS:ään ei kuitenkaan pitäisi lisätä kaksiarvoisia metalleja, kuten sinkkiä, sillä ne voivat aiheuttaa saostumista. Tällaisissa tapauksissa suositellaan Goodin puskureita. Lisäksi PBS-liuoksemme on hyväksyttävä vaihtoehto virusten kuljetusalustalle RNA-virusten, kuten SARS-CoV-2:n, kuljetuksessa ja säilytyksessä.
Laadunvalvonta
Steriilisuodatettu
Varastointi ja säilyvyys
Säilytetään +2 °C:n ja +25 °C:n välillä valolta suojattuna.
Kun se on avattu, säilytä 2°C-25°C:ssa ja käytä 24 kuukauden kuluessa.
Kuljetusolosuhteet
Ympäristön lämpötila
Huolto
Säilytettävä jääkaapissa +2°C
- +8°C:ssa pimeässä. Vältä pakastamista ja usein tapahtuvaa lämmittämistä +37°C:een, koska se heikentää tuotteen laatua.
Älä lämmitä väliaineen lämpötilaa yli 37°C äläkä käytä kontrolloimattomia lämmönlähteitä, kuten mikroaaltolaitteita.
Jos väliaineesta käytetään vain osa, poista tarvittava määrä ja lämmitä se huoneenlämpöiseksi ennen käyttöä.
Koostumus
Luokka
Ainesosat
Pitoisuus (mg/l)
Suolat
Kaliumkloridi
200
Kaliumfosfaattimonobasinen vedetön kaliumfosfaatti
200
Natriumkloridi
8000
Vedetön dibasinen natriumfosfaatti
115020,00 €*





