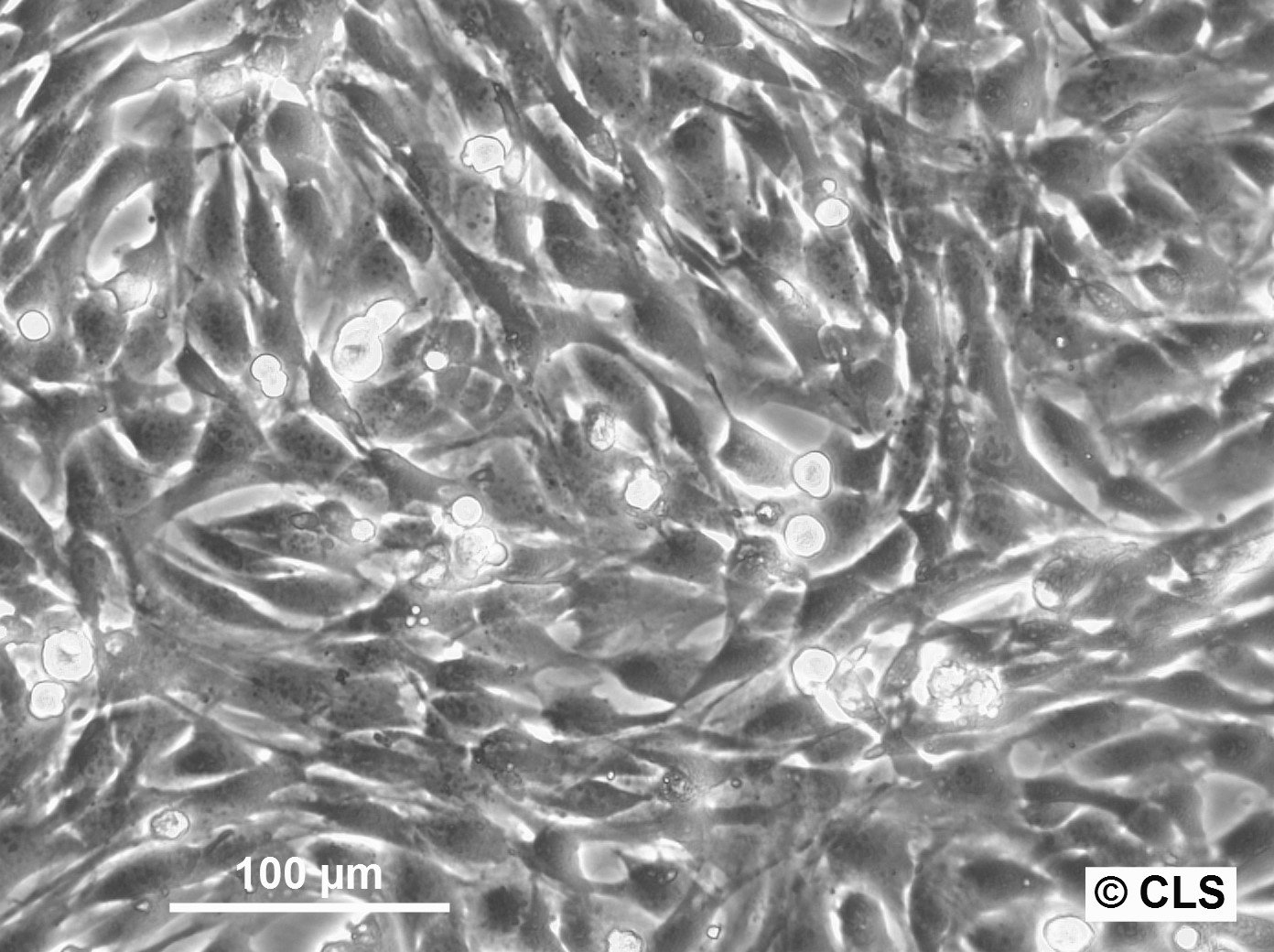
C2C12-Myoblasten-Zellen: Wegweisend in der Muskelbiologie und Regenerationsforschung
Die in der Muskelbiologie und -regeneration bekannten C2C12-Myoblastenzellen sind ein unverzichtbares Werkzeug für Forscher, die sich mit den Feinheiten der Skelettmuskelbildung, Differenzierung und molekularen Dynamik befassen. Diese aus Mäusen stammende Zelllinie bietet eine robuste Plattform für die Erforschung der zellulären und genetischen Grundlagen der Muskelfunktion und -reparatur.
Bevor Sie sich auf die Reise mit C2C12-Zellen begeben, sollten Sie sich unbedingt mit ihrer Herkunft, ihren Eigenschaften und ihren Anwendungsmöglichkeiten vertraut machen. Dieser Überblick bietet wesentliche Einblicke in:
Erforschung der Grundlagen von C2C12-Myoblastenzellen
Zu verstehen, woher C2C12-Zellen kommen und welche einzigartigen Eigenschaften sie haben, ist von grundlegender Bedeutung, um ihr Potenzial in der Forschung zu nutzen. Dieser Abschnitt gibt Aufschluss über:
- Die Anfänge der C2C12-Zellen gehen auf die Pionierarbeit von Yaffe und Saxel im Jahr 1977 zurück, die diese Zelllinie aus dem Oberschenkelmuskel einer zwei Monate alten C3H-Maus nach einer Quetschverletzung herstellten. Diese Entstehungsgeschichte verdeutlicht die Widerstandsfähigkeit und Regenerationsfähigkeit dieser Zellen.
- In Kultur zeigen C2C12-Zellen eine bemerkenswerte Anpassungsfähigkeit: Sie gedeihen unter Bedingungen mit hohem Serumgehalt, um sich zu vermehren, und gehen zur Bildung von Myotubes über , wenn sie in Serumersatz-Kultursystemen Bedingungen mit niedrigem Serumgehalt ausgesetzt werden, und differenzieren sich von proliferierenden Myoblasten zu reifen Myotubes. Dieser Übergang wird durch ein gut orchestriertes Netzwerk von Signalen gesteuert, das von intrazellulären Stoffwechselverschiebungen bis hin zu Veränderungen der Membrantransporter reicht und einen Einblick in die zelluläre Anpassung und Spezialisierung ermöglicht.
- Die charakteristische myoblastenähnliche Morphologie der C2C12-Zellen, die durch radiale Verzweigungen und längliche Fasern gekennzeichnet ist, bietet ein dynamisches Modell für die Untersuchung des Verhaltens und der Interaktionen von Muskelzellen.
- Mit ihrem diploiden Chromosomenstatus bieten C2C12-Zellen einen stabilen genetischen Hintergrund für Experimente und gewährleisten so Konsistenz und Zuverlässigkeit der Forschungsergebnisse.
Begeben Sie sich auf eine Forschungsreise mit C2C12-Myoblastenzellen, um neue Dimensionen in der Muskelbiologie und -regeneration zu entdecken und ihr Potenzial zu nutzen, um unser Verständnis von Muskelkrankheiten und therapeutischen Strategien zu verbessern.
Informationen zur Kultivierung von C2C12-Zellen
C2C12-Zellen, die für ihre Rolle in der muskelbiologischen Forschung weithin bekannt sind, benötigen spezifische Bedingungen für optimales Wachstum und Differenzierung. Hier sind die wichtigsten Punkte, die bei der Kultivierung von C2C12-Myoblasten zu beachten sind:
Verdopplungszeit: C2C12-Zellen haben in der Regel eine Verdopplungszeit von 12 bis 24 Stunden, was auf ihre schnelle Vermehrungsrate unter idealen Bedingungen hinweist.
Zelltyp: Diese Myoblasten sind adhärent und benötigen eine geeignete Oberfläche für Anhaftung und Wachstum.
Aussaatdichte: Die ideale Aussaatdichte für C2C12-Zellen beträgt etwa 1 x 10^4 Zellen/cm^2. Bei dieser Dichte erreichen die Zellen in der Regel nach etwa 4 Tagen die Konfluenz, so dass es wichtig ist, die Zellkonfluenz zu überwachen, um ein Überwachsen zu verhindern.
Wachstumsmedium: Das empfohlene Medium für die Kultivierung von C2C12-Zellen ist RPMI 1640, angereichert mit 10 % fötalem Rinderserum (FBS) und 2,1 mM L-Glutamin. Dieses Medium unterstützt den Nährstoffbedarf der Zellen und fördert eine gesunde Vermehrung.
Wachstumsbedingungen: Die Kultivierung erfolgt am besten bei 37 °C in einem befeuchteten Inkubator mit 5 % CO2, wodurch eine Umgebung geschaffen wird, die physiologische Bedingungen imitiert.
Lagerung: Zur langfristigen Konservierung werden C2C12-Zellen in der Dampfphase von Flüssigstickstoff oder in Ultratiefkühltruhen bei Temperaturen unter -150 °C gelagert.
Einfrieren und Auftauen: Bei Verwendung von CM-1- oder CM-ACF-Einfriermedien wird eine langsame Einfriermethode empfohlen, um die Temperatur schrittweise zu senken und die Lebensfähigkeit der Zellen zu erhalten. Nach dem Auftauen werden die Zellen vorsichtig in frischem Medium resuspendiert, zentrifugiert, um das Gefriermedium zu entfernen, und dann in neue Kulturflaschen übertragen.
Biologische Sicherheit: Die Kultivierung von C2C12-Zellen erfordert eine Einstellung der Biologischen Schutzstufe 1, die eine sichere Handhabung und Pflege im Labor gewährleistet.
Die Einhaltung dieser Kultivierungsparameter gewährleistet die Gesundheit und Lebensfähigkeit von C2C12-Zellen und erleichtert erfolgreiche Experimente und Forschungsergebnisse in der Muskelbiologie und darüber hinaus.
C2C12-Zelllinie: Vorteile und Beschränkungen
Die C2C12-Mausmyoblasten-Zelllinie, die aus Skelettmuskelgewebe gewonnen wird, ist in der biomedizinischen Forschung wegen ihrer einzigartigen Vorteile und Einschränkungen weithin anerkannt.
Vorteile
Gut charakterisiert: C2C12-Zellen sind umfassend untersucht worden, was ein tiefes Verständnis ihrer physiologischen und biologischen Eigenschaften wie Morphologie, Differenzierungspotenzial und Reaktion auf verschiedene Stimuli ermöglicht. Diese gründliche Charakterisierung gewährleistet Zuverlässigkeit und Reproduzierbarkeit der Forschungsergebnisse.
Muskeldifferenzierung: Eine wesentliche Stärke von C2C12-Zellen ist ihre Fähigkeit, sich in Myotubes zu differenzieren und so die Entwicklung von Muskelzellen nachzuahmen. Dies macht sie zu einem unverzichtbaren Instrument für die Erforschung der Muskelbiologie, einschließlich der Bildung von Muskelzellen, der Entwicklung und der Expression von kontraktilen Proteinen, die für die Muskelfunktion entscheidend sind.
Vielseitiges Modell für die Zellbiologie: Als gut dokumentiertes Modell bieten C2C12-Zellen Einblicke in zahlreiche zelluläre Prozesse, darunter Reaktionen auf oxidativen Stress, Glukosestoffwechsel, Insulinsignale und die Mechanismen der Insulinresistenz. Ihre Verwendung ermöglicht ein tieferes Verständnis dieser Prozesse sowohl auf zellulärer als auch auf molekularer Ebene.
Beschränkungen
Spezies-spezifische Unterschiede: Da es sich bei den C2C12-Zellen um eine aus Mäusen stammende Zelllinie handelt, können sie die menschliche Muskelbiologie nicht perfekt nachbilden. Unterschiede in der Genexpression, im Zellstoffwechsel und in den physiologischen Reaktionen zwischen Mäusen und Menschen können die direkte Übertragbarkeit von Forschungsergebnissen auf menschliche Bedingungen einschränken.
Diese Aspekte unterstreichen die kritische Rolle von C2C12-Zellen in der Muskelforschung und verdeutlichen gleichzeitig, wie wichtig es ist, ihre Grenzen zu berücksichtigen, insbesondere bei der Extrapolation von Daten auf die Biologie des Menschen.
Verbessern Sie Ihre Forschung mit C2C12-Zellen
Forschungsanwendungen der C2C12-Zelllinie
Entdecken Sie die vielfältigen Forschungsanwendungen der C2C12-Mauszelllinie.
Untersuchung der Muskelbiologie: C2C12-Zellen dienen als robustes In-vitro-Modell für die muskelbiologische Forschung und ermöglichen Studien zu Muskelentwicklung, -stoffwechsel und -differenzierung. Diese Zellen können sich in muskelähnliche Zellen differenzieren, was Einblicke in die Bildung von Myotuben und die Mechanismen der Muskelregeneration ermöglicht. In einer bemerkenswerten Studie wurde die Rolle von TGF-β1 und microRNA-22 bei den Funktionen von C2C12-Zellen hervorgehoben, wobei ihre regulierende Wirkung auf die Zellproliferation und -differenzierung betont wurde.
Medikamenten-Screening und Toxizitätstests: Die C2C12-Zelllinie ist von entscheidender Bedeutung für die Bewertung potenzieller Therapeutika für Muskelkrankheiten. Sie bietet eine Plattform zur Bewertung der Auswirkungen von Medikamenten auf den Stoffwechsel und die Differenzierung von Muskelzellen. Forschungen haben gezeigt, dass der Extrakt aus den Blättern vonCnidoscolus aconitifolius sich positiv auf die C2C12-Zellen auswirkt , indem er die Fettsäureoxidation und die mitochondriale Bioenergetik verbessert, während der Extrakt aus den Blättern vonMoringa oleifera die C2C12-Myotubes vor oxidativem Stress schützt. C2c12-Zellen sind von unschätzbarem Wert für das Screening epigenetischer Arzneimittel, die die Muskeldifferenzierung oder die Myofilamentproteinkonzentration beeinflussen könnten. Das epigenetische Medikamentenmodell ermöglicht es den Forschern, die Follistatin-Expression und die smad1-Phosphorylierung zu beobachten, entscheidende Faktoren bei der Reifung und Regeneration von Muskelstammzellen.
- 3D-Gewebekonstrukte und Entwicklung von Skelettmuskelgewebe: Unter Verwendung des Myoblasten-Kulturmediums c2c12 haben Wissenschaftler erfolgreich Myoblasten und Myotubes in dreidimensionalen Zellkulturen kultiviert, die die Struktur und Funktion von Skelettmuskelgewebe nachahmen. Diese dreidimensionalen Gewebekonstrukte bieten ein detailliertes Modell zur Untersuchung der Sarkomerbildung, der Grundeinheit der Muskelkontraktion. Durch die Bereitstellung eines dreidimensionalen Rahmens tragen solche Konstrukte wesentlich zu unserem Verständnis der Myogenese und der Entwicklung verschiedener Muskelphänotypen bei und geben Aufschluss über die komplexe Orchestrierung anderer Proteine und den Gehalt an kontraktilen Proteinen während der Muskelbildung.
Herstellung von Skelettmuskelzellen: Das Endziel bleibt die praktische Anwendung dieser Forschung auf die In-vivo-Muskelreifung und die Produktion von Skelettmuskelzellen, um geschädigtes Gewebe in klinischen Situationen zu reparieren oder zu ersetzen. Die Kultivierung von Satellitenzellen in Verbindung mit der konventionellen Kultivierung von Serum-Supplementen legt den Grundstein für die Entwicklung von Therapien, die die Behandlung von Muskelkrankheiten revolutionieren könnten.
Sarkomerbildung und kontraktile Funktion: Die Sarkomerbildung in den aus C2C12-Zellen gewonnenen Myotubes ist ein Hauptinteresse der Forscher. Die Sarkomere sind die grundlegenden kontraktilen Einheiten der Muskelzellen, und ihr ordnungsgemäßer Aufbau ist entscheidend für die Muskelfunktion. Die Untersuchung dieser Strukturen liefert wertvolle Informationen über den Gehalt an kontraktilen Proteinen und die allgemeine Muskelgesundheit, insbesondere wenn C2C12-Zellen verschiedenen Medikamenten ausgesetzt werden, die diese Prozesse beeinflussen können.
Transfektionsprotokoll für C2C12-Zellen
Benötigte Materialien:
C2C12-Myoblastenzellen
Wachstumsmedium: DMEM mit 10-20% FBS
Transfektionsreagenz (z. B. Lipofectamine)
Plasmid-DNA oder siRNA
Opti-MEM oder ähnliche serumfreie Medien
6-Well-Platten oder Kulturschalen
Inkubator, eingestellt auf 37°C mit 5% CO2
Verfahren:
Zellaussaat:
Einen Tag vor der Transfektion säen Sie C2C12-Zellen in eine 6-Well-Platte, um sicherzustellen, dass sie zum Zeitpunkt der Transfektion zu 70-80% konfluent sind.
DNA-Reagenzien-Mischung:
Verdünnen Sie die Plasmid-DNA oder siRNA in Opti-MEM (ohne Serum) auf ein Endvolumen, das ein optimales DNA-Reagenz-Verhältnis ermöglicht.
Mischen Sie das Transfektionsreagenz mit Opti-MEM in einem separaten Röhrchen und inkubieren Sie es 5 Minuten lang bei Raumtemperatur.
Kombinieren Sie die DNA- und Reagenzmischungen und inkubieren Sie 20 Minuten bei Raumtemperatur, um die Komplexbildung zu ermöglichen.
Transfektion:
Entfernen Sie das Wachstumsmedium von den Zellen und ersetzen Sie es durch den DNA-Reagenzien-Komplex in Opti-MEM.
Die Zellen mit der Transfektionsmischung 4-6 Stunden lang im Inkubator inkubieren.
Austausch des Mediums:
Nach der Inkubation ersetzen Sie die Transfektionsmischung durch frisches Wachstumsmedium und bringen die Zellen zurück in den Inkubator.
Expressionsanalyse:
Analysieren Sie die Transfektionseffizienz nach 24-48 Stunden, indem Sie die Expression des transfizierten Gens oder die Auswirkungen der siRNA überprüfen.
Differenzierungsprotokoll für C2C12-Zellen
Benötigte Materialien:
C2C12-Myoblastenzellen
Wachstumsmedium: DMEM mit 10-20% FBS
Differenzierungsmedium: DMEM mit 2% Pferdeserum
6-Well-Platten oder Kulturschalen
Inkubator bei 37°C und 5% CO2
Verfahren:
Zellaussaat:
C2C12-Zellen in eine 6-Well-Platte oder eine Kulturschale säen und in Wachstumsmedium wachsen lassen, bis sie die volle Konfluenz erreichen.
Induktion der Differenzierung:
Sobald die Zellen konfluent sind, wird das Wachstumsmedium abgesaugt und durch Differenzierungsmedium ersetzt.
Die niedrige Serumkonzentration ist entscheidend für die Einleitung der Differenzierung.
Pflege:
Wechseln Sie das Differenzierungsmedium täglich, um frische Nährstoffe zuzuführen und Zelltrümmer zu entfernen.
Überwachung der Differenzierung:
Beobachten Sie die Zellen täglich unter dem Mikroskop. Innerhalb von 1-2 Tagen sollten sich die Myoblasten ausrichten und zu Myotuben verschmelzen.
Die vollständige Differenzierung und Myotubusbildung erfolgt in der Regel innerhalb von 3-5 Tagen.
Analyse:
Nach 5-7 Tagen sollten die differenzierten Myotubes für nachgeschaltete Anwendungen wie Immunfluoreszenz- oder Proteinexpressionsanalysen bereit sein.
Hinweis: Die genauen Bedingungen für die Transfektion und Differenzierung (z. B. die Konzentration des Transfektionsreagenzes oder der Serumanteil im Differenzierungsmedium) können variieren und sollten je nach den spezifischen experimentellen Anforderungen optimiert werden. Konsultieren Sie immer die Produktdatenblätter oder die wissenschaftliche Literatur für optimale Bedingungen.
Ressourcen für die C2C12-Zelllinie: Protokolle, Videos und mehr
Entdecken Sie wertvolle Ressourcen für die C2C12-Zelllinie:
C2C12-Transfektionsprotokoll: Ein umfassendes Video-Tutorial, das die In-vitro-Transfektion von C2C12-Zellen beschreibt.
C2C12-Myoblasten: Dieser Protokollleitfaden enthält die wichtigsten Informationen zur Passage und Transfektion von C2C12-Muskelzellen.
C2C12-Kultur: Bietet wichtige Erkenntnisse zur Kultivierung und Differenzierung von C2C12-Zellen.
C2C12-Differenzierung: Dieses Dokument bietet einen detaillierten Leitfaden für die Kultivierung und Differenzierung von C2C12-Zellen aus gefrorenen Kulturen.
C2C12-Zellen: Forschungspublikationen
Nachfolgend sind wichtige Veröffentlichungen über C2C12-Zellen aufgeführt:
Interleukin-6 induziert myogene Differenzierung über JAK2-STAT3-Signalisierung: Diese 2019 im International Journal of Molecular Sciences veröffentlichte Studie untersucht die Rolle von IL-6 bei der myogenen Differenzierung von C2C12-Zellen und beleuchtet den zugrunde liegenden JAK2/STAT3-Signalweg.
Auswirkung des Blattextrakts von Rubus Anatolicus auf den Glukosestoffwechsel: Diese im Jahr 2023 veröffentlichte Forschungsarbeit untersucht die Modulation des Glukosestoffwechsels durch Rubus Anatolicus in C2C12- und anderen Zelllinien, was darauf hindeutet, dass er die Glykogenese fördern kann.
Die reduzierte Wirkung von Myostatin auf die Differenzierung von C2C12-Zellen: In diesem Artikel von 2020 Biomolecules wird erörtert, wie die Differenzierung von C2C12-Zellen den Einfluss von Myostatin auf die intrazelluläre Signalübertragung deutlich verringert, was neue Erkenntnisse über die Muskelentwicklung liefert.
Die Auswirkungen von Genistein auf Gene, die mit dem Insulinweg in Verbindung stehen: Eine 2018 in Folia Histochemica et Cytobiologica veröffentlichte Studie, in der differenzierte C2C12-Zellen verwendet wurden, um den Einfluss von Genistein auf Insulinweg-Gene zu bewerten.
Die Rolle von Moringa Oleifera im oxidativen Stoffwechsel: Diese Forschung in Phytomedicine Plus (2021) geht davon aus, dass der Extrakt aus Moringa Oleifera-Blättern die mitochondriale Biogenese in C2C12-Myotubes über den SIRT1-PPARα-Weg fördert.
Häufig gestellte Fragen zu C2C12-Zellen
Referenzen
- Denes, L.T., et al., Culturing C2C12 myotubes on micromolded gelatin hydrogels accelerates myotube maturation. Skeletal muscle, 2019. 9(1): p. 1-10.
- Wong, C.Y., H. Al-Salami, and C.R. Dass, C2C12 cell model: its role in understanding of insulin resistance at the molecular level and pharmaceutical development at the preclinical stage. J Pharm Pharmacol, 2020. 72(12): p. 1667-1693.
- Wang, H., et al. miR-22 reguliert die Proliferation und Differenzierung von C2C12-Myoblasten durch Targeting von TGFBR1. European Journal of Cell Biology, 2018. 97(4): p. 257-268.
- Avila-Nava, A., et al., Chaya (Cnidoscolus aconitifolius (Mill.) IM Johnst) leaf extracts regulate mitochondrial bioenergetics and fatty acid oxidation in C2C12 myotubes and primary hepatocytes. Zeitschrift für Ethnopharmakologie, 2023. 312: p. 116522.
- Ceci, R., et al., Moringa oleifera leaf extract protects C2C12 myotubes against H2O2-induced oxidative stress. Antioxidants, 2022. 11(8): p. 1435.