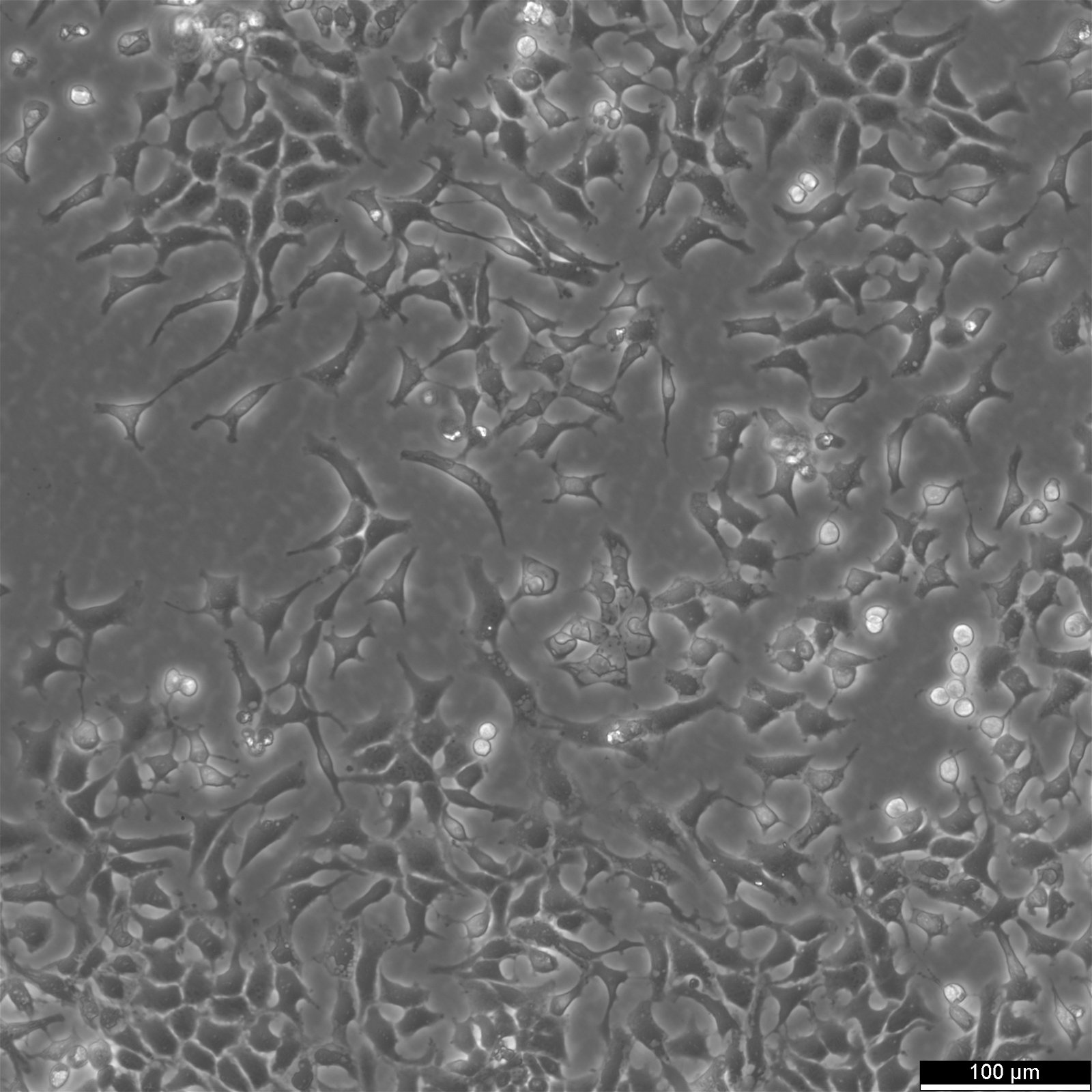
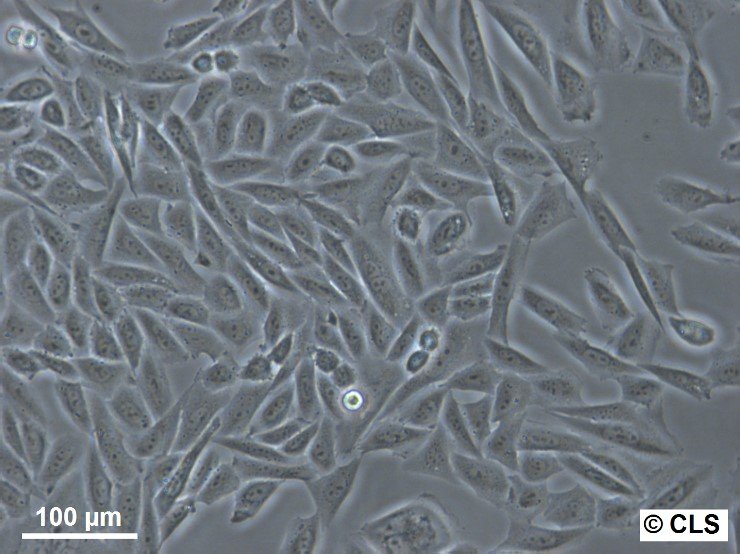
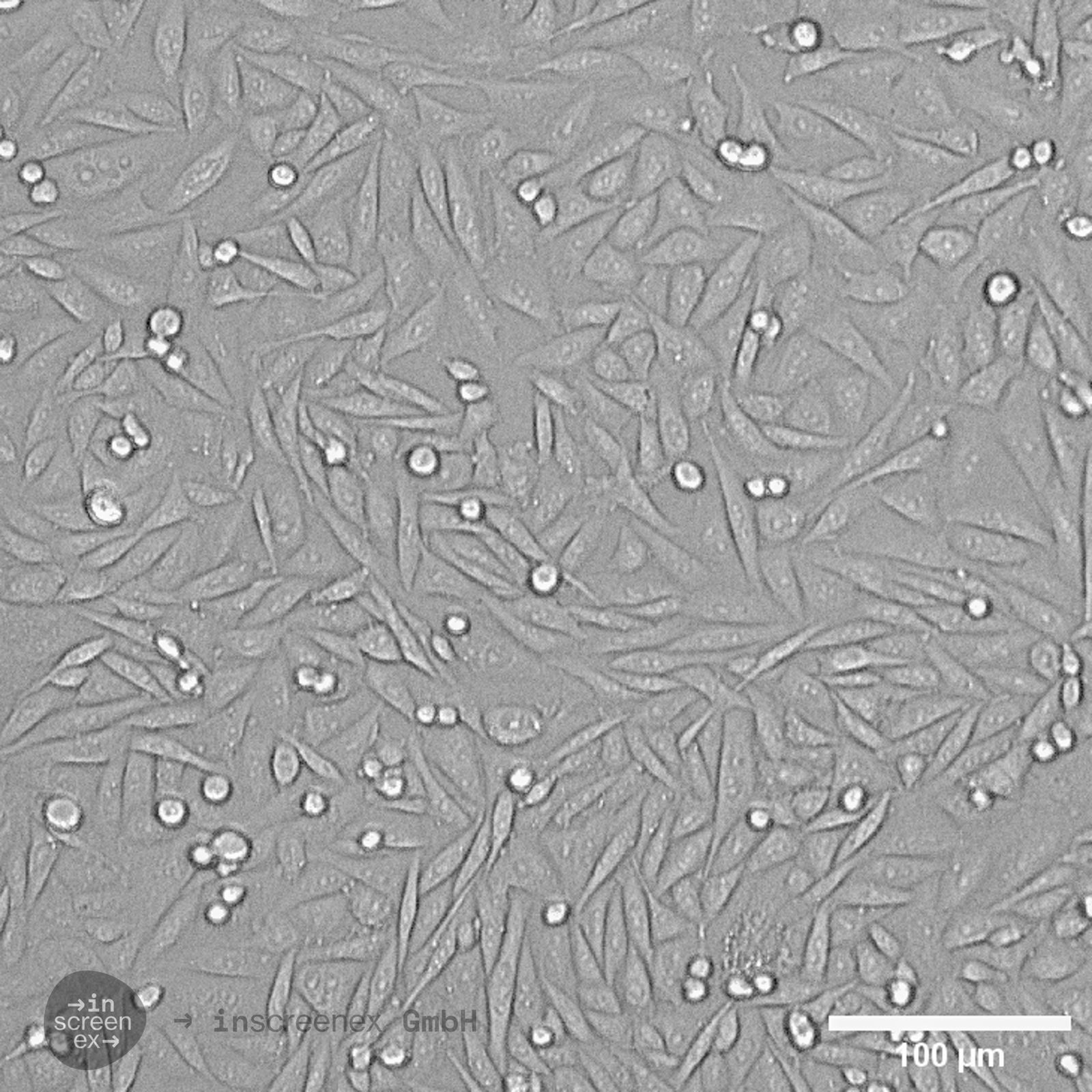
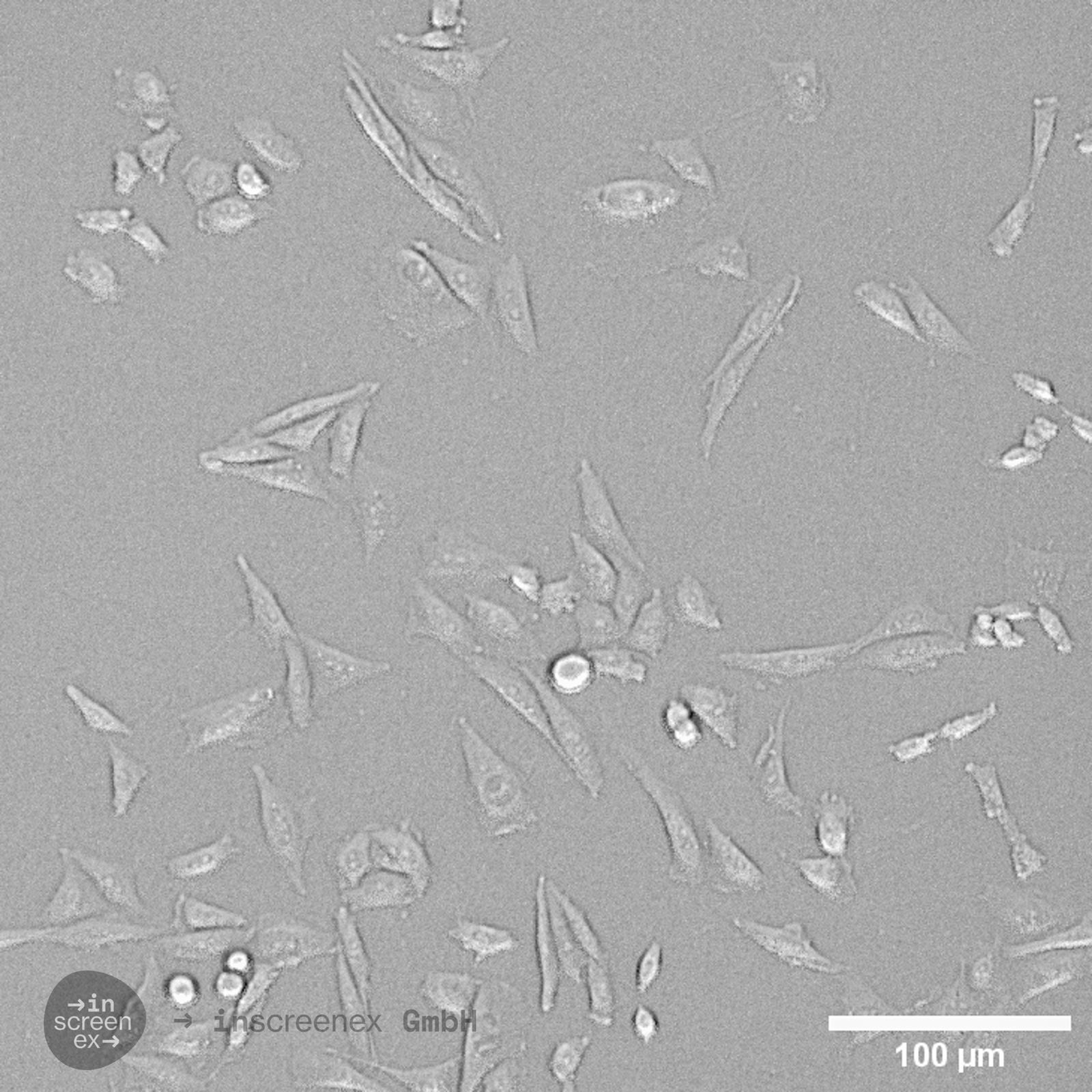
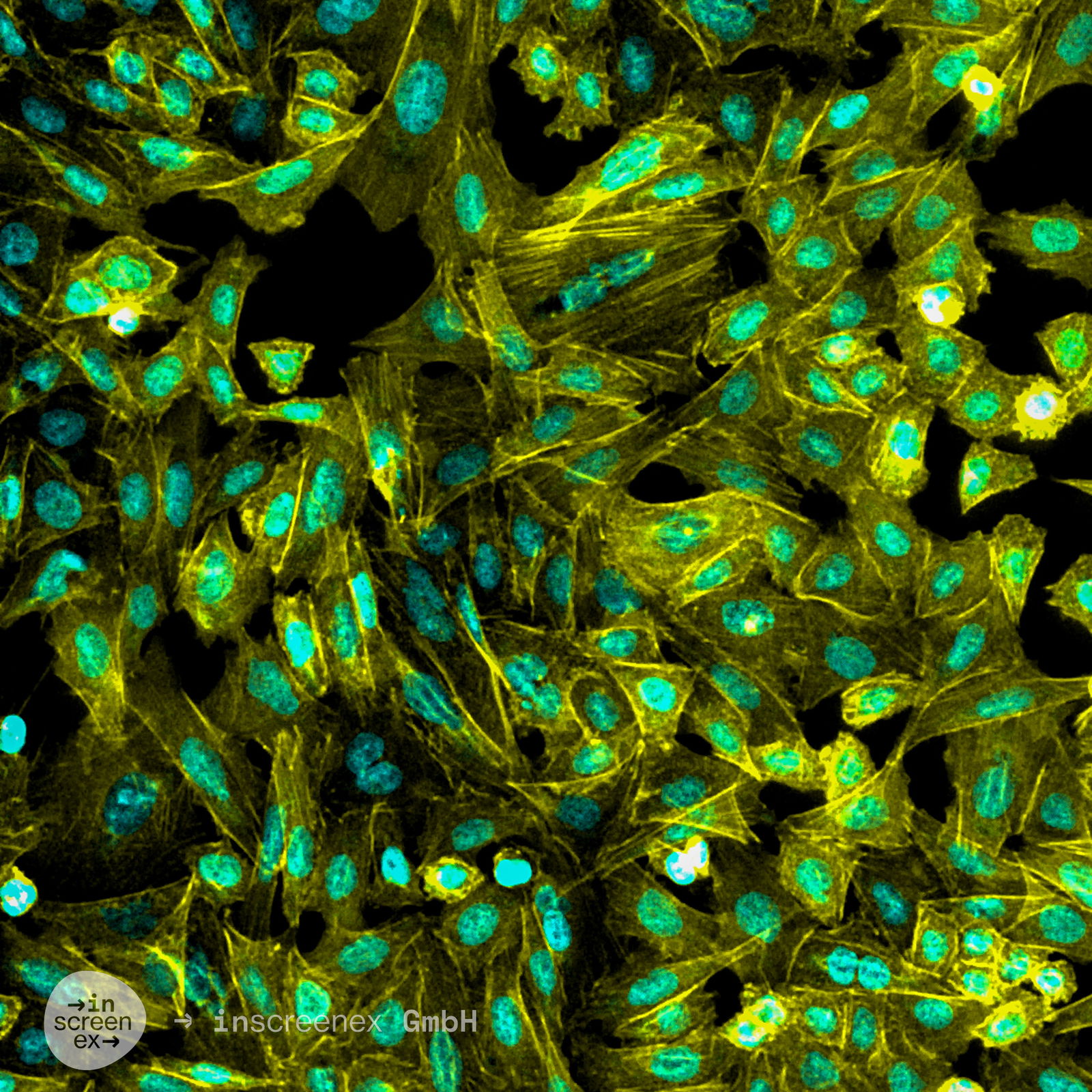
CHO-CCR8-Zellen









1.900,00 €*
Die Produkte werden tiefgefroren in Trockeneis in Kryoröhrchen versandt. Jedes Kryoröhrchen enthält in der Regel 3 × 10 6 Zellen für adhärente Linien oder 5 × 106 Zellen für Suspensionslinien (Einzelheiten finden Sie im Chargenzertifikat).
Allgemeine Informationen
| Beschreibung | Haftungsausschluss: Die für Zelllinien angegebenen Preise gelten ausschließlich für akademische/gemeinnützige Kunden. Für kommerzielle Einrichtungen beträgt der Preis ca. 6.250 €. Die CHO-CCR8-Zelllinie ist eine stabile rekombinante CHO-Zelllinie (Chinese Hamster Ovary), die so entwickelt wurde, dass sie den CCR8-Rezeptor in mittlerer bis hoher Konzentration exprimiert, etwa 8.000 Moleküle pro Zelle. Diese Zelllinie wurde unter Verwendung fortschrittlicher Landing-Pad-Technologie entwickelt, wodurch eine präzise und reproduzierbare Integration des CCR8-Gens an einem spezifischen, vorab validierten genomischen Locus gewährleistet ist. CCR8, auch bekannt als CHEMR1 oder CDw198, ist ein G-Protein-gekoppelter Rezeptor (GPCR), der auf verschiedenen Immunzellen, insbesondere regulatorischen T-Zellen (Tregs), exprimiert wird. CCR8 spielt eine entscheidende Rolle im Immunsuppressionsprozess innerhalb der Tumormikroumgebung und erleichtert es Tumorzellen, der Erkennung durch das Immunsystem zu entgehen. Daher ist die gezielte Beeinflussung von CCR8 zu einer vielversprechenden Strategie in der Krebsimmuntherapie geworden, um die durch Tregs vermittelte Suppression zu verringern und die Antitumorimmunität zu stärken. Die Expression von CCR8 in dieser Zelllinie wurde mittels Durchflusszytometrie unter Verwendung eines zielspezifischen Antikörpers bestätigt, wodurch eine zuverlässige und konsistente Rezeptordichte über die gesamte Zellpopulation hinweg gewährleistet wurde. |
|---|---|
| Organismus | Chinesischer Hamster |
| Gewebe | Eierstock |
Merkmale
| Alter | Erwachsener |
|---|---|
| Geschlecht | Weiblich |
| Morphologie | Epithelähnlich |
| Wachstumseigenschaften | Adhärent/Suspension |
Regulatorische Daten
| Zitat | CHO-CCR8 (Cytion-Katalognummer 305418) |
|---|---|
| Biosicherheitsstufe | 1 |
| NCBI_TaxID | 10029 |
| GVO-Status | GMO-S1: Diese CHO-Zelllinie enthält ein CCR8-Expressionskonstrukt, das Analysen der GPCR-Signalübertragung unterstützt. Diese Klassifizierung gilt nur innerhalb Deutschlands und kann in anderen Ländern abweichen. |
Biomolekulare Daten
| Exprimierte Rezeptoren | CCR8 (CHEMR1 oder CDw198) |
|---|
Handhabung
| Nährboden | Für adhärente Kulturen: DMEM:Ham's F12 (1:1), w: 3,1 g/L Glucose, w: 2,5 mM L-Glutamin, w: 15 mM HEPES, w: 0,5 mM Natriumpyruvat, w: 1,2 g/L NaHCO3 (Cytion-Artikelnummer 820400a) Für Suspensionskulturen: CHO-Wachstumsmedium A (von InSCREENeX; InSCREENeX-Katalognummer INS-ME-1039) |
|---|---|
| Supplemente | Für adhärente Kulturen: Ergänzen Sie das Medium mit 5% FBS. Geneticin (G418-Sulfat) hinzufügen, um eine Endkonzentration von 0,5 mg/ml zu erreichen. |
| Dissoziationsreagenz | Für adhärente Kulturen: Trypsin-EDTA |
| Subkultivierung | Für die routinemäßige adhärente Zellkultur: Saugen Sie das alte Kulturmedium von den adhärenten Zellen ab und waschen Sie sie mit PBS, um das restliche Medium zu entfernen. Nach dem Absaugen des PBS die entsprechende Menge Trypsin/EDTA-Lösung je nach Größe des Kulturgefäßes zugeben (z. B. 1 ml für einen T25-Kolben, 3 ml für einen T75-Kolben) und bei Raumtemperatur oder 37 °C 5-10 Minuten lang inkubieren, oder bis sich die Zellen ablösen. Überwachen Sie die Ablösung unter dem Mikroskop und klopfen Sie bei Bedarf vorsichtig auf das Gefäß, um die Zellen freizusetzen. Sobald sich die Zellen abgelöst haben, fügen Sie vollständiges Medium hinzu, um das Trypsin/EDTA zu inaktivieren, resuspendieren Sie die Zellen vorsichtig und transferieren Sie einen aliquoten Teil der Zellsuspension in ein neues Kulturgefäß mit frischem Medium. Stellen Sie das Gefäß in einen auf 37°C und 5%CO2 eingestellten Inkubator und wechseln Sie das Medium alle 2-3 Tage. |
| Splitverhältnis | Für den ersten Split nach dem Auftauen wird ein Verhältnis von 1:2 empfohlen. Für die Routinekultur wird ein Verhältnis von 1:5 bis 1:10 empfohlen. |
| Medienwechsel | 2 bis 3 Mal pro Woche |
| Erholung nach dem Tauwetter | Nach dem Auftauen die Zellen im Verhältnis 1:2 bis 1:3 in T25-Kolben aufteilen und die Zellen mindestens 24 Stunden lang vom Gefrierprozess erholen und anhaften lassen (bei adhärenten Kulturen). |
| Einfriermedium | Als Kryokonservierungsmedium verwenden wir komplettes Wachstumsmedium (einschließlich FBS) + 10 % DMSO für eine angemessene Lebensfähigkeit nach dem Auftauen oder CM-1 (Cytion Katalognummer 800100), das optimierte Osmoprotektoren und Stoffwechselstabilisatoren enthält, um die Erholung zu verbessern und kryoinduzierten Stress zu reduzieren. |
| Auftauen und Kultivierung von Zellen |
|
| Inkubationsatmosphäre | 37°C, 5%CO2, befeuchtete Atmosphäre. |
| Kolbenbeschichtung | Keine |
| Verfahren zum Einfrieren | Kryokonservierte Zelllinien werden auf Trockeneis in einer validierten, isolierten Verpackung mit ausreichend Kühlmittel versandt, um während des gesamten Transports eine Temperatur von etwa -78 °C aufrechtzuerhalten. Prüfen Sie den Behälter bei Erhalt sofort und bringen Sie die Fläschchen unverzüglich in ein geeignetes Lager. |
| Versandbedingungen | Kryokonservierte Zelllinien werden auf Trockeneis in einer validierten, isolierten Verpackung mit ausreichend Kühlmittel versandt, um während des gesamten Transports eine Temperatur von etwa -78 °C aufrechtzuerhalten. Prüfen Sie den Behälter bei Erhalt sofort und bringen Sie die Fläschchen unverzüglich in ein geeignetes Lager. |
| Lagerungsbedingungen | Zur Langzeitkonservierung werden die Fläschchen in flüssigem Stickstoff bei etwa -150 bis -196 °C gelagert. Eine Lagerung bei -80 °C ist nur als kurzer Zwischenschritt vor der Überführung in flüssigen Stickstoff akzeptabel. |
Qualitätskontrolle / Genetisches Profil / HLA
| Sterilität | Eine Kontamination mit Mykoplasmen wird sowohl durch PCR-basierte Assays als auch durch lumineszenzbasierte Mykoplasmen-Nachweisverfahren ausgeschlossen. Um sicherzustellen, dass keine Kontamination mit Bakterien, Pilzen oder Hefen vorliegt, werden die Zellkulturen täglich visuell überprüft. |
|---|

Abkommen mit Dritten
Bitte beachten Sie, dass diese Zelllinie nicht unter einem Standard-MTA von Cytion erhältlich ist, da sie eine Vereinbarung mit einem Dritten erfordert und/oder mit dem ursprünglichen Lizenzgeber verhandelt werden muss.-
Erforderliche Produkte
Erforderliche Produkte
Gefriermedium CM-1 - 50 mlVarianten von Kryokonservierungsmedien: 50 mlDas Gefriermedium CM-1 von Cytion ist ein hochmodernes Kryokonservierungsmedium, das ein Höchstmaß an Lebensfähigkeit und Funktionalität der Zellen nach dem Auftauen gewährleistet. Dieses vielseitige Medium eignet sich für ein breites Spektrum von Zelltypen, einschließlich menschlicher und tierischer Zellen, was es zu einem unverzichtbaren Werkzeug für verschiedene Forschungsanwendungen macht. Freeze Medium CM-1 enthält eine sorgfältig ausgewogene Kombination von Kryoprotektoren und essentiellen Nährstoffen und minimiert die Bildung von Eiskristallen und den zellulären Stress während des Einfriervorgangs, so dass die zelluläre Integrität erhalten bleibt.
Zu den wichtigsten Eigenschaften von Freeze Medium CM-1 gehören:
Breite Kompatibilität: Wirksam für eine breite Palette von Zelltypen, einschließlich Primärzellen, Stammzellen und etablierte Zelllinien.
Hohe Lebensfähigkeit: Optimiert, um die Wiederherstellung und Lebensfähigkeit von Zellen nach dem Auftauen zu maximieren und zuverlässige Versuchsergebnisse zu gewährleisten.
Fertig zum Gebrauch: Praktisch vorbereitet und sterilisiert für die sofortige Anwendung, wodurch die Vorbereitungszeit und das Kontaminationsrisiko reduziert werden.
Erhöhte Stabilität: Bewahrt eine gleichbleibende Leistung unter Standard-Kryokonservierungsbedingungen und gewährleistet reproduzierbare Ergebnisse.
Lange Haltbarkeitsdauer: CM-1 ist ein serumhaltiges, gebrauchsfertiges Kryokonservierungsmedium, das bis zu einem Jahr im Kühlschrank aufbewahrt werden kann.
Verwendung von CM-1 zum Einfrieren von Zellen
Gehen Sie wie folgt vor, um CM-1 für das Einfrieren von adhärenten und Suspensionszellen zu verwenden
Bei adhärenten Zellen waschen Sie diese und lösen sie vom Kultursubstrat. Bei Suspensionszellen fahren Sie direkt mit dem nächsten Schritt fort.
Zählen Sie die Zellen, um sicherzustellen, dass sie die richtige Konzentration haben.
Zentrifugieren Sie die Zellen, um sie zu pelletieren, und resuspendieren Sie sie dann in CM-1-Gefriermedium.
Überführen Sie die resuspendierten Zellen in Kryogefäße.
Verwenden Sie eine langsame Gefriermethode, bevor Sie die Zellen in die Langzeitlagerung überführen
Methode
Beschreibung
Schritte
❄️
Manuelles Einfrieren
Eine schrittweise Methode, bei der die Temperatur schrittweise gesenkt wird, um die Lebensfähigkeit der Zellen zu gewährleisten
1️⃣ Zellen in Gefriermedium für 40 Minuten in einen 4°C Gefrierschrank legen.
2️⃣ Für 24 Stunden in einen Gefrierschrank mit -80°C transferieren.
3️⃣ Lagern Sie die Zellen zur langfristigen Konservierung in flüssigem Stickstoff
❄️
Verwendung von Mr. Frosty
Ein praktisches Gerät, das kontrollierte Einfrierraten ohne elektrische Energie ermöglicht
1️⃣ Zellen in Kryo-Gefäßen mit Gefriermedium vorbereiten.
2️⃣ Kryovials in den Mr. Frosty-Behälter stellen.
3️⃣ Lagern Sie die Zellen bei -80°C für 24 Stunden, bevor Sie sie in flüssigen Stickstoff umfüllen
❄️
Controlled-Rate Freezer
Ein hochpräziser Gefrierschrank von Thermo Fisher oder anderen Herstellern, der für eine kontrollierte Temperaturabsenkung ausgelegt ist
1️⃣ Programmieren Sie das Gerät so, dass die Temperatur schrittweise gesenkt wird.
2️⃣ Legen Sie die vorbereiteten Zellen in den Gefrierschrank.
3️⃣ Überführen Sie die Zellen nach dem Gefrierzyklus in flüssigen Stickstoff
Lagern Sie die Kryoflaschen bei Temperaturen unter -130°C oder in flüssigem Stickstoff zur langfristigen Aufbewahrung.
Inhaltsstoffe
Enthält FBS, DMSO, Glucose, Salze
Pufferkapazität: pH = 7,2 bis 7,6
Cytion's Freeze Medium CM-1 bietet eine zuverlässige Lösung für die Kryokonservierung, die eine hohe Lebensfähigkeit und Funktionalität der Zellen nach dem Auftauen für eine Vielzahl von Forschungsanwendungen gewährleistet.59,00 €*DMEM:Ham's F12 (1:1), w: 3,1 g/L Glucose, w: 2,5 mM L-Glutamin, w: 15 mM HEPES, w: 0,5 mM Natriumpyruvat, w: 1,2 g/L NaHCO3DMEM:Ham’s F12 ist ein weithin anerkanntes und in der Zellkultur für die biologische Forschung weit verbreitetes Basalmedium. Es dient als grundlegende Nährstoffquelle für das Wachstum verschiedener Säugetierzelllinien, insbesondere wenn es mit fötalem Rinderserum (FBS) ergänzt wird.
Diese einzigartige Formulierung kombiniert Dulbecco's Modified Eagle Medium (DMEM) und Ham's F-12 (Ham's Nutrient Mixture F-12) im exakten Verhältnis 1:1. Die Zugabe von L-Glutamin verbessert die Zusammensetzung zusätzlich.
DMEM, abgeleitet von Eagles Minimal Essential Medium (EMEM), bietet im Vergleich zu seinem Vorgänger eine erhöhte Konzentration an Aminosäuren und Vitaminen. Im Gegensatz dazu basiert Hams F-12 auf dem Ham's F-10-Medium und liefert eine ergänzende Reihe essenzieller Komponenten.
Um ein optimales Zellwachstum zu unterstützen, ist es gängige Praxis, DMEM:Ham's F12 mit FBS in einer typischen Konzentration von 5–10 % zu ergänzen. Diese Zugabe ist notwendig, da dem Medium Wachstumshormone, Lipide und Proteine fehlen, die für die Zellentwicklung entscheidend sind.
DMEM:Ham's F12 enthält ein pH-Puffersystem und wird häufig mit Phenolrot, einem pH-Indikator, ergänzt. Zellkulturen in DMEM:Ham's F12 oder jedem anderen Medium, das das Bicarbonat-Puffersystem nutzt, erfordern eine kontrollierte CO₂-Umgebung von 5–10 %, um angemessene pH-Werte aufrechtzuerhalten.
Qualitätskontrolle
Steril gefiltert
Lagerung und Haltbarkeit
Bei +2 °C bis +8 °C lichtgeschützt lagern.
Nach dem Öffnen bei 4 °C lagern und innerhalb von 6–8 Wochen verbrauchen.
Versandbedingungen
Raumtemperatur
Lagerung
Im Dunkeln bei +2 °C bis +8 °C gekühlt lagern. Einfrieren und häufiges Erwärmen auf +37 °C vermeiden, da dies die Produktqualität beeinträchtigt.
Erhitzen Sie das Medium nicht über 37 °C und verwenden Sie keine unkontrollierten Wärmequellen wie Mikrowellen.
Soll nur ein Teil des Mediums verwendet werden, entnehmen Sie die benötigte Menge und erwärmen Sie diese vor Gebrauch auf Raumtemperatur.
Zusammensetzung
Kategorie
Bestandteile
Konzentration (mg/L)
Aminosäuren
Glycin
18,75
L-Alanin
4,45
L-Arginin-HCl
147,50
L-Asparagin H₂O
7,50
L-Asparaginsäure
6,65
L-Cystein-HCl-H₂O
17,56
L-Cystin-2-HCl
31,29
L-Glutaminsäure
7,35
L-Glutamin
365,00
L-Histidin-HCl-H₂O
31,48
L-Isoleucin
54,47
L-Leucin
59,05
L-Lysin-HCl
91,25
L-Methionin
17,24
L-Phenylalanin
35,48
L-Prolin
17,25
L-Serin
26,25
L-Threonin
53,45
L-Tryptophan
9,02
L-Tyrosin-2-Na-2-H₂O
55,79
L-Valin
52,85
Vitamine
D-Biotin
0,0035
Cholinchlorid
8,98
D-Calciumpantothenat
2,24
Folsäure
2,66
Myo-Inositol
12,60
Nicotinamid
2,02
Pyridoxin-HCl
0,031
Pyridoxal-HCl
2,00
Riboflavin
0,219
Thiamin-HCl
2,17
Vitamin B12
0,68
Anorganische Salze
CaCl₂·2H₂O
154,50
CuSO₄·5H₂O
0,0013
Fe(NO₃)₃·9H₂O
0,05
FeSO₄·7H₂O
0,417
KCl
311,80
MgCl₂·6 H₂O
61,20
MgSO₄·7H₂O
100,00
NaCl
6996,00
NaHCO₃
1200,00
Na₂HPO₄
71,02
NaH₂PO₄·2H₂O
70,87
ZnSO₄ 7 H₂O
0,432
Sonstige Bestandteile
D-Glucose
3151,00
Hypoxanthin
2,40
HEPES
3574,50
Linolsäure
0,042
Liponsäure
0,105
Phenolrot-Natriumsalz
8,63
Putrescin-2-HCl
0,081
Natrium-Pyruvat
55,00
Thymidin
0,36525,00 €*Accutase-Lösung zur Zellablösung – 100 mlVarianten: 100 mlAccutase-Zellablösungslösung mit EDTA und Phenolrot – 100 ml
Accutase ist eine gebrauchsfertige, steril gefilterte Zellablösungslösung, die als schonende Alternative zu Trypsin/EDTA entwickelt wurde, um adhärente Säugetierzellen von Standard-Gewebekultur-Kunststoffgefäßen und adhäsionsbeschichteten Oberflächen zu lösen. Sie kombiniert proteolytische und kollagenolytische Enzymaktivität in einer ausgewogenen Salzlösung, um eine effektive und dennoch kontrollierte Dissoziation zu ermöglichen, wobei die Zelloberflächenproteine erhalten bleiben und eine hohe Lebensfähigkeit nach der Passagierung sowie eine schnelle Wiederanhaftung unterstützt werden.
Die Accutase-Formulierung basiert auf Dulbecco’s phosphatgepufferter Kochsalzlösung (DPBS) mit EDTA und Phenolrot als visuellem pH-Indikator. Die Enzyme sind nicht-säugetierischen und nicht-bakteriellen Ursprungs, wodurch sich Accutase besonders gut für die Stammzellenforschung, Impfstoff-Workflows und alle Anwendungen eignet, bei denen Kontaminationen tierischen oder mikrobiellen Ursprungs minimiert werden müssen. Die Lösung hemmt sich bei 37 °C selbst, sodass nach der Ablösung kein Neutralisationsreagenz oder serumhaltiges Medium erforderlich ist – die Zellen können direkt in frisches Medium überführt werden.
Hauptmerkmale
Gebrauchsfertige 1x steril gefilterte Flüssigkeit – keine Verdünnung oder Rekonstitution erforderlich
Kombinierte proteolytische und kollagenolytische Enzymaktivität für eine schonende Dissoziation
Jede Charge ist auf eine definierte Dissoziationsaktivität standardisiert, um eine Chargenkonsistenz zu gewährleisten
Enzyme nicht-mammalierischer und nicht-bakterieller Herkunft
Autoinhibiert bei 37 °C – keine Neutralisationslösung erforderlich
Formuliert in Dulbecco’s PBS mit EDTA
Phenolrot als visueller pH-Indikator enthalten
pH 6,8 – 7,8
Typische Anwendungen
Accutase löst eine Vielzahl von adhärenten und empfindlichen Zelltypen schonend auf, darunter humane embryonale Stammzellen (hESCs), humane induzierte pluripotente Stammzellen (iPSCs), neurale Stammzellen, primäre Neuronen sowie routinemäßig kultivierte adhärente Zelllinien wie HeLa, HEK 293, CHO, MDCK, Vero, NIH/3T3, BHK-21 und A549. Typische Anwendungsfälle sind:
Routinemäßige Subkultur und Passagierung von adhärenten Säugetierzellen
Schonende Einzelzell-Dissoziation von hESCs, iPSCs und anderen empfindlichen Zelllinien
Probenvorbereitung für Durchflusszytometrie und FACS-Analyse
Analyse von Zelloberflächenmarkern, bei denen die Epitopintegrität entscheidend ist
Assays zur Zellmigration, Proliferation und Apoptose
Quieszenztests durch Serumentzug und Onkogen-Transfektionsstudien
Migrationsassays für Tumorzellen und Neuralleistenzellen
Produktionsskalierung in Bioreaktor-Workflows
Für Routinearbeiten etwa 10 ml Accutase pro 75 cm² Kulturfläche auftragen und 5–10 Minuten bei Raumtemperatur inkubieren. Die optimale Inkubationszeit sollte für jede Zelllinie bestimmt werden und eine Stunde nicht überschreiten. Vor der Zugabe die Zellschicht mit einer Ca²⁺/Mg²⁺-freien Salzlösung wie DPBS ohne Calcium und Magnesium spülen, um Serumrückstände und zweiwertige Kationen zu entfernen.
Handhabung und Lagerung
Lagern Sie die ungeöffnete Flasche tiefgefroren bei -15 °C oder darunter. Tauen Sie das Produkt entweder bei Raumtemperatur oder über Nacht bei +2 °C bis +8 °C auf. Tauen Sie Accutase nicht in einem 37 °C warmen Wasserbad auf, da erhöhte Temperaturen die Enzymaktivität verringern. Nach dem Auftauen kann die Lösung bis zu 2 Monate bei +2 °C bis +8 °C gelagert werden; lagern Sie sie nicht bei Raumtemperatur. Das Reagenz vor der Anwendung nicht auf 37 °C vorwärmen – es direkt bei Raumtemperatur zu den gewaschenen Zellen geben. Für eine lange Haltbarkeit wird die Aufteilung in Einmalaliquots empfohlen, um wiederholte Auftauzyklen zu vermeiden. Arbeiten Sie stets unter aseptischen Bedingungen.
Qualität
Hergestellt unter strengen Qualitätsstandards. Jede Charge von Accutase wird steril gefiltert und auf Sterilität, pH-Wert, Aussehen und Dissoziationsaktivität geprüft, um eine konsistente, reproduzierbare Leistung von Charge zu Charge zu gewährleisten.
Produktspezifikationen
Spezifikation
Detail
ProdukttypReagenz zur Zellablösung/Dissoziation
FormatSteril gefilterte Flüssigkeit, gebrauchsfertig
Volumen100 ml
Arbeitskonzentration1x (gebrauchsfertig)
EnzymaktivitätKombiniert proteolytisch und kollagenolytisch
EnzymherkunftNicht-säugetierisch und nicht-bakteriell
PuffersystemDulbecco’s PBS mit EDTA
pH-IndikatorPhenolrot
pH-Bereich6,8 – 7,8
AussehenKlare, hellrote bis orangefarbene Lösung
Lagertemperatur-15 °C oder darunter
Haltbarkeit nach dem AuftauenBis zu 2 Monate bei +2 °C bis +8 °C
Empfohlenes Verwendungsvolumen~10 ml pro 75 cm² Kulturfläche
Typische Inkubationszeit5 – 10 Minuten bei Raumtemperatur
VersandbedingungenGefroren auf Trockeneis
VerwendungszweckNur für Forschungszwecke und zur Weiterverarbeitung
Formulierung (Zusammensetzung pro Liter)
Komponente
Konzentration (mg/l)
Anorganische Salze
Natriumchlorid (NaCl)8000,00
Dinatriumhydrogenphosphat (Na₂HPO₄)1150,00
Kaliumchlorid (KCl)200,00
Kaliumdihydrogenphosphat (KH₂PO₄)200,00
Sonstige Bestandteile
EDTA · 4Na (Tetranatrium-EDTA)220,00
Phenolrot3,00
Proprietäre Enzymmischung (proteolytische und kollagenolytische Aktivität)1x
Accutase ist eine eingetragene Marke von Innovative Cell Technologies, Inc.75,00 €*Antibiotika/Antimykotika-Lösung (100x)Produktübersicht
Volumen: 100 ml Lagerung: ≤-15°C Sterilität: Steril-gefiltert
Antibiotika-/Antimykotika-Lösung (100x) ist ein steriles, gebrauchsfertiges Konzentrat zur Verringerung des Risikos einer mikrobiellen Kontamination in Zellkulturen und ähnlichen Laboranwendungen. Diese 100-fache Lösung enthält eine bewährte Kombination aus Penicillin, Streptomycin und Amphotericin B, die ein breites antimikrobielles Wirkungsspektrum gegen grampositive und gramnegative Bakterien, Hefen und filamentöse Pilze bietet. Die Formulierung eignet sich für den Einsatz in eukaryotischen Zellkulturen, bakteriellen Medien und anderen kontaminationsanfälligen Systemen und unterstützt saubere und konsistente Laborabläufe.
Anwendung und Vorteile Diese Lösung wurde für routinemäßige Forschungsprotokolle optimiert und wird häufig zur Aufrechterhaltung aseptischer Bedingungen in Zellkultur-Workflows verwendet. Sie bietet zuverlässige Leistung in kontaminationsanfälligen Umgebungen und hilft Forschern, das Risiko einer mikrobiellen Überwucherung zu reduzieren, ohne die Gesundheit der Zellen oder die Reproduzierbarkeit der Experimente zu beeinträchtigen. Die steril gefilterte Formulierung macht zusätzliche Solubilisierungsschritte überflüssig, unterstützt eine rationalisierte Medienvorbereitung und reduziert die Variabilität in den täglichen Laborabläufen.
Verwendung und Kompatibilität Um Standard-Arbeitskonzentrationen zu erreichen, verdünnen Sie die Lösung 1:100 in Ihr komplettes Kulturmedium. Das Produkt ist mit einer breiten Palette von Säugetierzelllinien und Basalmedien kompatibel. Dank der konstanten Verfügbarkeit der Vorräte profitieren Forscher von einer zuverlässigen Lieferkontinuität und einer vereinfachten Logistikplanung. Die Lösung sollte bei ≤ -15 °C gelagert und vor wiederholten Gefrier-Auftau-Zyklen geschützt werden, um die Stabilität zu erhalten. Nur für den Forschungsgebrauch. Nicht zur Verwendung in diagnostischen oder therapeutischen Verfahren. Nicht zur Anwendung bei Menschen oder Tieren.45,00 €*PBSPhosphatgepufferte Kochsalzlösung (PBS)
Phosphatgepufferte Kochsalzlösung (PBS) ist eine weit verbreitete Pufferlösung in der biologischen und chemischen Forschung. Sie spielt eine entscheidende Rolle bei der Aufrechterhaltung des pH-Gleichgewichts und der Osmolarität während verschiedener experimenteller Verfahren, einschließlich Gewebeverarbeitung und Zellkultur. Unsere PBS-Lösung wird sorgfältig mit hochreinen Inhaltsstoffen formuliert, um Stabilität und Zuverlässigkeit bei jedem Experiment zu gewährleisten. Die Osmolarität und die Ionenkonzentration unserer PBS-Lösung sind denen des menschlichen Körpers sehr ähnlich, so dass sie isotonisch und für die meisten Zellen ungiftig ist.
Zusammensetzung unserer PBS-Lösung
Unsere PBS-Lösung ist eine pH-angepasste Mischung aus hochreinen Phosphatpuffern und Kochsalzlösungen. Bei einer 1fachen Arbeitskonzentration enthält sie:
8000 mg/L Natriumchlorid (NaCl)
200 mg/L Kaliumchlorid (KCl)
1150 mg/L Natriumphosphat dibasisch wasserfrei (Na2HPO4)
200 mg/L Kaliumphosphat einbasig wasserfrei (KH2PO4)
Diese Zusammensetzung gewährleistet ein optimales pH
- und Ionengleichgewicht und eignet sich für eine breite Palette biologischer Anwendungen.
Anwendungen unserer PBS-Lösung
Unsere PBS-Lösung ist ideal für verschiedene Anwendungen in der biologischen Forschung. Aufgrund ihrer isotonischen und ungiftigen Eigenschaften eignet sie sich für die Verdünnung von Substanzen und die Spülung von Zellbehältern. PBS-Lösungen, die EDTA enthalten, sind wirksam, um anhaftende und verklumpte Zellen abzulösen. Zweiwertige Metalle wie Zink sollten jedoch nicht zu PBS hinzugefügt werden, da dies zu Ausfällungen führen kann. In solchen Fällen werden Good's Puffer empfohlen. Außerdem ist unsere PBS-Lösung eine akzeptable Alternative zu viralen Transportmedien für den Transport und die Lagerung von RNA-Viren, einschließlich SARS-CoV-2.
Qualitätskontrolle
Steril gefiltert
Lagerung und Haltbarkeit
Vor Licht geschützt bei +2°C bis +25°C lagern.
Nach dem Öffnen bei 2°C bis 25°C lagern und innerhalb von 24 Monaten verbrauchen.
Versandbedingungen
Umgebungstemperatur
Pflege
Gekühlt bei +2°C bis +8°C im Dunkeln aufbewahren. Vermeiden Sie Einfrieren und häufiges Erwärmen auf +37°C, da dies die Produktqualität beeinträchtigt.
Erwärmen Sie das Medium nicht über 37°C und verwenden Sie keine unkontrollierten Wärmequellen wie Mikrowellengeräte.
Wenn nur ein Teil des Mediums verwendet werden soll, entnehmen Sie die erforderliche Menge und erwärmen Sie sie vor der Verwendung auf Raumtemperatur.
Zusammensetzung
Kategorie
Bestandteile
Konzentration (mg/L)
Salze
Kaliumchlorid
200
Kaliumphosphat monobasisch wasserfrei
200
Natriumchlorid
8000
Natriumphosphat zweibasisch wasserfrei
115020,00 €* -
Ähnliche Produkte
Ähnliche Produkte