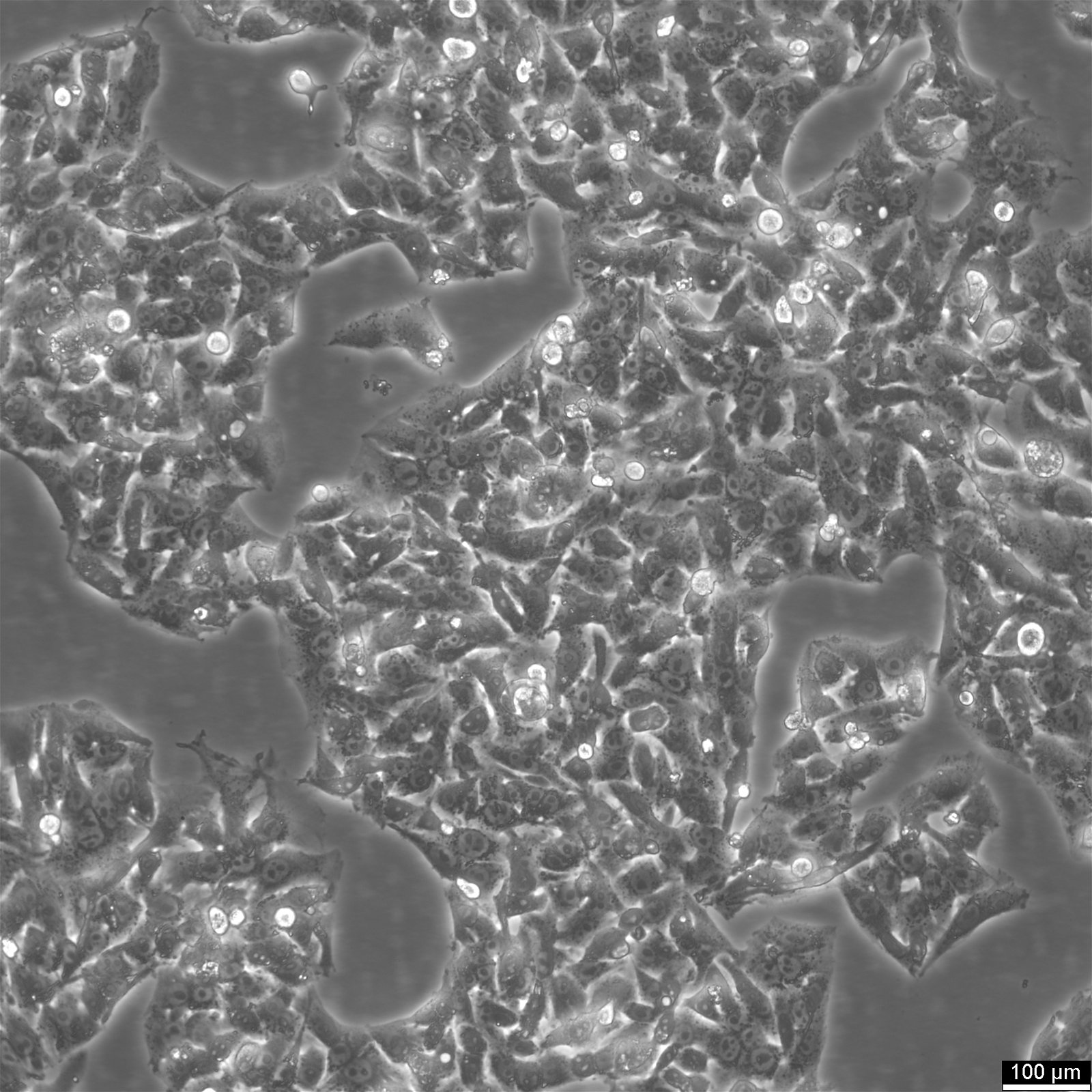
HepG2-celler - en ressource til forskning i leverkræft
Hep-G2 er en human leverkræftcellelinje, der stammer fra levervæv fra en 15-årig kaukasisk mand med hepatocellulært karcinom. Disse celler bruges ofte i undersøgelser af lægemiddelmetabolisme og hepatotoksicitet. Selv om HepG2-celler har en høj proliferationsrate og et epitellignende udseende, er de ikke-tumorogene og udfører forskellige differentierede leverfunktioner. I 1975 udledte forskere HepG2-celler fra hepatocellulært karcinom, hvilket gjorde den til den første levercellelinje, der udviste hepatocytternes kritiske egenskaber. I modsætning til den tidligere etablerede SK-Hep1-cellelinje, som mangler vigtige levercellemarkører, kan HepG2-celler udskille forskellige plasmaproteiner og er en værdifuld model til at studere den intracellulære dynamik af celleoverfladedomæner i humane hepatocytter. Disse celler udviser en epitel-lignende morfologi, har et modalt kromosomtal på 55 og kan stimuleres med humant væksthormon
HepG2-karakteristika
Primære hepatocytters typiske form er kubisk og indeholder normalt to kerner. I modsætning hertil har HepG2-celler en epitellignende morfologi med en enkelt kerne og et kromosomtal på mellem 48 og 54 pr. celle. Selvom HepG2-celler kan udgøre op til 25 % af det samlede cellulære protein, er de større end normale hepatocytter og udgør ca. 10 % af det samlede protein i cellen. Celleproteiner er kritiske aktører i cellen, som udfører de funktioner, der er specificeret af generne.
Tumorceller, herunder dem med et unormalt antal kromosomer, udviser ofte en stigning i antallet af kerner, op til syv pr. celle. På grund af deres høje grad af differentiering in vitro er HepG2-celler en ideel model til at studere den intracellulære transport og dynamikken i galdekanalsystemet, sinusformede membranproteiner og lipider i humane hepatocytter.
Den gennemsnitlige diameter på en HepG2-celle er omkring 10-20 µm, hvilket er mindre end en hepatocyt med en diameter på 15 µm, men svarer til tumorceller med Hepatoblastoma (HB), som varierer fra 10-20 µm.
HepG2's genetik
Hep-G2-cellelinjen udviser flere translokationer, herunder dem mellem de korte arme af kromosom 1 og 21, trisomier af kromosom 2, 16 og 17 og tetrasomi af kromosom 20. Tabet af kromosom 4q3-regionen ses også i forbindelse med translokationen t(1;4), der ofte ses ved hepatoblastom (HB), og andre kromosomale abnormiteter, såsom trisomier 2 og 20. Antallet af kromosomer i HepG2-celler varierer fra 50 til 60, hvilket indikerer en hyperdiploid karyotype, mens nogle tilfælde udviser mere end 100 kromosomer og er karakteriseret ved tetraploid forstørrelse. HepG2-celler indeholder ca. 7,5 pg DNA, hvilket er 15 % mere end en gennemsnitlig somatisk celle. Til sammenligning har primære hepatocytter en kubisk celleform og indeholder typisk to kerner [1].
Mutationsprofil af HepG2-celler
HepG2-cellelinjen bærer mutationen C228T i TERT-promoterregionen, som også findes i hepatocellulært karcinom (HCC) og hepatoblastom (HB). Denne mutation bidrager til udødelighed ved at beskytte telomerer i kræftceller. Derudover udviser HepG2-celler wild-type TP53, et kritisk gen til at undertrykke menneskelig kræft, da det spiller en rolle i cellecyklusstop, apoptose og aldring. Mutationer i dette gen kan fremme celleproliferation.
HepG2-celler deltager i flere veje, herunder dysregulering af cellevækst, overlevelsesveje som føtal og embryonal HB og Wnt/β-catenin-vejen. Desuden har cellelinjen en karakteristisk deletion af den tredje exon i CTNNB1-genet, som er identisk med den, der ses i epitelial type HB [2,3].
Oversigt over HepG2 hepatocellulære karcinomceller i leverforskning
HepG2-celler, der stammer fra humant hepatom, er blevet et uvurderligt værktøj til forskning i leverfunktioner og sygdomme, herunder hepatocellulært karcinom. Disse levercellelinjer giver indsigt i de humane hepatocytters cellulære reaktioner under forskellige eksperimentelle forhold. Brugen af luciferase-reporterplasmider i HepG2-celler har været særlig effektiv til at spore genekspression og cellulære transfektioner, som er grundlæggende i metabolisk forskning, som f.eks. undersøgelsen af ethanols virkninger på leverceller
Undersøgelser af virusinfektioner og leversygdomme ved hjælp af HepG2-celler
Immortaliserede tumorcellelinjer i leveren som HepG2 og Huh7 er vigtige i studiet af virusinfektioner, idet de viser en fuldstændig cellecyklusreplikation af hepatitis D (HDV) og ekspression af hepatitis B (HBV) [5,6]. Samtidig spiller HepaRG-cellelinjer en afgørende rolle i belysningen af HBV's indtrængningsmekanismer [7]. HepG2-celler anvendes også til at undersøge en række forskellige leversygdomme hos mennesker, fra genetiske tilstande som progressiv familiær intrahepatisk kolestase (PFIC) og Dubin-Johnsons syndrom til miljø- og kostundersøgelser i forbindelse med cytotoksiske og genotoksiske stoffer samt til forskning i lægemiddelmålretning og hepatocarcinogenese [8,9]. Brugen af dem strækker sig også til forsøg med biokunstige leveranordninger
HepG2-cellers interaktion med biomaterialer i vævsteknik
HepG2-cellers interaktion med forskellige biomaterialer er afgørende for vævsteknologien. Teknikker som den kolloide sondeteknik hjælper med at forstå disse interaktioner ved at måle celleadhæsionsegenskaber, som er afgørende for at bestemme cellelevedygtighed til udvikling af stilladser og nøjagtige levervævsmodeller
Celleadfærd og innovationer i HepG2-baserede modeller
Undersøgelse af celleadfærd i HepG2-baserede modeller er afgørende for forskning i leversygdomme. Fremskridt inden for tredimensionelle sfæroidcellekulturer har ført til skabelsen af HepG2-cellesfæroider, som tilbyder en mere fysiologisk relevant model, der nøje afspejler normale hepatocytter. Disse 3D-modeller med øget metabolisk aktivitet viser, at HepG2-celler har potentiale til at fungere som model for hepatoblastom og er vigtige i forskning i kræftbehandling, især til at simulere levertumorer og teste nye terapeutiske tilgange [10-12]
Sammenligning og karakteristik af HepG2 blandt andre tumorcellelinjer
HepG2 er en af de mest anvendte levertumorcellelinjer, der er udvalgt på grund af sin brede anvendelse i videnskabelig forskning blandt ca. 40 tilgængelige levertumorcellelinjer [13]. På trods af det svage eller fraværende udtryk for visse cytokrom P450-enzymer sammenlignet med normale hepatocytter har HepG2's metaboliske profil drevet indsatsen for at modificere cellelinjen til bedre undersøgelser af lægemiddelmetabolisme [13]. Sammenlignet med tumorcellelinjer som MCF7, PC3, 143B og HEK293 udviser HepG2-celler unikke aminosyreindholdsprofiler, der har betydelig indflydelse på proteinsyntese og sekretion, hvilket fremhæver deres unikke metaboliske veje [14]
Udforskning af leversygdomme med HepG2
Subkulturering af HepG2-celler
Her er fem trin til at fjerne klæbende celler fra celledyrkningskolber ved hjælp af Accutase:
- Fjern mediet fra celledyrkningskolben, og skyl de klæbende celler med PBS uden calcium og magnesium. Brug 3-5 ml PBS til T25-kolber og 5-10 ml til T75-kolber.
- Tilsæt Accutase til celledyrkningskolben, brug 1-2 ml pr. T25-kolbe og 2,5 ml pr. T75-kolbe. Sørg for, at Accutase dækker hele cellepladen.
- Inkuber kolben ved stuetemperatur i 8-10 minutter.
- Resuspender forsigtigt cellerne med medium ved at bruge 10 ml frisk medium.
- Centrifuger de resuspenderede celler i 5 minutter ved 300xg, resuspender dem i frisk medium, og fordel dem i nye kolber, der indeholder frisk medium.
Fremtidsudsigter for HepG2-celler
Jagten på at frigøre HepG2-cellelinjens fulde potentiale fortsætter med banebrydende fremskridt i forhold til at øge udtrykket af cytokromer. Forskerne undersøger også muligheden for tredimensionelle sfæroidcellekulturer, som giver et mere fysiologisk relevant system. Den metaboliske aktivitet, herunder cytokromer, er bemærkelsesværdigt højere i 3D-sfæroidale HepG2-modeller end i 2D-celler, hvilket bringer os tættere på at skabe en model, der afspejler normale hepatocytter. Derudover kan udforskningen af de dynamiske processer, der ligger til grund for den forkerte fordeling af celleoverfladeproteiner, bane vejen for en bedre forståelse af leversygdomme
HepG2-celler: Forståelse af deres rolle og forskelle i biomedicinsk forskning - Ofte stillede spørgsmål
Referencer
- Vyas, R.C., Darroudi, F., Natarajan, A.T. Radiation-induced chromosomal breakage and rejoining in interphase-metaphase chromosomes of human lymphocytes, Mutat Res, 1991; 249(1):29-35.
- Woodfield, S.E., Shi, Y., Patel, R.H., Chen, Z., Shah, A.P., Srivastava, R.K., Whitlock, R.S., Ibarra, A.M., Larson, S.R., Sarabia, S.F., et al. MDM4 Inhibition: En ny terapeutisk strategi til at genaktivere P53 i hepatoblastom. Sci. Rep. 2021, 11, 2967.
- Hussain, S.P., Schwank, J., Staib, F., Wang, X.W., Harris, C.C. TP53 Mutations and hepatocellular Carcinoma: Insights into the Etiology and Pathogenesis of Liver Cancer. Oncogene 2004.
- Schicht, G., Seidemann, L., Haensel, R., Seehofer, D., Damm, G. Kritisk undersøgelse af anvendeligheden af hepatomcellelinjerne HepG2 og Huh7 som modeller for den metaboliske repræsentation af resektabelt hepatocellulært karcinom. Cancers 2022, 14(17), 4227.
- Verrier, E.R., Colpitts, C.C., Schuster, C., Zeisel, M.B., Baumert, T.F. Cell Culture Models for the Investigation of Hepatitis B and D Virus Infection. Viruses 2016, 8, 261.
- Verrier, E.R., Colpitts, C.C., Bach, C., Heydmann, L., Weiss, A., Renaud, M., Durand, S.C., Habersetzer, F., Durantel, D., AbouJaoudé, G., et al. A Targeted Functional RNA Interference screen Uncoverages Glypican 5 as an Entry Factor for Hepatitis B and D Viruses. Hepatology 2016, 63, 35-48.
- Gripon, P., Rumin, S., Urban, S., Le Seyec, J., Glaise, D., Cannie, I., Guyomard, C., Lucas, J., Trepo, C., Guguen-Guillouzo, C. Infection of a Human Hepatoma Cell Line by Hepatitis B Virus. Proc. Natl. Acad. Sci. USA 2002, 99, 15655-15660.
- Mersch-Sundermann, V., Knasmüller, S., Wu, X.J., Darroudi, F., Kassie, F. Brug af en menneskelig levercellelinje til påvisning af cytobeskyttende, antigenotoksiske og kogenotoksiske midler. Toxicology. 2004; 198(1-3): 329-340.
- Fanelli, A. HepG2 (hepatocellulært karcinom i leveren): cellekultur. HepG2. Hentet 3. december 2017.
- Xuan, J., Chen, S., Ning, B., Tolleson, W.H., Guo, L. Development of HepG2-Derived Cells Expressing Cytochrome P450s for Assessing Metabolism-Associated Drug-Induced Liver Toxicity (Udvikling af HepG2-afledte celler, der udtrykker cytokrom P450 til vurdering af stofskifteassocieret lægemiddelinduceret levertoksicitet). Physiol. Behav. 2017, 176, 139-148.
- Ooka, M., Lynch, C., Xia, M. Anvendelse af in vitro-metabolismeaktivering i high-throughput-screening. Int. J. Mol. Sci. 2020, 21, 8182.
- Huang, L., Coughtrie, M.W.H., Hsu, H. Down-Regulation of Dehydroepiandrosterone Sulfotransferase Gene in Human Hepatocellular Carcinoma. Mol. Cell. Endocrinol.
- Zhu, Z., Hao, X., Yan, M., et al. Kræftstamceller/progenitorceller er stærkt beriget i CD133 + CD44 + -populationen i hepatocellulært karcinom. Int J Cancer. 2010; 126:2067-2078.
- Arbus, C., Benyamina, A., Llorca, P.-M., Baylé, F., Bromet, N., Massiere, F., Garay, R.P., Hameg, A. Karakterisering af humane cytokrom P450-enzymer, der er involveret i metabolismen af cyamemazin. Eur J Pharm Sci. 2007 Dec;32(4-5):357-66.