
Indledning
I det store landskab af biomedicinsk forskning har cellelinjer vist sig at være de ubesungne helte, der stille og roligt revolutionerer vores forståelse af menneskers sundhed og sygdom. Disse små, levende laboratorier har åbnet dørene til utallige opdagelser, lige fra at afdække de indviklede cellulære mekanismer til udvikling af livreddende behandlinger. For hvert år, der går, vokser betydningen af cellelinjer i videnskabelig forskning, da de tilbyder et enestående vindue ind i biologiens komplekse verden.
Men blandt de utallige cellelinjer, der er til rådighed, er der nogle få udvalgte, der har fået en fremtrædende plads som den moderne biomedicins arbejdsheste. Disse cellelinjer har gang på gang bevist deres værd og givet forskere de værktøjer, de har brug for til at flytte grænserne for videnskabelig viden. I denne artikel tager vi på en fængslende rejse gennem de 5 bedste cellelinjer, der har sat et uudsletteligt præg på den biomedicinske forskningsverden. Fra HeLa-cellernes ydmyge begyndelse til de banebrydende innovationer, som HEK293-cellerne har muliggjort, vil vi udforske de fascinerende historier bag disse cellulære kraftcentre og den dybe indflydelse, de har haft på vores forståelse af selve livet. Så vær med, når vi dykker ned i hemmelighederne bag disse ekstraordinære cellelinjer og opdager, hvordan de giver næring til morgendagens biomedicinske gennembrud.
Top 5 cellelinjer, der giver brændstof til biomedicinsk forskning
HeLa-celler
Den første udødelige menneskelige cellelinje, etableret i 1951 fra livmoderhalskræftceller fra Henrietta Lacks. HeLa-celler har været medvirkende til adskillige videnskabelige gennembrud, herunder udviklingen af poliovaccinen.
HEK293-celler
Epitelceller fra humane embryonale nyrer, der i vid udstrækning anvendes til forbigående og stabile transformationseksperimenter, proteinekspression og -produktion samt elektrofysiologiske eksperimenter.
MCF-7-celler
En brystkræftcellelinje, der ofte bruges til forskning i hormonel regulering, lægemiddeludvikling og undersøgelse af brystkræftbiologi.
CHO-celler
Ovarieceller fra kinesisk hamster, der i vid udstrækning anvendes i biologisk, medicinsk og farmaceutisk forskning, f.eks. rekombinant proteinproduktion og undersøgelser af den epidermale vækstfaktorreceptor.
PC-12-celler
En cellelinje, der stammer fra binyremarven hos rotter, og som bruges meget i neurovidenskabelig forskning, især i studier af neuronal differentiering, syntese af neurotransmittere og neurotoksicitet.
Nummer 5: Sf9-celler

Sf9-celler, der stammer fra æggestoksvævet hos høstmåleren(Spodoptera frugiperda), er blevet en hjørnesten i studier af insektcellekulturer og proteinekspression. Disse alsidige celler har den unikke evne til at vokse som adhærente eller suspenderede kulturer, hvilket gør dem velegnede til en lang række anvendelser, fra laboratorieforskning i lille skala til industriel produktion i stor skala.
En af de vigtigste fordele ved Sf9-celler er deres kompatibilitet med baculovirus-ekspressionsvektorsystemet (BEVS). Dette kraftfulde værktøj gør det muligt for forskere at indføre fremmede gener i cellerne ved hjælp af manipulerede baculovirus, hvilket resulterer i produktion af store mængder rekombinante proteiner. Sf9/BEVS-kombinationen har vist sig at være særlig effektiv til at udtrykke komplekse pattedyrsproteiner, der kræver posttranslationelle modifikationer, såsom glykosylering og korrekt foldning, som er afgørende for deres biologiske aktivitet.
Sf9-cellernes succes med proteinproduktion har ført til udbredt brug af dem til fremstilling af vacciner, terapeutiske proteiner og diagnostiske reagenser. Et bemærkelsesværdigt eksempel er produktionen af HPV-vaccinen CERVARIX®, som bruger Sf9-celler til at udtrykke vaccinens nøglekomponent, L1-proteinet fra humant papillomavirus. Evnen til at producere dette protein i store mængder og med høj renhed har været afgørende for udviklingen og distributionen af denne livreddende vaccine.
Ud over deres anvendelse inden for bioteknologi har Sf9-celler også vist sig at være uvurderlige inden for grundforskning, især i studiet af insektbiologi og værts-patogen-interaktioner. Da insekter er vigtige vektorer for mange sygdomme hos mennesker og dyr, kan forståelsen af de cellulære og molekylære mekanismer, der ligger til grund for deres biologi, give afgørende indsigt i sygdomsoverførsel og kontrolstrategier.
Sf9-celler har opnået en plads blandt de fem bedste cellelinjer inden for biomedicinsk forskning på grund af deres alsidighed, robusthed og uovertrufne succes med proteinudtryk. Når forskere fortsætter med at flytte grænserne for videnskabelig viden, vil Sf9-celler utvivlsomt forblive et vigtigt værktøj i deres arsenal og skabe gennembrud inden for både grundforskning og anvendt forskning.
Nummer 4: CHO-celler
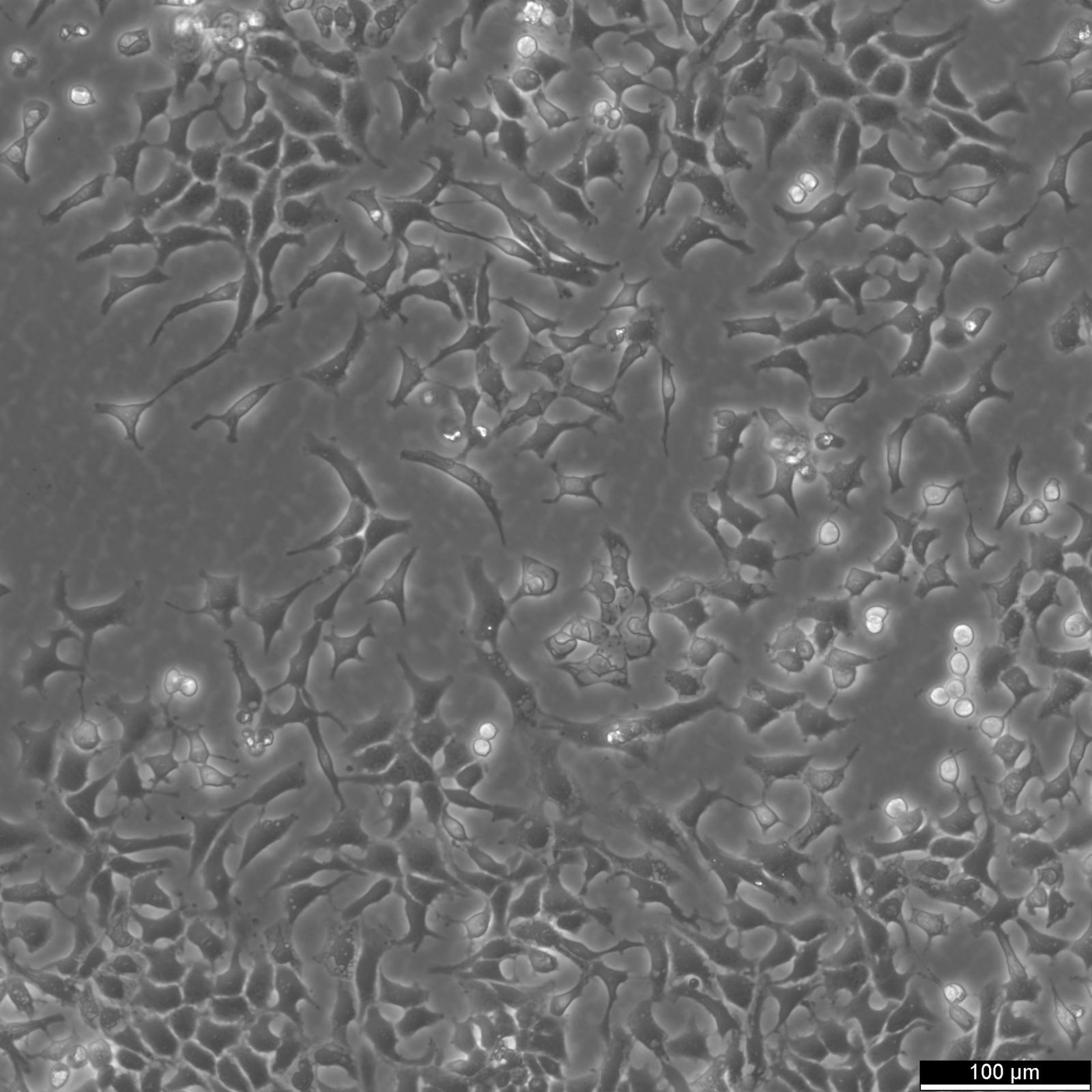
CHO-celler, eller ovarieceller fra kinesiske hamstere, er blevet en grundpille i den biomedicinske forskning og bioteknologi. Disse pattedyrsceller, der først blev isoleret i 1957 af Theodore Puck, har vist sig at være et bemærkelsesværdigt alsidigt og robust værktøj til en lang række anvendelser, lige fra grundforskning til produktion af livreddende lægemidler.
En af de vigtigste faktorer, der bidrager til CHO-cellernes succes, er deres tilpasningsevne til forskellige dyrkningsbetingelser. De kan dyrkes som adhærente kulturer eller suspensionskulturer, hvilket giver forskerne mulighed for at opskalere produktionen efter behov. Derudover er CHO-celler i stand til at udføre komplekse posttranslationelle modifikationer, såsom glykosylering, som er afgørende for den korrekte funktion af mange pattedyrsproteiner.
CHO-cellers evne til at producere biologisk aktive proteiner har gjort dem til en arbejdshest i den biofarmaceutiske industri. I dag bruges CHO-celler til at fremstille en lang række terapeutiske proteiner, herunder monoklonale antistoffer, hormoner og enzymer. Faktisk er CHO-celler ansvarlige for at producere omkring 70 % af alle rekombinante proteinterapier på markedet, med en anslået global markedsværdi på over 100 milliarder dollars.
Ud over deres anvendelse inden for bioteknologi har CHO-celler også været medvirkende til at fremme vores forståelse af grundlæggende biologiske processer. De er f.eks. blevet brugt til at studere den epidermale vækstfaktorreceptor (EGFR), en vigtig aktør i cellevækst og -overlevelse, som ofte er dysreguleret i kræft. Ved at udtrykke EGFR i CHO-celler har forskere været i stand til at belyse dens signalveje og udvikle målrettede terapier til at hæmme dens aktivitet i tumorer.
Efterspørgslen efter biofarmaceutiske produkter fortsætter med at vokse, og det samme gør betydningen af CHO-celler i forskning og produktion. Den igangværende indsats for at optimere CHO-cellelinjer, såsom at øge proteinudbyttet, forbedre glykosyleringsmønstre og reducere risikoen for viruskontaminering, vil yderligere cementere deres position som et kritisk værktøj i kampen mod sygdomme.
Kort sagt har CHO-celler fået deres plads blandt de bedste cellelinjer i biomedicinsk forskning på grund af deres tilpasningsevne, evne til at producere komplekse pattedyrsproteiner og omfattende resultater i den biofarmaceutiske industri. I takt med at vi fortsætter med at opklare biologiens mysterier og udvikle nye behandlingsformer, vil CHO-celler utvivlsomt forblive en vigtig ressource for både forskere og producenter.
Nummer 3: Immortaliserede humane cellelinjer
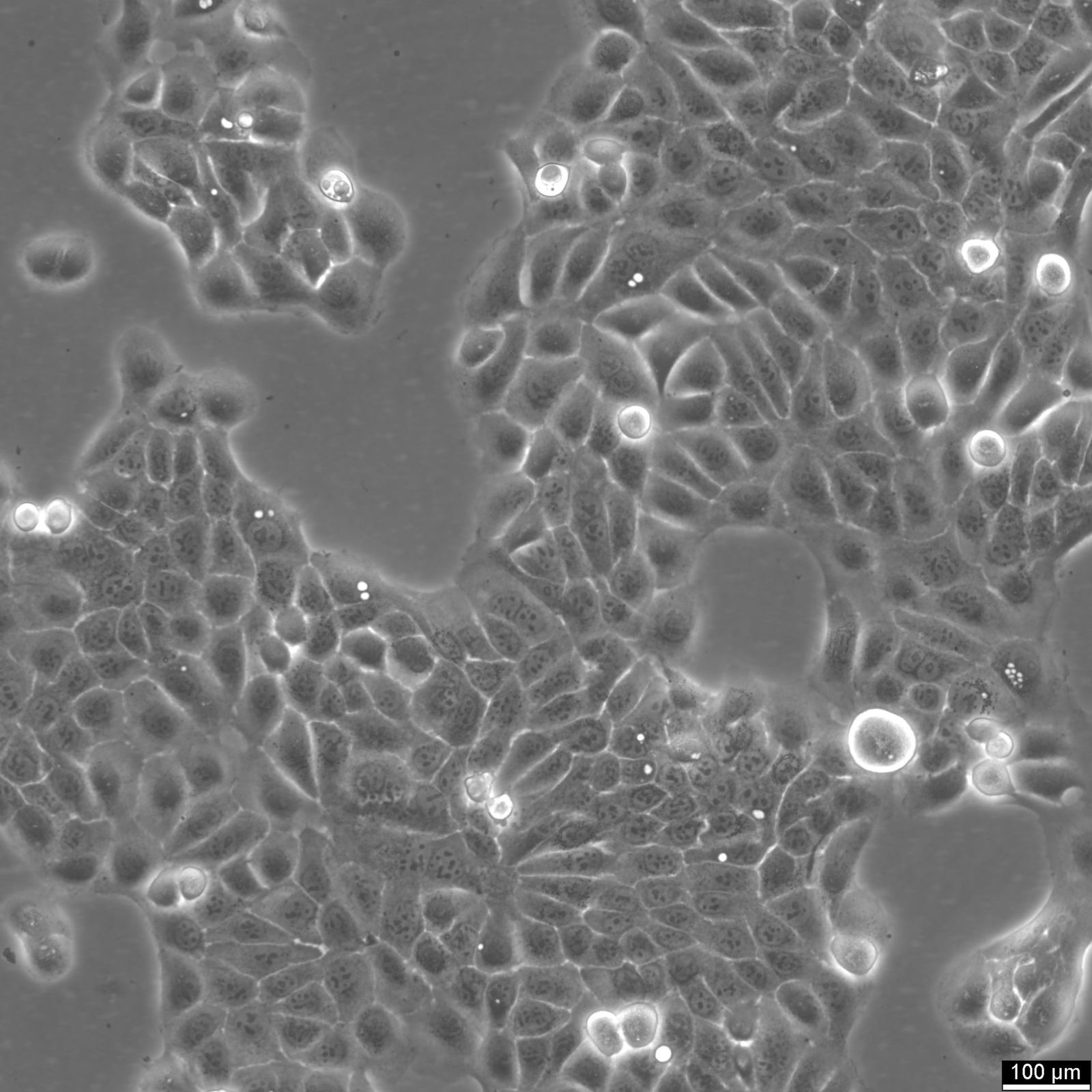
Immortaliserede humane cellelinjer er blevet et uundværligt værktøj i biomedicinsk forskning og giver forskere en næsten uendelig forsyning af genetisk ensartede celler til studier af human biologi og sygdom. Disse cellelinjer stammer fra forskellige væv og er blevet genetisk modificeret eller naturligt udvalgt til at overvinde de normale begrænsninger for celledeling, så de kan sprede sig på ubestemt tid i kultur.
En af de største fordele ved udødeliggjorte humane cellelinjer er deres evne til at skabe en konsistent og reproducerbar model for studier af humanbiologi. Ved at eliminere den variation, der er forbundet med primære celler, som har en begrænset levetid og kan variere fra donor til donor, gør udødeliggjorte cellelinjer det muligt for forskere at udføre eksperimenter med større præcision og pålidelighed.
Udvalget af udødelige humane cellelinjer, der er tilgængelige i dag, er stort, og hver cellelinje giver unik indsigt i specifikke aspekter af human biologi eller sygdom. For eksempel har Jurkat-celler, der stammer fra human T-celle leukæmi, været medvirkende til at studere T-cellesignalering og immunrespons. På samme måde er MCF-7-celler, en brystkræftcellelinje, blevet brugt i vid udstrækning til at undersøge de molekylære mekanismer i brystkræft og til at screene potentielle terapeutiske midler.
NCI-60 Human Tumor Cell Lines Screen, en samling af 60 immortaliserede humane kræftcellelinjer, der repræsenterer ni forskellige tumortyper, har været en værdifuld ressource for kræftforskningen, siden den blev etableret i slutningen af 1980'erne. Dette panel er blevet brugt til at screene hundredtusindvis af stoffer for kræftaktivitet, hvilket har ført til identifikation af adskillige lovende lægemiddelkandidater og øget vores forståelse af kræftbiologi.
På trods af deres mange fordele er det vigtigt at anerkende begrænsningerne ved udødeliggjorte humane cellelinjer. Disse celler har gennemgået betydelige genetiske ændringer for at opnå udødelighed, hvilket måske ikke nøjagtigt afspejler normale humane cellers adfærd in vivo. Derudover kan den langvarige dyrkning af disse celler føre til yderligere genetiske og fænotypiske ændringer, hvilket understreger vigtigheden af regelmæssig godkendelse af cellelinjer og kvalitetskontrolforanstaltninger.
Immortaliserede humane cellelinjer har revolutioneret den biomedicinske forskning ved at udgøre en standardiseret og uudtømmelig kilde til humane celler til undersøgelse af en lang række biologiske processer og sygdomme. Efterhånden som forskerne fortsætter med at udvikle nye cellelinjer og forfine de eksisterende, vil disse kraftfulde værktøjer uden tvivl spille en central rolle i at fremme vores forståelse af den menneskelige biologi og drive udviklingen af nye behandlingsformer i de kommende år.
Nummer 2: HEK293-celler
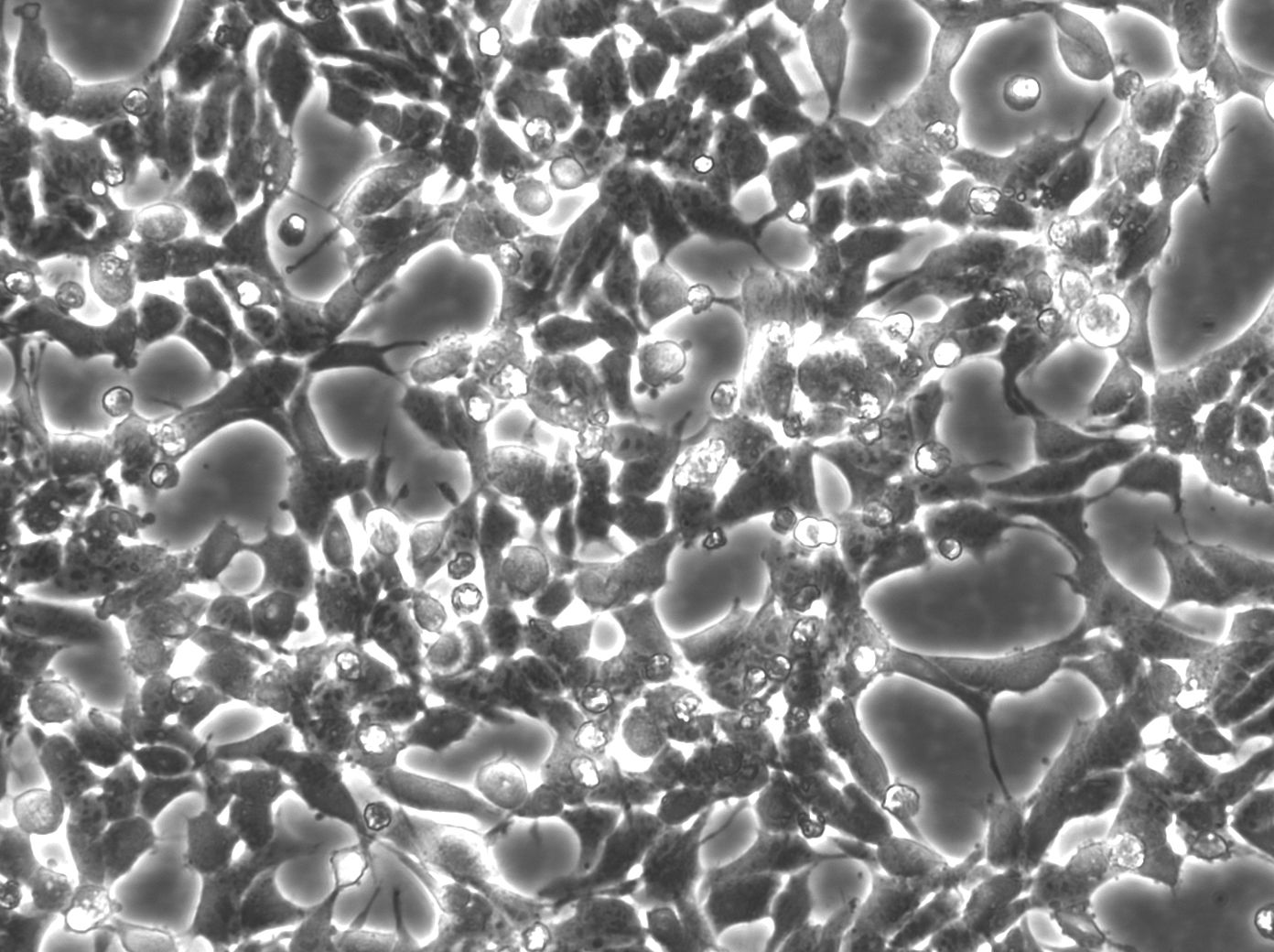
HEK293-celler, eller Human Embryonic Kidney 293-celler, er blevet en af de mest anvendte cellelinjer i biomedicinsk forskning på grund af deres alsidighed, lette dyrkning og høje transfekteringsevne. Disse celler blev oprindeligt fremstillet af humane embryonale nyreceller i 1973 ved transformation med adenovirus-DNA, og de er siden blevet tilpasset til en lang række anvendelser.
En af de vigtigste styrker ved HEK293-celler er deres evne til at udtrykke høje niveauer af rekombinante proteiner, når de transfekteres med de rette ekspressionsvektorer. Det har gjort dem til et uvurderligt værktøj til at studere proteinfunktion, signaltransduktionsveje og lægemiddel-protein-interaktioner. Derudover er HEK293-celler i stand til at udføre mange af de posttranslationelle modifikationer, der er nødvendige for korrekt proteinfunktion, hvilket sikrer, at de rekombinante proteiner, der produceres i disse celler, ligner deres oprindelige modstykker.
Ud over deres anvendelighed i proteinekspressionsstudier er HEK293-celler også blevet brugt i vid udstrækning inden for genterapi. Disse celler er meget tolerante over for virusinfektion og replikation, hvilket gør dem til en ideel platform til produktion af virale vektorer, der bruges til genlevering. Faktisk er HEK293-celler blevet brugt til at producere flere FDA-godkendte genterapiprodukter, såsom Zolgensma® til behandling af spinal muskelatrofi.
I de senere år har HEK293-celler også vist sig at være et værdifuldt værktøj i studiet af ionkanaler og G-proteinkoblede receptorer (GPCR'er). Ved at udtrykke disse proteiner i HEK293-celler og bruge avancerede elektrofysiologiske teknikker har forskere været i stand til at få ny indsigt i deres struktur, funktion og farmakologi. Det har ført til identifikation af nye lægemiddelmål og udvikling af mere selektive og potente lægemidler.
På trods af deres mange fordele er det vigtigt at erkende, at HEK293-celler ikke er uden begrænsninger. Som en udødeliggjort cellelinje afspejler de måske ikke altid nøjagtigt normale humane cellers adfærd in vivo. Desuden har den adenovirale transformation, der bruges til at skabe disse celler, resulteret i betydelige genomiske omlejringer og ændringer i genekspressionen, hvilket kan påvirke deres biologiske egenskaber.
Sammenfattende har HEK293-celler opnået en plads som en af de bedste cellelinjer inden for biomedicinsk forskning på grund af deres alsidighed, høje transfekterbarhed og omfattende resultater inden for proteinekspression, genterapi og ionkanal-/GPCR-studier. I takt med at forskere fortsætter med at flytte grænserne for videnskabelig viden, vil HEK293-celler uden tvivl forblive et vigtigt værktøj til at afdække kompleksiteten i menneskelig biologi og sygdom.
Nummer 1: HeLa-celler

HeLa-celler, den første udødelige menneskelige cellelinje, har en fascinerende og kontroversiel historie, der har sat et uudsletteligt præg på den biomedicinske forskning. HeLa-cellerne, der stammer fra livmoderhalskræftceller fra Henrietta Lacks i 1951, har været på forkant med videnskabelige opdagelser i over et halvt århundrede og har bidraget til adskillige gennembrud inden for alt fra kræftforskning til vaccineudvikling.
Et af de mest bemærkelsesværdige træk ved HeLa-cellerne er deres enestående modstandskraft og tilpasningsevne. Disse celler kan overleve og sprede sig under en lang række forhold, hvilket gør dem til en ideel model til undersøgelse af virkningerne af lægemidler, toksiner og andre miljøfaktorer på menneskeceller. Desuden har HeLa-celler en usædvanlig høj telomeraseaktivitet, som gør det muligt for dem at vedligeholde deres telomerer og undgå cellulær senescens, hvilket bidrager til deres udødelighed.
HeLa-cellernes betydning for den biomedicinske forskning kan ikke overvurderes. De er blevet brugt til at studere stort set alle aspekter af cellulær biologi, fra grundlæggende cellulære processer som DNA-replikation og proteinsyntese til komplekse sygdomsmekanismer som virusinfektion og kræftudvikling. Faktisk var HeLa-celler medvirkende til udviklingen af poliovaccinen i 1950'erne og er siden blevet brugt til at studere en lang række vira, herunder HIV, Zika og SARS-CoV-2.
Historien om HeLa-cellerne er dog ikke uden kontroverser. I årtier var disse cellers oprindelse ukendt for offentligheden, og Henrietta Lacks' familie var uvidende om, at hendes celler var blevet taget og brugt til forskning uden hendes samtykke. Det rejser vigtige etiske spørgsmål om informeret samtykke, patienters privatliv og kommercialisering af menneskeligt væv.
I de senere år er der blevet gjort en indsats for at anerkende Henrietta Lacks' bidrag til videnskaben og for at inddrage hendes familie i diskussioner om brugen af HeLa-celler. I 2013 indgik National Institutes of Health en aftale med Lacks-familien om at etablere HeLa Genome Data Access Working Group, som giver familien en vis kontrol over, hvordan HeLa genomdata bruges i forskningen.
På trods af de etiske bekymringer omkring deres oprindelse er HeLa-celler fortsat et vigtigt redskab i biomedicinsk forskning. Deres unikke egenskaber og historiske betydning har cementeret deres plads som den mest udbredte og indflydelsesrige cellelinje i verden. Mens vi fortsat kæmper med de videnskabelige og etiske implikationer af HeLa-celler, er det klart, at deres indflydelse på videnskaben og samfundet vil vare ved i generationer fremover.
Konklusion
De fem cellelinjer, der er blevet undersøgt i denne artikel - Sf9, CHO, immortaliserede humane cellelinjer, HEK293 og HeLa - har hver især spillet en afgørende rolle for vores forståelse af biologi og sygdom. Disse cellelinjer har fungeret som uvurderlige værktøjer for forskere, der har muliggjort banebrydende opdagelser og banet vejen for nye terapier og behandlinger.
Når vi ser på fremtiden for biomedicinsk forskning, er det klart, at cellelinjer fortsat vil være en drivkraft bag videnskabelige fremskridt. Ved at levere en standardiseret og tilgængelig model til at studere komplekse biologiske processer gør cellelinjer det muligt for forskere at stille nye spørgsmål, teste dristige hypoteser og skubbe grænserne for, hvad der er muligt.
Men som historien om HeLa-cellerne minder os om, er brugen af cellelinjer i forskning ikke uden etiske og sociale konsekvenser. Som forskere har vi et ansvar for at engagere os i disse spørgsmål og sikre, at vores arbejde udføres med den største respekt for patienternes autonomi, privatliv og værdighed.
I sidste ende afhænger den biomedicinske forsknings succes ikke kun af styrken i vores videnskabelige værktøjer, men også af den integritet og medfølelse, hvormed vi bruger dem. Ved at omfavne både det videnskabelige potentiale og de etiske udfordringer ved cellelinjeforskning kan vi fortsætte med at opklare livets mysterier og arbejde hen imod en fremtid, hvor fordelene ved videnskabelige fremskridt deles af alle.
