Objem: 100 ml
Skladování: ≤ –15 °C
Sterilita: Sterilně filtrovaný
Stabilní glutaminový roztok (L-alanyl-L-glutamin, 200 mM) je vysoce stabilní dipeptidová forma L-glutaminu navržená jako přímá náhrada za konvenční L-glutamin v médiích pro buněčné kultury. L-glutamin je esenciální aminokyselina a hlavní zdroj energie pro kultivované buňky, který hraje klíčovou roli v buněčném růstu, metabolismu a syntéze bílkovin.
Použití a výhody
Ve standardních tekutých médiích se L-glutamin relativně rychle rozkládá při teplotě 37 °C, což vede k tvorbě toxických vedlejších produktů, jako jsou amonné ionty, které mohou negativně ovlivnit životaschopnost buněk a výsledky experimentů. Stabilní glutamin překonává toto omezení tím, že poskytuje nerozložitelnou dipeptidovou formu, která zůstává v kultivačních podmínkách neporušená.
Buňky enzymaticky štěpí dipeptidovou vazbu, aby uvolnily L-glutamin podle potřeby, čímž zajišťují nepřetržitý přísun čerstvého glutaminu a zároveň zabraňují hromadění škodlivých odpadních produktů. Díky tomu je tento roztok obzvláště výhodný pro dlouhodobé buněčné kultury a růstové systémy s vysokou hustotou.
Složení a použití
Roztok L-alanyl-L-glutaminu se připravuje ve vodě vhodné pro buněčné kultury v koncentraci 200 mM a je sterilně filtrován pro aplikace citlivé na kontaminaci. Lze jej ředit přímo do kompletních médií podle experimentálních požadavků. Skladujte při teplotě ≤ –15 °C a vyhněte se opakovaným cyklům zmrazování a rozmrazování, aby byla zachována stabilita produktu.
Pouze pro výzkumné účely. Není určeno pro diagnostické nebo terapeutické postupy. Není určeno pro použití u lidí nebo zvířat.
Objem: 100 ml
Skladování: +2 °C až +8 °C
Sterilita: Sterilně filtrovaný
HEPES pufrovací roztok (1 M), také známý jako kyselina N-2-hydroxyethylpiperazin-N-2-etansulfonová, je zwitteriontové organické pufrovací činidlo široce používané v médiích pro buněčné kultury. Je navržen tak, aby udržoval stabilní pH v fyziologickém rozmezí 6,7 až 8,6 a podporoval optimální buněčnou funkci při in vitro aplikacích.
Použití a výhody
HEPES poskytuje spolehlivou pufrovací kapacitu v systémech buněčných kultur, zejména při manipulaci s buňkami mimo CO₂ inkubátor. Přidání 10–25 mM HEPES do kultivačních médií nabízí zvýšenou stabilitu pH během delších manipulačních období, což pomáhá udržovat konzistentní experimentální podmínky.
Tento pufr je nepropustný pro membrány, má minimální vliv na biochemické reakce a vykazuje silnou chemickou a enzymatickou stabilitu. Díky těmto vlastnostem je vhodný pro širokou škálu buněčných kultur a biochemických aplikací.
Složení a použití
Roztok se dodává jako 1 M koncentrát připravený ve vodě vhodné pro buněčné kultury a je sterilně filtrován pro použití v prostředí citlivém na kontaminaci. Lze jej zředit na požadovanou pracovní koncentraci v závislosti na požadavcích aplikace. Skladujte při teplotě +2 °C až +8 °C a manipulujte za aseptických podmínek, aby byla zachována integrita produktu.
Pouze pro výzkumné účely. Není určeno pro diagnostické nebo terapeutické postupy. Není určeno pro použití u lidí nebo zvířat.
Objem: 50 ml
Skladování: +2 °C až +8 °C
Sterilita: Sterilně filtrovaný
Roztok D-(+)-glukózy (roztok dextrózy) je sterilní, připravený k použití doplněk obsahující přirozeně se vyskytující cukr D-(+)-glukózu, která je ústřední složkou buněčného metabolismu. Glukóza se podílí na základních biologických procesech, jako je výroba energie, glykosylace a tvorba glykanů, které přispívají k buněčné struktuře a funkci.
Použití a výhody
Tento roztok glukózy je široce používán jako doplněk v médiích pro buněčné kultury a v mnoha aplikacích buněčné a molekulární biologie. Jako primární zdroj uhlíku a energie podporuje glukóza buněčný růst, proliferaci a metabolickou aktivitu. Díky své účasti v biosyntetických drahách je také nezbytná pro udržení normální buněčné fyziologie a experimentální konzistence.
Složení a použití
Roztok je dodáván ve vysoké koncentraci 250 g/l glukózy, což umožňuje flexibilní ředění do kultivačních médií podle experimentálních požadavků. Je sterilně filtrován, aby byla zajištěna vhodnost pro aplikace citlivé na kontaminaci. Skladujte při teplotě +2 °C až +8 °C a zacházejte s ním asepticky, aby byla zachována kvalita a stabilita produktu.
Pouze pro výzkumné účely. Není určeno pro diagnostické nebo terapeutické postupy. Není určeno pro použití u lidí nebo zvířat.
Objem: 10 ml
Skladování: +2 °C až +8 °C
Sterilita: Sterilně filtrováno
Roztok inzulínu-transferinu-selenu (ITS) (100x) je chemicky definovaný doplněk určený pro širokou škálu aplikací v buněčných kulturách. Nejčastěji se používá jako přísada do bazálních buněčných kultivačních médií na podporu růstu buněk v podmínkách se sníženým obsahem séra nebo bez séra.
Použití a výhody
Náš doplněk ITS poskytuje základní složky potřebné pro optimální výkon bezsérových médií. Doplněním konvenčních živných médií o ITS lze výrazně snížit potřebu fetálního bovinního séra (FBS) pro rutinní udržování mnoha buněčných linií. To pomáhá minimalizovat variabilitu spojenou s používáním séra a zároveň udržuje konzistentní růst a životaschopnost buněk.
Inzulín podporuje buněčnou absorpci a metabolismus klíčových živin, transferin usnadňuje transport železa a selen přispívá k antioxidační obraně a enzymatické aktivitě. Společně tyto složky podporují vyvážený buněčný metabolismus a zlepšují reprodukovatelnost v definovaných kultivačních systémech.
Složení a použití
Insulin-Transferrin-Selenium (ITS) se dodává jako 100x koncentrovaný roztok v Earle's Balanced Salt Solution (EBSS) bez fenolové červeně. Pro standardní použití zřeďte v poměru 1:100 do vhodného bazálního média, abyste dosáhli doporučené pracovní koncentrace. Skladujte při teplotě +2 °C až +8 °C a manipulujte v aseptických podmínkách, aby byla zachována stabilita a sterilita produktu.
Pouze pro výzkumné účely. Není určeno pro diagnostické nebo terapeutické postupy. Není určeno pro použití u lidí nebo zvířat.
Objem: 5 ml
Skladování: +2 °C až +8 °C
Sterilita: Sterilně filtrováno
Roztok rekombinantního lidského inzulínu je chemicky definovaný doplněk běžně používaný pro kultivaci savčích buněčných linií, včetně buněk vaječníků čínského křečka (CHO). Tento roztok pro buněčné kultury obsahuje rekombinantní lidský inzulín exprimovaný v Saccharomyces cerevisiae, což zajišťuje vysokou čistotu a konzistentní výkon ve výzkumných aplikacích.
Použití a výhody
Inzulín se běžně přidává do bezsérumových a chemicky definovaných médií, aby podpořil růst a produktivitu buněk. Jako klíčový regulační hormon podporuje inzulín buněčnou absorpci, využití a ukládání glukózy, aminokyselin a mastných kyselin. Inhibuje také rozklad glykogenu, bílkovin a lipidů, čímž přispívá ke zlepšení životaschopnosti buněk a metabolické stability v kultivačních systémech. Chemicky definované složení podporuje reprodukovatelnost a minimalizuje variabilitu v citlivých pracovních postupech buněčných kultur.
Biologické vlastnosti a použití
Inzulín je dvouvláknový polypeptidový hormon přirozeně produkovaný β-buňkami pankreatických ostrůvků. Má molekulovou hmotnost přibližně 5 800 Da. α
- a β-řetězce jsou spojeny dvěma mezireťazcovými disulfidovými vazbami a α-řetězec obsahuje jednu intrareťazcovou disulfidovou vazbu. Pro aplikace v buněčných kulturách by se s roztokem mělo zacházet za aseptických podmínek a skladovat při teplotě +2 °C až +8 °C, aby byla zachována stabilita a účinnost.
Pouze pro výzkumné účely. Není určeno pro diagnostické nebo terapeutické postupy. Není určeno pro použití u lidí nebo zvířat.
Objem: 100 ml
Skladování: +2 °C až +8 °C
Sterilita: Sterilně filtrovaný
Roztok pyruvátu sodného (100 mM) je sterilní, připravený k použití doplněk určený k poskytnutí dodatečného, snadno dostupného zdroje energie pro buněčná kultivační média. Pyruvát sodný hraje klíčovou roli v buněčném energetickém metabolismu a podporuje růst metabolicky aktivních a rychle se množících buněk, jako jsou například nádorové buňky. Doplnění může zvýšit životaschopnost buněk a pomoci udržet metabolickou stabilitu v kultivačních systémech.
Použití a výhody
Tento roztok se široce používá v rutinní buněčné kultuře k obohacení médií pyruvátem a podpoře optimálních růstových podmínek. Podporuje produkci ATP, může pomoci snížit oxidační stres a přispívá ke zlepšení metabolické výkonnosti kultivovaných buněk. Produkt je vyráběn ve vodě vhodné pro buněčné kultury a sterilně filtrován, což zajišťuje konzistentní kvalitu a reprodukovatelnost ve výzkumných pracovních postupech.
Použití a kompatibilita
Doporučená konečná koncentrace pro většinu aplikací buněčné kultury je 1 mM pyruvát sodný, kterého se dosáhne zředěním 100 mM zásobního roztoku v poměru 1:100 do kompletního kultivačního média. Roztok je kompatibilní s širokou škálou bazálních médií a savčích buněčných linií. Skladujte při teplotě +2 °C až +8 °C a chraňte před kontaminací, aby byla zachována stabilita produktu.
Pouze pro výzkumné účely. Není určeno pro diagnostické nebo terapeutické postupy. Není určeno pro použití u lidí nebo zvířat.
Objem: 100 ml Skladování: ≤-15 °C Sterilita: Sterilně filtrováno
Antibiotický/antimykotický roztok (100x ) je sterilní koncentrát připravený k použití, určený ke snížení rizika mikrobiální kontaminace v buněčných kulturách a příbuzných laboratorních aplikacích. Tento 100x roztok obsahuje osvědčenou kombinaci penicilinu, streptomycinu a amfotericinu B, která poskytuje široké spektrum antimikrobiální aktivity proti grampozitivním a gramnegativním bakteriím, kvasinkám a vláknitým houbám. Složení je vhodné pro použití v eukaryotických buněčných kulturách, bakteriálních médiích a dalších systémech citlivých na kontaminaci, což podporuje čistý a konzistentní laboratorní provoz.
Použití a výhody Tento roztok je optimalizován pro rutinní výzkumné protokoly a je široce používán k udržování aseptických podmínek v pracovních postupech buněčných kultur. Nabízí spolehlivý výkon v prostředí citlivém na kontaminaci a pomáhá výzkumníkům snížit riziko přemnožení mikroorganismů, aniž by bylo ohroženo zdraví buněk nebo reprodukovatelnost experimentů. Sterilně filtrované složení eliminuje potřebu dalších solubilizačních kroků, čímž podporuje zefektivnění přípravy médií a snižuje variabilitu každodenních laboratorních postupů.
Použití a kompatibilita Pro dosažení standardních pracovních koncentrací roztok nařeďte v poměru 1:100 do kompletního kultivačního média. Produkt je kompatibilní se širokou škálou savčích buněčných linií a základních médií. Díky stálé skladové dostupnosti mohou výzkumní pracovníci těžit ze spolehlivé kontinuity dodávek a zjednodušeného plánování logistiky. Roztok by měl být skladován při teplotě ≤ -15 °C a chráněn před opakovanými cykly zmrazování a rozmrazování, aby byla zachována jeho stabilita. Pouze pro výzkumné použití. Není určeno k použití při diagnostických nebo terapeutických postupech. Není určeno k použití u lidí nebo zvířat.
Objem: 100 ml Skladování: skladování: +2°C až +8°C Sterilita: Sterilně filtrováno
MEM Non-Essential Amino Acids (100x ) je sterilní doplněk určený ke zvýšení růstu a životaschopnosti buněk v systémech buněčných kultur savců. Složení odpovídá 100násobnému koncentrátu neesenciálních aminokyselin obsažených ve standardním minimálním esenciálním médiu (MEM), což umožňuje přímé doplnění základního média s minimální přípravou.
Použití a výhody Tento doplněk poskytuje dodatečnou zásobu aminokyselin pro rychle se množící buňky nebo pro buněčné linie, které ztratily schopnost syntetizovat neesenciální aminokyseliny de novo. Tím, že zmírňuje metabolickou zátěž biosyntézy, podporuje lepší kinetiku růstu, prodlouženou životaschopnost a větší experimentální konzistenci
- zejména v kulturách citlivých na živiny nebo s vysokou hustotou.
Složení a použití Roztok obsahuje glycin, L-alanin, L-asparagin, kyselinu L-asparagovou, kyselinu L-glutamovou, L-prolin a L-serin. Je kompatibilní s MEM a většinou dalších standardních médií. Pro použití se ředí v poměru 1:100 do konečného kultivačního média. Tento produkt je sterilně filtrovaný a připravený k použití bez dalších manipulačních kroků. Pouze pro výzkumné použití. Není určen k použití při diagnostických nebo terapeutických postupech. Není určeno pro použití u lidí nebo zvířat.
Accutase je sterilně filtrovaný roztok pro odloučení buněk připravený k okamžitému použití, který byl vyvinut jako šetrná alternativa k trypsinu/EDTA pro disociaci adhezivních savčích buněk ze standardních plastových nádob pro tkáňové kultury a povrchů potažených adhezivním povlakem. Kombinuje proteolytickou a kolagenolytickou enzymatickou aktivitu ve vyváženém solném roztoku, aby zajistil účinnou, ale kontrolovanou disociaci, zachoval proteiny na povrchu buněk a podpořil vysokou životaschopnost po pasážování a rychlé opětovné přilnutí.
Složení přípravku Accutase je založeno na Dulbeccově fosfátovém pufru (DPBS) s EDTA a fenolovou červení jako vizuálním indikátorem pH. Enzymy jsou ne-savčího a ne-bakteriálního původu, díky čemuž je Accutase obzvláště vhodný pro výzkum kmenových buněk, pracovní postupy při vývoji vakcín a jakékoli aplikace, kde je nutné minimalizovat kontaminaci pocházející ze zvířat nebo mikroorganismů. Roztok se při teplotě 37 °C automaticky inhibuje, takže po oddělení buněk není zapotřebí žádné neutralizační činidlo ani médium obsahující sérum – buňky lze přenést přímo do čerstvého média.
Hlavní vlastnosti
Připravená k použití 1x sterilně filtrovaná kapalina – není nutné ředění ani rekonstituce
Kombinovaná proteolytická a kolagenolytická enzymová aktivita pro šetrnou disociaci
Každá šarže je standardizována na definovanou disociační aktivitu pro konzistenci mezi šaržemi
Enzymy nepocházejí ze savců ani z bakterií
Automatická inhibice při 37 °C – není potřeba neutralizační roztok
Formulováno v Dulbeccoově PBS s EDTA
Obsahuje fenolovou červeň jako vizuální indikátor pH
pH 6,8 – 7,8
Typické aplikace
Accutase šetrně disociuje širokou škálu adhezivních a citlivých buněčných typů, včetně lidských embryonálních kmenových buněk (hESCs), lidských indukovaných pluripotentních kmenových buněk (iPSCs), neurálních kmenových buněk, primárních neuronů a běžně kultivovaných adhezivních linií, jako jsou HeLa, HEK 293, CHO, MDCK, Vero, NIH/3T3, BHK-21 a A549. Mezi typické příklady použití patří:
Rutinní subkultivace a pasážování adhezivních savčích buněk
Šetrná disociace jednotlivých buněk hESCs, iPSCs a dalších citlivých linií
Příprava vzorků pro průtokovou cytometrii a analýzu FACS
Analýza markerů na povrchu buněk, kde záleží na integritě epitopu
Testování migrace, proliferace a apoptózy buněk
Testování klidového stavu pomocí deprivace séra a studie transfekce onkogenů
Testování migrace nádorových buněk a buněk neurální lišty
Zvýšení produkce v bioreaktorových pracovních postupech
Pro rutinní práci naneste přibližně 10 ml přípravku Accutase na 75 cm2 kultivační plochy a inkubujte 5–10 minut při pokojové teplotě. Optimální doba inkubace by měla být stanovena pro každou buněčnou linii a neměla by přesáhnout jednu hodinu. Před přidáním opláchněte buněčnou vrstvu roztokem soli bez Ca2+/Mg2+, například DPBS bez vápníku a hořčíku, aby se odstranily zbytky séra a dvojmocné kationty.
Manipulace a skladování
Neotevřenou lahvičku skladujte zmrazenou při teplotě -15 °C nebo nižší. Rozmrazujte buď při pokojové teplotě, nebo přes noc při teplotě +2 °C až +8 °C. Accutase nerozmrazujte ve vodní lázni o teplotě 37 °C, protože zvýšené teploty snižují enzymovou aktivitu. Po rozmrazení lze roztok skladovat až 2 měsíce při teplotě +2 °C až +8 °C; neskladujte při pokojové teplotě. Před použitím reagencií neohřívejte na 37 °C – přidejte ji přímo k promytým buňkám při pokojové teplotě. Pro dlouhodobou skladovatelnost se doporučuje rozdělit reagenci na jednorázové alikvoty, aby se zabránilo opakovaným cyklům rozmrazování. Vždy pracujte za aseptických podmínek.
Kvalita
Vyrobeno podle přísných standardů kvality. Každá šarže přípravku Accutase je sterilizována filtrací a testována na sterilitu, pH, vzhled a disociační aktivitu, aby byla zajištěna konzistentní a reprodukovatelná výkonnost mezi jednotlivými šaržemi.
Specifikace produktu
Specifikace
Detail
Typ produktuReagencie pro odloučení/disociaci buněk
FormátSterilně filtrovaná kapalina, připravená k použití
Objem100 ml
Pracovní koncentrace1x (připraveno k použití)
Enzymová aktivitaKombinovaná proteolytická a kolagenolytická
Původ enzymuNesavčí a nebakteriální
Pufrovací systémDulbeccoův PBS s EDTA
Indikátor pHFenolová červeň
Rozsah pH6,8 – 7,8
VzhledČirý, světle červený až oranžový roztok
Skladovací teplota-15 °C nebo nižší
Stabilita po rozmrazeníAž 2 měsíce při teplotě +2 °C až +8 °C
Doporučený objem pro použití~10 ml na 75 cm2 kultivační plochy
Typická doba inkubace5 – 10 minut při pokojové teplotě
Podmínky přepravyZmrazené v suchém ledu
Určené použitíPouze pro výzkumné účely a další výrobu
Složení (složení na litr)
Složka
Koncentrace (mg/l)
Anorganické soli
Chlorid sodný (NaCl)8000,00
Hydrogenfosforečnan disodný (Na2HPO4)1150,00
Chlorid draselný (KCl)200,00
Dihydrogenfosforečnan draselný (KH₂PO₄)200,00
Ostatní složky
EDTA · 4Na (EDTA tetrasodný)220,00
Fenolová červeň3,00
Patentovaná směs enzymů (proteolytická a kolagenolytická aktivita)1x
Accutase je registrovaná ochranná známka společnosti Innovative Cell Technologies, Inc.
Tato sterilně filtrovaná kapalná formulace připravená k okamžitému použití je doplněna o Earleův vyvážený solný roztok (EBSS), 2 mM L-glutamin, D-glukózu (1,0 g/l) a 2,2 g/l hydrogenuhličitanu sodného (NaHCO3), díky čemuž je vhodná pro použití v atmosféře inkubátoru s regulovaným obsahem CO2 (obvykle 5 % CO2). Obsažený fenolrudý slouží jako indikátor pH, což umožňuje pohodlné vizuální sledování stavu média během buněčné kultury.
Hlavní vlastnosti
Klasické složení Eagle’s MEM s Earle’s Balanced Salt Solution (EBSS)
Obsahuje 2 mM L-glutamin – připraveno k okamžitému použití
2,2 g/l hydrogenuhličitanu sodného – pufrováno pro inkubaci s 5 % CO2
S D-glukózou (1,0 g/l) jako primárním zdrojem uhlíku
S fenolovou červení jako indikátorem pH
Bez HEPES a bez pyruvátu sodného
Sterilně filtrované tekuté médium, připravené k použití
pH 7,0 – 7,6
Typické aplikace
EMEM podporuje kultivaci široké škály savčích buněčných linií, včetně HeLa, HEK 293, Vero, MRC-5, L-929, BHK-21 a mnoha primárních buněk. Mezi běžné aplikace patří:
Rutinní udržování a expanze adhezivních buněčných linií
Pracovní postupy pro množení virů a výrobu vakcín
Aplikace v oblasti cytotoxicity a biologických testů
Studie transfekce a exprese proteinů
Základní výzkum v oblasti buněčné biologie a molekulární biologie
Pro optimální růst buněk se EMEM obvykle doplňuje 5–10 % fetálního bovinního séra (FBS) a, v závislosti na buněčné linii, neesenciálními aminokyselinami (NEAA) a antibiotiky, jako je penicilin/streptomycin.
Manipulace a skladování
Neotevřenou lahvičku skladujte při teplotě +2 °C až +8 °C, chráněnou před světlem. Po otevření používejte za aseptických podmínek. L-glutamin v roztoku podléhá postupné degradaci – pro dosažení nejlepšího výkonu doporučujeme médium spotřebovat do 4 týdnů od otevření, nebo v případě delšího skladování doplnit před použitím čerstvým L-glutaminem. Než médium přidáte k buňkám, nechte jej ohřát na 37 °C.
Kvalita
Vyrobeno podle přísných standardů kvality. Každá šarže je testována na sterilitu, pH, osmolalitu a hladinu endotoxinů, aby byla zajištěna konzistentní výkonnost při použití v buněčných kulturách.
Specifikace produktu
Specifikace
Detail
Typ produktuMEM
Kategorie produktuMédia pro buněčné kultury
FormátKapalina
SterilníAno
Velikost500 ml
L-glutaminS L-glutaminem (2 mM)
GlukózaS glukózou (1,0 g/l)
Hydrogenuhličitan sodnýS NaHCO3 (2,2 g/l)
HEPESBez HEPES
Pyruvát sodnýBez pyruvátu sodného
Fenolová červeňS fenolovou červení
Solný roztokEarleův vyvážený solný roztok (EBSS)
pH7,0 – 7,6
Obsah endotoxinůNení specifikováno
Skladování+2 °C až +8 °C
Složení (složení na litr)
Složka
Koncentrace (mg/l)
Anorganické soli
Chlorid vápenatý · 2H2O265,00
Síran hořečnatý97,72
Chlorid draselný400,00
Chlorid sodný6 800,00
Dihydrogenfosforečnan sodný, bezvodý122,00
Hydrogenuhličitan sodný (NaHCO3)2 200,00
Aminokyseliny
L-arginin · HCl126,00
L-cystin · 2HCl31,30
L-glutamin292,00
L-histidin · HCl · H2O42,00
L-isoleucin52,00
L-leucin52,00
L-lysin · HCl72,50
L-metionin15,00
L-fenylalanin32,00
L-threonin48,00
L-tryptofan10,00
L-tyrosin · 2Na · 2H2O51,90
L-valin46,00
Vitamíny
D-pantothenát vápenatý1,00
Cholin chlorid1,00
Kyselina listová1,00
myo-inositol2,00
Nikotinamid1,00
Pyridoxal · HCl1,00
Riboflavin0,10
Thiamin · HCl1,00
Ostatní složky
D(+)-glukóza1 000,00
Fenolová červeň10,00
Mezi hlavní vlastnosti Freeze Medium CM-1 patří:
Široká kompatibilita: Účinné pro širokou škálu buněčných typů, včetně primárních buněk, kmenových buněk a zavedených buněčných linií.
Vysoká životaschopnost: Optimalizováno pro maximální obnovu a životaschopnost buněk po rozmrazení, což zajišťuje spolehlivé výsledky experimentů.
Připraveno k použití: Pohodlně připravené a sterilizované pro okamžité použití, což zkracuje dobu přípravy a snižuje riziko kontaminace.
Zvýšená stabilita: Udržuje konzistentní výkonnost za standardních podmínek kryokonzervace a zajišťuje reprodukovatelné výsledky.
Dlouhá skladovatelnost: CM-1 je médium pro kryokonzervaci obsahující sérum, připravené k použití, které lze uchovávat v chladničce až jeden rok.
Použití přípravku CM-1 ke zmrazování buněk
Chcete-li použít CM-1 ke zmrazení adherentních i suspenzních buněk, postupujte podle následujících kroků
Pro adherentní buňky je omyjte a oddělte od kultivačního substrátu. U suspenzních buněk přejděte přímo k dalšímu kroku.
Spočítejte buňky, abyste zajistili jejich správnou koncentraci.
Odstřeďte buňky, abyste je peletovali, a poté je znovu rozpusťte v mrazicím médiu CM-1.
Resuspendované buňky přeneste do kryovialek.
Před přenosem buněk do dlouhodobého skladu použijte metodu pomalého zmrazování
Metoda
Popis
Kroky
❄️
Ruční zmrazení
Postupná metoda zahrnující postupné snižování teploty pro zajištění životaschopnosti buněk
1️⃣ Umístěte buňky do mrazicího média do mrazničky o teplotě 4 °C na 40 minut.
2️⃣ Přeneste na 24 hodin do mrazničky o teplotě -80 °C.
3️⃣ Pro dlouhodobé uchování uchovávejte buňky v tekutém dusíku
❄️
Použití přístroje Mr. Frosty
Praktické zařízení, které umožňuje řízenou rychlost zmrazování bez použití elektrické energie
1️⃣ Připravte buňky do kryovialek s mrazicím médiem.
2️⃣ Umístěte kryovialy do nádoby Mr. Frosty.
3️⃣ Před přenesením do kapalného dusíku uchovávejte při teplotě -80 °C po dobu 24 hodin
❄️
Mraznička s řízenou rychlostí
Vysoce přesný mrazák od společnosti Thermo Fisher nebo jiných výrobců určený k řízenému snižování teploty
1️⃣ Zařízení naprogramujte tak, aby postupně snižovalo teplotu.
2️⃣ Vložte připravené buňky do mrazničky.
3️⃣ Po skončení mrazicího cyklu přeneste buňky do tekutého dusíku
Kryovaky skladujte při teplotě nižší než -130 °C nebo v kapalném dusíku pro dlouhodobé uchování.
Složení
Obsahuje FBS, DMSO, glukózu, soli
Pufrovací schopnost: pH = 7,2 až 7,6
Mrazicí médium CM-1 společnosti Cytion nabízí spolehlivé řešení pro kryokonzervaci, které zajišťuje vysokou životaschopnost a funkčnost buněk po rozmrazení pro širokou škálu výzkumných aplikací.
Médium Ham's F-12K (Kaighn's) je pečlivě sestaveno tak, aby optimalizovalo podmínky kultivace buněk. Má obohacené složení, které poskytuje zvýšené množství základních složek, jako jsou aminokyseliny a pyruvát sodný, a také dalších prvků včetně putrescinu, thymidinu, hypoxantinu a zinku. Tyto přídavky umožňují výzkumným pracovníkům doplnit médium o minimální množství séra nebo definovaných složek pro specifické typy buněk, což usnadňuje přesné experimentální podmínky.
Pozoruhodné je, že Hamovo médium F-12K (Kaighnovo) neobsahuje proteiny ani růstové faktory. V důsledku toho je často nutné doplnění růstovými faktory a fetálním hovězím sérem (FBS), což výzkumníkům umožňuje přizpůsobit médium požadavkům jejich specifických buněčných linií. Pro dosažení optimálního výkonu musí být koncentrace FBS pečlivě optimalizována pro každou buněčnou linii, čímž se zajistí optimální růst a funkčnost.
Pro udržení fyziologického pH využívá médium Ham's F-12K (Kaighn's) pufrovací systém hydrogenuhličitanu sodného (2,5 g/l), což vyžaduje kontrolované prostředí s 5-10 % CO2 během kultivace. To zajišťuje, že pH média zůstává v ideálním rozmezí pro růst a životaschopnost buněk
Kontrola kvality
pH = 7,2 +/
- 0,02 při 20-25 °C.
Každá šarže byla testována na sterilitu a nepřítomnost mykoplazmy a bakterií.
Údržba
Uchovávejte v chladu při teplotě +2 °C až +8 °C ve tmě. Zmrazení i zahřátí na +37 °C snižuje kvalitu přípravku na minimum.
Nezahřívejte médium na teplotu vyšší než 37 °C a nepoužívejte nekontrolovatelné zdroje tepla (např. mikrovlnné přístroje).
Pokud má být použita pouze část média, odeberte toto množství z lahvičky a zahřejte jej při pokojové teplotě.
Doba použitelnosti jakéhokoli média kromě základního média je 8 týdnů od data výroby.
Složení
Složení
mg/l
Anorganické soli
Chlorid vápenatý x 2H2O
135,24
Síran měďnatý(II) x 5H2O
0,00
Síran železnatý x 7H2O
0,83
Chlorid hořečnatý x 6H2O
105,72
Síran hořečnatý x 7H2O
394,49
Chlorid draselný
283,29
Dihydrogenfosforečnan draselný
58,52
Chlorid sodný
7597,20
hydrogenfosforečnan sodnýbezvodý
115,02
Síran zinečnatý x 7H2O
0,14
Ostatní složky
D(+)-glukóza bezvodá
1260,00
Hypoxantin
4,08
DL-α-Lipoová kyselina
0,21
Fenolová červeň
3,00
Putrescin x 2HCl
0,32
Pyruvát sodný
220,00
NaHCO3
2500,00
Thymidine
0,73
Aminokyseliny
L-Alanin
17,82
L-Arginin x HCl
421,40
L-Asparagin x H2O
30,02
Kyselina L-asparagová
26,62
L-cystein x HCl x H2O
70,24
L-Glutamin
292,20
Kyselina L-glutamová
29,42
Glycin
15,01
L-histidin x HCl x H2O
41,92
L-Isoleucin
7,87
L-leucin
26,24
L-Lysin x HCl
73,04
L-methionin
8,95
L-fenylalanin
9,91
L-Prolin
69,06
L-serin
21,02
L-treonin
23,82
L-tryptofan
4,08
L-Tyrosin
10,87
L-Valin
23,42
Vitamíny
D(+)-Biotin
0,07
D-pantothenát vápenatý
0,48
Cholinchlorid
13,96
Kyselina listová
1,32
myo-Inositol
18,02
Nikotinamid
0,04
Pyridoxin x HCl
0,06
Riboflavin
0,04
Thiamin x HCl
0,34
Vitamin B12
1,36
Fosfátem pufrovaný fyziologický roztok (PBS) je široce používaný pufrovací roztok v biologickém a chemickém výzkumu. Hraje klíčovou roli při udržování rovnováhy pH a osmolarity během různých experimentálních postupů, včetně zpracování tkání a buněčných kultur. Náš roztok PBS je pečlivě sestaven z vysoce čistých složek, aby byla zajištěna stabilita a spolehlivost při každém experimentu. Osmolarita a koncentrace iontů našeho roztoku PBS věrně kopíruje osmolaritu a koncentraci iontů v lidském těle, takže je izotonický a netoxický pro většinu buněk.
Složení našeho roztoku PBS
Náš roztok PBS je směs fosfátových pufrů a fyziologických roztoků ultračisté kvality s upraveným pH. V pracovní koncentraci 1X obsahuje:
8000 mg/l chloridu sodného (NaCl)
200 mg/l chloridu draselného (KCl)
1150 mg/L bezvodý fosforečnan sodný dvoubazický (Na2HPO4)
200 mg/L Fosforečnan draselný jednobazický bezvodý (KH2PO4)
Toto složení zajišťuje optimální pH a iontovou rovnováhu vhodnou pro širokou škálu biologických aplikací.
Aplikace našeho roztoku PBS
Náš roztok PBS je ideální pro různé aplikace v biologickém výzkumu. Díky svým izotonickým a netoxickým vlastnostem je vhodný pro ředění látek a oplachování buněčných nádob. Roztoky PBS s obsahem EDTA jsou účinné pro uvolnění připojených a shlukovaných buněk. Do PBS by se však neměly přidávat dvojmocné kovy, jako je zinek, protože mohou způsobit srážení. V takových případech se doporučují Goodovy pufry. Kromě toho je náš roztok PBS přijatelnou alternativou virového transportního média pro transport a skladování RNA virů, včetně SARS-CoV-2.
Kontrola kvality
Sterilně filtrované
Skladování a doba použitelnosti
Skladujte při teplotě +2 °C až +25 °C, chráněné před světlem.
Po otevření skladujte při teplotě 2 °C až 25 °C a spotřebujte do 24 měsíců.
Přepravní podmínky
Okolní teplota
Údržba
Uchovávejte v chladu při teplotě +2°C až +8°C v temnu. Vyhněte se zmrazování a častému zahřívání na +37 °C, protože to snižuje kvalitu výrobku.
Nezahřívejte médium na teplotu vyšší než 37 °C a nepoužívejte nekontrolované zdroje tepla, jako jsou mikrovlnné spotřebiče.
Pokud má být použita pouze část média, odeberte požadované množství a před použitím jej zahřejte na pokojovou teplotu.
Složení
Kategorie
Složky
Koncentrace (mg/l)
Soli
Chlorid draselný
200
Fosforečnan draselný monobazický bezvodý
200
Chlorid sodný
8000
Fosforečnan sodný dvoubazický bezvodý
1150
Médium RPMI 1640, původně určené k podpoře růstu lidských leukemických buněk v suspenzních i monovrstvých kulturách, se díky úpravám výzkumníků a komerčních dodavatelů vyvinulo tak, aby bylo vhodné pro nejrůznější savčí buňky. Je mimořádně kompatibilní s buněčnými liniemi, jako jsou HeLa, Jurkat, MCF-7, PC12, PBMC, astrocyty a karcinomy.
Médium RPMI 1640 se od ostatních médií pro kultivaci buněk odlišuje svým jedinečným složením. Obsahuje značné množství fosfátů, aminokyselin a vitaminů. Zejména obsahuje biotin, vitamin B12 a PABA, které se v Eagle's Minimal Essential Medium nebo Dulbecco's Modified Eagle Medium nevyskytují. Kromě toho médium RPMI 1640 vykazuje výrazně zvýšené koncentrace vitaminů inositolu a cholinu. Neobsahuje však bílkoviny, lipidy ani růstové faktory. V důsledku toho je běžně vyžadováno doplnění 10% fetálního hovězího séra (FBS), aby byly zajištěny optimální podmínky pro růst buněk.
Pufrovací systém média RPMI 1640 je založen na hydrogenuhličitanu sodném a k udržení fyziologicky vhodného pH vyžaduje prostředí s 5-10 % CO2. Začlenění redukčního činidla glutathionu dále odlišuje toto médium od ostatních.
Kontrola kvality
Sterilně filtrované
Skladování a trvanlivost
Skladujte při teplotě +2 °C až +8 °C, chraňte před světlem.
Po otevření skladujte při 4 °C a spotřebujte do 6-8 týdnů.
Přepravní podmínky
Okolní teplota
Údržba
Uchovávejte v chladu při teplotě +2°C až +8°C v temnu. Vyhněte se zmrazování a častému zahřívání na +37 °C, protože to snižuje kvalitu výrobku.
Nezahřívejte médium na teplotu vyšší než 37 °C a nepoužívejte nekontrolované zdroje tepla, jako jsou mikrovlnné spotřebiče.
Pokud má být použita pouze část média, odeberte požadované množství a před použitím jej zahřejte na pokojovou teplotu.
Složení
Kategorie
Složky
Koncentrace (mg/l)
Aminokyseliny
Glycin
10.00
L-Alanyl-L-Glutamin
434.40
L-arginin
200.00
L-AsparaginH2O
56.82
Kyselina L-asparagová
20.00
L-Cystin 2HCl
65.20
Kyselina L-glutamová
20.00
L-histidin HClH2O
20.27
L-Hydroxy-L-Prolin
20.00
L-Isoleucin
50.00
L-leucin
50.00
L-Lysin HCl
40.00
L-methionin
15.00
L-fenylalanin
15.00
L-Prolin
20.00
L-serin
30.00
L-Treonin
20.00
L-tryptofan
5.00
L-Tyrosin 2Na 2H2O
28.83
L-Valin
20.00
Vitamíny
kyselina p-aminobenzoová
1.00
D-biotin
0.20
Cholinchlorid
3.00
D-pantothenát vápenatý
0.25
Kyselina listová
1.00
myo-Inositol
35.00
Nikotinamid
1.00
Pyridoxin HCl
1.00
Riboflavin
0.20
Thiamin HCl
1.00
Vitamin B12
0.005
Anorganické soli
Ca(NO3)2 4H2O
100.00
KCl
400.00
MgSO4 7H2O
100.00
NaCl
6000.00
NaHCO3
2000.00
Na2HPO4
800.00
Ostatní složky
D-glukóza
2000.00
L-Glutathion redukovaný
1.00
Sodná sůl fenolové červeně
5.30
Tato jedinečná formulace kombinuje Dulbecco's Modified Eagle Medium (DMEM) a Ham's F-12 (Ham's Nutrient Mixture F-12) v přesném poměru 1:1. Přidání L-glutaminu dále vylepšuje jeho složení.
DMEM, odvozené od Eagle's Minimal Essential Medium (EMEM), nabízí ve srovnání se svým předchůdcem zvýšenou koncentraci aminokyselin a vitamínů. Naproti tomu Ham's F-12 je založeno na médiu Ham's F-10 a poskytuje doplňkovou sadu esenciálních složek.
Pro podporu optimálního růstu buněk je běžnou praxí doplňovat DMEM:Ham's F12 o FBS v typické koncentraci 5–10 %. Tento přídavek je nezbytný, protože médiu chybí růstové hormony, lipidy a proteiny, které jsou pro buněčný vývoj zásadní.
DMEM:Ham's F12 obsahuje pH pufrovací systém a je často doplňováno fenolovou červení, indikátorem pH. Kultivované buňky v DMEM:Ham's F12 nebo v jakémkoli médiu využívajícím bikarbonátový pufrovací systém vyžadují kontrolované prostředí s obsahem CO2 5–10 % k udržení vhodné hladiny pH.
Kontrola kvality
Sterilně filtrováno
Skladování a trvanlivost
Skladujte při teplotě +2 °C až +8 °C, chráněno před světlem.
Po otevření skladujte při teplotě 4 °C a spotřebujte do 6–8 týdnů.
Přepravní podmínky
Okolní teplota
Skladování
Skladujte v chladu při teplotě +2 °C až +8 °C v temnu. Vyhněte se zmrazení a častému ohřívání na +37 °C, protože to snižuje kvalitu produktu.
Nezahřívejte médium nad 37 °C ani nepoužívejte nekontrolované zdroje tepla, jako jsou mikrovlnné trouby.
Pokud se má použít pouze část média, odeberte potřebné množství a před použitím jej ohřejte na pokojovou teplotu.
Složení
Kategorie
Složky
Koncentrace (mg/l)
Aminokyseliny
Glycin
18,75
L-alanin
4,45
L-arginin HCl
147,50
L-asparagin H₂O
7,50
Kyselina L-asparagová
6,65
L-cystein HCl H₂O
17,56
L-cystin 2 HCl
31,29
Kyselina L-glutamová
7,35
L-glutamin
365,00
L-histidin HCl H₂O
31,48
L-isoleucin
54,47
L-leucin
59,05
L-lysin HCl
91,25
L-metionin
17,24
L-fenylalanin
35,48
L-prolin
17,25
L-serin
26,25
L-threonin
53,45
L-tryptofan
9,02
L-tyrosin 2 Na 2 H2O
55,79
L-valin
52,85
Vitamíny
D-biotin
0,0035
Cholin chlorid
8,98
D-pantothenát vápenatý
2,24
Kyselina listová
2,66
myo-inositol
12,60
Nikotinamid
2,02
Pyridoxin HCl
0,031
Pyridoxal HCl
2,00
Riboflavin
0,219
Thiamin HCl
2,17
Vitamin B12
0,68
Anorganické soli
CaCl2 2 H2O
154,50
CuSO4 5 H2O
0,0013
Fe(NO₃)₃·9H₂O
0,05
FeSO4 7 H2O
0,417
KCl
311,80
MgCl2 6 H2O
61,20
MgSO4 7 H2O
100,00
NaCl
6996,00
NaHCO3
1200,00
Na₂HPO₄
71,02
NaH2PO4 2 H2O
70,87
ZnSO4 7 H2O
0,432
Ostatní složky
D-glukóza
3151,00
Hypoxantin
2,40
HEPES
3574,50
Kyselina linolová
0,042
Kyselina lipoová
0,105
Fenolová červená, sodná sůl
8,63
Putrescin 2 HCl
0,081
Pyruvát sodný
55,00
Thymidin
0,365
- 0,02 při 20-25 °C. Každá šarže byla testována na sterilitu a nepřítomnost mykoplazmat a bakterií. Skladování Skladujte v chladu při teplotě +2 °C až +8 °C v temnu. Zmrazení a ohřátí na +37 °C snižuje kvalitu produktu. Neohřívejte médium na více než 37 °C a nepoužívejte nekontrolovatelné zdroje tepla (např. mikrovlnné trouby). Pokud má být použita pouze část média, odeberte toto množství z lahve a ohřejte jej na pokojovou teplotu. Skladovatelnost všech médií s výjimkou základního média je 6 až 8 týdnů od data otevření. Složení Složky mg/l Anorganické soliChlorid vápenatý x 2H2O132,00 Síran hořečnatý97,67 Chlorid draselný400 Chlorid sodný6 460,00 Hydrogenfosforečnan sodný (bezvodý)504,00 Ostatní složkyD(+)-glukóza (bezvodá)3 000 Glutathion (redukovaný)0 Masový pepton600 Fenolová červená sodná sůl11 AminokyselinyL-alanin13,3 L-arginin x HCl42,14 L-asparagin x H2O45,03 Kyselina L-asparagová19,97 L-cystein x HCl x H2O31,75 L-glutamin (stabilní)219,15 Kyselina L-glutamová22,07 Glycin7,5 L-histidin x HCl x H2O20,96 L-hydroxyprolin19,67 L-isoleucin39,36 L-leucin39,36 L-lysin x HCl36,54 L-methionin14,92 L-fenylalanin16,52 L-prolin17,27 L-serin26,28 L-threonin17,87 L-tryptofan3,06 L-tyrosin disodná sůl26,1 L-valin17,57 VitamínyKyselina p-aminobenzoová1 Kyselina askorbová0,56 D(+)-biotin0 D-pantothenát vápenatý0 Cholin chlorid5 Kyselina listová10 myo-inositol36 Nikotinamid0 Kyselina nikotinová0 Pyridoxal HCl0,5 Pyridoxin HCl0,5 Riboflavin0,2 Thiamin HCl0 Vitamin B122,0
Médium 199 nabízí celou řadu aplikací v této oblasti. Dokáže účinně udržovat komplex kumulus-oocyt (COC) a podporovat in vitro zrání oocytů. Kromě toho se používá při oplachování aspiračních linií během odběru vajíček od německých holštýnských krav. Medium 199 navíc slouží jako vynikající médium pro kultivaci srdečních endoteliálních buněk získaných z potkanů. Tyto aplikace ukazují univerzálnost a přizpůsobivost média 199 různým experimentálním potřebám.
Historie
Vývoj média 199 v 50. letech 20. století znamenal významný pokrok v oblasti médií pro tkáňové kultury. Před jeho zavedením se mnoho kultivačních médií opíralo o produkty živočišného původu a tkáňové extrakty. Morgan a jeho kolegové však způsobili revoluci v této oblasti tím, že vytvořili zcela definovaný zdroj živin pro buněčné kultury. Svými pokusy s různými kombinacemi vitaminů, aminokyselin a dalších faktorů objevili výjimečné vlastnosti média 199 podporující růst.
Kontrola kvality
pH = 7,2 +/
- 0,02 při 20-25 °C.
Každá šarže byla testována na sterilitu a nepřítomnost mykoplazmy a bakterií.
Údržba
Uchovávejte v chladu při teplotě +2 °C až +8 °C ve tmě. Zmrazování a zahřívání až do +37 °C snižuje kvalitu přípravku na minimum.
Nezahřívejte médium na teplotu vyšší než 37° C a nepoužívejte nekontrolovatelné zdroje tepla (např. mikrovlnné přístroje).
Pokud má být použita pouze část média, odeberte toto množství z lahvičky a zahřejte jej při pokojové teplotě.
Doba použitelnosti jakéhokoli média s výjimkou základního média je 8 týdnů od data výroby.
Složení
Složení
mg/l
Anorganické soli
Chlorid vápenatý x 2H2O
264,92
Dusičnan železitý (III) x 9H2O
0,72
Síran hořečnatý
97,67
Chlorid draselný
400,00
Octan sodný x 3H2O
82,95
Chlorid sodný
6,800.00
Dihydrogenfosforečnan sodný x H2O
140,00
Ostatní složky
Adenin sulfát
10,00
AMP
0,20
ATP
1,00
Cholesterol
0,20
2'-Deoxyribóza
0,50
D(+)-glukóza bezvodá
1,000.00
Glutathion (červený)
0,05
Guanin x HCl
0,30
Hypoxantin
0,30
Fenolová červeň
10,00
D-ribóza
0,50
Thymin
0,30
Tween 80
4,90
Uracil
0,30
Xanthin
0,30
NaHCO3
2,200.00
Aminokyseliny
L-Alanin
25,00
L-Arginin x HCl
70,00
Kyselina L-asparagová
30,00
L-Cystein x HCl x H2O
0,10
L-Cystin
20,00
L-Glutamin stabilní
149,00
Kyselina L-glutamová
67,00
Glycin
50,00
L-histidin x HCl x H2O
21,88
L-hydroxyprolin
10,00
L-Isoleucin
20,00
L-leucin
60,00
L-Lysin x HCl
70,00
L-methionin
15,00
L-fenylalanin
25,00
L-Prolin
40,00
L-serin
25,00
L-Treonin
30,00
L-tryptofan
10,00
L-Tyrosin
40,00
L-Valin
25,00
Vitamíny
kyselina 4-amino-benzoová
0,05
Kyselina askorbová
0,05
D(+)-Biotin
0,01
Kalciferol
0,10
D-pantothenát vápenatý
0,01
Cholinchlorid
0,50
Kyselina listová
0,01
myo-Inositol
0,05
Menadion
0,01
Kyselina nikotinová
0.025
Nikotinamid
0.025
Pyridoxal x HCl
0.025
Pyridoxol x HCl
0.025
Riboflavin
0,01
DL-α-tokoferolfosforečnan disodná sůl
0,01
Thiamin x HCl
0,01
Vitamín A acetát
0,14
IMDM je vhodný pro rychle se množící buněčné kultury s vysokou hustotou, včetně buněk Jurkat, COS-7 a makrofágů. Různé modifikace IMDM, které jsou k dispozici pro celou řadu aplikací buněčných kultur, naleznete pomocí nástroje pro výběr médií. Kapalná média poskytují základní živiny pro všechny aplikace buněčných kultur. Každé z našich vysoce kvalitních médií pro buněčné kultury je vyráběno podle původně zveřejněného vzorce nebo modifikací nezbytných pro konzistentní výkon a stabilitu kultivačního média.
IMDM vs. DMEM
IMDM obsahuje dusičnan draselný místo dusičnanu železitého a HEPES a pyruvát sodný. Díky dalším složkám v IMDM je vhodnější pro specializované typy buněk a specifické aplikace než DMEM.
IMDM vs. RPMI
IMDM a RPMI mají odlišné složení, které může být důležité pro stimulaci PMA/ionomycinem. Jedním z významných rozdílů je koncentrace Ca2+. Zatímco RPMI obsahuje 0,42 mM Ca2+, IMDM obsahuje 1,49 mM.
Kontrola kvality
pH = 7,2 +/
- 0,02 při 20-25 °C.
Každá šarže byla testována na sterilitu a nepřítomnost mykoplazmy a bakterií.
Údržba
Uchovávejte v chladu při teplotě +2 °C až +8 °C ve tmě. Zmrazování a zahřívání až do +37 °C snižuje kvalitu přípravku na minimum.
Nezahřívejte médium na teplotu vyšší než 37° C a nepoužívejte nekontrolovatelné zdroje tepla (např. mikrovlnné přístroje).
Pokud má být použita pouze část média, odeberte toto množství z lahvičky a zahřejte jej při pokojové teplotě.
Doba použitelnosti jakéhokoli média s výjimkou základního média je 8 týdnů od data výroby.
Složení
Složení
mg/l
Anorganické soli
Chlorid vápenatý x 2 H2O
219,00
Chlorid draselný
330,00
Dusičnan draselný
0.076
Síran hořečnatý bezvodý
97,73
Chlorid sodný
4,505.00
Dihydrogenfosforečnan sodný bezvodý
109,00
Seleničitan sodný
0,02
Ostatní složky
D(+)-glukosa bezvodá
4,500.00
HEPES
5,958.00
Pyruvát sodný
110,00
Fenolová červeň
15,00
Aminokyseliny
L-Alanin
25,00
L-Arginin x HCl
84,00
L-Asparagin x H2O
25,00
Kyselina L-asparagová
30,00
L-Cystin x 2HCl
91,24
L-Glutamin
584,00
Kyselina L-glutamová
75,00
Glycin
30,00
L-histidin x HCl x H2O
42,00
L-Isoleucin
104,80
L-leucin
104,80
L-Lysin x HCl
146,20
L-methionin
30,00
L-fenylalanin
66,00
L-Prolin
40,00
L-serin
42,00
L-Treonin
95,20
L-tryptofan
16,00
L-Tyrosin x 2Na
104,20
L-Valin
93,60
Vitamíny
D(+)-Biotin
0.013
D-pantothenát vápenatý
4,00
Cholinchlorid
4,00
Kyselina listová
4,00
myo-Inositol
7,20
Média pro buněčné kultury: Přehled
V oblasti věd o živé přírodě je jednou z nejdůležitějších metodik pěstování buněk. Pod pojmem "buněčná kultura" se rozumí odebrání buněk, tkání nebo orgánů ze zvířete nebo rostliny a následná implantace těchto buněk, tkání nebo orgánů do umělého prostředí, které je příznivé pro jejich přežití a/nebo růst Základními potřebami prostředí pro optimální vývoj buněk jsou řízená teplota, substrát pro uchycení buněk, vhodné růstové médium a inkubátor, který udržuje optimální pH a osmolalitu. Buňky musí mít tyto podmínky zajištěny, aby mohly plně rozvinout svůj potenciál.
Výběr vhodného růstového média pro kultivaci in vitro je fází kultivace buněk, která je nejkritičtější a zároveň nejdůležitější. Růstové médium, známé také jako kultivační médium, je kapalina nebo gel, jehož složení podporuje vývoj organismů v mikroskopickém, buněčném nebo rostlinném měřítku. Médium používané ke kultivaci buněk často obsahuje dostatečný přísun energie a látek, které řídí buněčný cyklus. Mezi hlavní složky kultivačního média patří aminokyseliny, vitaminy, anorganické soli, glukóza a sérum. Sérum se do média přidává, protože funguje jako zdroj růstových faktorů, hormonů a faktorů vazby. Kromě poskytování živin přispívá médium také k udržování hladiny pH a osmolality.
Typy médií používaných v buněčných kulturách
Lidské i živočišné buňky lze pěstovat buď v umělém nebo syntetickém médiu, nebo ve zcela přírodním médiu, které je doplněno přírodními prvky. V následujícím textu vám poskytneme přehled různých typů v současnosti dostupných médií.
Přírodní média
V přírodních médiích se mohou nacházet pouze biologické tekutiny, které existují ve svém přirozeném stavu. Přírodní média jsou velmi užitečná a snadná pro kultivaci široké škály typů živočišných buněk. Nedostatečná znalost přesných složek, které tvoří přírodní média, je hlavním faktorem, který přispívá k nízké opakovatelnosti výsledků získaných pomocí přírodních médií.
Umělá média
Příprava umělých nebo syntetických médií zahrnuje přídavek živin (organických i anorganických), sérových bílkovin, sacharidů, kofaktorů, vitaminů a solí, jakož i plynných fází O2 a CO2 [1].
Byly vyvinuty různé typy umělých médií, aby plnily jednu nebo více z následujících funkcí: 1) Okamžité přežití (vyvážený roztok soli s přesným pH a osmotickým tlakem). 2) Prodloužené přežití (vyvážený roztok soli doplněný o různé formulace organických chemických látek a/nebo sérum). 3) Časově neomezený vývoj. 4) Specializované funkce.
Existují čtyři odlišné klasifikace umělých médií:
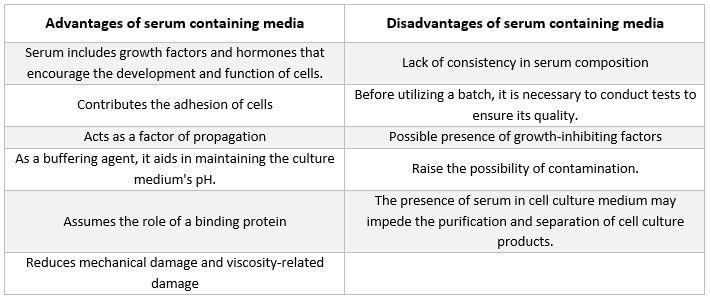
Média obsahující sérum
Nejčastějším druhem doplňku, který se vyskytuje v médiích používaných pro pěstování živočišných buněk, je fetální hovězí sérum. Přidává se do kultivačního média jako levný doplněk, aby se dosáhlo co nejlepších podmínek růstu. Kromě toho, že sérum funguje jako transportér nebo chelátor pro živiny, které jsou nestabilní nebo nerozpustné ve vodě, hormony a růstové faktory, inhibitory proteáz a další látky, váže a neutralizuje také škodlivé molekuly.
Médium bez séra
Přítomnost séra v médiu má řadu nevýhod a může způsobit velké chyby v interpretaci při imunologickém výzkumu [2, 3]. Byla vytvořena řada různých bezsérových médií [4, 5]. Tato média jsou většinou speciálně vytvořena pro podporu kultivace jednoho typu buněk, například Knockout Serum Replacement a Knockout DMEM od společnosti Thermo Fisher Scientific a mTESR médium od Stem Cell Technologies [6] pro kmenové buňky [7].
Tato média navíc obsahují definovaná množství purifikovaných růstových faktorů, lipoproteinů a dalších proteinů, které jinak obvykle dodává sérum [8]. Tato média se často označují jako "definovaná kultivační média", protože složky, které tato média tvoří, jsou dobře známy.
Chemicky definovaná média
Tato média obsahují ultračisté anorganické a organické složky, které nebyly kontaminovány žádným druhem znečištění. Mohou také obsahovat přídavky čistých bílkovin, jako jsou růstové faktory.
genetická modifikace bakterií nebo kvasinek spolu s přídavkem určitých mastných kyselin, vitaminů, cholesterolu a aminokyselin vede k výrobě jejich složek [9].
Bezbílkovinná média
Bezbílkovinná média jsou taková, která neobsahují vůbec žádné bílkoviny a místo toho obsahují pouze nebílkovinné prvky. Ve srovnání s médii s přidaným sérem podporuje použití médií bez přidaných bílkovin větší proliferaci buněk a expresi bílkovin a usnadňuje čištění jakéhokoli produktu vzniklého v následném procesu [10-12]. Ve složeních, jako jsou MEM a RPMI-1640, nejsou bílkoviny obsaženy. V případě potřeby je však možné bílkovinný doplněk podávat.
Kultivační média a jejich základní složky
Komerční kultivační médium lze zakoupit jako prášek nebo tekutinu a často obsahuje různé živiny, jako jsou aminokyseliny, glukóza, soli, vitaminy a další doplňky stravy.
Potřeby těchto složek jsou pro každou buněčnou linii jiné a tyto rozdíly jsou příčinou velkého množství různých složení médií. Každá složka je zodpovědná za určitou funkci, která bude nastíněna v následujících odstavcích:
Pufrovací systémy
Pro udržení optimálních podmínek pěstování je třeba kontrolovat pH, což se často provádí jedním ze dvou pufrovacích systémů:
Přírodní pufrovací systém
Poměr CO2/H2CO3 v atmosféře je stejný jako v médiu, což vytváří přirozený pufrovací mechanismus. Aby se zachoval jejich přirozený pufrovací mechanismus, musí být kultury udržovány ve vzdušném prostředí s 5-10 % CO2, čehož se často dosahuje použitím inkubátoru s CO2. Jednou z nejlepších věcí na používání přirozeného pufru je to, jak je levný a bezpečný.
HEPES
Chemické pufrování pomocí zwitterionu HEPES má větší pufrovací schopnost v rozmezí pH 7,2-7,4 a nepotřebuje regulované plynné prostředí. Pro určité typy buněk může být větší dávka HEPES škodlivá. Média obsahující HEPES jsou rovněž mnohem náchylnější k fototoxickým účinkům fluorescenčního světla [13].
Fenolová červeň
Indikátor pH fenolová červeň je často součástí komerčně dostupného kultivačního média, což umožňuje průběžné sledování pH. Rozšířením buněk způsobují metabolity produkované těmito buňkami změnu pH, a tím i změnu barvy média. Fenolová červeň má dvojí účinek na barvu média, při kyselém pH se zbarvuje do žluta a při zásaditém pH do fialova. pH 7,4, což je optimální hodnota pro buněčné kultury, způsobuje, že se médium jeví jako fluorescenční červená.
Fenolová červeň má však několik nevýhod: Za prvé, fenolová červeň dokáže simulovat působení řady steroidních hormonů, především estrogenu [14]. Proto se při studiu buněk citlivých na estrogeny, jako je prsní tkáň, doporučuje médium bez fenolové červeně. Rovnováha sodíku a draslíku je narušena přítomností fenolové červeně v několika přípravcích bez séra. Přidání séra nebo hovězího hypofyzárního hormonu do média může tento účinek potlačit [15]. Za třetí, přítomnost fenolové červeně brání detekci při průtokových cytometrických experimentech.
Anorganické soli
Média obsahující anorganické soli, jako jsou sodné, draselné a vápenaté ionty, pomáhají udržovat osmotickou rovnováhu a regulovat membránový potenciál.
Aminokyseliny
Protože aminokyseliny jsou základními složkami bílkovin, jsou nezbytnou součástí všech buněčných růstových médií, která kdy byla vynalezena. Protože buňky nejsou schopny samy produkovat určité aminokyseliny, je důležité, aby kultivační médium obsahovalo esenciální aminokyseliny. Jsou nezbytné pro množení buněk a jejich koncentrace určuje maximální hustotu buněk, které lze dosáhnout. Zejména L-glutamin, esenciální aminokyselina, je obzvláště důležitý.
L-glutamin funguje jako sekundární zdroj energie pro metabolismus a přispívá dusíkem k produkci NAD, NADPH a nukleotidů. Vzhledem k tomu, že L-glutamin je nestabilní aminokyselina, která se časem mění na formu, kterou buňky nejsou schopny využít, musí být podáván do média.
Kromě toho mohou být do média dodávány neesenciální aminokyseliny, aby se doplnily ty, které byly v průběhu růstu spotřebovány. Růst buněk se podpoří a jejich životaschopnost se zvýší, když se do růstového média přidají neesenciální aminokyseliny.
Sacharidy
Sacharidy ve formě cukrů jsou hlavním zdrojem energie. Mnohá média obsahují kromě běžnějších cukrů glukózy a galaktózy také maltózu a fruktózu.
Bílkoviny a peptidy
Nejčastěji používanými proteiny a peptidy jsou albumin, transferin a fibronektin. Jsou významné zejména v médiích, která neobsahují sérum. Albumin, transferin, aprotinin, fetuin a fibronektin jsou některé z proteinů, které se mohou nacházet v séru, které je bohatou zásobou bílkovin.
Albumin je základní bílkovinou, která se nachází v krvi, a jeho funkcí je vázat a přenášet různé látky, včetně vody, solí, volných mastných kyselin, hormonů a vitaminů, mezi různými orgány a buňkami. Schopnost albuminu vázat chemické látky z něj činí účinného kandidáta na odstranění škodlivých sloučenin z média, v němž jsou kultivovány buňky.
Aprotinin je ochranným prostředkem v systémech buněčných kultur, protože je stabilní při neutrálním i kyselém pH a také odolný vůči vysokým teplotám a destrukci, kterou mohou způsobit proteolytické enzymy. Je schopen inhibovat řadu serinových proteáz, mimo jiné včetně trypsinu.
Fetuin je glykoprotein, který může být detekován ve větším množství v séru plodu a novorozenců ve srovnání se sérem dospělých zvířat. Kromě toho působí jako inhibitor serinových proteáz. Protein fibronektin je základní složkou v procesu buněčné adheze. Transferin je bílkovina, která přenáší železo a je zodpovědná za dodávání železa do membrán buněk.
Mastné kyseliny a lipidy
Hrají klíčovou roli v bezsérovém médiu, když sérum chybí.
Vitamíny
Řada vitaminů je nezbytná pro vývoj a proliferaci buněk. Vitaminy si buňky nemohou v dostatečném množství vyrobit, a proto jsou v tkáňových kulturách nezbytné jako doplňky stravy.
V buněčných kulturách je primárním zdrojem vitaminů sérum; média se však také upravují různými vitaminy, aby byla vhodná pro určitý typ buněk. Nejčastěji se pro stimulaci růstu používají vitaminy skupiny B.
Stopové prvky
Chemické prvky, jako je měď, zinek, selen a meziprodukty trikarboxylových kyselin, se označují jako stopové prvky. Stopové prvky se často přidávají do médií, která neobsahují sérum, aby nahradily ty, které jsou obvykle přítomny v séru. Tyto prvky jsou důležitými chemickými složkami, které jsou nezbytné pro zdravý vývoj buněk. Mnoho biochemických reakcí závisí na určitých mikroživinách, například aktivita enzymů.
Doplňky média
Plnohodnotné růstové médium navržené pro určité buněčné linie potřebuje další složky, které v základním médiu a séru chybí. Tyto doplňky stravy podporují růst buněk a odpovídající metabolické funkce.
Ačkoli jsou hormony, růstové faktory a signální molekuly nezbytné pro odpovídající proliferaci konkrétních buněčných linií, je třeba vždy dodržovat následující opatření: Vzhledem k tomu, že přidání doplňků může změnit osmolalitu kompletního růstového média, což může inhibovat vývoj buněk, doporučuje se po přidání doplňků vždy ověřit osmolalitu. Pro většinu buněčných linií se optimální osmolalita pohybuje mezi 260 a 320 mOSM/kg.
Antibiotika
Antibiotika se často používají k potlačení rozvoje bakteriálních a plísňových škodlivin [16], ačkoli pro růst buněk nejsou nezbytná. Protože antibiotika mohou skrývat kontaminaci mykoplasmaty a rezistentními bakteriemi, jejich rutinní používání se pro buněčné kultury nedoporučuje [17, 18].
Kromě toho mohou antibiotika narušit metabolismus hypersenzitivních buněk. Často se používají kombinace penicilinu a treptomycinu vyráběné společnostmi MilliporeSigma a Life Technologies. Plasmocin byl využit při kultivaci gliomových buněčných linií TS603, TS516 a BT260 [19] a ukázalo se, že je účinný při odstraňování kontaminace mykoplazmaty [20].
Sérum
V séru jsou přítomny albuminy, růstové faktory a inhibitory růstu. Sérum je jednou z nejvýznamnějších složek média pro buněčné kultury, protože poskytuje aminokyseliny, bílkoviny, vitaminy (zejména vitaminy rozpustné v tucích, jako jsou A, D, E a K), sacharidy, lipidy, hormony, růstové faktory, minerály a stopové prvky.
K podpoře vývoje kultivovaných buněk se často používá sérum z fetálních a telecích hovězích zdrojů. Fetální sérum je bohatou zásobou růstových faktorů a je vhodné pro klonování buněk a vývoj citlivých buněk. Telecí sérum se vzhledem ke svým sníženým schopnostem podporovat růst používá při pokusech s kontaktní inhibicí. Normální růstová média často obsahují 2 % až 10 % séra. Přídavek séra do kultivačního média slouží k následujícím účelům [21]:
-
Sérum dodává buňkám základní živiny (v roztoku i navázané na proteiny).
-
Sérum obsahuje několik růstových faktorů a hormonů, které se podílejí na podpoře růstu a specializované činnosti buněk.
-
Nabízí mnoho vazebných proteinů, jako je albumin a transferin, které transportují další chemické látky do buňky. Například albumin dopravuje do buněk tuky, vitaminy, hormony atd.
-
Poskytuje také bílkoviny, jako je fibronektin, které zvyšují přilnavost buněk k podkladu. Kromě toho produkuje roztírací elementy, které napomáhají expanzi buněk před dělením.
-
Dodává inhibitory proteáz, které zabraňují proteolýze v buňkách.
-
Obsahuje také minerální látky, jako jsou Na+, K+, Zn2+ a Fe2+.
-
Zvyšuje viskozitu média, takže chrání buňky před mechanickým poškozením při míchání suspenzní kultury.
-
Je to také pufr.
Odkazy
[1] Morgan J, Morton H, Parker R. Nutrition of animal cells in tissue culture; initial studies on a synthetic medium (Výživa živočišných buněk v tkáňových kulturách; první studie syntetického média). Proc Soc Exp Biol Med. 1950;73:1-8
[2] Kerbel R, Blakeslee D. Rapid adsorption of a foetal calf serum component by mammalian cells in culture (Rychlá adsorpce složky fetálního telecího séra savčími buňkami v kultuře). Potenciální zdroj artefaktů ve studiích antisér proti buněčně specifickým antigenům. Immunology. 1976;31:881-91
[3] Sula K, Draber P, Nouza K. Přídavek séra do média používaného pro přípravu buněčných suspenzí jako možný zdroj artefaktů při studiu buněčných reakcí pomocí testu na podkolenní lymfatické uzlině. J Immunogenet. 1980;7:483-9
[4] Mariani E, Mariani A, Monaco M, Lalli E, Vitale M, Facchini A. Komerční média bez séra: růst hybridomů a produkce monoklonálních protilátek. J Immunol Methods. 1991;145:175-83
[5] Barnes D, Sato G. Methods for growth of cultured cells in serum-free medium (Metody růstu kultivovaných buněk v bezsérovém médiu). Anal Biochem. 1980;102:255-70
[6] Yu H, Lu S, Gasior K, Singh D, Vazquez Sanchez S, Tapia O,et al. HSP70 chaperones RNA-free TDP-43 into anisotropic intranuclear liquid spherical shells. Science. 2021;371:
[7] Meharena H, Marco A, Dileep V, Lockshin E, Akatsu G, Mullahoo J,et al. Down-syndromem indukovaná senescence narušuje jadernou architekturu neurálních progenitorů. Cell Stem Cell. 2022;29:116-130.e7
[8] Iscove N, Melchers F. Úplná náhrada séra albuminem, transferinem a sójovým lipidem v kulturách lipopolysacharid-reaktivních B lymfocytů. J Exp Med. 1978;147:923-33
[9] Stoll T, Muhlethaler K, von Stockar U, Marison I. Systematic improvement of a chemically-defined protein-free medium for hybridoma growth and monoclonal antibody production. J Biotechnol. 1996;45:111-23
[10] Darfler F. A protein-free medium for the growth of hybridomas and other cells of the immune system (Bezproteinové médium pro růst hybridomů a dalších buněk imunitního systému). In Vitro Cell Dev Biol. 1990;26:769-78
[11] Barnes D, Sato G. Bezsérové buněčné kultury: sjednocující přístup. Cell. 1980;22:649-55
[12] Hamilton W, Ham R. Clonal growth of chinese hamster cell lines in protein-free media (Klonální růst buněčných linií čínského křečka v bezproteinových médiích). In Vitro. 1977;13:537-47
[13] Zigler J, Lepe Zuniga J, Vistica B, Gery I. Analysis of the cytotoxic effects of light-exposed HEPES-containing culture medium. In Vitro Cell Dev Biol. 1985;21:282-7
[14] Berthois Y, Katzenellenbogen J, Katzenellenbogen B. Phenol red in tissue culture media is a weak estrogen: implications concerning the study of estrogen-responsive cells in culture. Proc Natl Acad Sci U S A. 1986;83:2496-500
[15] Karmiol S. Vývoj bezsérových médií. In: Master JRW, editor. Animal Cell culture, 3. vyd. Oxford:Oxford University Press; 2000.
16] Perlman D. Use of antibiotics in cell culture media [Použití antibiotik v médiích pro buněčné kultury]. Methods Enzymol. 1979;58:110-6
17] McGarrity G. Spread and control of mycoplasmal infection of cell cultures [Šíření a kontrola mykoplazmové infekce buněčných kultur]. In Vitro. 1976;12:643-8
18] Masters J, Stacey G. Changing medium and passaging cell lines [Změna média a pasážování buněčných linií]. Nat Proto se snažíme. 2007;2:2276-84
[19] Chakraborty A, Laukka T, Myllykoski M, Ringel A, Booker M, Tolstorukov M,et al. Histone demethylase KDM6A directly senses oxygen to control chromatin and cell fate. Science. 2019;363:1217-1222
[20] Molla Kazemiha V, Azari S, Amanzadeh A, Bonakdar S, Shojaei Moghadam M, Habibi Anbouhi M,et al. Efficiency of Plasmocin™ on various mammalian cell lines infected by mollicutes in comparison with commonly used antibiotics in cell culture: a local experience. Cytotechnologie. 2011;63:609-20
[21] Kragh Hansen U. Molekulární aspekty vazby ligandů na sérový albumin. Pharmacol Rev. 1981;33:17-53