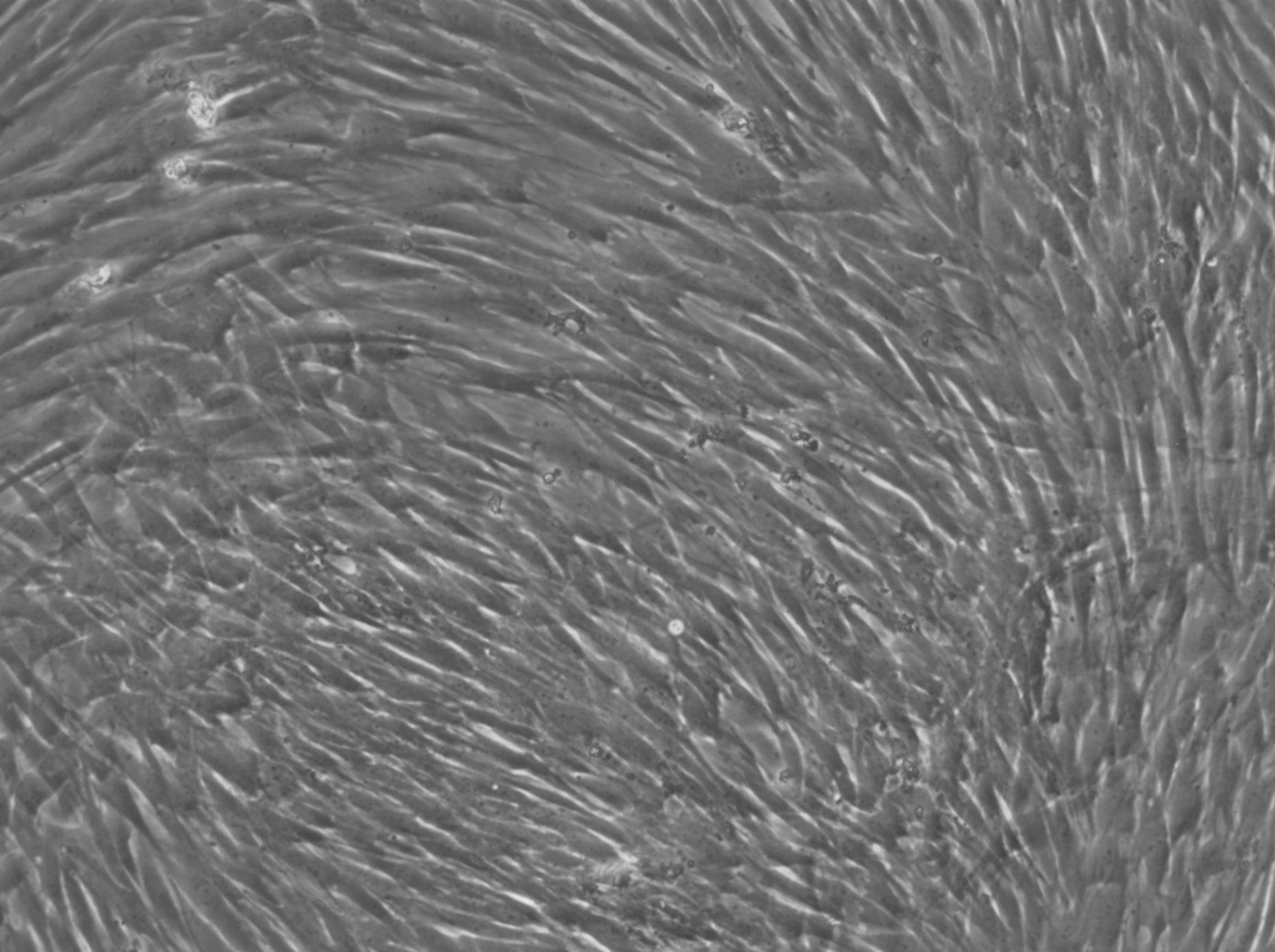
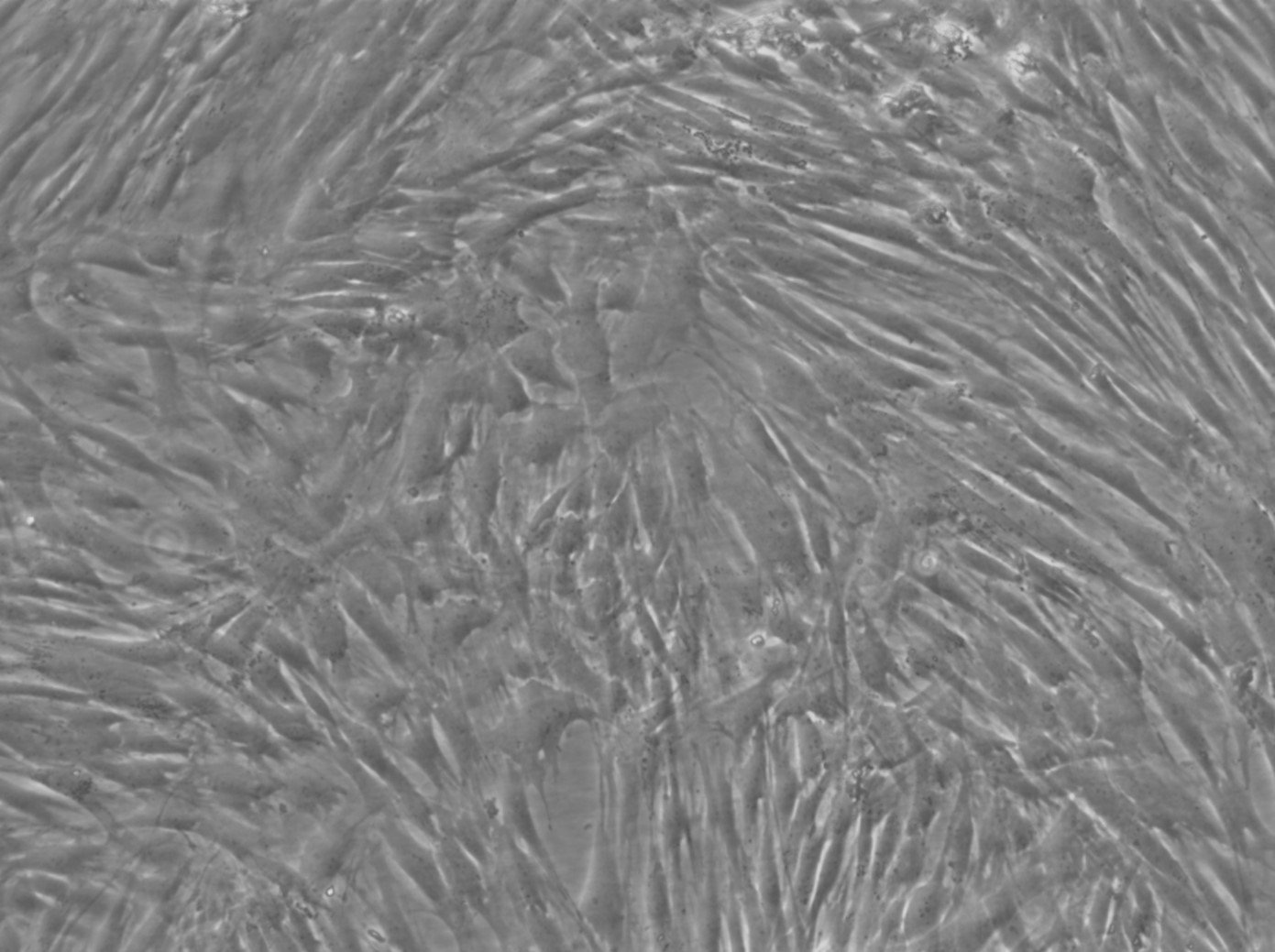
Stamceller från mänsklig tandpulpa (hDPSC) celler






Allmän information
| Beskrivning | Humana stamceller från tandpulpan (DPSC, hDPSC) är multipotenta stamceller som isolerats från tandpulpan i vuxna tänder, vanligen tredje molaren. Dessa celler är särskilt värdefulla inom regenerativ medicin på grund av deras förmåga att differentiera till en mängd olika celltyper, inklusive de som bildar ben, brosk, fett och tandvävnad. DPSC är kända för sin höga proliferativa kapacitet, vilket gör dem till ett robust val för vävnadsteknik och cellbaserade terapeutiska tillämpningar. DPSC har också betydande immunmodulerande egenskaper, vilket bidrar till deras potentiella användning vid behandling av inflammatoriska tillstånd. Utöver regenerering av tandvävnad har de undersökts för sin förmåga att reparera bendefekter och för sin användning inom neurologiska terapier. Deras relativt enkla tillgänglighet och förmåga att bibehålla livskraften efter kryokonservering gör DPSC till ett attraktivt alternativ för klinisk forskning och terapeutisk utveckling, särskilt inom områdena regenerativ tandvård, ortopedi och neurodegenerativa sjukdomar. |
|---|---|
| Organism | Människan |
| Vävnad | Tandvård |
| Tillämpningar | Läkemedelstester, regenerativ medicin, sjukdomsforskning |
Egenskaper
| Egenskaper för tillväxt | Följsam |
|---|
Lagstadgade uppgifter
| Citationstecken | Stamceller från mänsklig tandpulpa (DPSC, hDPSC) (Cytion katalognummer 300702) |
|---|---|
| Biosäkerhetsnivå | 1 |
| NCBI_TaxID | 9606 |
Biomolekylära data
Hantering
| Kulturmedium | Alpha MEM, med: 2,0 mM stabilt glutamin, utan Ribonukleosider, w/o: Deoxyribonukleosider, w: 1,0 mM Natriumpyruvat, w: 2,2 g/L NaHCO3 |
|---|---|
| Kosttillskott | Komplettera mediet med 10% FBS, 2 ng/ml bFGF |
| Dissociationsreagens | Accutase |
| Subkulturering | Ta bort det gamla mediet från de adherenta cellerna och tvätta dem med PBS som saknar kalcium och magnesium. Använd 3-5 ml PBS för T25-kolvar och 5-10 ml för T75-kolvar. Täck sedan cellerna helt med Accutase, använd 1-2 ml för T25-kolvar och 2,5 ml för T75-kolvar. Låt cellerna inkubera i rumstemperatur i 8-10 minuter så att de lossnar. Efter inkubationen, blanda cellerna försiktigt med 10 ml medium för att resuspendera dem och centrifugera sedan vid 300xg i 3 minuter. Kassera supernatanten, resuspendera cellerna i färskt medium och överför dem till nya kolvar som redan innehåller färskt medium. |
| Frys mediet | Som kryokonserveringsmedium använder vi 90% FBS + 10% DMSO för att bibehålla livskraften, eller CM-1 (Cytion katalognummer 800100), som innehåller optimerade osmoprotektanter och metaboliska stabilisatorer för att förbättra återhämtningen och minska kryoinducerad stress. |
| Upptining och odling av celler |
|
| Inkubationsatmosfär | 37°C, 5%CO2, befuktad atmosfär. |
| Ytbeläggning av flaska | För optimal vidhäftning och viabilitet efter upptining rekommenderar vi att kollagenbelagda kolvar eller plattor används. |
| Frysningsprocedur | Kryopreserverade cellinjer skickas på torris i validerade, isolerade förpackningar med tillräckligt med kylmedel för att hålla cirka -78 °C under hela transporten. Vid mottagandet ska behållaren omedelbart inspekteras och flaskorna utan dröjsmål överföras till lämplig förvaring. |
| Leveransvillkor | Kryopreserverade cellinjer skickas på torris i validerade, isolerade förpackningar med tillräckligt med kylmedel för att hålla cirka -78 °C under hela transporten. Vid mottagandet ska behållaren omedelbart inspekteras och flaskorna utan dröjsmål överföras till lämplig förvaring. |
| Förvaringsförhållanden | För långtidsförvaring, placera flaskorna i flytande kväve i ångfas vid ca -150 till -196 °C. Förvaring vid -80 °C är acceptabelt endast som ett kort mellanliggande steg innan överföring till flytande kväve. |
Kvalitetskontroll / Genetisk profil / HLA
| Sterilitet | Mykoplasmakontaminering utesluts med hjälp av både PCR-baserade analyser och luminiscensbaserade metoder för mykoplasmadiagnostik. För att säkerställa att det inte finns någon kontaminering av bakterier, svamp eller jäst utsätts cellkulturerna för dagliga visuella inspektioner. |
|---|
Avtal om materialöverföring
Om du avser att använda Cytions cellinjer enbart för intern forskning på en enda forskningsplats, vänligen fyll i och underteckna vårt materialöverföringsavtal (MTA) och skicka in det tillsammans med din beställning.
För alla kommersiella tillämpningar – inklusive men inte begränsat till tjänster mot ersättning, kvalitetskontroll, produktlansering, diagnostisk användning eller regulatoriska studier – vänligen fyll i formuläret för avsedd användning så att vi kan utarbeta ett avtal som är anpassat till ditt projekt.
Observera: MTA gäller endast för vissa cellinjer. Om detta meddelande och MTA-dokumentet visas på en produktsida är avtalet tillämpligt. För cellinjer som inte omfattas av MTA visas ingen hänvisning till avtalet. MTA gäller inte för kunder i Amerika, Kina eller Taiwan. Kontakta vårt amerikanska företag för att få det lämpliga avtalet.
