HeLa-cellen: Revolutionair onderzoek
Sinds hun ontdekking in 1951 worden Hela cellen, een stam van onsterfelijke cellen vernoemd naar Henrietta Lacks, op grote schaal gebruikt in wetenschappelijk onderzoek. Henrietta Lacks, een 31-jarige Afro-Amerikaanse moeder van vijf kinderen, werd gediagnosticeerd met baarmoederhalskanker in hetzelfde jaar dat ze stierf. George Otto Gey, de directeur van het Tissue Culture Laboratory in het Johns Hopkins Hospital, verzamelde en vermenigvuldigde haar baarmoederhalskankercellen, die uitzonderlijk veerkrachtig en productief bleken, waardoor ze breed konden worden toegepast in wetenschappelijk onderzoek. In tegenstelling tot andere menselijke cellen konden HeLa-cellen in vitro worden onderhouden en vermenigvuldigd, wat een aanzienlijke vooruitgang betekende in het medisch onderzoek.
De geschiedenis en tijdlijn van Hela cellen
Henrietta Lacks, een zwarte tabaksboerin, werd in 1951 naar het Johns Hopkins ziekenhuis gebracht voor abnormale vaginale bloedingen en werd later behandeld voor baarmoederhalskanker. Haar eerste behandeling bestond uit het nemen van weefselmonsters van haar baarmoederhals zonder haar toestemming. De baarmoederhalsbiopsie leverde weefselmonsters op voor het klinisch onderzoek van George Otto Gey, die werden bestudeerd in het weefselkweeklaboratorium. In tegenstelling tot eerdere monsters merkte Gey's laborant op dat de cellen zich elke 20-24 uur verdubbelden en zich snel uitbreidden. Gey vermeerderde de baarmoederhalskankercellen vlak voor de dood van Lacks en zij waren de eerste levensvatbare menselijke in vitro cellijn. De cellen werden vernoemd naar de eerste twee letters van Henrietta Lacks' voor- en achternaam en werden aan elke wetenschapper gegeven die erom vroeg om het onderzoek te bevorderen.
Hoewel de cellen zonder toestemming van Lacks of haar familie werden verzameld, was toestemming in die tijd niet nodig en ook niet gebruikelijk. Er was geen plicht om patiënten of hun familieleden te waarschuwen dat weggegooid of chirurgisch verkregen materiaal eigendom was van de arts of de medische instelling. In de jaren 1970 werd de werkelijke naam van Henrietta openbaar gemaakt door een openbaar lek en werd de familie Lacks om DNA-monsters gevraagd om te helpen bij het identificeren van besmette cellijnen. De HeLa cellijn is afkomstig van een monster van Lacks' baarmoederhalsweefsel en is in celkweek zodanig vermenigvuldigd dat het totale aantal cellen in haar lichaam wordt overschreden. Er zijn verschillende stammen van HeLa-cellen die in celkweken blijven muteren, maar ze stammen allemaal af van de tumorcellen die uit Lacks zijn gehaald.
Historische misstanden aanpakken
Het verhaal rond Henrietta Lacks en het afleiden van HeLa cellen zonder haar medeweten of toestemming heeft een discussie op gang gebracht over de ethiek van medische onderzoekspraktijken en de bescherming van individuele rechten, in het bijzonder met betrekking tot het gebruik van menselijk biologisch materiaal in de wetenschap. Henrietta Lacks werd zonder het te weten de bron van de eerste onsterfelijke menselijke cellijn, die sindsdien tot talloze wetenschappelijke doorbraken heeft geleid. Het besef van deze ethische misstand heeft een verschuiving in de richting van rigoureuzere toestemmingsprocessen en een verhoogd bewustzijn van de morele verplichtingen van onderzoekers teweeggebracht. Deze zaak heeft niet alleen de noodzaak van hervorming van onderzoekspraktijken aan het licht gebracht, maar ook een breder gesprek op gang gebracht over rechtvaardigheid, respect en erkenning in medisch onderzoek, wat heeft geleid tot inspanningen om onrechtvaardigheden uit het verleden recht te zetten en ervoor te zorgen dat degenen die bijdragen aan wetenschappelijke vooruitgang worden erkend en met waardigheid worden behandeld.
Thermo Fisher en HeLa-cellen
De rechtszaak tegen biotechbedrijf Thermo Fisher Scientific in verband met HeLa-cellen was geworteld in een dieper ethisch en juridisch debat over de commercialisering van biologisch materiaal afkomstig van individuen zonder hun toestemming. De zaak draaide om de HeLa-cellijn, die leidde tot belangrijke wetenschappelijke doorbraken, waaronder de ontwikkeling van het poliovaccin en vooruitgang in de behandeling van kanker.
De rechtszaak bracht verschillende ethische overwegingen aan het licht: de rechten van individuen en hun families op hun biologisch materiaal, de historische context van het nemen van monsters van gemarginaliseerde individuen zonder toestemming en de verantwoordelijkheden van bedrijven die profiteren van dergelijk materiaal. De zaak tegen Thermo Fisher Scientific benadrukte de noodzaak van duidelijker beleid en ethische normen met betrekking tot het gebruik van menselijk biologisch materiaal in onderzoek en handel, zodat de rechten van individuen worden gerespecteerd en de voordelen van wetenschappelijke ontdekkingen eerlijk worden verdeeld.
Voor een gedetailleerde verkenning van de oorsprong, juridische gevechten en oplossingen rondom HeLa cellen, bekijk ons artikel"HeLa Cells: Geschiedenis, rechtszaak en schikkingen"
Fascinerende eigenschappen van HeLa-cellen
HeLa-cellen zijn gemakkelijk te kweken en vermenigvuldigen zich snel. Ze staan ook bekend om hun hoge gevoeligheid voor virusinfecties. Ze zijn vooral gevoelig voor het menselijke adenovirus 3, het encefalomyocarditisvirus en het poliovirus 1, 2 en 3. Dit kenmerk maakt HeLa-cellen essentieel voor het bestuderen van deze virale infecties. Deze eigenschap maakt HeLa-cellen essentieel voor het bestuderen van de replicatie, assemblage en pathogenese van deze virussen en voor het ontwikkelen van nieuwe antivirale strategieën. Daarnaast worden HeLa cellen veel gebruikt als transfectiegastheer voor het bestuderen van genfunctie en -regulatie, recombinante eiwitproductie en gentherapie.
- Zelfs voor kankercellen hebben HeLa cellen een abnormaal hoge snelheid van celproliferatie en een onbeperkte levensduur, waardoor ze uitstekend geschikt zijn voor wetenschappelijk onderzoek.
- HeLa-cellen hebben een actieve telomerase-vorm, waardoor eindeloze celdeling en onsterfelijkheid mogelijk zijn.
- HeLa cellen overwinnen de Hayflick limiet, het maximale aantal celdelingen dat de meeste normale cellen kunnen ondergaan voordat ze senescent worden.
- HeLa-cellen hebben een hypertriploïde chromosoomnummer (3n+). Het gemiddelde chromosoomnummer in HeLa cellen is 82, maar kan variëren van 70 tot 164 (in plaats van het standaard diploïde aantal van 46). Deze chromosomen worden "HeLa signatuurchromosomen" genoemd. Helacellen hebben een complex karyotype dat wordt gekenmerkt door een hoge mate van aneuploïdie en structurele herschikkingen. HeLa cellen hebben een klein telocentrisch chromosoom in 98% van de cellen en 100% aneuploïdie in 1385 onderzochte cellen. Deze chromosoomafwijkingen spelen een essentiële rol in de snelle groei en onsterfelijkheid van HeLa-cellen en worden ook in verband gebracht met baarmoederhalskanker.
- Door horizontale genoverdracht van humaan papillomavirus 18 (HPV18) naar menselijke baarmoederhalscellen hebben HeLa-cellen een ander genoom dan Henrietta Lacks.
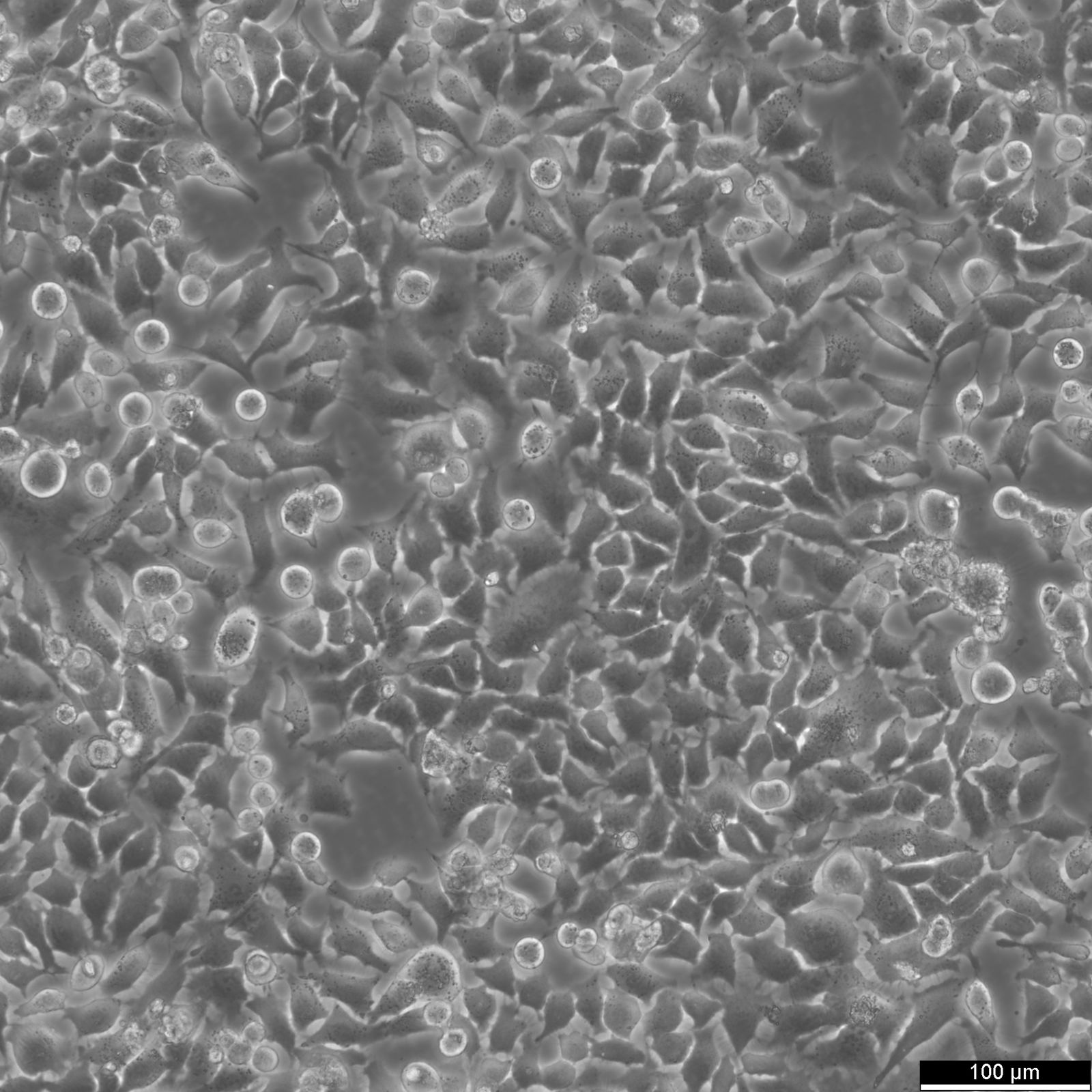
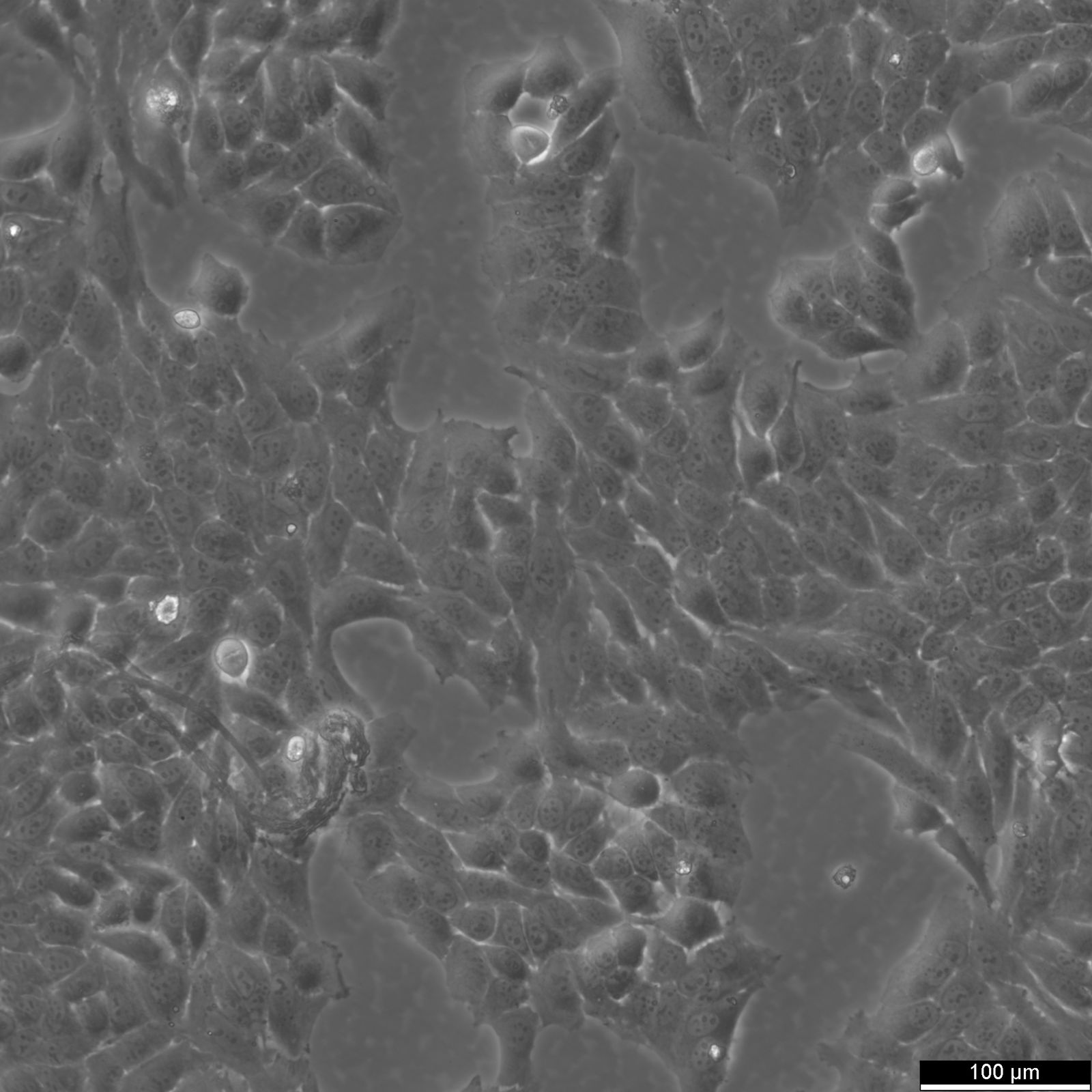
Structuur van HeLa-cellen
HeLa-cellen hebben een diameter van 10-20 µm, afhankelijk van de kweekomstandigheden. De meeste zoogdiercellen hebben een diameter tussen 10 en 100 µm. Een van de kleinste menselijke cellen, rode bloedcellen, hebben een diameter van ongeveer 8 µm. Anderzijds kunnen spiervezelcellen en neuronen extreem lang zijn.
Vooruitgang in onderzoek dankzij HeLa
HeLa cellen hebben aan de basis gestaan van belangrijke onderzoeksvorderingen, waaronder ontdekkingen in genetica, virologie en therapeutische ontwikkeling. De HeLa cellijn is gebruikt om kanker, AIDS, de effecten van straling en gifstoffen, het in kaart brengen van genen en talloze andere wetenschappelijke activiteiten te bestuderen. Er zijn meer dan 60.000 wetenschappelijke artikelen gepubliceerd over HeLa-onderzoek en dit aantal neemt maandelijks met meer dan 300 toe.
Uitroeiing van polio
In de jaren 1950 testte Jonas Salk het eerste poliovaccin met HeLa cellen. Deze cellen waren gevoelig voor infectie met poliomyelitis, wat resulteerde in de dood van geïnfecteerde cellen. Hierdoor was er veel vraag naar HeLa cellen voor het testen van poliovaccins, omdat de resultaten snel beschikbaar waren.
Virologie
HeLa cellen zijn geïnfecteerd met talloze virussen, waaronder HIV, Zika, herpes en de bof, om nieuwe vaccins en medicijnen te testen en te ontwikkelen. Dr. Richard Axel ontdekte dat HeLa-cellen geïnfecteerd kunnen worden met HIV door het CD4-eiwit toe te voegen, zodat het virus bestudeerd kan worden. HeLa cellen zijn gebruikt om papillomavirus E2 expressie en apoptose te onderzoeken en ze hebben ook een essentiële rol gespeeld in de ontwikkeling van humaan papillomavirus (HPV) vaccins.
Kanker
HeLa cellen zijn gebruikt voor talloze onderzoeken naar kanker, onder andere naar geslachtssteroïdhormonen zoals oestradiol, oestrogeen en oestrogeenreceptoren en oestrogeenachtige verbindingen zoals quercetine en de kankerpreventieve eigenschappen daarvan. HeLa cellen zijn ook gebruikt om de effecten van flavonoïden en antioxidanten met estradiol op de proliferatie van kankercellen te bestuderen.
Andere opmerkelijke toepassingen zijn
- Behandelingen van kanker: Hela cellen waren cruciaal bij het creëren van medicijnen tegen kanker, zoals camptothecine, een door de FDA goedgekeurd geneesmiddel voor de behandeling van eierstok-, long- en baarmoederhalskanker.
- Thalidomide en multipel myeloom: HeLa cellen werden gebruikt om te illustreren hoe het medicijn thalidomide, dat oorspronkelijk werd gebruikt voor ochtendmisselijkheid, aangeboren handicaps kan veroorzaken, wat leidde tot het gebruik ervan bij de behandeling van multipel myeloom.
- Inzicht in HIV en AIDS: De onthulling dat HIV problemen had met het infecteren van HeLa-cellen verbeterde het begrip van onderzoekers van het virus en opende de deur voor de ontwikkeling van medicijnen tegen HIV en AIDS.
- Cellulaire veroudering: HeLa cellen hebben onderzoekers in staat gesteld om de biologie van veroudering en de ziekten die vroegtijdige veroudering veroorzaken te onderzoeken, wat leidde tot de ontdekking van regenereerbare chromosomen die cellulaire degeneratie en schade in de loop van de tijd voorkomen.
- Bloedziekten: HeLa cellen werden gebruikt om de efficiëntie van hydroxyurea tegen verschillende bloedmaligniteiten en bloedarmoede te evalueren; hydroxyurea wordt nu gebruikt om sikkelcelziekte en witte bloedcelmaligniteiten te behandelen.
- Röntgenstraling: In 1956 gebruikten wetenschappers HeLa-cellen om de effecten van röntgenstraling op levende organismen te onderzoeken, waardoor ze een beter inzicht kregen in de gevaren van hoge en terugkerende stralingsdoses van medische röntgenstraling.
- Innovatieve ontdekkingen: HeLa cellen hebben een cruciale rol gespeeld in verschillende belangrijke ontdekkingen in de biologie, die hebben geleid tot vooruitgang in medicijnen tegen kanker, kennis over HIV/AIDS en nog veel meer.
- Cellulaire veroudering: Onderzoekers die HeLa cellen gebruiken kregen de Nobelprijs voor hun bevindingen over celveroudering en het voorkomen van cellulaire degeneratie en schade na verloop van tijd.
Verken HeLa-cellen en hun derivaten
Wat zijn potentieel geïmmortaliseerde cellen?
Geïmmortaliseerde cellijnen zijn cellen die zo gemodificeerd zijn dat ze zich continu delen en langdurig gekweekt kunnen worden. Ze zijn afkomstig van bronnen met chromosomale afwijkingen of mutaties en kunnen afkomstig zijn van tumoren. Om te kunnen blijven groeien, delen wetenschappers een deel van de cellen in nieuwe celkweekvaten en vermenigvuldigen ze deze voor verdere experimenten.
HeLa cellen worden, net als andere cellijnen, beschouwd als "onsterfelijk" omdat ze zich oneindig kunnen delen in celkweekvaten zolang de primaire voorwaarden voor het overleven van de cellen worden gehandhaafd (d.w.z. ondersteund en verzorgd in een geschikte omgeving). Er zijn talloze stammen van HeLa-cellen omdat ze blijven muteren in celkweken, maar ze zijn allemaal afgeleid van dezelfde Lacks tumorcellen. Het aantal HeLa cellen dat in celculturen wordt vermeerderd is veel groter dan het aantal dat in het lichaam van Henrietta Lacks werd gevonden.
HeLa cel productie, kwaliteitscontrole en houdbaarheid
HeLa cellen kunnen worden gekweekt en geoogst met behulp van standaard celkweekmethoden bij ongeveer 80-90% confluentie. De cellen zijn relatief eenvoudig te manipuleren en kunnen in verschillende instellingen worden gekweekt.
Hoe bevroren HeLa cellen te ontdooien
- Plaats de cryovial in een antibacterieel waterbad van 37°C met schoon water.
- Ontdooi snel gedurende 40 tot 60 seconden. De flacon moet worden verwijderd en overgebracht naar een steriele flowkast.
- Veeg de injectieflacon af met 70% alcohol en breng de celsuspensie over in een centrifugebuis van 15 ml met 8 ml kweekmedium.
- Reconstitueer de cellen, centrifugeer bij 300 x g gedurende drie minuten en gooi het supernatant weg (of verdun met medium en verwijder het vriesmedium 24 uur later als u niet meteen centrifugeert).
- Breng de cellen, gesuspendeerd in 10 ml nieuwe kweekmedia, over in twee T25 celkweekkolven.
Subculturen van HeLa-cellen
- Verwijder het oude medium uit de celkweekkolf.
- Spoel de aanhangende cellen met PBS zonder calcium en magnesium. Gebruik 3-5 ml PBS voor T25 en 5-10 ml voor T75 celkweekflessen.
- Voeg Accutase toe aan de celkweekkolf. Gebruik 1-2 ml per T25 en 2,5 ml per T75 celkweekkolf. Zorg ervoor dat het celblad volledig bedekt is.
- Incubeer de celkweekkolf gedurende 8-10 minuten bij omgevingstemperatuur.
- Resuspendeer de cellen voorzichtig met het medium. Voeg 10 ml medium toe en pipetteer voorzichtig op en neer om celaggregaten op te breken.
- Centrifugeer de celsuspensie 3 minuten bij 300 x g.
- Resuspendeer de cellen in vers medium.
- Breng de geresuspendeerde cellen over in nieuwe celkweekflesjes met vers medium.
- Bewaar de cellen in vloeibare stikstof voor langdurige opslag.
Door deze stappen te volgen, kunt u cellen subkweken en een gezonde celkweek voor toekomstige experimenten behouden.