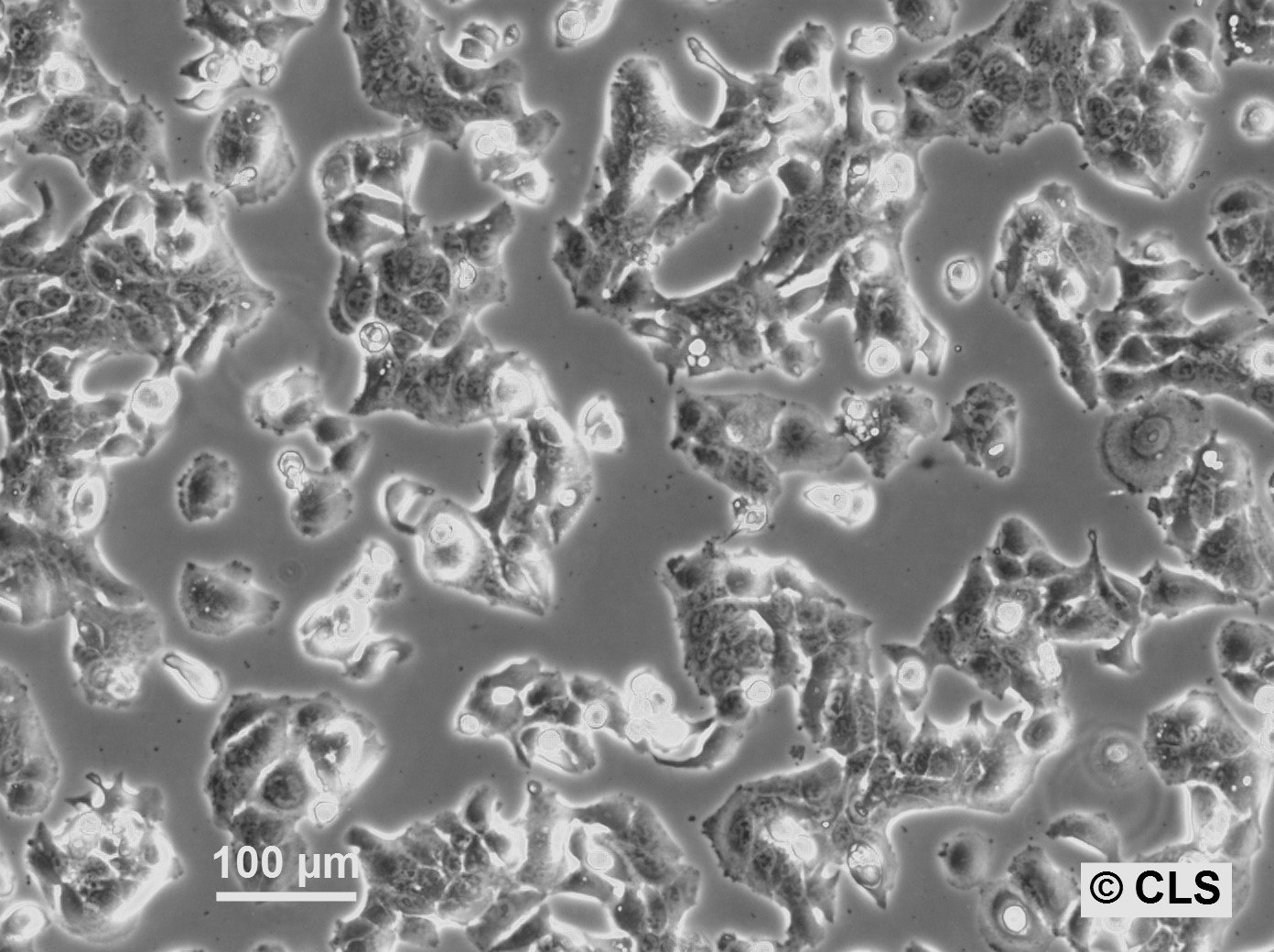
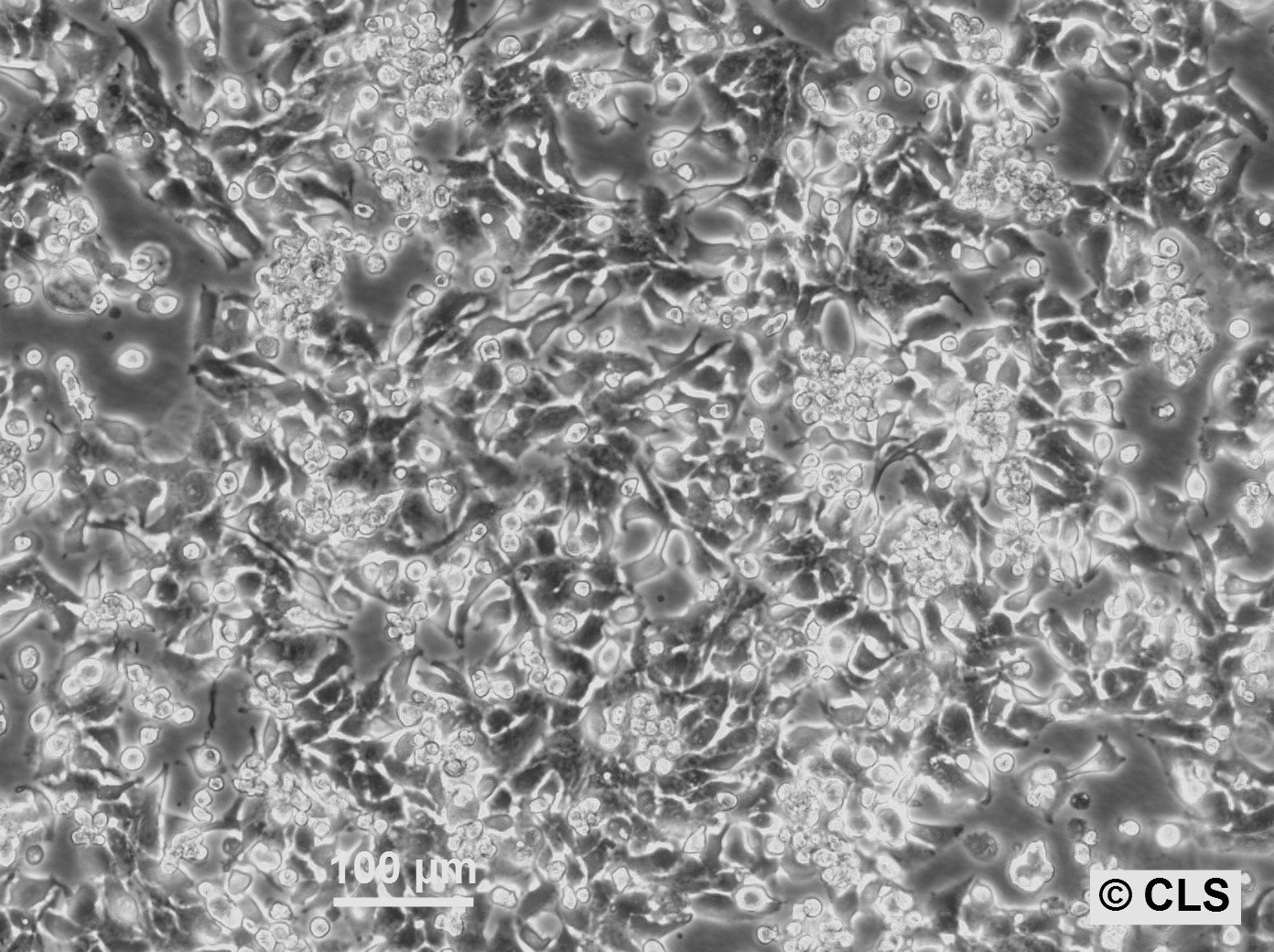
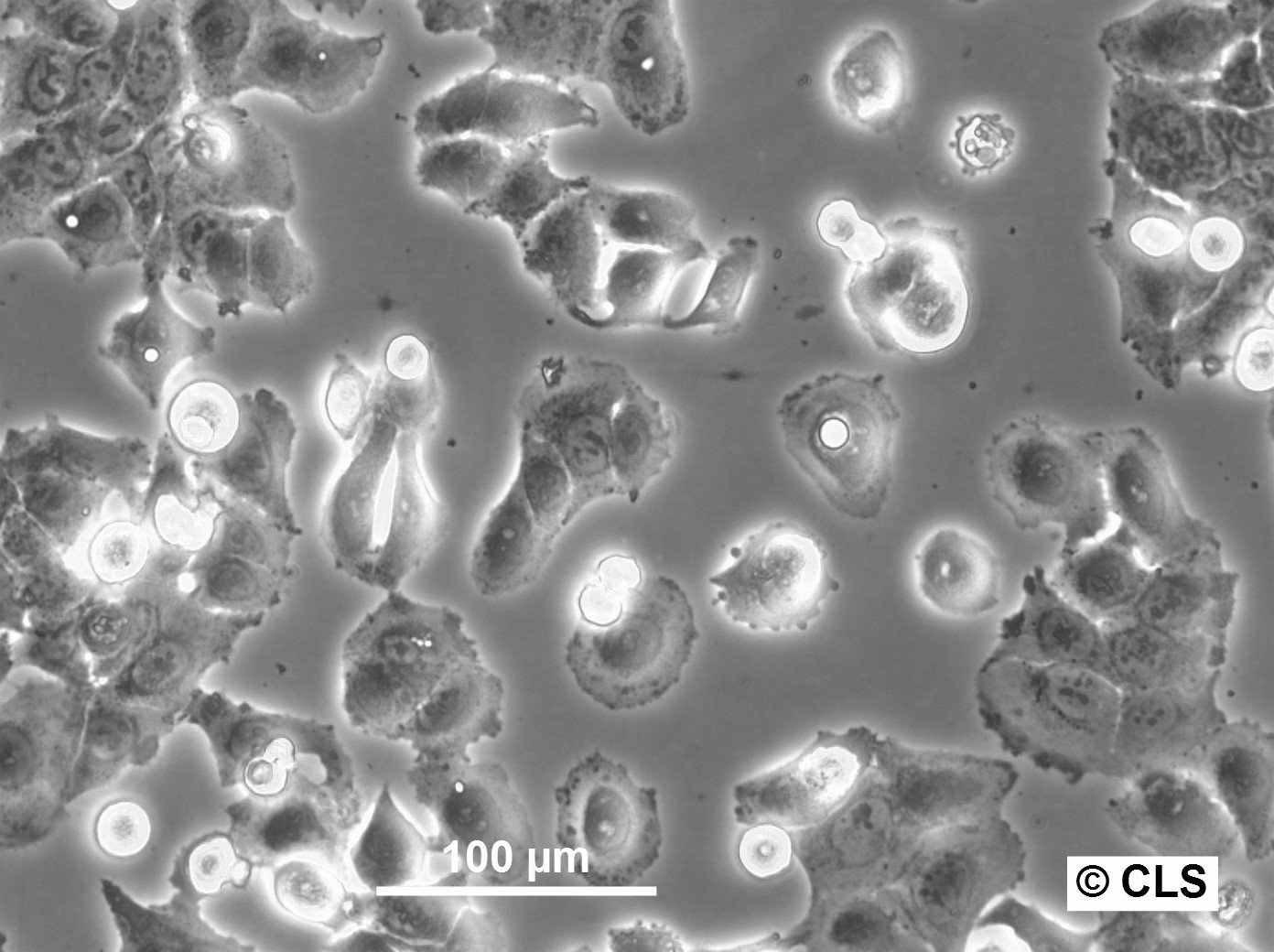
Cellules RT-112-D21













800,00 €*
Les produits sont expédiés congelés dans de la glace carbonique dans des cryotubes. Chaque cryotube contient généralement 3 × 10 6 cellules pour les lignées adhérentes ou 5 × 106 cellules pour les lignées en suspension (voir le certificat d'analyse du lot pour plus de détails).
Informations générales
| Description | Cytokératine (4),5,(6), 7, 8, 13, 17, 18, 19, Desmoplakin. DNA-index=2,1 (La lignée cellulaire a été rendue résistante à une concentration de Doxorubicine de 0,1 μg/ml par une augmentation successive de Doxorubicine dans le milieu de culture) |
|---|---|
| Organisme | Humain |
| Tissus | Vessie |
| Maladie | Carcinome |
| Synonymes | RT112/D21 |
Caractéristiques
| L'âge | Non spécifié |
|---|---|
| Genre | Femme |
| Ethnicité | Caucasien |
| Morphologie | De type épithélial |
| Propriétés de croissance | Adhérent |
Données réglementaires
| Citation | RT-112-D21 (numéro de catalogue Cytion 300325) |
|---|---|
| Niveau de biosécurité | 1 |
| NCBI_TaxID | 9606 |
| CellosaurusAccession | CVCL_6215 |
Données biomoléculaires
| Tumorigène | Oui, sur des souris nues |
|---|
Manipulation
| Milieu de culture | RPMI 1640, w : 2.0 mM Glutamine stable, w : 2.0 g/L NaHCO3 (numéro d'article Cytion 820700a) |
|---|---|
| Suppléments | Compléter le milieu avec 10% de FBS |
| Réactif de dissociation | Accutase |
| Sous-culture | Retirer l'ancien milieu des cellules adhérentes et les laver avec du PBS dépourvu de calcium et de magnésium. Pour les flacons T25, utiliser 3-5 ml de PBS, et pour les flacons T75, 5-10 ml. Ensuite, recouvrir complètement les cellules avec Accutase, en utilisant 1 à 2 ml pour les flacons T25 et 2,5 ml pour les flacons T75. Laisser les cellules incuber à température ambiante pendant 8-10 minutes pour les détacher. Après incubation, mélanger délicatement les cellules avec 10 ml de milieu pour les remettre en suspension, puis centrifuger à 300xg pendant 3 minutes. Jeter le surnageant, remettre les cellules en suspension dans du milieu frais et les transférer dans de nouveaux flacons contenant déjà du milieu frais. |
| Taux de fractionnement | Un rapport de 1:4 à 1:8 est recommandé |
| Renouvellement des fluides | 2 à 3 fois par semaine |
| Congélation du milieu | Comme milieu de cryoconservation, nous utilisons un milieu de croissance complet (comprenant du FBS) + 10 % de DMSO pour une viabilité adéquate après décongélation, ou CM-1 (numéro de catalogue 800100 de Cytion), qui comprend des osmoprotectants et des stabilisateurs métaboliques optimisés pour améliorer la récupération et réduire le stress induit par la cryogénisation. |
| Décongélation et culture des cellules |
|
| Atmosphère d'incubation | 37°C, 5%CO2, atmosphère humidifiée. |
| Revêtement des flacons | Pour une fixation et une viabilité optimales après décongélation, nous recommandons d'utiliser des flacons ou des plaques recouverts de collagène. |
| Procédure de congélation | Les lignées cellulaires cryoconservées sont expédiées sur glace sèche dans des emballages isolés et validés, avec suffisamment de réfrigérant pour maintenir une température d'environ -78 °C tout au long du transport. À la réception, inspecter immédiatement le conteneur et transférer sans délai les flacons dans un lieu de stockage approprié. |
| Conditions d'expédition | Les lignées cellulaires cryoconservées sont expédiées sur glace sèche dans des emballages isolés et validés, avec suffisamment de réfrigérant pour maintenir une température d'environ -78 °C tout au long du transport. À la réception, inspecter immédiatement le conteneur et transférer sans délai les flacons dans un lieu de stockage approprié. |
| Conditions de stockage | Pour une conservation à long terme, placer les flacons dans de l'azote liquide en phase vapeur à une température comprise entre -150 et -196 °C environ. Le stockage à -80 °C n'est acceptable qu'en tant qu'étape intermédiaire de courte durée avant le transfert dans l'azote liquide. |
Contrôle de qualité / Profil génétique / HLA
| Stérilité | La contamination par les mycoplasmes est exclue à l'aide de tests basés sur la PCR et de méthodes de détection des mycoplasmes basées sur la luminescence. Pour s'assurer de l'absence de contamination bactérienne, fongique ou levurienne, les cultures cellulaires font l'objet d'inspections visuelles quotidiennes. |
|---|---|
| Profil STR |
CSF1PO: 10,11
D13S317: 13,14
D16S539: 11,13
D5S818: 10,13
D7S820: 11,12
TH01: 7
TPOX: 8,11
vWA: 14,17
D3S1358: 15
D21S11: 27,30
D18S51: 15
Penta E: 12,16
Penta D: 10,11
D8S1179: 13,15
FGA: 23
PEZ6: RJ2.2.5
|
Accord de transfert de matériel
Si vous avez l'intention d'utiliser les lignées cellulaires Cytion uniquement pour la recherche interne sur un seul site de recherche, veuillez remplir et signer notre accord de transfert de matériel (MTA) et le joindre à votre commande.
Pour toute application commerciale, y compris, mais sans s'y limiter, les travaux rémunérés, les tests de contrôle qualité, la mise sur le marché de produits, l'utilisation à des fins diagnostiques ou les études réglementaires, veuillez remplir le formulaire d'utilisation prévue afin que nous puissions préparer un accord adapté à votre projet.
Remarque : le MTA s'applique uniquement à certaines lignées cellulaires. Si cet avis et le document MTA apparaissent sur une page produit, l'accord est applicable. Pour les lignées cellulaires non couvertes par le MTA, aucune référence à l'accord ne sera affichée. Le MTA n'est pas valable pour les clients situés en Amérique, en Chine ou à Taïwan. Veuillez contacter notre entité américaine pour recevoir l'accord approprié.
