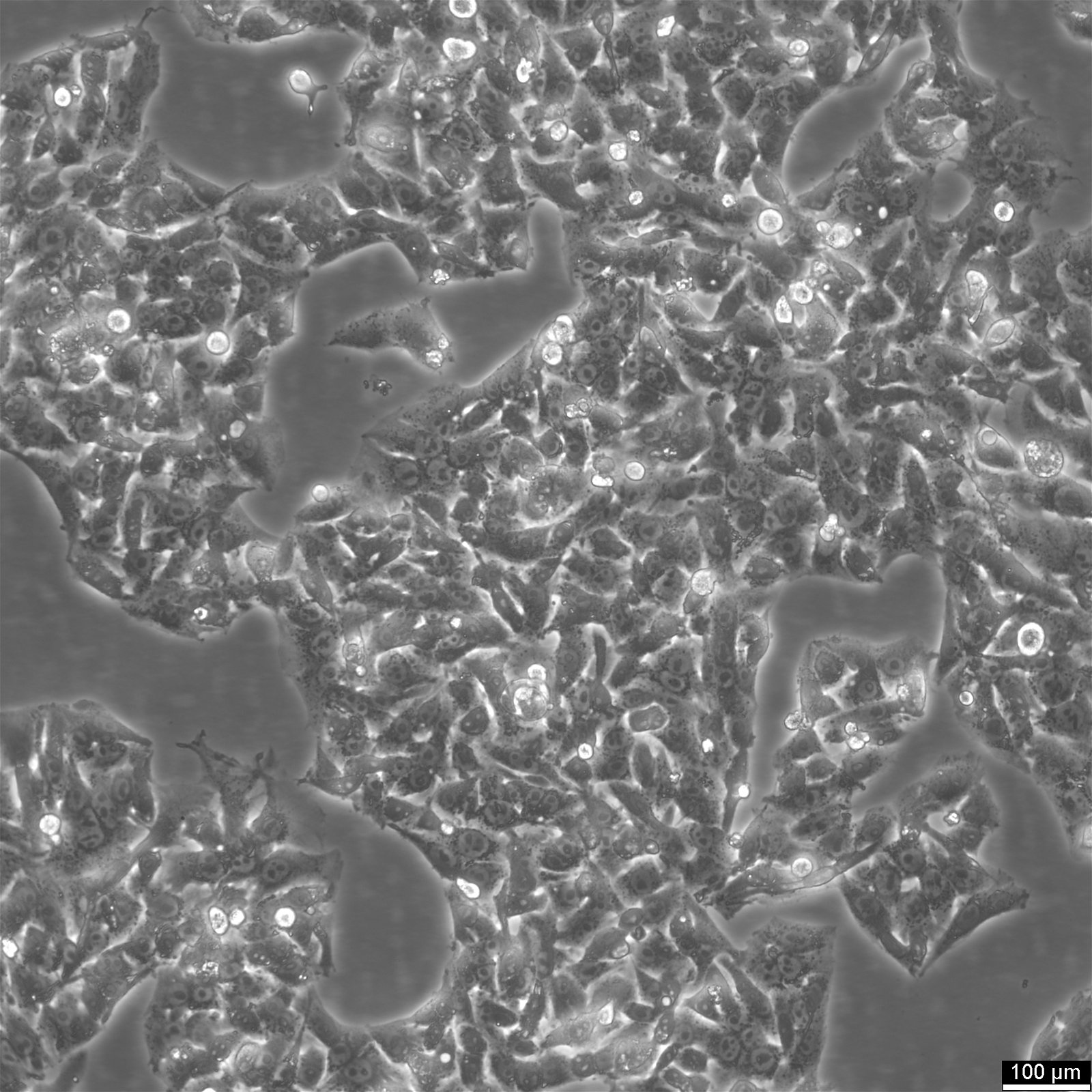
Cellules HepG2 - Une ressource pour la recherche sur le cancer du foie
Hep-G2 est une lignée de cellules cancéreuses du foie humain provenant du tissu hépatique d'un homme caucasien de 15 ans atteint d'un carcinome hépatocellulaire. Ces cellules sont fréquemment utilisées dans les études sur le métabolisme des médicaments et l'hépatotoxicité. Bien que les cellules HepG2 aient un taux de prolifération élevé et un aspect épithélial, elles ne sont pas tumorigènes et remplissent diverses fonctions hépatiques différenciées. En 1975, des chercheurs ont dérivé les cellules HepG2 d'un carcinome hépatocellulaire, ce qui en a fait la première lignée cellulaire hépatique à présenter les caractéristiques essentielles des hépatocytes. Contrairement à la lignée cellulaire SK-Hep1 précédemment établie, qui ne présente pas les marqueurs essentiels des cellules hépatiques, les cellules HepG2 peuvent sécréter diverses protéines plasmatiques et constituent un modèle précieux pour l'étude de la dynamique intracellulaire des domaines de la surface cellulaire dans les hépatocytes humains. Ces cellules présentent une morphologie de type épithélial, ont un nombre modal de chromosomes de 55 et peuvent être stimulées par l'hormone de croissance humaine
Caractéristiques de HepG2
Les hépatocytes primaires ont une forme cubique et contiennent généralement deux noyaux. En revanche, les cellules HepG2 ont une morphologie de type épithélial avec un seul noyau et un nombre de chromosomes allant de 48 à 54 par cellule. Bien que les cellules HepG2 puissent représenter jusqu'à 25 % des protéines cellulaires totales, leur taille est supérieure à celle des hépatocytes normaux, puisqu'elles représentent environ 10 % de l'ensemble des protéines de la cellule. Les protéines cellulaires sont des acteurs essentiels de la cellule, qui exécutent les fonctions spécifiées par les gènes.
Les cellules tumorales, y compris celles qui présentent un nombre anormal de chromosomes, présentent souvent une augmentation du nombre de noyaux, jusqu'à sept par cellule. En raison de leur haut degré de différenciation in vitro, les cellules HepG2 constituent un modèle idéal pour l'étude du trafic intracellulaire et de la dynamique des protéines membranaires des canaux biliaires et des sinusoïdes, ainsi que des lipides dans les hépatocytes humains.
Le diamètre moyen d'une cellule HepG2 est d'environ 10-20 µm, ce qui est plus petit qu'un hépatocyte dont le diamètre est de 15 µm, mais similaire aux cellules tumorales de l'hépatoblastome (HB), dont le diamètre est compris entre 10 et 20 µm.
Génétique de HepG2
La lignée cellulaire Hep-G2 présente plusieurs translocations, notamment entre les bras courts des chromosomes 1 et 21, des trisomies des chromosomes 2, 16 et 17 et une tétrasomie du chromosome 20. La perte de la région du chromosome 4q3 est également observée, associée à la translocation t(1;4) souvent observée dans l'hépatoblastome (HB) et à d'autres anomalies chromosomiques, telles que les trisomies 2 et 20. Le nombre de chromosomes dans les cellules HepG2 varie entre 50 et 60, ce qui indique un caryotype hyperdiploïde, tandis que certains cas présentent plus de 100 chromosomes et sont caractérisés par un élargissement tétraploïde. Les cellules HepG2 contiennent environ 7,5 pg d'ADN, soit 15 % de plus qu'une cellule somatique moyenne. En comparaison, les hépatocytes primaires ont une forme cubique et contiennent généralement deux noyaux [1].
Profil mutationnel des cellules HepG2
La lignée cellulaire HepG2 est porteuse de la mutation C228T de la région promotrice de TERT, également présente dans le carcinome hépatocellulaire (CHC) et l'hépatoblastome (HB). Cette mutation contribue à l'immortalisation en protégeant les télomères des cellules cancéreuses. En outre, les cellules HepG2 présentent un TP53 de type sauvage, un gène essentiel pour la suppression du cancer humain, car il joue un rôle dans l'arrêt du cycle cellulaire, l'apoptose et le vieillissement. Les mutations de ce gène peuvent favoriser la prolifération cellulaire.
Les cellules HepG2 participent à plusieurs voies, notamment la dysrégulation de la croissance cellulaire, les voies de survie telles que la HB fœtale et embryonnaire, et la voie Wnt/β-caténine. De plus, cette lignée cellulaire présente une délétion caractéristique du troisième exon du gène CTNNB1, identique à celle observée dans l'HB de type épithélial [2,3].
Vue d'ensemble des cellules de carcinome hépatocellulaire HepG2 dans la recherche sur le foie
Les cellules HepG2, issues d'un hépatome humain, sont devenues un outil précieux pour la recherche sur les fonctions et les maladies du foie, y compris le carcinome hépatocellulaire. Ces lignées cellulaires hépatiques permettent de mieux comprendre les réponses cellulaires des hépatocytes humains dans diverses conditions expérimentales. L'utilisation de plasmides rapporteurs de la luciférase dans les cellules HepG2 s'est avérée particulièrement efficace pour suivre l'expression des gènes et les transfections cellulaires, qui sont fondamentales dans la recherche métabolique, comme l'étude des effets de l'éthanol sur les cellules hépatiques
Infections virales et études sur les maladies du foie à l'aide de cellules HepG2
Les lignées cellulaires tumorales hépatiques immortalisées comme HepG2 et Huh7 sont essentielles pour l'étude des infections virales, car elles démontrent une réplication complète du cycle cellulaire de l'hépatite D (HDV) et l'expression de l'hépatite B (HBV) [5,6]. Parallèlement, les lignées cellulaires HepaRG jouent un rôle essentiel dans l'élucidation des mécanismes d'entrée du VHB [7]. Les cellules HepG2 sont également utilisées pour étudier diverses maladies hépatiques humaines, qu'il s'agisse d'affections génétiques telles que la cholestase intrahépatique familiale progressive (PFIC) et le syndrome de Dubin-Johnson, d'études environnementales et alimentaires liées à des agents cytotoxiques et génotoxiques, ou encore de recherches sur le ciblage des médicaments et l'hépatocarcinogénèse [8,9]. Leur utilisation s'étend aux essais de dispositifs de foie bio-artificiel
Interactions des cellules HepG2 avec les biomatériaux dans l'ingénierie tissulaire
L'interaction des cellules HepG2 avec divers biomatériaux est essentielle dans l'ingénierie tissulaire. Des techniques telles que la technique des sondes colloïdales permettent de comprendre ces interactions en mesurant les propriétés d'adhésion des cellules, ce qui est essentiel pour déterminer la viabilité des cellules en vue du développement d'échafaudages et de modèles précis de tissus hépatiques
Comportement cellulaire et innovations dans les modèles basés sur HepG2
L'étude du comportement cellulaire dans les modèles basés sur HepG2 est cruciale pour la recherche sur les maladies du foie. Les progrès réalisés dans les cultures de cellules sphéroïdes tridimensionnelles ont conduit à la création de sphéroïdes de cellules HepG2, offrant un modèle plus pertinent sur le plan physiologique et reflétant plus fidèlement les hépatocytes normaux. Ces modèles 3D, avec une activité métabolique accrue, indiquent que les cellules HepG2 peuvent servir de modèle pour l'hépatoblastome et sont importants pour la recherche sur le traitement du cancer, en particulier pour simuler des tumeurs du foie et tester de nouvelles approches thérapeutiques [10-12]
Comparaison et caractéristiques de HepG2 par rapport à d'autres lignées cellulaires tumorales
HepG2 est l'une des lignées de cellules tumorales hépatiques les plus utilisées, sélectionnée pour ses nombreuses applications dans la recherche scientifique parmi une quarantaine de lignées de cellules tumorales hépatiques disponibles [13]. Malgré l'expression faible ou absente de certaines enzymes du cytochrome P450 par rapport aux hépatocytes normaux, le profil métabolique de HepG2 a incité à modifier la lignée cellulaire pour améliorer les études sur le métabolisme des médicaments [13]. Par rapport aux lignées cellulaires tumorales telles que MCF7, PC3, 143B et HEK293, les cellules HepG2 présentent des profils de contenu en acides aminés uniques qui influencent de manière significative la synthèse et la sécrétion des protéines, mettant en évidence leurs voies métaboliques uniques [14]
Explorer la recherche sur les maladies du foie avec HepG2
Sous-culture des cellules HepG2
Voici cinq étapes pour éliminer les cellules adhérentes des flacons de culture cellulaire à l'aide d'Accutase :
- Retirer le milieu de la fiole de culture cellulaire et rincer les cellules adhérentes à l'aide de PBS sans calcium ni magnésium. Utiliser 3-5 ml de PBS pour les flacons T25 et 5-10 ml pour les flacons T75.
- Ajouter l'Accutase à la fiole de culture cellulaire, en utilisant 1 à 2 ml par fiole T25 et 2,5 ml par fiole T75. S'assurer que l'Accutase couvre la totalité de la feuille de cellules.
- Incuber le ballon à température ambiante pendant 8-10 minutes.
- Remettre soigneusement les cellules en suspension avec du milieu, en utilisant 10 ml de milieu frais.
- Centrifuger les cellules remises en suspension pendant 5 minutes à 300xg, les remettre en suspension dans du milieu frais et les distribuer dans de nouveaux flacons contenant du milieu frais.
Perspectives d'avenir pour les cellules HepG2
La quête du plein potentiel de la lignée cellulaire HepG2 se poursuit avec des progrès révolutionnaires dans l'augmentation de l'expression des cytochromes. Les chercheurs explorent également la possibilité de cultures cellulaires sphéroïdes tridimensionnelles, qui offrent un système plus pertinent d'un point de vue physiologique. L'activité métabolique, y compris les cytochromes, est remarquablement plus élevée dans les modèles sphéroïdaux 3D HepG2 que dans les cellules 2D, ce qui nous rapproche de la création d'un modèle qui reflète les hépatocytes normaux. En outre, l'exploration des processus dynamiques qui sous-tendent la distribution incorrecte des protéines de surface cellulaire peut ouvrir la voie à une meilleure compréhension des maladies du foie
Cellules HepG2 : Comprendre leur rôle et leurs distinctions dans la recherche biomédicale - FAQs
Références
- Vyas, R.C., Darroudi, F., Natarajan, A.T. Radiation-induced chromosomal breakage and rejoining in interphase-metaphase chromosomes of human lymphocytes, Mutat Res, 1991 ; 249(1):29-35.
- Woodfield, S.E., Shi, Y., Patel, R.H., Chen, Z., Shah, A.P., Srivastava, R.K., Whitlock, R.S., Ibarra, A.M., Larson, S.R., Sarabia, S.F., et al. MDM4 Inhibition : A Novel Therapeutic Strategy to Reactivate P53 in Hepatoblastoma (Inhibition de MDM4 : une nouvelle stratégie thérapeutique pour réactiver P53 dans l'hépatoblastome). Sci. Rep. 2021, 11, 2967.
- Hussain, S.P., Schwank, J., Staib, F., Wang, X.W., Harris, C.C. TP53 Mutations and hepatocellular Carcinoma : Insights into the Etiology and Pathogenesis of Liver Cancer. Oncogene 2004.
- Schicht, G., Seidemann, L., Haensel, R., Seehofer, D., Damm, G. Critical Investigation of the Usability of Hepatoma Cell Lines HepG2 and Huh7 as Models for the Metabolic Representation of Resectable Hepatocellular Carcinoma. Cancers 2022, 14(17), 4227.
- Verrier, E.R., Colpitts, C.C., Schuster, C., Zeisel, M.B., Baumert, T.F. Cell Culture Models for the Investigation of Hepatitis B and D Virus Infection. Viruses 2016, 8, 261.
- Verrier, E.R., Colpitts, C.C., Bach, C., Heydmann, L., Weiss, A., Renaud, M., Durand, S.C., Habersetzer, F., Durantel, D., AbouJaoudé, G., et al. A Targeted Functional RNA Interference screen Uncovers Glypican 5 as an Entry Factor for Hepatitis B and D Viruses. Hepatology 2016, 63, 35-48.
- Gripon, P., Rumin, S., Urban, S., Le Seyec, J., Glaise, D., Cannie, I., Guyomard, C., Lucas, J., Trepo, C., Guguen-Guillouzo, C. Infection d'une lignée cellulaire d'hépatome humain par le virus de l'hépatite B. Proc. Natl. Acad. Sci. USA 2002, 99, 15655-15660.
- Mersch-Sundermann, V., Knasmüller, S., Wu, X.J., Darroudi, F., Kassie, F. Use of a human-derived liver cell line for the detection of cytoprotective, antigenotoxic and cogenotoxic agents. Toxicology. 2004 ; 198(1-3) : 329-340.
- Fanelli, A. HepG2 (carcinome hépatocellulaire du foie) : culture cellulaire. HepG2. Consulté le 3 décembre 2017.
- Xuan, J., Chen, S., Ning, B., Tolleson, W.H., Guo, L. Development of HepG2-Derived Cells Expressing Cytochrome P450s for Assessing Metabolism-Associated Drug-Induced Liver Toxicity. Physiol. Behav. 2017, 176, 139-148.
- Ooka, M., Lynch, C., Xia, M. Application de l'activation du métabolisme in vitro dans le criblage à haut débit. Int. J. Mol. Sci. 2020, 21, 8182.
- Huang, L., Coughtrie, M.W.H., Hsu, H. Down-Regulation of Dehydroepiandrosterone Sulfotransferase Gene in Human Hepatocellular Carcinoma. Mol. Cell. Endocrinol.
- Zhu, Z., Hao, X., Yan, M., et al. Cancer stem/progenitor cells are highly enriched in CD133 + CD44 + population in hepatocellular carcinoma. Int J Cancer. 2010 ; 126:2067-2078.
- Arbus, C., Benyamina, A., Llorca, P.-M., Baylé, F., Bromet, N., Massiere, F., Garay, R.P., Hameg, A. Characterization of human cytochrome P450 enzymes involved in the metabolism of cyamemazine. Eur J Pharm Sci. 2007 Dec;32(4-5):357-66.