Ihmisen mesenkymaaliset kantasolut - luuydin (HMSC-BM)

























Yleisiä tietoja
| Kuvaus | Luuytimestä peräisin olevat ihmisen mesenkymaaliset kantasolut (HMSC-BM) ovat vankka ja monipuolinen työkalu in vitro -tutkimukseen. Näillä monipotenttisilla mesenkymaalisilla stromasoluilla (MSC) on ainutlaatuinen kyky uusiutua ja erilaistua monenlaisiksi solutyypeiksi, kuten rasvasoluiksi, osteoblastiksi ja kondrosyytteiksi. HMSC-BM:n kyky erilaistua näiksi kolmeksi avainlinjaksi on hyvin dokumentoitu, mikä tekee niistä korvaamattomia regeneratiivisen lääketieteen, kudostekniikan ja solujen erilaistumisreittien tutkimuksessa. Näitä MSC-soluja viljellään tiukkojen ehtojen mukaisesti, mikä varmistaa niiden monipotentiaalisuuden ja korkean elinkelpoisuuden sulatuksen jälkeen. Yksi HMSC-BM:n erottavista piirteistä verrattuna muista lähteistä, kuten rasvakudoksesta tai napanuorasta, peräisin oleviin MSC-soluille on niiden ylivoimainen kyky osteogeeniseen erilaistumiseen. Tämä tekee niistä erityisen hyödyllisiä luubiologiassa ja ortopedisessa tutkimuksessa, joissa luun muodostumista ja korjautumista ohjaavien molekyylimekanismien ymmärtäminen on ratkaisevan tärkeää. Lisäksi HMSC-BM-soluilla on vahva immunomoduloiva profiili, mikä tekee niistä erinomaisen mallin immuunivasteiden ja tulehdusreaktioiden tutkimiseen. Nämä ainutlaatuiset ominaisuudet tekevät HMSC-BM-soluista myös ensisijaisen valinnan prekliinisissä tutkimuksissa, joissa tutkitaan luuytimen mikroympäristöä, hematopoieesia ja luuytimeen liittyvien sairauksien patofysiologiaa. Jokainen HMSC-BM-kryoputki sisältää vähintään 1 x 106 solua, joiden elinkykyisyysaste on 92–95 % Trypan Blue -väriaineen poissulkemistestin mukaan. Nämä solut on peräisin terveiltä aikuisilta luovuttajilta kerätystä luuytimestä, ja kaikki luovuttajat ovat antaneet tietoon perustuvan suostumuksensa. Korkeimpien standardien varmistamiseksi jokainen erä käy läpi tiukat laadunvalvontatestit, joissa arvioidaan solujen tunnistettavuus, puhtaus, teho ja elinkelpoisuus. Nämä perusteelliset testit takaavat, että MSC-solut täyttävät tiukat kriteerit, minkä ansiosta ne soveltuvat monenlaisiin tutkimussovelluksiin, kuten solubiologian tutkimuksiin, lääkekehitykseen ja solujen reaktioiden tutkimiseen erilaisille ärsykkeille. Näitä soluja ei ole tarkoitettu terapeuttisiin tai in vivo -sovelluksiin, ja niiden käyttö on rajoitettu tutkimustarkoituksiin kontrolloidussa laboratorioympäristössä. |
|---|---|
| Organismi | Ihminen |
| Kudos | Luuydin |
| Sovellukset | Lääketestaus, regeneratiivinen lääketiede, sairauksien tutkimus |
Ominaisuudet
| Ikä | Kysy lisää |
|---|---|
| Sukupuoli | Kysy lisää |
| Etnisyys | Kaukasialainen |
| Morfologia | Hyvin levinnyt karanmuotoinen, fibroblastin kaltainen morfologia vähintään 5 läpiviennin ajan. Alle 2 %:lla soluista on spontaani myofibroblastin kaltainen morfologia kussakin läpiviennissä. |
| Solutyyppi | Kantasolu |
| Kasvuominaisuudet | Tarttuva |
Sääntelytiedot
| Viittaus | Ihmisen mesenkymaaliset kantasolut, luuydin (HMSC-BM) (Cytionin luettelonumero 300665) |
|---|---|
| Bioturvallisuustaso | 1 |
| NCBI_TaxID | 9606 |
Biomolekyylitiedot
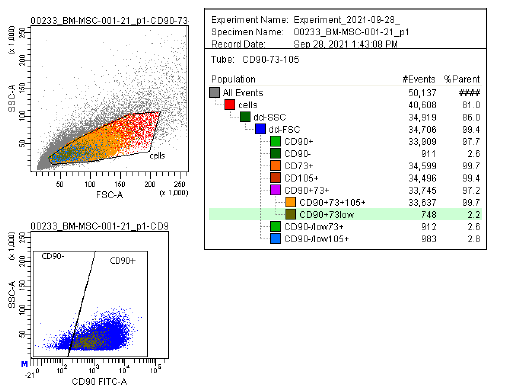
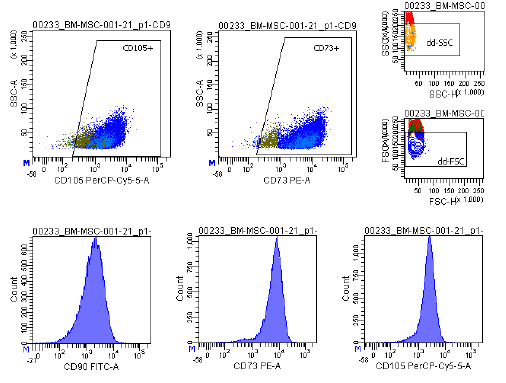
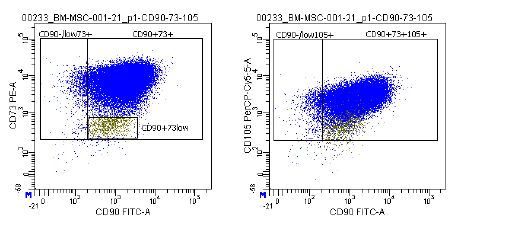
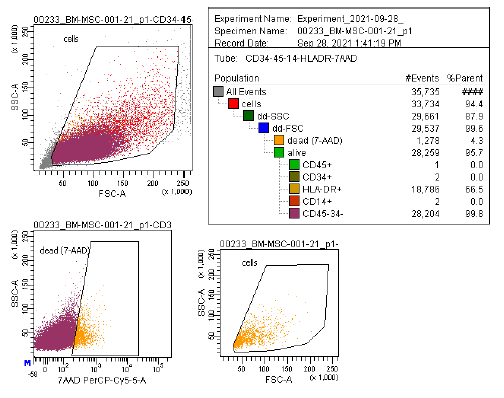
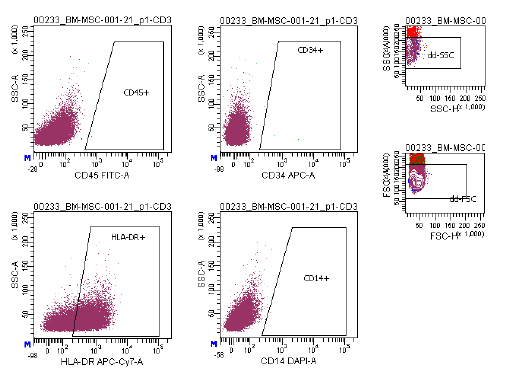
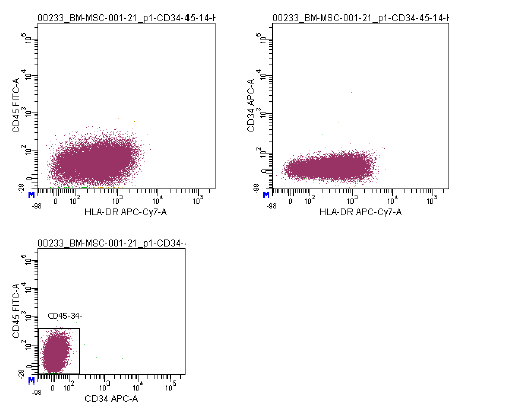
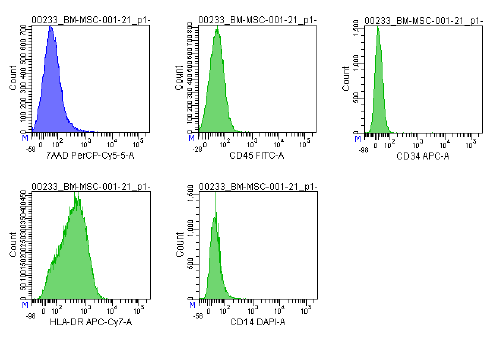
| Antigeenin ilmentyminen | Virtaussytometria-analyysissä käytetään kattavaa merkkiainepaneelia, mukaan lukien CD73/CD90/CD105 (positiivinen) ja CD14/CD34/CD45/HLA-DR (negatiivinen), viljeltyjen MSC:iden (P2-P3) tunnistamiseksi ennen kryosäilytystä. ISCT:n MSC-komitea suosittelee näitä merkkiaineita. |
|---|---|
| Virukset | Luovuttaja on negatiivinen HBV:n (PCR), Treponema pallidumin (PCR) ja HIV-1/2:n (IFA) suhteen. Solut ovat negatiivisia HBV:n, HCV:n, HSV1:n, HSV2:n, CMV:n, EBV:n, HHV6:n, Toxoplasma gondii:n, Treponema pallidumin, Chlamydia trachomatis:n, Ureaplasma urealyticum:n ja Ureaplasma parvum:n suhteen. |
Käsittely
| Viljelyalusta | Alpha MEM, w: 2,0 mM stabiili glutamiini, w/o: Ribonukleosidit, w/o: Deoksiribonukleosidit, w: 1,0 mM natriumpyruvaattia, w: 2,2g/L NaHCO3 |
|---|---|
| Lisäravinteet | Lisätään väliaineeseen 10 % FBS, 2 ng/ml bFGF |
| Dissosiaatioreagenssi | Trypsin-EDTA |
| Alakulttuuri | Rutiininomaiseen adherenttiseen soluviljelyyn: Imeytä vanha elatusaine adheesiosoluista ja pese ne PBS:llä jäljellä olevan elatusaineen poistamiseksi. Kun PBS on imetty, lisätään sopiva määrä trypsiini/EDTA-liuosta viljelyastian koon mukaan (esim. 1 ml T25-pulloon, 3 ml T75-pulloon) ja inkuboidaan huoneenlämmössä tai 37 °C:ssa, kunnes solut irtoavat (5-10 minuuttia). Seuraa irtoamista mikroskoopilla ja napauta astiaa tarvittaessa varovasti solujen irrottamiseksi. Kun solut ovat irronneet, lisätään täyttä elatusainetta trypsiinin/EDTA:n inaktivoimiseksi, solut suspendoidaan varovasti uudelleen ja siirretään solususpensiosta aliquota uuteen kasvatusastiaan, joka sisältää tuoretta elatusainetta. Aseta astia inkubaattoriin, jonka lämpötila on 37 °C jahiilidioksidipitoisuus 5 %, ja vaihda väliaine 2-3 päivän välein. |
| Kylvötiheys | 1–3 x 104 solua/cm2 |
| Nesteen uusiminen | Ensimmäinen nesteen uusiminen 24 tunnin kuluttua, sitten 2-3 päivän välein. |
| Jäädytä väliaine | Kryosäilytysmediana käytämme 80 % FBS + 10 % perusmediaa + 10 % DMSO:ta elinkelpoisuuden säilyttämiseksi tai CM-1:tä (Cytionin luettelonumero 800100), joka tarjoaa erinomaisen kryosuojan ja estää ei-toivotun erilaistumisen säilyttäen samalla pluripotenssin. |
| Solujen sulattaminen ja viljely |
|
| Inkubaatioilmapiiri | 37 °C, 5 %CO2, kostutettu ilmakehä. |
| Pullon pinnoite | Optimaalisen kiinnittymisen ja elinkelpoisuuden saavuttamiseksi sulatuksen jälkeen suosittelemme kollageenipinnoitettujen pullojen tai levyjen käyttöä. |
| Jäädytysmenettely | Kryosäilytetyt solulinjat kuljetetaan kuivajäässä validoidussa, eristetyssä pakkauksessa, jossa on riittävästi kylmäainetta, jotta lämpötila pysyy noin -78 °C:ssa koko kuljetuksen ajan. Pakkaus on tarkastettava välittömästi sen vastaanottamisen jälkeen ja injektiopullot on siirrettävä viipymättä asianmukaiseen varastoon. |
| Toimitusehdot | Kryosäilytetyt solulinjat kuljetetaan kuivajäässä validoidussa, eristetyssä pakkauksessa, jossa on riittävästi kylmäainetta, jotta lämpötila pysyy noin -78 °C:ssa koko kuljetuksen ajan. Pakkaus on tarkastettava välittömästi sen vastaanottamisen jälkeen ja injektiopullot on siirrettävä viipymättä asianmukaiseen varastoon. |
| Varastointiolosuhteet | Pitkäaikaissäilytystä varten injektiopullot asetetaan höyryfaasissa olevaan nestemäiseen typpeen noin -150 - -196 °C:een. Säilytys -80 °C:ssa on hyväksyttävää vain lyhyenä välivaiheena ennen siirtoa nestemäiseen typpeen. |
Laadunvalvonta / Geneettinen profiili / HLA
| Steriliteetti | Mykoplasmakontaminaatio suljetaan pois sekä PCR-pohjaisilla määrityksillä että luminesenssiin perustuvilla mykoplasman osoitusmenetelmillä. Bakteeri-, sieni- tai hiivakontaminaation välttämiseksi soluviljelmät tarkastetaan päivittäin silmämääräisesti. |
|---|
Analyysitodistus (CoA)
| Erän numero | Todistuksen tyyppi | Päivämäärä | Luettelonumero |
|---|---|---|---|
| 300665-240423P1 | Analyysitodistus | 26. Mar. 2026 | 300665 |
Materiaalin siirtosopimus
Jos aiot käyttää Cytion-solulinjoja yksinomaan sisäiseen tutkimukseen yhdellä tutkimuspaikalla, täytä ja allekirjoita materiaalinsiirtosopimus (MTA) ja lähetä se tilauksesi mukana.
Kaikissa kaupallisissa sovelluksissa – mukaan lukien mutta ei rajoittuen maksullisiin palveluihin, laadunvalvontatestaukseen, tuotteiden julkaisemiseen, diagnostiseen käyttöön tai sääntelytutkimuksiin – täytä käyttötarkoituksen lomake, jotta voimme laatia projektiisi sopivan sopimuksen.
Huomaa: MTA koskee vain tiettyjä solulinjoja. Jos tämä ilmoitus ja MTA-asiakirja näkyvät tuotesivulla, sopimus on voimassa. Solulinjoille, joita MTA ei koske, sopimusta ei mainita. MTA ei ole voimassa asiakkaille Amerikassa, Kiinassa tai Taiwanissa. Ota yhteyttä Yhdysvaltain yksikköömme saadaksesi sopivan sopimuksen.
