Ihmisen hammasytimen kantasolut (hDPSC-solut)






Yleisiä tietoja
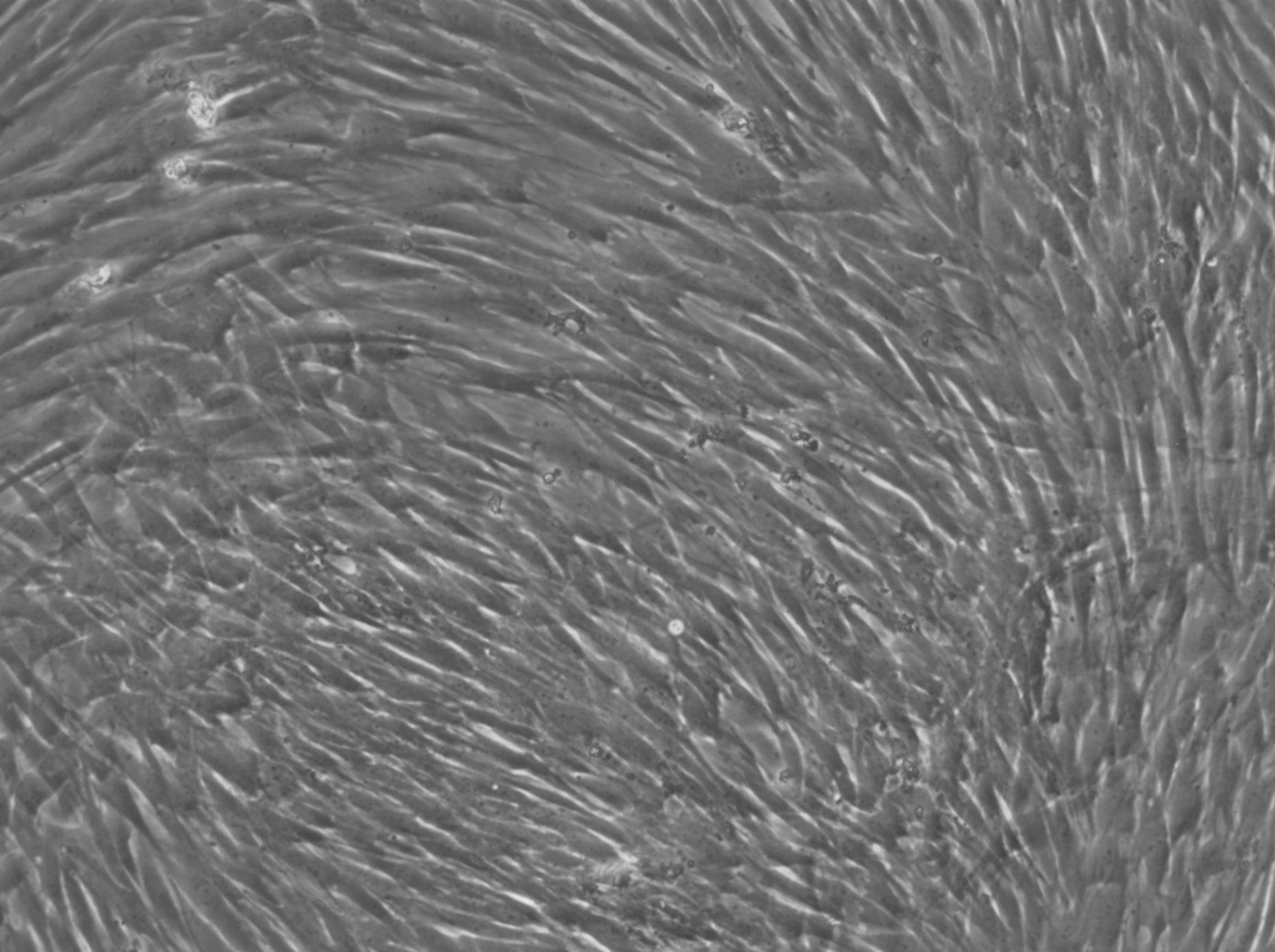
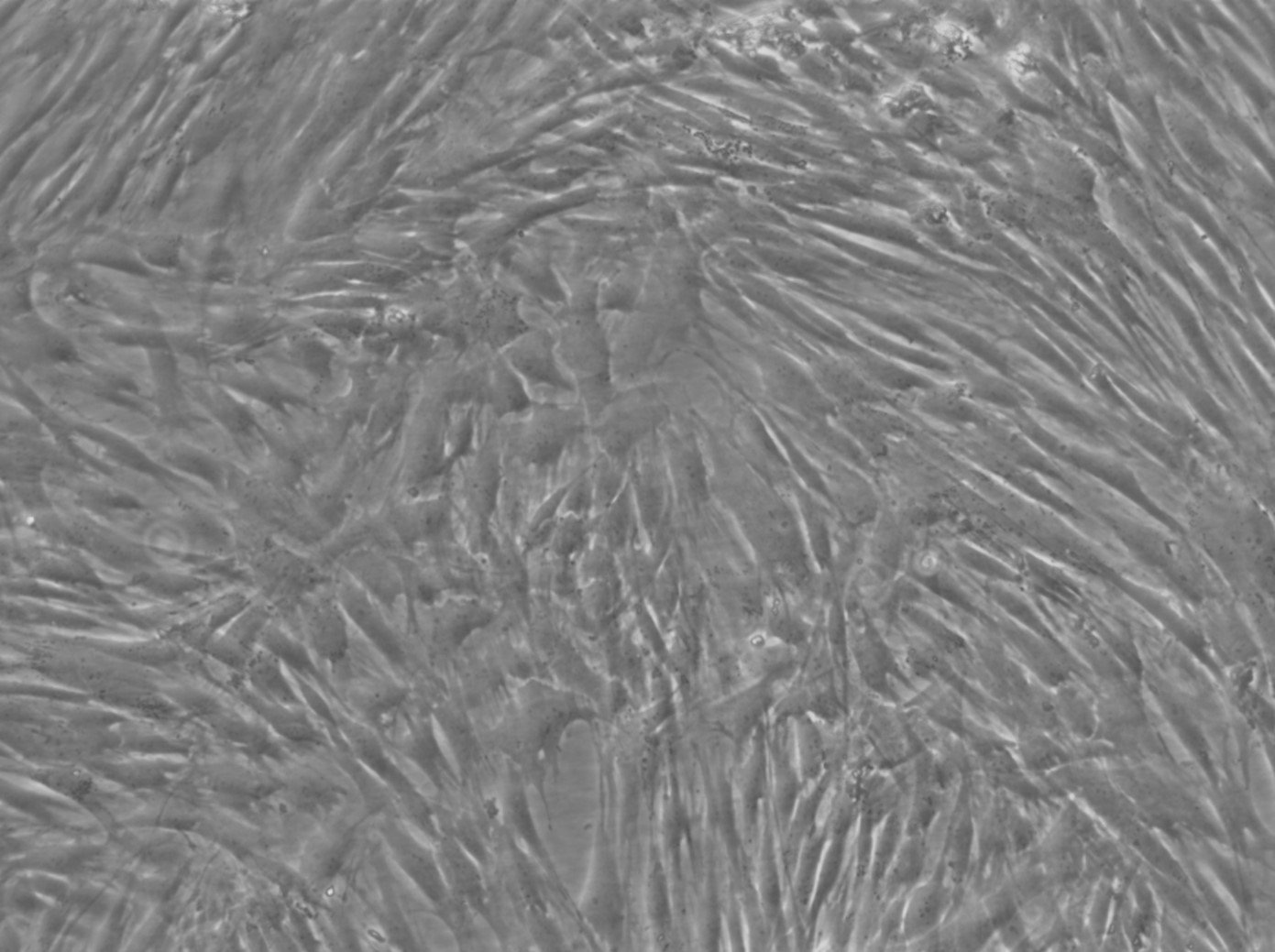
| Kuvaus | Ihmisen hammasytimen kantasolut (DPSC, hDPSC) ovat monipotentteja kantasoluja, jotka on eristetty aikuisten hampaiden, tavallisesti kolmansien poskihampaiden, hammasytimestä. Nämä solut ovat erityisen arvokkaita regeneratiivisessa lääketieteessä, koska ne kykenevät erilaistumaan erilaisiksi solutyypeiksi, kuten luu-, rusto-, rasva- ja hammaskudoksia muodostaviksi soluiksi. DPSC-solut ovat tunnettuja korkeasta proliferatiivisesta kapasiteetistaan, mikä tekee niistä vankan valinnan kudosteknologiaan ja solupohjaisiin terapeuttisiin sovelluksiin. DPSC:llä on myös merkittäviä immunomoduloivia ominaisuuksia, jotka edistävät niiden mahdollista käyttöä tulehdustilojen hoidossa. Hammaskudoksen uudistamisen lisäksi niiden kykyä korjata luuvikoja ja niiden käyttöä neurologisissa hoidoissa on tutkittu. Niiden suhteellisen helppo saatavuus ja kyky säilyttää elinkelpoisuus kryosäilytyksen jälkeen tekevät DPSC:stä houkuttelevan vaihtoehdon kliiniseen tutkimukseen ja terapeuttiseen kehitykseen erityisesti regeneratiivisen hammaslääketieteen, ortopedian ja hermoston rappeutumissairauksien aloilla. |
|---|---|
| Organismi | Ihminen |
| Kudos | Hammaslääkärit |
| Sovellukset | Lääketestaus, regeneratiivinen lääketiede, sairauksien tutkimus |
Ominaisuudet
| Kasvuominaisuudet | Tarttuva |
|---|
Sääntelytiedot
| Viittaus | Ihmisen hammasytimen kantasolut (DPSC, hDPSC) (Cytionin luettelonumero 300702) |
|---|---|
| Bioturvallisuustaso | 1 |
| NCBI_TaxID | 9606 |
Biomolekyylitiedot
Käsittely
| Viljelyalusta | Alpha MEM, w: 2,0 mM stabiili glutamiini, w/o: Ribonukleosidit, w/o: Deoksiribonukleosidit, w: 1,0 mM natriumpyruvaattia, w: 2,2g/L NaHCO3 |
|---|---|
| Lisäravinteet | Lisätään väliaineeseen 10 % FBS, 2 ng/ml bFGF |
| Dissosiaatioreagenssi | Accutase |
| Alakulttuuri | Poista vanha väliaine tarttuneista soluista ja pese ne PBS:llä, josta puuttuu kalsiumia ja magnesiumia. Käytä T25-pulloissa 3-5 ml PBS:ää ja T75-pulloissa 5-10 ml. Peitä sitten solut kokonaan Accutase-valmisteella, käyttäen 1-2 ml T25-pulloissa ja 2,5 ml T75-pulloissa. Anna solujen inkuboitua huoneenlämmössä 8-10 minuuttia solujen irtoamiseksi. Inkuboinnin jälkeen solut sekoitetaan varovasti 10 ml:n väliaineella niiden resuspendoimiseksi ja sentrifugoidaan sitten 300xg:n nopeudella 3 minuutin ajan. Hävitä supernatantti, suspendoi solut uudelleen tuoreessa väliaineessa ja siirrä ne uusiin pulloihin, jotka sisältävät jo tuoretta väliaineita. |
| Jäädytä väliaine | Kryosäilytysmediana käytämme 90 % FBS + 10 % DMSO:ta elinkelpoisuuden ylläpitämiseksi tai CM-1:tä (Cytionin luettelonumero 800100), joka sisältää optimoituja osmoprotectantteja ja metabolisia stabilisaattoreita, jotka parantavat elpymistä ja vähentävät kryosäilytyksen aiheuttamaa stressiä. |
| Solujen sulattaminen ja viljely |
|
| Inkubaatioilmapiiri | 37 °C, 5 %CO2, kostutettu ilmakehä. |
| Pullon pinnoite | Optimaalisen kiinnittymisen ja elinkelpoisuuden saavuttamiseksi sulatuksen jälkeen suosittelemme kollageenipinnoitettujen pullojen tai levyjen käyttöä. |
| Jäädytysmenettely | Kryosäilytetyt solulinjat kuljetetaan kuivajäässä validoidussa, eristetyssä pakkauksessa, jossa on riittävästi kylmäainetta, jotta lämpötila pysyy noin -78 °C:ssa koko kuljetuksen ajan. Pakkaus on tarkastettava välittömästi sen vastaanottamisen jälkeen ja injektiopullot on siirrettävä viipymättä asianmukaiseen varastoon. |
| Toimitusehdot | Kryosäilytetyt solulinjat kuljetetaan kuivajäässä validoidussa, eristetyssä pakkauksessa, jossa on riittävästi kylmäainetta, jotta lämpötila pysyy noin -78 °C:ssa koko kuljetuksen ajan. Pakkaus on tarkastettava välittömästi sen vastaanottamisen jälkeen ja injektiopullot on siirrettävä viipymättä asianmukaiseen varastoon. |
| Varastointiolosuhteet | Pitkäaikaissäilytystä varten injektiopullot asetetaan höyryfaasissa olevaan nestemäiseen typpeen noin -150 - -196 °C:een. Säilytys -80 °C:ssa on hyväksyttävää vain lyhyenä välivaiheena ennen siirtoa nestemäiseen typpeen. |
Laadunvalvonta / Geneettinen profiili / HLA
| Steriliteetti | Mykoplasmakontaminaatio suljetaan pois sekä PCR-pohjaisilla määrityksillä että luminesenssiin perustuvilla mykoplasman osoitusmenetelmillä. Bakteeri-, sieni- tai hiivakontaminaation välttämiseksi soluviljelmät tarkastetaan päivittäin silmämääräisesti. |
|---|
Materiaalin siirtosopimus
Jos aiot käyttää Cytion-solulinjoja yksinomaan sisäiseen tutkimukseen yhdellä tutkimuspaikalla, täytä ja allekirjoita materiaalinsiirtosopimus (MTA) ja lähetä se tilauksesi mukana.
Kaikissa kaupallisissa sovelluksissa – mukaan lukien mutta ei rajoittuen maksullisiin palveluihin, laadunvalvontatestaukseen, tuotteiden julkaisemiseen, diagnostiseen käyttöön tai sääntelytutkimuksiin – täytä käyttötarkoituksen lomake, jotta voimme laatia projektiisi sopivan sopimuksen.
Huomaa: MTA koskee vain tiettyjä solulinjoja. Jos tämä ilmoitus ja MTA-asiakirja näkyvät tuotesivulla, sopimus on voimassa. Solulinjoille, joita MTA ei koske, sopimusta ei mainita. MTA ei ole voimassa asiakkaille Amerikassa, Kiinassa tai Taiwanissa. Ota yhteyttä Yhdysvaltain yksikköömme saadaksesi sopivan sopimuksen.
