FAMPAC-solut












800,00 €*
Tuotteet toimitetaan jäädytettyinä kuivajäässä kryoputkissa. Jokainen kryoputki sisältää tyypillisesti 3 × 10 6 solua adheesiivisille soluille tai 5 × 106 solua suspensiosoluille (katso lisätietoja erän CoA-todistuksesta).
Yleisiä tietoja
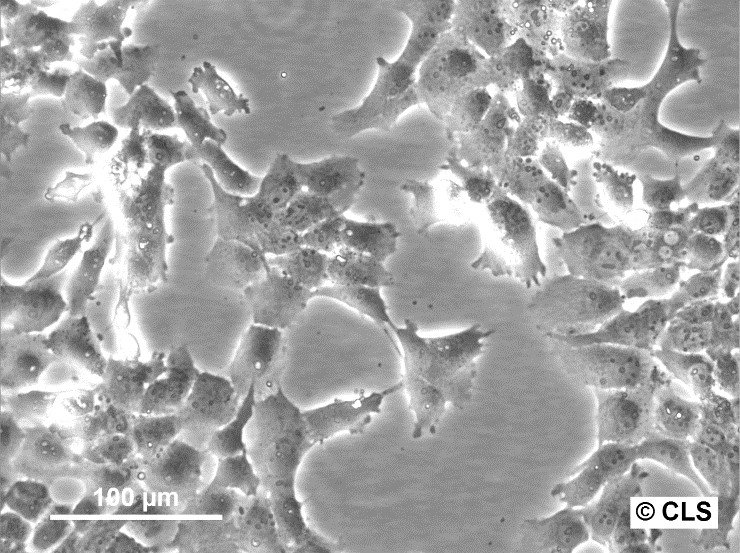
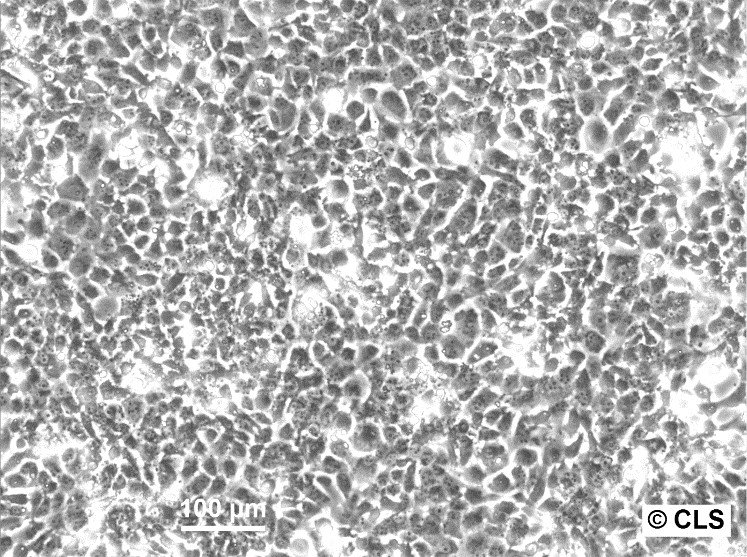
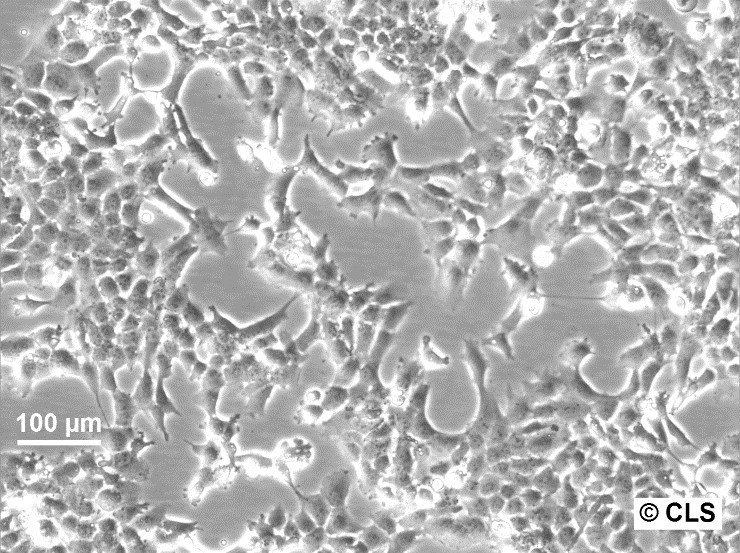
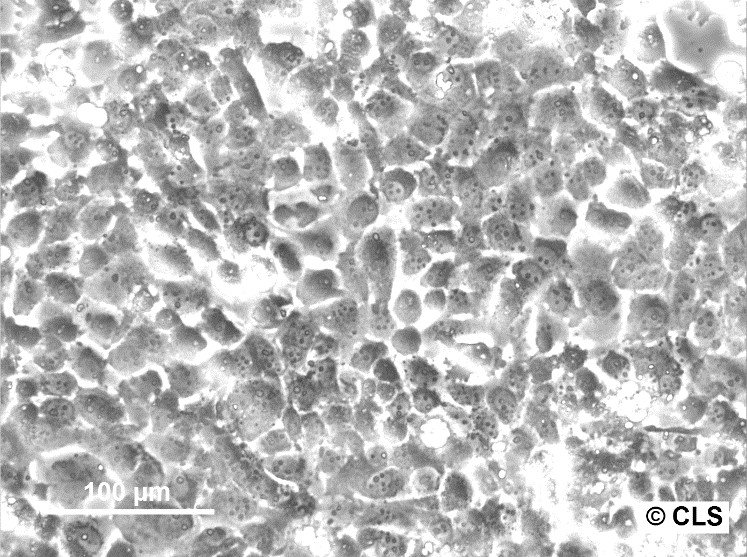
| Kuvaus | Fampac-solulinja perustettiin aikuisen naisen primaarisesta haiman adenokarsinoomasta, jolla oli familiaalinen alttius haimasyöpään. Nämä solut ovat luonteeltaan epiteelisoluja, ja niitä on hyödynnetty laajalti tutkimuksessa, jossa on keskitytty haimasyövän biologiseen käyttäytymiseen, mukaan lukien kasvaimen etenemistä, etäpesäkkeiden muodostumista ja terapeuttista vastetta koskevat tutkimukset. Fampac-solulinja tunnetaan aggressiivisesta kasvainten muodostuskyvystään ksenograft-malleissa, mikä tekee siitä arvokkaan in vivo -tutkimuksissa, jotka liittyvät lääkkeiden tehoon ja syöpäsolujen biologiaan. In vitro Fampac-soluilla on haiman adenokarsinoomalle tyypillisiä ominaisuuksia, kuten vastustuskyky apoptoosille ja kyky lisääntyä kemiallisesti määritellyissä olosuhteissa. Tämä resistenssi ohjelmoitua solukuolemaa vastaan on kriittinen ominaisuus tutkimuksissa, joissa pyritään tutkimaan uusia kemoterapeuttisia aineita ja niiden mahdollisuuksia aiheuttaa syöpäsolujen kuolemaa. Lisäksi Fampac-soluja on käytetty haimasyövän patogeneesin molekyylimekanismien tutkimiseen, mikä antaa tietoa geneettisistä mutaatioista, syövän lisääntymiseen liittyvistä signaalireiteistä ja vuorovaikutuksesta kasvaimen mikroympäristön kanssa. |
|---|---|
| Organismi | Ihminen |
| Kudos | Haima |
| Tauti | Adenokarsinooma |
| Synonyymit | FamPAC, Fampac, PA-CLS-13, PA-CLS 13, PA-CLS 13 |
Ominaisuudet
| Ikä | 43 vuotta |
|---|---|
| Sukupuoli | Nainen |
| Etnisyys | Kaukasialainen |
| Morfologia | Epiteelin kaltainen |
| Kasvuominaisuudet | Tarttuva |
Sääntelytiedot
| Viittaus | FAMPAC (Cytionin luettelonumero 300309) |
|---|---|
| Bioturvallisuustaso | 1 |
| NCBI_TaxID | 9606 |
| CellosaurusLiittyminen | CVCL_5749 |
Biomolekyylitiedot
| Proteiinin ilmentyminen | P53, pistemutaatio (CCG (Arg) - CAC (His)) |
|---|---|
| Antigeenin ilmentyminen | FAMPAC-soluissa on homotsygoottinen Kras-mutaatio kodonissa 12: GGT(Gly) >GTT(Val) |
| Tumorigeeninen | Kyllä, alastomilla hiirillä, adenokarsinooma |
| Karyotyyppi | 45-48, x,+3,-5,+der(5),+der(5),+der(5)add(p14),-7,+10,+2der(10)add(p15)add(q26),der(12)add(p13),der(12)add(p11),-13,-13,+der(13)add(p11),-14,der?(14),-15,i(15q),der(16)(q+),-19,-20,-21,-22,+3-5mar |
Käsittely
| Viljelyalusta | RPMI 1640, w: 2,0 mM stabiilia glutamiinia, w: 2,0 g/L NaHCO3 (Cytionin artikkelinumero 820700a) |
|---|---|
| Lisäravinteet | Täydennetään elatusainetta 10 %:lla FBS:llä |
| Dissosiaatioreagenssi | Accutase |
| Kaksinkertaistumisaika | 24-48 tuntia |
| Alakulttuuri | Poista vanha väliaine tarttuneista soluista ja pese ne PBS:llä, josta puuttuu kalsiumia ja magnesiumia. Käytä T25-pulloissa 3-5 ml PBS:ää ja T75-pulloissa 5-10 ml. Peitä sitten solut kokonaan Accutase-valmisteella, käyttäen 1-2 ml T25-pulloissa ja 2,5 ml T75-pulloissa. Anna solujen inkuboitua huoneenlämmössä 8-10 minuuttia solujen irtoamiseksi. Inkuboinnin jälkeen solut sekoitetaan varovasti 10 ml:n väliaineella niiden resuspendoimiseksi ja sentrifugoidaan sitten 300xg:n nopeudella 3 minuutin ajan. Hävitä supernatantti, suspendoi solut uudelleen tuoreessa väliaineessa ja siirrä ne uusiin pulloihin, jotka sisältävät jo tuoretta väliaineita. |
| Kylvötiheys | 1 x 104 solua/cm2 tuottaa yhtenäisen kerroksen noin 2–3 päivässä. |
| Nesteen uusiminen | 2-3 kertaa viikossa |
| Jäädytä väliaine | Kryosäilytysmediana käytämme täydellistä kasvualustaa (mukaan lukien FBS) + 10 % DMSO:ta riittävän sulatuksen jälkeisen elinkelpoisuuden varmistamiseksi tai CM-1:tä (Cytionin luettelonumero 800100), joka sisältää optimoituja osmoprotectantteja ja metabolisia stabilisaattoreita, jotka parantavat elpymistä ja vähentävät kryosäilytyksen aiheuttamaa stressiä. |
| Solujen sulattaminen ja viljely |
|
| Inkubaatioilmapiiri | 37 °C, 5 %CO2, kostutettu ilmakehä. |
| Pullon pinnoite | Optimaalisen kiinnittymisen ja elinkelpoisuuden saavuttamiseksi sulatuksen jälkeen suosittelemme kollageenipinnoitettujen pullojen tai levyjen käyttöä. |
| Jäädytysmenettely | Kryosäilytetyt solulinjat kuljetetaan kuivajäässä validoidussa, eristetyssä pakkauksessa, jossa on riittävästi kylmäainetta, jotta lämpötila pysyy noin -78 °C:ssa koko kuljetuksen ajan. Pakkaus on tarkastettava välittömästi sen vastaanottamisen jälkeen ja injektiopullot on siirrettävä viipymättä asianmukaiseen varastoon. |
| Toimitusehdot | Kryosäilytetyt solulinjat kuljetetaan kuivajäässä validoidussa, eristetyssä pakkauksessa, jossa on riittävästi kylmäainetta, jotta lämpötila pysyy noin -78 °C:ssa koko kuljetuksen ajan. Pakkaus on tarkastettava välittömästi sen vastaanottamisen jälkeen ja injektiopullot on siirrettävä viipymättä asianmukaiseen varastoon. |
| Varastointiolosuhteet | Pitkäaikaissäilytystä varten injektiopullot asetetaan höyryfaasissa olevaan nestemäiseen typpeen noin -150 - -196 °C:een. Säilytys -80 °C:ssa on hyväksyttävää vain lyhyenä välivaiheena ennen siirtoa nestemäiseen typpeen. |
Laadunvalvonta / Geneettinen profiili / HLA
| Steriliteetti | Mykoplasmakontaminaatio suljetaan pois sekä PCR-pohjaisilla määrityksillä että luminesenssiin perustuvilla mykoplasman osoitusmenetelmillä. Bakteeri-, sieni- tai hiivakontaminaation välttämiseksi soluviljelmät tarkastetaan päivittäin silmämääräisesti. |
|---|---|
| HLA-alleelit |
A*: '03:01:01
B*: '27:05:01
C*: '15:02:01
DRB1*: '12:01:01
DQA1*: '05:05:01
DQB1*: '03:01:01
DPB1*: '03.01:01
E: '01:01:01
|
Analyysitodistus (CoA)
| Erän numero | Todistuksen tyyppi | Päivämäärä | Luettelonumero |
|---|---|---|---|
| 300309-720 | Analyysitodistus | 23. May. 2025 | 300309 |
Materiaalin siirtosopimus
Jos aiot käyttää Cytion-solulinjoja yksinomaan sisäiseen tutkimukseen yhdellä tutkimuspaikalla, täytä ja allekirjoita materiaalinsiirtosopimus (MTA) ja lähetä se tilauksesi mukana.
Kaikissa kaupallisissa sovelluksissa – mukaan lukien mutta ei rajoittuen maksullisiin palveluihin, laadunvalvontatestaukseen, tuotteiden julkaisemiseen, diagnostiseen käyttöön tai sääntelytutkimuksiin – täytä käyttötarkoituksen lomake, jotta voimme laatia projektiisi sopivan sopimuksen.
Huomaa: MTA koskee vain tiettyjä solulinjoja. Jos tämä ilmoitus ja MTA-asiakirja näkyvät tuotesivulla, sopimus on voimassa. Solulinjoille, joita MTA ei koske, sopimusta ei mainita. MTA ei ole voimassa asiakkaille Amerikassa, Kiinassa tai Taiwanissa. Ota yhteyttä Yhdysvaltain yksikköömme saadaksesi sopivan sopimuksen.
