Medios de cultivo celular: Una visión general
En el campo de las ciencias de la vida, una de las metodologías más importantes es el cultivo celular. La extracción de células, tejidos u órganos de un animal o una planta y su posterior implantación en un entorno artificial favorable para su supervivencia y/o crecimiento es lo que se entiende por "cultivo celular" Las necesidades ambientales fundamentales para un desarrollo celular óptimo son una temperatura controlada, un sustrato para la fijación de las células, un medio de crecimiento adecuado y una incubadora que mantenga el pH y la osmolalidad óptimos. Las células deben disponer de estas condiciones para crecer en todo su potencial.
La selección de un medio de crecimiento adecuado para el cultivo in vitro es la fase más crítica y vital del cultivo celular. Un medio de crecimiento, también conocido como medio de cultivo, es un líquido o gel formulado para favorecer el desarrollo de los organismos a escala microscópica, celular o vegetal. El medio utilizado para cultivar células suele contener un aporte adecuado de energía y sustancias que controlan el ciclo celular. Los principales componentes de un medio de cultivo incluyen aminoácidos, vitaminas, sales inorgánicas, glucosa y suero. El suero se añade al medio porque actúa como fuente de factores de crecimiento, hormonas y factores de fijación. Además de proporcionar nutrientes, el medio también contribuye a mantener los niveles de pH y osmolalidad.
Tipos de medio utilizados en el cultivo celular
Tanto las células humanas como las animales pueden cultivarse en un medio artificial o sintético o en un medio totalmente natural que se complemente con elementos naturales. A continuación, le ofrecemos una visión general de los diferentes tipos de medios disponibles en la actualidad.
Medios naturales
En los medios naturales sólo pueden encontrarse fluidos biológicos que existan en su estado natural. Los medios naturales son muy útiles y fáciles para el cultivo de una amplia variedad de tipos de células animales. La falta de comprensión de los componentes precisos que constituyen los medios naturales es el principal factor que contribuye a la baja repetibilidad de los resultados obtenidos utilizando medios naturales.
Medios artificiales
La preparación de medios artificiales o sintéticos implica la adición de nutrientes (tanto orgánicos como inorgánicos), proteínas séricas, carbohidratos, cofactores, vitaminas y sales, así como fases gaseosas de O2 y CO2 [1].
Se han desarrollado varios tipos de medios artificiales para cumplir una o varias de las siguientes funciones: 1) Supervivencia inmediata (una solución salina equilibrada con un pH y una presión osmótica precisos). 2) Supervivencia prolongada (una solución salina equilibrada complementada con diferentes formulaciones de productos químicos orgánicos y/o suero). 3) Desarrollo indefinido. 4) Funciones especializadas.
Existen cuatro clasificaciones distintas para los medios artificiales:
Medios que contienen suero
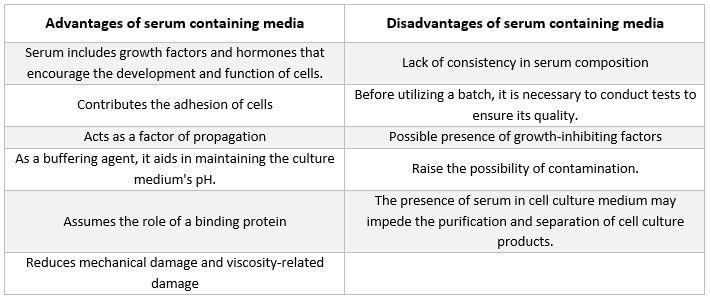
El tipo de suplemento más frecuente en los medios utilizados para el cultivo de células animales es el suero fetal bovino. Se añade al medio de cultivo como suplemento de bajo coste para conseguir las mejores condiciones de crecimiento posibles. Además de actuar como transportador o quelante de nutrientes inestables o insolubles en agua, hormonas y factores de crecimiento, inhibidores de proteasas y otras sustancias, el suero también fija y neutraliza moléculas nocivas.
Medio sin suero
La presencia de suero en los medios presenta una serie de desventajas y tiene el potencial de causar importantes errores de interpretación en la investigación inmunológica [2, 3]. Se han creado diversos medios sin suero [4, 5]. Por lo general, estos medios están formulados específicamente para el cultivo de un único tipo celular, como el Knockout Serum Replacement y el Knockout DMEM de Thermo Fisher Scientific, y el medio mTESR de Stem Cell Technologies [6], para células madre [7].
Además, estos medios incorporan cantidades definidas de factores de crecimiento purificados, lipoproteínas y otras proteínas, que de otro modo son típicamente proporcionadas por el suero [8]. Estos medios suelen denominarse "medios de cultivo definidos", ya que los componentes que los componen se conocen bien.
Medios químicamente definidos
Estos medios incluyen componentes inorgánicos y orgánicos ultrapuros que no han sufrido ningún tipo de contaminación. También pueden incluir adiciones de proteínas puras, como factores de crecimiento.
la modificación genética de bacterias o levaduras, junto con la adición de determinados ácidos grasos, vitaminas, colesterol y aminoácidos, da lugar a la producción de sus componentes [9].
Medios sin proteínas
Los medios sin proteínas son aquellos que no incluyen ninguna proteína en absoluto y, en su lugar, sólo incluyen elementos no proteicos. En comparación con los medios con suero añadido, el uso de medios sin proteínas añadidas promueve una mayor proliferación celular y expresión de proteínas y facilita la purificación de cualquier producto generado en un proceso posterior [10-12]. Las proteínas no se incluyen en formulaciones como MEM y RPMI-1640. Sin embargo, podría administrarse un suplemento proteico si fuera necesario.
Medio de cultivo y sus componentes básicos
Los medios de cultivo comerciales pueden adquirirse en forma de polvo o de líquido y suelen incluir diversos nutrientes como aminoácidos, glucosa, sales, vitaminas y otros suplementos dietéticos.
Las necesidades de estos componentes son diferentes para cada línea celular, y estas variaciones son responsables del gran número de formulaciones diferentes de medios. Cada componente es responsable de una función determinada, que se describirá en los párrafos siguientes:
Sistemas tampón
Para mantener unas condiciones de crecimiento óptimas, es necesario controlar el pH, lo que suele hacerse mediante uno de los dos sistemas de amortiguación siguientes:
Sistema tampón natural
La relación CO2/H2CO3 en la atmósfera es igual a la del medio, lo que crea un mecanismo natural de amortiguación. Para preservar su mecanismo de amortiguación natural, los cultivos deben mantenerse en un entorno de aire con un 5-10% de CO2, lo que a menudo se consigue utilizando una incubadora de CO2. Una de las mejores ventajas de utilizar un tampón natural es que es barato y seguro.
HEPES
La amortiguación química mediante el zwitterion HEPES tiene una mayor capacidad de amortiguación en el intervalo de pH de 7,2-7,4 y no necesita un entorno gaseoso regulado. Para determinados tipos de células, una dosis mayor de HEPES puede ser perjudicial. Asimismo, los medios que contienen HEPES son mucho más susceptibles a los efectos fototóxicos de la luz fluorescente [13].
Rojo de fenol
El indicador de pH rojo fenol se incluye a menudo en los medios de cultivo disponibles en el mercado, lo que permite una monitorización continua del pH. Al expandir las células, los metabolitos producidos por éstas provocan un cambio en el pH y, por tanto, un cambio de color del medio. El rojo de fenol tiene un doble efecto sobre el color de un medio, volviéndolo amarillo a pH ácido y púrpura a pH alcalino. pH 7,4, el valor óptimo para el cultivo celular, hace que el medio aparezca de color rojo fluorescente.
Pero el rojo de fenol tiene algunos inconvenientes: En primer lugar, el rojo de fenol es capaz de simular la actuación de una serie de hormonas esteroideas, principalmente el estrógeno [14]. Por lo tanto, cuando se estudian células sensibles a los estrógenos, como el tejido mamario, se recomienda un medio sin rojo de fenol. El equilibrio sodio-potasio se ve alterado por la presencia de rojo fenol en varias formulaciones libres de suero. La adición de suero u hormona pituitaria bovina al medio puede contrarrestar este efecto [15]. En tercer lugar, la presencia de rojo de fenol dificulta la detección en experimentos de citometría de flujo.
Sales inorgánicas
Los medios que contienen sales inorgánicas, como iones de sodio, potasio y calcio, ayudan a mantener el equilibrio osmótico y regulan el potencial de membrana.
Aminoácidos
Dado que los aminoácidos son los componentes fundamentales de las proteínas, son un componente esencial de todos y cada uno de los medios de crecimiento celular que se han concebido. Dado que las células son incapaces de producir ciertos aminoácidos por sí mismas, es importante que el medio de cultivo incluya aminoácidos esenciales. Son necesarios para la proliferación de las células, y la concentración a la que están presentes determina la densidad celular máxima que puede alcanzarse. En particular, la L-glutamina, un aminoácido esencial, es especialmente crucial.
La L-glutamina funciona como fuente secundaria de energía para el metabolismo y contribuye con nitrógeno a la producción de NAD, NADPH y nucleótidos. Debido al hecho de que la L-glutamina es un aminoácido inestable que, con el tiempo, cambia a una forma que las células son incapaces de utilizar, debe aportarse al medio.
Además, pueden aportarse al medio aminoácidos no esenciales para reponer los que se hayan consumido a lo largo del proceso de crecimiento. El crecimiento de las células se potencia y su viabilidad aumenta cuando el medio de crecimiento se complementa con aminoácidos no esenciales.
Carbohidratos
Los hidratos de carbono en forma de azúcares son la principal fuente de energía. Muchos de los medios también incluyen maltosa y fructosa, además de los azúcares más comunes de glucosa y galactosa.
Proteínas y péptidos
Las proteínas y los péptidos más utilizados son la albúmina, la transferrina y la fibronectina, que son especialmente importantes en los medios que no incluyen suero. La albúmina, la transferrina, la aprotinina, la fetuina y la fibronectina son algunas de las proteínas que pueden encontrarse en el suero, que es una fuente rica en proteínas.
La albúmina es la principal proteína que se encuentra en la sangre, y su función es unir y transportar diversas sustancias, como agua, sales, ácidos grasos libres, hormonas y vitaminas, entre distintos órganos y células. La capacidad de la albúmina para unirse a sustancias químicas la convierte en una candidata eficaz para eliminar compuestos nocivos del medio en el que se cultivan las células.
La aprotinina es un agente protector en los sistemas de cultivo celular, ya que es estable a pH neutro y ácido, así como resistente a las altas temperaturas y a la destrucción que pueden causar las enzimas proteolíticas. Es capaz de inhibir varias serina proteasas, incluida la tripsina, entre otras.
La fetuina es una glicoproteína que puede detectarse en mayores cantidades en el suero de animales fetales y recién nacidos en comparación con el suero de adultos. Además, actúa como inhibidor de la serina proteasa. La proteína fibronectina es un componente esencial en el proceso de adhesión celular. La transferrina es una proteína que transporta hierro y se encarga de llevarlo a las membranas de las células.
Ácidos grasos y lípidos
Desempeñan un papel crucial en el medio libre de suero cuando éste está ausente.
Vitaminas
Numerosas vitaminas son necesarias para el desarrollo y la proliferación celular. Las células no pueden producir las vitaminas en cantidades adecuadas, por lo que son esenciales en el cultivo de tejidos como suplementos dietéticos.
En el cultivo celular, el suero es la principal fuente de vitaminas; sin embargo, los medios también se tratan con diversas vitaminas para adecuarlos a un tipo celular específico. Normalmente, las vitaminas del grupo B se utilizan para estimular el crecimiento.
Oligoelementos
Elementos químicos como el cobre, el zinc, el selenio y los intermediarios del ácido tricarboxílico se conocen como oligoelementos. Los oligoelementos se añaden a menudo a los medios que no incluyen suero para sustituir a los que suelen estar presentes en el suero. Estos elementos son componentes químicos importantes necesarios para un desarrollo celular sano. Muchas reacciones bioquímicas dependen de ciertos micronutrientes, como la actividad enzimática.
Suplementos del medio
El medio de crecimiento completo sugerido para ciertas líneas celulares necesita componentes adicionales que están ausentes en los medios de base y en el suero. Estos suplementos alimenticios favorecen el crecimiento celular y la función metabólica adecuada.
Aunque las hormonas, los factores de crecimiento y las moléculas de señalización son esenciales para la proliferación adecuada de determinadas líneas celulares, siempre deben tomarse las siguientes precauciones: Dado que la adición de suplementos podría alterar la osmolalidad del medio de crecimiento completo, lo que puede inhibir el desarrollo celular, siempre es aconsejable verificar la osmolalidad después de añadir suplementos. Para la mayoría de las líneas celulares, la osmolalidad óptima oscila entre 260 y 320 mOSM/kg.
Antibióticos
Los antibióticos se emplean a menudo para inhibir el desarrollo de contaminantes bacterianos y fúngicos [16], aunque no son esenciales para el crecimiento celular. Dado que los antibióticos podrían ocultar la contaminación por micoplasmas y bacterias resistentes, no se sugiere su uso rutinario para el cultivo celular [17, 18].
Además, los antibióticos pueden alterar el metabolismo de las células hipersensibles. A menudo se utilizan las combinaciones de penicilina y estreptomicina fabricadas por MilliporeSigma y Life Technologies. La plasmocina se ha utilizado en el cultivo de las líneas celulares de glioma TS603, TS516 y BT260 [19], y ha demostrado ser eficaz para eliminar la contaminación por micoplasma (20).
Suero
El suero contiene albúminas, factores de crecimiento e inhibidores del crecimiento. El suero es uno de los componentes más importantes del medio de cultivo celular porque proporciona aminoácidos, proteínas, vitaminas (especialmente vitaminas liposolubles como la A, D, E y K), hidratos de carbono, lípidos, hormonas, factores de crecimiento, minerales y oligoelementos.
El suero procedente de fuentes fetales y de terneros bovinos se utiliza a menudo para promover el desarrollo de las células cultivadas. El suero fetal es un suministro abundante de factores de crecimiento y es adecuado para la clonación celular y el desarrollo de células sensibles. Debido a su menor capacidad para promover el crecimiento, el suero de ternera se emplea en experimentos de inhibición por contacto. Los medios de crecimiento normales suelen incluir entre un 2% y un 10% de suero. La adición de suero al medio de cultivo tiene las siguientes finalidades [21]:
-
El suero aporta los nutrientes esenciales para las células (tanto en solución como unidos a proteínas).
-
El suero incluye varios factores de crecimiento y hormonas que intervienen en la promoción del crecimiento y la actividad celular especializada.
-
Ofrece muchas proteínas de unión, como la albúmina y la transferrina, que transportan otras sustancias químicas al interior de la célula. Por ejemplo, la albúmina transporta grasas, vitaminas, hormonas, etc. al interior de las células.
-
También aporta proteínas, como la fibronectina, que aumentan la adhesión celular al sustrato. Además, produce elementos esparcidores que ayudan a la expansión celular antes de la división.
-
Aporta inhibidores de la proteasa que impiden la proteólisis en las células.
-
También contiene minerales como Na+, K+, Zn2+ y Fe2+.
-
Aumenta la viscosidad del medio, por lo que protege a las células de lesiones mecánicas durante la agitación del cultivo en suspensión.
-
También es un tampón.
Referencias
[1] Morgan J, Morton H, Parker R. Nutrition of animal cells in tissue culture; initial studies on a synthetic medium. Proc Soc Exp Biol Med. 1950;73:1-8
[2] Kerbel R, Blakeslee D. Rapid adsorption of a foetal calf serum component by mammalian cells in culture. A potential source of artifacts in studies of antisera to cell-specific antigens. Immunology. 1976;31:881-91
[3] Sula K, Draber P, Nouza K. Addition of serum to the medium used for preparation of cell suspensions as a possible source of artifacts in cell-mediated reactions studied by means of the popliteal lymph node test. J Immunogenet. 1980;7:483-9
[4] Mariani E, Mariani A, Monaco M, Lalli E, Vitale M, Facchini A. Commercial serum-free media: hybridoma growth and monoclonal antibody production. J Immunol Methods. 1991;145:175-83
[5] Barnes D, Sato G. Methods for growth of cultured cells in serum-free medium. Anal Biochem. 1980;102:255-70
[6] Yu H, Lu S, Gasior K, Singh D, Vazquez Sanchez S, Tapia O,et al. HSP70 chaperones RNA-free TDP-43 into anisotropic intranuclear liquid spherical shells. Science. 2021;371:
[7] Meharena H, Marco A, Dileep V, Lockshin E, Akatsu G, Mullahoo J,et al. Down-syndrome-induced senescence disrupts the nuclear architecture of neural progenitors. Cell Stem Cell. 2022;29:116-130.e7
[8] Iscove N, Melchers F. Complete replacement of serum by albumin, transferrin, and soybean lipid in cultures of lipopolysaccharide-reactive B lymphocytes. J Exp Med. 1978;147:923-33
[9] Stoll T, Muhlethaler K, von Stockar U, Marison I. Systematic improvement of a chemically-defined protein-free medium for hybridoma growth and monoclonal antibody production. J Biotechnol. 1996;45:111-23
[10] Darfler F. A protein-free medium for the growth of hybridomas and other cells of the immune system. In Vitro Cell Dev Biol. 1990;26:769-78
[11] Barnes D, Sato G. Cultivo celular sin suero: un enfoque unificador. Cell. 1980;22:649-55
[12] Hamilton W, Ham R. Clonal growth of chinese hamster cell lines in protein-free media. In Vitro. 1977;13:537-47
[13] Zigler J, Lepe Zuniga J, Vistica B, Gery I. Analysis of the cytotoxic effects of light-exposed HEPES-containing culture medium. In Vitro Cell Dev Biol. 1985;21:282-7
[14] Berthois Y, Katzenellenbogen J, Katzenellenbogen B. Phenol red in tissue culture media is a weak estrogen: implications concerning the study of estrogen-responsive cells in culture. Proc Natl Acad Sci U S A. 1986;83:2496-500
[15] Karmiol S. Development of serum free media. In: Master JRW, editor. Animal Cell culture, 3rd ed. Oxford:Oxford University Press; 2000.
[16] Perlman D. Use of antibiotics in cell culture media. Methods Enzymol. 1979;58:110-6
[17] McGarrity G. Spread and control of mycoplasmal infection of cell cultures. In Vitro. 1976;12:643-8
[18] Masters J, Stacey G. Changing medium and passaging cell lines. Nat Protoc. 2007;2:2276-84
[19] Chakraborty A, Laukka T, Myllykoski M, Ringel A, Booker M, Tolstorukov M,et al. La histona desmetilasa KDM6A detecta directamente el oxígeno para controlar la cromatina y el destino celular. Science. 2019;363:1217-1222
[20] Molla Kazemiha V, Azari S, Amanzadeh A, Bonakdar S, Shojaei Moghadam M, Habibi Anbouhi M,et al. Eficacia de Plasmocin™ en varias líneas celulares de mamíferos infectadas por mollicutes en comparación con antibióticos de uso común en cultivo celular: una experiencia local. Cytotechnology. 2011;63:609-20
[21] Kragh Hansen U. Molecular aspects of ligand binding to serum albumin. Pharmacol Rev. 1981;33:17-53