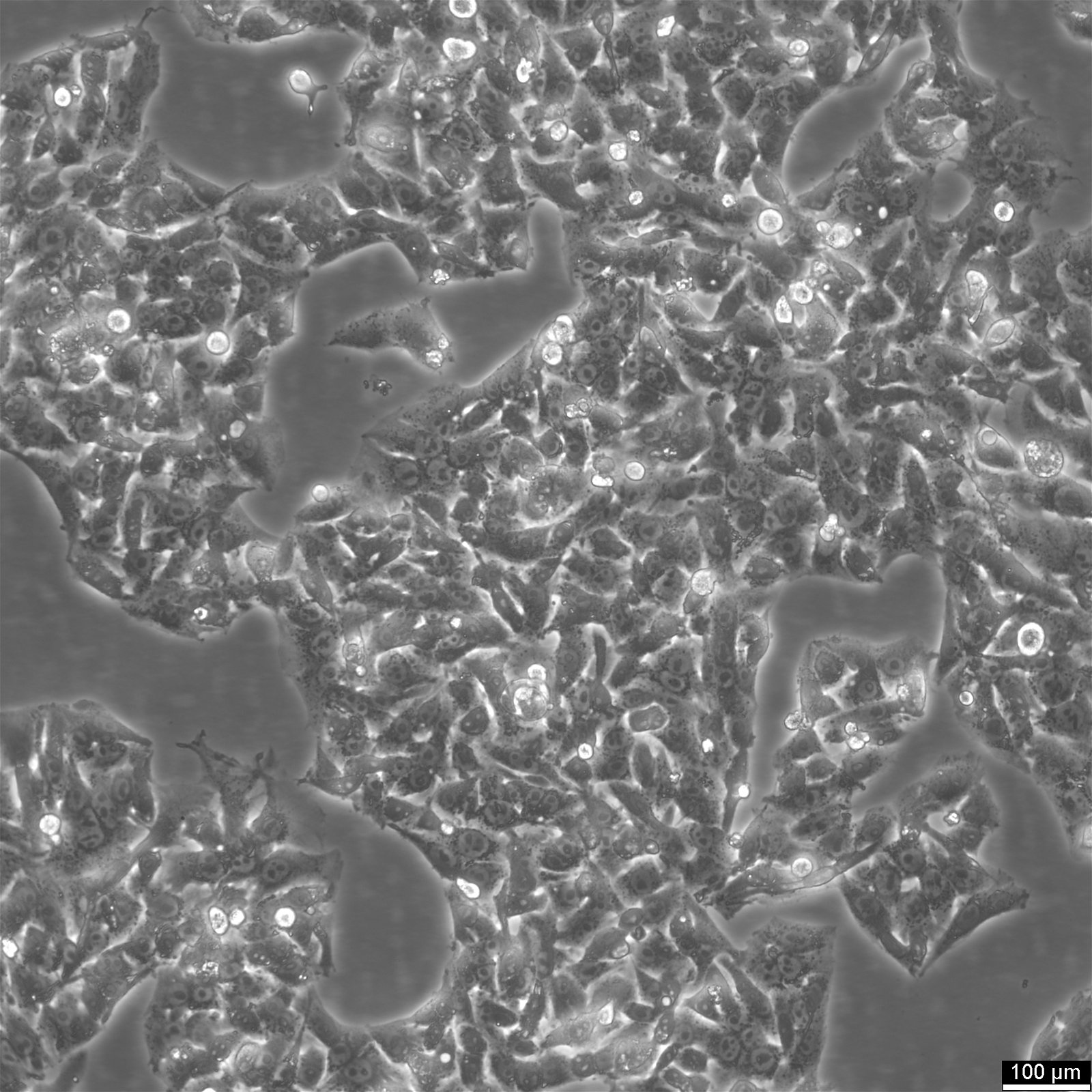
HepG2-Zellen - eine Ressource für die Leberkrebsforschung
Hep-G2 ist eine menschliche Leberkrebszelllinie, die aus dem Lebergewebe eines 15-jährigen kaukasischen Mannes mit hepatozellulärem Karzinom stammt. Diese Zellen werden häufig in Studien zum Arzneimittelmetabolismus und zur Hepatotoxizität verwendet. Obwohl HepG2-Zellen eine hohe Proliferationsrate und ein epithelähnliches Aussehen haben, sind sie nicht tumorigen und erfüllen verschiedene differenzierte Leberfunktionen. HepG2-Zellen wurden 1975 aus hepatozellulären Karzinomen gewonnen und waren damit die erste hepatische Zelllinie, die die entscheidenden Merkmale von Hepatozyten aufwies. Im Gegensatz zur zuvor etablierten SK-Hep1-Zelllinie, der wesentliche Leberzellmarker fehlen, können HepG2-Zellen verschiedene Plasmaproteine sezernieren und sind ein wertvolles Modell für die Untersuchung der intrazellulären Dynamik von Zelloberflächendomänen in menschlichen Hepatozyten. Diese Zellen weisen eine epithelähnliche Morphologie auf, haben eine modale Chromosomenzahl von 55 und können mit menschlichem Wachstumshormon stimuliert werden
HepG2 Merkmale
Primäre Hepatozyten haben eine typische kubische Form und enthalten in der Regel zwei Zellkerne. Im Gegensatz dazu haben HepG2-Zellen eine epithelähnliche Morphologie mit einem einzigen Zellkern und einer Chromosomenzahl von 48 bis 54 pro Zelle. Obwohl HepG2-Zellen bis zu 25 % des gesamten zellulären Proteins ausmachen können, sind sie größer als normale Hepatozyten und machen etwa 10 % des gesamten Proteins in der Zelle aus. Zelluläre Proteine sind entscheidende Akteure innerhalb der Zelle, die die von den Genen festgelegten Funktionen ausführen.
Tumorzellen, auch solche mit einer abnormen Chromosomenzahl, weisen oft eine erhöhte Anzahl von Kernen auf, bis zu sieben pro Zelle. Aufgrund ihres hohen Differenzierungsgrades in vitro sind HepG2-Zellen ein ideales Modell für die Untersuchung des intrazellulären Transports und der Dynamik von Proteinen der Gallenkanälchen, der Sinusoidmembran und von Lipiden in menschlichen Hepatozyten.
Der durchschnittliche Durchmesser einer HepG2-Zelle beträgt etwa 10-20 µm und ist damit kleiner als der eines Hepatozyten mit einem Durchmesser von 15 µm, aber ähnlich wie bei Tumorzellen des Hepatoblastoms (HB), die 10-20 µm groß sind.
Genetik von HepG2
Die Hep-G2-Zelllinie weist mehrere Translokationen auf, u. a. zwischen den kurzen Armen der Chromosomen 1 und 21, Trisomien der Chromosomen 2, 16 und 17 sowie eine Tetrasomie des Chromosoms 20. Auch der Verlust der Chromosomenregion 4q3 wird beobachtet, der mit der Translokation t(1;4), die häufig beim Hepatoblastom (HB) auftritt, und anderen Chromosomenanomalien wie den Trisomien 2 und 20 einhergeht. Die Anzahl der Chromosomen in HepG2-Zellen liegt zwischen 50 und 60, was auf einen hyperdiploiden Karyotyp hinweist, während einige Fälle mehr als 100 Chromosomen aufweisen und durch eine tetraploide Vergrößerung gekennzeichnet sind. HepG2-Zellen enthalten etwa 7,5 pg DNA, 15 % mehr als eine durchschnittliche somatische Zelle. Im Vergleich dazu haben primäre Hepatozyten eine kubische Zellform und enthalten typischerweise zwei Zellkerne [1].
Mutationsprofil von HepG2-Zellen
Die HepG2-Zelllinie trägt die Mutation C228T im Bereich des TERT-Promotors, die auch bei hepatozellulären Karzinomen (HCC) und Hepatoblastomen (HB) auftritt. Diese Mutation trägt zur Immortalisierung bei, indem sie die Telomere in Krebszellen schützt. Darüber hinaus weisen HepG2-Zellen den Wildtyp von TP53 auf, einem kritischen Gen für die Unterdrückung von Krebs beim Menschen, da es eine Rolle bei Zellzyklusstillstand, Apoptose und Alterung spielt. Mutationen in diesem Gen können die Zellproliferation fördern.
HepG2-Zellen sind an mehreren Signalwegen beteiligt, darunter die Dysregulation des Zellwachstums, Überlebenswege wie die fötale und embryonale HB und der Wnt/β-Catenin-Weg. Darüber hinaus weist die Zelllinie eine charakteristische Deletion des dritten Exons des CTNNB1-Gens auf, die mit der Deletion des epithelialen HB-Typs identisch ist [2,3].
Überblick über HepG2-Zellen des hepatozellulären Karzinoms in der Leberforschung
HepG2-Zellen, die aus einem menschlichen Hepatom stammen, sind zu einem unschätzbaren Werkzeug für die Erforschung von Leberfunktionen und -krankheiten, einschließlich des hepatozellulären Karzinoms, geworden. Diese Leberzelllinien bieten Einblicke in die zellulären Reaktionen menschlicher Hepatozyten unter verschiedenen Versuchsbedingungen. Die Verwendung von Luciferase-Reporterplasmiden in HepG2-Zellen hat sich als besonders effektiv für die Verfolgung der Genexpression und der Zelltransfektion erwiesen, die für die Stoffwechselforschung von grundlegender Bedeutung sind, z. B. für die Untersuchung der Auswirkungen von Ethanol auf Leberzellen
Studien zu Virusinfektionen und Leberkrankheiten mit HepG2-Zellen
Immortalisierte hepatische Tumorzelllinien wie HepG2 und Huh7 sind für die Untersuchung von Virusinfektionen unerlässlich, da sie eine vollständige Zellzyklusreplikation von Hepatitis D (HDV) und eine Expression von Hepatitis B (HBV) zeigen [5,6]. Parallel dazu spielen HepaRG-Zelllinien eine entscheidende Rolle bei der Aufklärung von HBV-Eintrittsmechanismen [7]. HepG2-Zellen werden auch zur Untersuchung verschiedener menschlicher Lebererkrankungen eingesetzt, von genetischen Erkrankungen wie der progressiven familiären intrahepatischen Cholestase (PFIC) und dem Dubin-Johnson-Syndrom bis hin zu Umwelt- und Ernährungsstudien im Zusammenhang mit zytotoxischen und genotoxischen Wirkstoffen sowie zur Erforschung von Medikamenten und Hepatokarzinogenese [8,9]. Ihr Einsatz erstreckt sich auch auf Versuche mit biokünstlichen Lebervorrichtungen
Wechselwirkungen von HepG2-Zellen mit Biomaterialien im Tissue Engineering
Die Interaktion von HepG2-Zellen mit verschiedenen Biomaterialien ist für die Gewebezüchtung von zentraler Bedeutung. Techniken wie die Kolloidsondentechnik helfen, diese Wechselwirkungen zu verstehen, indem sie die Adhäsionseigenschaften der Zellen messen, die für die Bestimmung der Lebensfähigkeit der Zellen bei der Entwicklung von Gerüsten und präzisen Lebergewebemodellen von entscheidender Bedeutung sind
Zellverhalten und Innovationen in HepG2-basierten Modellen
Die Untersuchung des Zellverhaltens in HepG2-basierten Modellen ist für die Erforschung von Lebererkrankungen entscheidend. Fortschritte bei dreidimensionalen Sphäroid-Zellkulturen haben zur Schaffung von HepG2-Zellsphäroiden geführt, die ein physiologisch relevanteres Modell bieten, das normalen Hepatozyten sehr ähnlich ist. Diese 3D-Modelle mit erhöhter Stoffwechselaktivität weisen auf das Potenzial von HepG2-Zellen hin, als Modell für Hepatoblastome zu dienen, und sind für die Krebsbehandlungsforschung von Bedeutung, insbesondere für die Simulation von Lebertumoren und die Erprobung neuer therapeutischer Ansätze [10-12]
Vergleich und Merkmale von HepG2 mit anderen Tumorzelllinien
HepG2 ist eine der am weitesten verbreiteten Lebertumor-Zelllinien, die aufgrund ihrer breiten Anwendung in der wissenschaftlichen Forschung unter den etwa 40 verfügbaren Lebertumor-Zelllinien ausgewählt wurde [13]. Trotz der schwachen oder fehlenden Expression bestimmter Cytochrom-P450-Enzyme im Vergleich zu normalen Hepatozyten hat das Stoffwechselprofil von HepG2 zu Bemühungen geführt, die Zelllinie für bessere Studien des Arzneimittelstoffwechsels zu modifizieren [13]. Im Vergleich zu Tumorzelllinien wie MCF7, PC3, 143B und HEK293 weisen HepG2-Zellen einzigartige Profile des Aminosäuregehalts auf, die die Proteinsynthese und -sekretion erheblich beeinflussen, was ihre einzigartigen Stoffwechselwege verdeutlicht [14]
Erforschung von Leberkrankheiten mit HepG2
Subkultivierung von HepG2-Zellen
Nachfolgend finden Sie fünf Schritte zur Entfernung adhärenter Zellen aus Zellkulturflaschen mit Accutase:
- Entfernen Sie das Medium aus dem Zellkulturkolben und spülen Sie die anhaftenden Zellen mit PBS ohne Kalzium und Magnesium ab. Verwenden Sie 3-5 ml PBS für T25-Kolben und 5-10 ml für T75-Kolben.
- Geben Sie Accutase in die Zellkulturflasche, wobei Sie 1-2 ml pro T25- und 2,5 ml pro T75-Kolben verwenden. Stellen Sie sicher, dass die Accutase die gesamte Zellschicht bedeckt.
- Inkubieren Sie den Kolben 8-10 Minuten bei Raumtemperatur.
- Die Zellen vorsichtig mit Medium resuspendieren, wobei 10 ml frisches Medium zu verwenden sind.
- Zentrifugieren Sie die resuspendierten Zellen 5 Minuten lang bei 300xg, resuspendieren Sie sie in frischem Medium und geben Sie sie in neue Flaschen mit frischem Medium.
Zukunftsperspektiven für HepG2-Zellen
Das Bestreben, das volle Potenzial der HepG2-Zelllinie zu erschließen, wird mit bahnbrechenden Fortschritten bei der Steigerung der Cytochrom-Expression fortgesetzt. Die Forscher untersuchen auch die Möglichkeit dreidimensionaler sphäroidischer Zellkulturen, die ein physiologisch relevanteres System darstellen. Die Stoffwechselaktivität, einschließlich der Cytochrome, ist in dreidimensionalen sphäroidalen HepG2-Modellen deutlich höher als in zweidimensionalen Zellen, was uns der Schaffung eines Modells näher bringt, das normale Hepatozyten widerspiegelt. Darüber hinaus kann die Erforschung der dynamischen Prozesse, die der falschen Verteilung von Zelloberflächenproteinen zugrunde liegen, den Weg für ein besseres Verständnis von Lebererkrankungen ebnen
HepG2-Zellen: Ihre Rolle und Unterscheidungsmerkmale in der biomedizinischen Forschung verstehen - FAQs
Referenzen
- Vyas, R.C., Darroudi, F., Natarajan, A.T. Radiation-induced chromosomal breakage and rejoining in interphase-metaphase chromosomes of human lymphocytes, Mutat Res, 1991; 249(1):29-35.
- Woodfield, S.E., Shi, Y., Patel, R.H., Chen, Z., Shah, A.P., Srivastava, R.K., Whitlock, R.S., Ibarra, A.M., Larson, S.R., Sarabia, S.F., et al. MDM4 Inhibition: Eine neuartige therapeutische Strategie zur Reaktivierung von P53 bei Hepatoblastomen. Sci. Rep. 2021, 11, 2967.
- Hussain, S.P., Schwank, J., Staib, F., Wang, X.W., Harris, C.C. TP53 Mutationen und hepatozelluläres Karzinom: Einblicke in die Ätiologie und Pathogenese von Leberkrebs. Oncogene 2004.
- Schicht, G., Seidemann, L., Haensel, R., Seehofer, D., Damm, G. Critical Investigation of the Usability of Hepatoma Cell Lines HepG2 and Huh7 as Models for the Metabolic Representation of Resectable Hepatocellular Carcinoma. Krebserkrankungen 2022, 14(17), 4227.
- Verrier, E.R., Colpitts, C.C., Schuster, C., Zeisel, M.B., Baumert, T.F. Cell Culture Models for the Investigation of Hepatitis B and D Virus Infection. Viruses 2016, 8, 261.
- Verrier, E.R., Colpitts, C.C., Bach, C., Heydmann, L., Weiss, A., Renaud, M., Durand, S.C., Habersetzer, F., Durantel, D., AbouJaoudé, G., et al. A Targeted Functional RNA Interference screen Uncovers Glypican 5 as an Entry Factor for Hepatitis B and D Viruses. Hepatology 2016, 63, 35-48.
- Gripon, P., Rumin, S., Urban, S., Le Seyec, J., Glaise, D., Cannie, I., Guyomard, C., Lucas, J., Trepo, C., Guguen-Guillouzo, C. Infection of a Human Hepatoma Cell Line by Hepatitis B Virus. Proc. Natl. Acad. Sci. USA 2002, 99, 15655-15660.
- Mersch-Sundermann, V., Knasmüller, S., Wu, X.J., Darroudi, F., Kassie, F. Use of a human-derived liver cell line for the detection of cytoprotective, antigenotoxic and cogenotoxic agents. Toxikologie. 2004; 198(1-3): 329-340.
- Fanelli, A. HepG2 (Leber hepatozelluläres Karzinom): Zellkultur. HepG2. Abgerufen am 3. Dezember 2017.
- Xuan, J., Chen, S., Ning, B., Tolleson, W.H., Guo, L. Development of HepG2-Derived Cells Expressing Cytochrome P450s for Assessing Metabolism-Associated Drug-Induced Liver Toxicity. Physiol. Behav. 2017, 176, 139-148.
- Ooka, M., Lynch, C., Xia, M. Application of in Vitro Metabolism Activation in High-Throughput Screening. Int. J. Mol. Sci. 2020, 21, 8182.
- Huang, L., Coughtrie, M.W.H., Hsu, H. Down-Regulation of Dehydroepiandrosterone Sulfotransferase Gene in Human Hepatocellular Carcinoma. Mol. Cell. Endocrinol.
- Zhu, Z., Hao, X., Yan, M., et al. Cancer stem/progenitor cells are highly enriched in CD133 + CD44 + population in hepatocellular carcinoma. Int J Cancer. 2010; 126:2067-2078.
- Arbus, C., Benyamina, A., Llorca, P.-M., Baylé, F., Bromet, N., Massiere, F., Garay, R.P., Hameg, A. Characterization of human cytochrome P450 enzymes involved in the metabolism of cyamemazine. Eur J Pharm Sci. 2007 Dec;32(4-5):357-66.