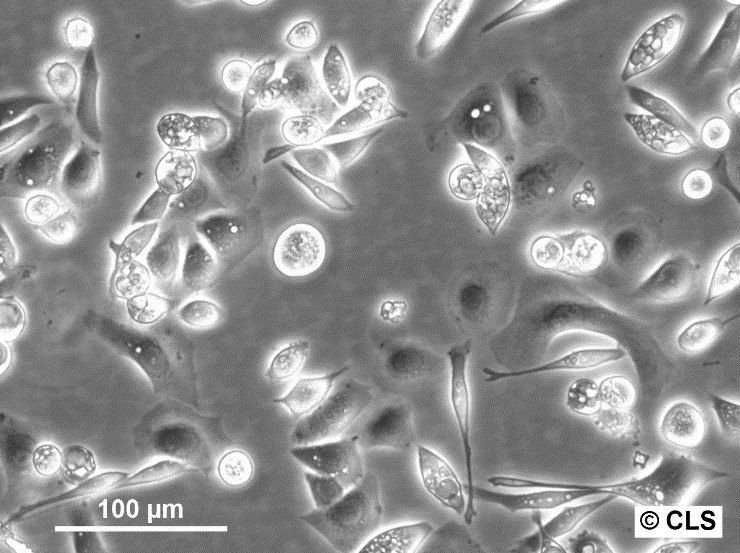
AGS-Zellen - Erforschung des Magen-Adenokarzinoms AGS-Zellen in Krebsstudien
AGS-Zellen sind eine menschliche Adenokarzinom-Zelllinie des Magens, die in der biomedizinischen Forschung weit verbreitet ist. Sie wird insbesondere zur Untersuchung der Biologie des Magenkrebses eingesetzt, einschließlich des Tumorwachstums, der Entwicklung, des Fortschreitens und der therapeutischen Interventionen. Darüber hinaus wird sie zur Untersuchung von Wirt-Pathogen-Interaktionen eingesetzt.
In diesem Artikel werden die Grundlagen der AGS-Zellen des Magenepithels erörtert. Er behandelt insbesondere:
- Allgemeine Merkmale und Herkunft von AGS-Zellen
- Informationen zur Kultivierung der AGS-Zelllinie
- AGS-Zelllinie: Vorteile und Beschränkungen
- Anwendungen von AGS-Zellen
- Forschungspublikationen über AGS-Zelllinie
- Ressourcen für AGS-Zelllinie: Protokolle, Videos und mehr
1.allgemeine Merkmale und Herkunft von AGS-Zellen
Bevor Sie mit einer Zelllinie arbeiten, müssen Sie deren Herkunft und allgemeine Merkmale kennen. In diesem Abschnitt werden die folgenden Punkte behandelt: Was sind AGS-Zellen? Was ist der Ursprung der AGS-Zellen? Wie ist die Morphologie der AGS-Krebszelllinie?
- Die AGS-Zelllinie wurde aus dem Magengewebe einer 54-jährigen kaukasischen Frau mit einem Magenadenokarzinom gewonnen. Sie wurde 1979 isoliert [1].
- AGS-Zellen haben eine epithelähnliche Morphologie.
- Die epithelialen AGS-Zellen des Magens sind hyperdiploid. Die modale Chromosomenzahl für AGS-Zellen beträgt 49, was bei fast 60 % der Zellen der Fall ist. Polyploidie tritt auch bei etwa 3,6 % der Zellen auf.
2.informationen zur Kultivierung der AGS-Zelllinie
Für die ordnungsgemäße Handhabung und Verwaltung einer Zelllinie müssen Sie deren grundlegende Kultivierungskonzepte kennen. Insbesondere sollten Sie lernen: Was ist die Verdopplungszeit der AGS-Zellen? Was ist das AGS-Zellmedium? Wie subkultiviert man AGS-Zellen? Welche Gefriermedien werden für AGS-Zellen aus Magenepithel verwendet?
Wichtige Punkte für die Kultivierung von AGS-Zellen
|
Verdopplungszeit: |
Die Verdopplungszeit von AGS-Zellen liegt zwischen 24 und 48 Stunden. |
|
Adhärent oder in Suspension: |
AGS-Zellen sind adhärent. Sie wachsen in Monolayern. |
|
Aussaatdichte: |
AGS-Zellen werden mit einer Zelldichte von 1 x104 Zellen/cm2 ausgesät. Bei dieser Dichte bilden die Zellen in 3 bis 5 Tagen eine konfluente Monolage. Nach Entfernung der alten Medien werden die Zellen mit 1 x PBS gespült und mit Accutase-Dissoziationslösung inkubiert. Die abgelösten Zellen wurden in Kulturmedium resuspendiert und zentrifugiert. Das Zellpellet wurde erneut resuspendiert, und nach der Zählung der AGS-Zellen werden sie zum Wachstum in die neue Flasche gegeben. |
|
Wachstumsmedium: |
Für die Kultivierung von AGS-Zellen wird DMEM-Medium mit 10 % FBS, 4 mM L-Glutamin, 4,5 g/L Glucose, 1,5 g/L NaHCO3 und 1,0 mM Natriumpyruvat verwendet. Die Medien sollten 2 bis 3 Mal pro Woche ausgetauscht werden. |
|
Wachstumsbedingungen: |
AGS-Zellen werden in einem befeuchteten Inkubator (bei einer Temperatur von 37°C) mit einer 5%igen CO2-Zufuhr gehalten. |
|
Lagerung: |
Gefrorene AGS-Zellen werden in elektrischen Gefrierschränken bei Temperaturen unter -150°C oder in der Dampfphase von flüssigem Stickstoff für längere Zeit aufbewahrt. |
|
Einfrierverfahren und Medium: |
Zum Einfrieren von AGS-Zellen wird CM-1- oder CM-ACF-Medium verwendet. Das Einfrieren der Zellen erfolgt durch einen langsamen Gefrierprozess, der nur einen Temperaturabfall von 1 °C pro Minute zulässt und die Lebensfähigkeit der Zellen schützt. |
|
Auftauprozess: |
Die eingefrorenen Magenepithelzellen werden in einem 37 °C warmen Wasserbad 40 bis 60 Sekunden lang schnell geschüttelt. Die aufgetauten Zellen werden in frischem Kulturmedium resuspendiert und zum Wachstum in neue Flaschen gefüllt. Nach 24-stündiger Inkubation wird das Medium erneuert, um gefrierende Medienbestandteile zu entfernen. Im Gegensatz dazu werden die aufgetauten Zellen zentrifugiert und die Gefriermediumbestandteile entfernt. Anschließend werden die geernteten Zellen wieder resuspendiert und in den Kolben mit dem Nährmedium gegeben. |
|
Biosicherheitsstufe: |
Für die Kultivierung von AGS-Zellen sind Laborbedingungen der Biosicherheitsstufe 2 erforderlich. |
3.aGS-Zelllinie: Vorteile und Beschränkungen
In diesem Abschnitt des Artikels werden einige der wichtigsten Vorteile und Einschränkungen im Zusammenhang mit AGS-Zellen erläutert.
Vorteile
Die wichtigsten Vorteile von AGS-Zellen aus Magenepithel sind:
|
Einfach zu kultivieren |
Die AGS-Magenkarzinom-Zelllinie ist in Zellkulturlabors leicht zu kultivieren. Sie stellt keine komplizierten und aufwändigen Anforderungen an die Zellkultur. Darüber hinaus weist sie gute Wachstumseigenschaften auf, was sie zu einer idealen Wahl für die Untersuchung der Biologie des Magenkrebses macht. |
|
Relevanz für Magenkrebs |
AGS-Zellen wurden aus menschlichen Magenadenokarzinomen gewonnen und werden daher häufig zur Untersuchung der Biologie des Magenkarzinoms und therapeutischer Maßnahmen eingesetzt. |
Beschränkungen
Die mit der AGS-Zelllinie verbundenen Einschränkungen sind:
|
In-vitro-Zellmodell |
AGS-Zellen werden in biomedizinischen Forschungslabors unter künstlichen Bedingungen gezüchtet. Daher können sie die Mikroumgebung von Magenkrebs in vivo und andere Zell- und Molekularinteraktionen nicht vollständig nachbilden. |
4.anwendungen von AGS-Zellen
AGS-Zellen werden speziell zur Untersuchung der Biologie von Magenkrebs eingesetzt. Sie haben viele andere vielversprechende Anwendungen im biomedizinischen Bereich. Einige der interessanten Forschungsanwendungen von AGS-Zellen sind:
- Untersuchung von Magenkrebs: AGS-Zellen sind ein hervorragendes Forschungsinstrument zur Untersuchung der Zell- und Molekularmechanismen, die dem Wachstum, der Metastasierung und der Invasion von Magenkrebs zugrunde liegen. Forscher setzen AGS-Zellen aus Magenepithel auch ein, um verschiedene zelluläre Prozesse, genetische Mutationen und Signalwege bei der Entstehung von Magenkrebs zu untersuchen. Eine Studie in Oncology Reports (2019) ergab, dass die microRNA-183-5p.1 die Proliferation, Migration und Invasion von Tumorzellen fördert, indem sie die Bcl 2/P53-Signalkaskade hemmt. Außerdem wird das TPM1-Gen herunterreguliert, um diese Wirkungen zu erzielen. Daher werden sowohl microRNA als auch TPM1 als wirksame molekulare Ziele für die Entwicklung gezielter Therapien gegen Magenkrebs vorgeschlagen [2].
- Wirkstoff-Screening: AGS-Zellen wurden häufig zum Screening neuer und wirksamer Medikamente gegen Magenkrebs verwendet. Forscher bewerten die Zytotoxizität und Wirksamkeit potenzieller Medikamente anhand der AGS-Zelllinie. Es wurden auch Studien zur Identifizierung neuer molekularer Ziele und zur Entwicklung neuer zielgerichteter Therapien zur Bekämpfung von Magenkarzinomen durchgeführt. In einer im Jahr 2021 durchgeführten Studie wurden AGS-Magenkrebszellen verwendet und die therapeutische Wirkung des Medikaments Paclitaxel untersucht. Die Ergebnisse zeigten, dass Paclitaxel eine mitotische Katastrophe auslöst, einen wesentlichen Mechanismus der Apoptose oder des Zelltods in AGS-Zellen. Darüber hinaus förderte es auch die Autophagie in Magenkrebszellen [3].
- Wirt-Pathogen-Wechselwirkungen: Die AGS-Krebszelllinie dient auch der Untersuchung von Wirt-Pathogen-Interaktionen. Dies hilft den Forschern, die zellulären Mechanismen und Reaktionen im Zusammenhang mit einer Infektion zu verstehen. In einer Studie aus dem Jahr 2020 wurde beispielsweise beobachtet, dass kleine nichtkodierende RNAs in den äußeren Membranvesikeln von Helicobacter pylori die Sekretion von Interleukin 8 in menschlichen AGS-Zellen verringern [4].
5.forschungspublikationen über die AGS-Zelllinie
In diesem Abschnitt des Artikels werden einige interessante und meist zitierte Forschungspublikationen über AGS-Zellen vorgestellt.
In dieser Studie in Biomedicine & Pharmacotherapy (2020) wird vorgeschlagen, dass Salidrosid, ein natürlicher Wirkstoff, die schützende Autophagie und den Zelltod in AGS-Zellen des Magenepithels durch Modulation des PI3K/AKT/mTOR-Signalwegs auslöst.
Diese Studie wurde in Biomedicine & Pharmacotherapy (2018) veröffentlicht. Sie untersuchte die synergistischen Antikrebseffekte von Astragalus-Polysaccharid und dem Medikament Apatinib in AGS-Zellen. Die Ergebnisse der Studie zeigten, dass Astragalus die Antitumorwirkung von Apatinib über die Unterdrückung der AKT-Signalisierung verstärkt.
Diese in der Fachzeitschrift Journal of Ethnopharmacology (2018) veröffentlichte Forschungsarbeit schlug vor, dass Curcuzedoalide, eine natürliche Verbindung aus der Pflanze Curcuma zedoaria Roscoe, zu ihrem zytotoxischen Potenzial gegen AGS-Zellen beiträgt.
Diese Veröffentlichung in Gene (2018) schlug vor, dass die Hochregulierung von FOXA1 die Proliferation und den epithelialen zu mesenchymalen Übergang (EMT) und die Invasion von AGS-Magenadenokarzinomzellen unterdrückt.
Dieser Forschungsartikel wurde im International Journal of Medical Microbiology im Jahr 2020 veröffentlicht. In dieser Studie wurden AGS-Zellen zur Untersuchung von Wirt-Pathogen-Interaktionen eingesetzt. Die Ergebnisse zeigten, dass Helicobacter pylori einige nichtcodierende RNA in seinen äußeren Membranvesikeln enthält, die den IL-8-Spiegel in AGS-Zellen beeinflussen.
6.ressourcen für die AGS-Zelllinie: Protokolle, Videos und mehr
Im Folgenden finden Sie einige Ressourcen, die sich mit AGS-Zellen befassen.
- AGS-Zelltransfektionsprotokoll: Dieses Video ist eine schrittweise Anleitung zum Erlernen des Transfektionsprotokolls für AGS-Zellen aus Magenepithel.
Der folgende Link enthält das AGS-Zellkulturprotokoll.
- AGS-Zellkulturprotokoll: Diese Website enthält nützliche Informationen über AGS-Zellmedien und Zellkulturprotokolle. Sie enthält ein Protokoll für die Subkultivierung von AGS-Zellen aus dem Magenepithel und den Umgang mit proliferierenden und kryokonservierten AGS-Kulturen.
- Subkultivierung von AGS-Zellen: Auf dieser Seite wird das Subkultivierungsverfahren für AGS-Zellen im Detail erläutert.
Referenzen
- Phuc, B.H., et al., Comparative genomics of two Vietnamese Helicobacter pylori strains, CHC155 from a non-cardia gastric cancer patient and VN1291 from a duodenal ulcer patient. Wissenschaftliche Berichte, 2023. 13(1): p. 8869.
- Lin, J., et al., miRNA-183-5p. 1 fördert die Migration und Invasion von AGS-Zellen des Magenkrebses, indem sie auf TPM1 abzielt Korrigendum in/10.3892/or. 2020.7902. Oncology Reports, 2019. 42(6): p. 2371-2381.
- Khing, T.M., et al., The effect of paclitaxel on apoptosis, autophagy and mitotic catastrophe in AGS cells. Scientific Reports, 2021. 11(1): p. 23490.
- Zhang, H., et al., sncRNAs, die von Vesikeln der äußeren Membran von Helicobacter pylori verpackt werden, dämpfen die IL-8-Sekretion in menschlichen Zellen. Internationale Zeitschrift für Medizinische Mikrobiologie, 2020. 310(1): p. 151356.