Zellkulturmedien: Ein Überblick
Im Bereich der Biowissenschaften ist eine der wichtigsten Methoden die Zellkultur. Mit dem Begriff "Zellkultur" ist die Entnahme von Zellen, Geweben oder Organen aus einem Tier oder einer Pflanze und die anschließende Implantation dieser Zellen, Gewebe oder Organe in eine künstliche Umgebung gemeint, die ihr Überleben und/oder Wachstum begünstigt Die grundlegenden Voraussetzungen für eine optimale Zellentwicklung sind eine kontrollierte Temperatur, ein Substrat für die Zellanhaftung, ein geeignetes Wachstumsmedium und ein Inkubator, der den optimalen pH-Wert und die optimale Osmolalität aufrechterhält. Die Zellen müssen diese Bedingungen vorfinden, damit sie ihr volles Potenzial entfalten können.
Die Auswahl eines geeigneten Wachstumsmediums für die In-vitro-Kultivierung ist der kritischste und zugleich wichtigste Schritt in der Zellkultur. Ein Wachstumsmedium, auch Kulturmedium genannt, ist eine Flüssigkeit oder ein Gel, das die Entwicklung von Organismen auf mikroskopischer, zellulärer oder pflanzenähnlicher Ebene fördert. Das Medium, das für die Kultivierung von Zellen verwendet wird, enthält häufig eine ausreichende Menge an Energie und Substanzen, die den Zellzyklus steuern. Zu den Hauptbestandteilen eines Nährbodens gehören Aminosäuren, Vitamine, anorganische Salze, Glukose und Serum. Das Serum wird dem Medium zugesetzt, weil es als Quelle für Wachstumsfaktoren, Hormone und Bindungsfaktoren dient. Das Medium liefert nicht nur Nährstoffe, sondern trägt auch zur Aufrechterhaltung des pH-Werts und der Osmolalität bei.
In der Zellkultur verwendete Medientypen
Sowohl menschliche als auch tierische Zellen können entweder in einem künstlichen oder synthetischen Medium gezüchtet werden oder in einem völlig natürlichen Medium, das mit natürlichen Elementen angereichert ist. Im Folgenden geben wir Ihnen einen Überblick über die verschiedenen derzeit verfügbaren Medientypen.
Natürliche Medien
In natürlichen Medien sind nur biologische Flüssigkeiten zu finden, die in ihrem natürlichen Zustand vorliegen. Natürliche Medien sind sehr hilfreich und einfach für die Kultivierung einer Vielzahl von tierischen Zelltypen. Die mangelnde Kenntnis der genauen Bestandteile, aus denen natürliche Medien bestehen, ist der Hauptgrund für die geringe Wiederholbarkeit der mit natürlichen Medien erzielten Ergebnisse.
Künstliche Medien
Bei der Herstellung künstlicher oder synthetischer Medien werden Nährstoffe (sowohl organische als auch anorganische), Serumproteine, Kohlenhydrate, Cofaktoren, Vitamine und Salze sowie O2 und CO2-Gasphasen hinzugefügt [1].
Es wurden verschiedene Arten von künstlichen Medien entwickelt, um eine oder mehrere der folgenden Funktionen zu erfüllen: 1) Sofortiges Überleben (eine ausgewogene Salzlösung mit einem genauen pH-Wert und osmotischem Druck). 2) Längeres Überleben (eine ausgewogene Salzlösung, die mit verschiedenen Formulierungen von organischen Chemikalien und/oder Serum ergänzt wird). 3) Unbegrenzte Entwicklung. 4) Spezialisierte Funktionen.
Es gibt vier verschiedene Klassifizierungen für künstliche Medien:
Serumhaltige Medien
Die häufigste Art von Zusatzstoffen, die in Nährmedien für tierische Zellen verwendet werden, ist fötales Rinderserum. Es wird dem Nährmedium als kostengünstige Ergänzung zugesetzt, um bestmögliche Wachstumsbedingungen zu erreichen. Das Serum fungiert nicht nur als Transporter oder Chelator für instabile oder wasserunlösliche Nährstoffe, Hormone und Wachstumsfaktoren, Proteaseinhibitoren und andere Substanzen, sondern bindet und neutralisiert auch schädliche Moleküle.
Serumfreies Medium
Das Vorhandensein von Serum in den Medien hat eine Reihe von Nachteilen und kann in der immunologischen Forschung zu erheblichen Interpretationsfehlern führen [2, 3]. Es wurde eine Vielzahl verschiedener serumfreier Medien entwickelt [4, 5]. Diese Medien sind in der Regel speziell für die Kultur eines einzelnen Zelltyps formuliert, wie z. B. Knockout Serum Replacement und Knockout DMEM von Thermo Fisher Scientific und mTESR-Medium von Stem Cell Technologies [6] für Stammzellen [7].
Zusätzlich enthalten diese Medien definierte Mengen an gereinigten Wachstumsfaktoren, Lipoproteinen und anderen Proteinen, die sonst üblicherweise durch das Serum bereitgestellt werden [8]. Diese Medien werden oft als "definierte Kulturmedien" bezeichnet, da die Komponenten, aus denen sie bestehen, gut bekannt sind.
Chemisch definierte Medien
Diese Medien enthalten hochreine anorganische und organische Bestandteile, die durch keinerlei Verunreinigungen verunreinigt wurden. Sie können auch reine Proteinzusätze, wie z. B. Wachstumsfaktoren, enthalten.
durch die genetische Veränderung von Bakterien oder Hefen und die Zugabe von bestimmten Fettsäuren, Vitaminen, Cholesterin und Aminosäuren werden deren Bestandteile hergestellt [9].
Proteinfreie Medien
Proteinfreie Medien enthalten keinerlei Proteine, sondern nur Nicht-Protein-Elemente. Im Vergleich zu Medien mit Serumzusatz fördert die Verwendung von Medien ohne Proteinzusatz die Zellproliferation und Proteinexpression und erleichtert die Reinigung der in einem nachgeschalteten Prozess erzeugten Produkte [10-12]. Proteine sind in Formulierungen wie MEM und RPMI-1640 nicht enthalten. Bei Bedarf kann jedoch ein Proteinzusatz verabreicht werden.
Kulturmedien und ihre Grundbestandteile
Kommerzielle Nährmedien können als Pulver oder Flüssigkeit gekauft werden und enthalten oft eine Vielzahl von Nährstoffen wie Aminosäuren, Glukose, Salze, Vitamine und andere Nahrungsergänzungsmittel.
Der Bedarf an diesen Bestandteilen ist für jede Zelllinie unterschiedlich, und diese Unterschiede sind der Grund für die große Anzahl verschiedener Medienformulierungen. Jeder Bestandteil ist für eine bestimmte Funktion verantwortlich, die in den folgenden Abschnitten erläutert wird:
Puffersysteme
Um optimale Wachstumsbedingungen aufrechtzuerhalten, muss der pH-Wert kontrolliert werden, was häufig durch eines von zwei Puffersystemen geschieht:
Natürliches Puffersystem
Das CO2/H2CO3-Verhältnis in der Atmosphäre ist gleich dem des Mediums, wodurch ein natürlicher Puffermechanismus entsteht. Um den natürlichen Pufferungsmechanismus zu erhalten, müssen die Kulturen in einer Luftumgebung mit 5-10 % CO2 gehalten werden, was häufig durch die Verwendung eines CO2-Brutschranks erreicht wird. Eines der besten Argumente für die Verwendung eines natürlichen Puffers ist, dass er preiswert und sicher ist.
HEPES
Die chemische Pufferung mit dem Zwitterion HEPES hat ein größeres Puffervermögen im pH-Bereich von 7,2 bis 7,4 und benötigt keine geregelte gasförmige Umgebung. Für bestimmte Zelltypen kann eine höhere Dosis HEPES schädlich sein. HEPES-haltige Medien sind auch viel anfälliger für die phototoxischen Wirkungen von Fluoreszenzlicht [13].
Phenolrot
Der pH-Indikator Phenolrot ist häufig in handelsüblichen Nährmedien enthalten und ermöglicht eine kontinuierliche Überwachung des pH-Werts. Durch die Ausdehnung der Zellen bewirken die von diesen Zellen produzierten Metaboliten eine Verschiebung des pH-Werts und damit eine Farbänderung des Mediums. Phenolrot hat eine doppelte Wirkung auf die Farbe eines Mediums, indem es es bei saurem pH-Wert gelb und bei alkalischem pH-Wert violett färbt. pH 7,4, der optimale Wert für Zellkulturen, lässt das Medium rot fluoreszieren.
Phenolrot hat jedoch einige Nachteile: Erstens ist Phenolrot in der Lage, die Wirkung einer Reihe von Steroidhormonen zu simulieren, vor allem von Östrogen [14]. Daher wird bei der Untersuchung östrogenempfindlicher Zellen wie Brustgewebe ein Medium empfohlen, das frei von Phenolrot ist. Das Natrium-Kalium-Gleichgewicht wird durch die Anwesenheit von Phenolrot in mehreren serumfreien Formulierungen gestört. Die Zugabe von Serum oder Rinderhypophysenhormon zu den Medien kann diesem Effekt entgegenwirken [15]. Drittens wird der Nachweis in durchflusszytometrischen Experimenten durch das Vorhandensein von Phenolrot behindert.
Anorganische Salze
Medien, die anorganische Salze wie Natrium-, Kalium- und Kalziumionen enthalten, tragen zur Aufrechterhaltung des osmotischen Gleichgewichts und zur Regulierung des Membranpotenzials bei.
Aminosäuren
Da Aminosäuren die grundlegenden Bestandteile von Proteinen sind, sind sie ein wesentlicher Bestandteil jedes einzelnen Zellwachstumsmediums, das jemals erdacht wurde. Da die Zellen nicht in der Lage sind, bestimmte Aminosäuren selbst zu produzieren, ist es wichtig, dass das Nährmedium essenzielle Aminosäuren enthält. Sie sind für die Vermehrung der Zellen notwendig, und die Konzentration, in der sie vorhanden sind, bestimmt die maximale Zelldichte, die erreicht werden kann. Insbesondere L-Glutamin, eine essentielle Aminosäure, ist besonders wichtig.
L-Glutamin fungiert als sekundäre Energiequelle für den Stoffwechsel und trägt Stickstoff zur Produktion von NAD, NADPH und Nukleotiden bei. Da es sich bei L-Glutamin um eine instabile Aminosäure handelt, die mit der Zeit in eine Form übergeht, die von den Zellen nicht verwertet werden kann, muss sie dem Medium zugeführt werden.
Darüber hinaus können dem Medium auch nicht-essentielle Aminosäuren zugeführt werden, um die während des Wachstumsprozesses verbrauchten aufzufüllen. Das Wachstum der Zellen wird gefördert und ihre Lebensfähigkeit erhöht, wenn das Wachstumsmedium mit nicht-essentiellen Aminosäuren angereichert wird.
Kohlenhydrate
Kohlenhydrate in Form von Zuckern sind die Hauptenergiequelle. Viele Nährböden enthalten neben den häufigeren Zuckern Glucose und Galactose auch Maltose und Fructose.
Proteine und Peptide
Albumin, Transferrin und Fibronektin sind die am häufigsten verwendeten Proteine und Peptide. Sie sind besonders wichtig in Medien, die kein Serum enthalten. Albumin, Transferrin, Aprotinin, Fetuin und Fibronektin sind einige der Proteine, die im Serum, einem reichhaltigen Eiweißlieferanten, vorkommen können.
Albumin ist das wichtigste Protein im Blut und hat die Aufgabe, verschiedene Substanzen wie Wasser, Salze, freie Fettsäuren, Hormone und Vitamine zu binden und zwischen verschiedenen Organen und Zellen zu transportieren. Die Fähigkeit von Albumin, sich an Chemikalien zu binden, macht es zu einem wirksamen Kandidaten, um schädliche Verbindungen aus dem Medium zu entfernen, in dem Zellen gezüchtet werden.
Aprotinin ist ein Schutzmittel in Zellkultursystemen, da es bei neutralem und saurem pH-Wert stabil ist und auch hohen Temperaturen und der Zerstörung durch proteolytische Enzyme standhält. Es ist in der Lage, eine Reihe von Serinproteasen zu hemmen, unter anderem Trypsin.
Fetuin ist ein Glykoprotein, das im Serum von fötalen und neugeborenen Tieren in höheren Mengen nachgewiesen werden kann als im Serum von Erwachsenen. Darüber hinaus wirkt es als Serinproteaseinhibitor. Das Protein Fibronektin ist ein wesentlicher Bestandteil im Prozess der Zelladhäsion. Transferrin ist ein Protein, das Eisen transportiert und für den Transport von Eisen zu den Zellmembranen verantwortlich ist.
Fettsäuren und Lipide
Sie spielen eine entscheidende Rolle im serumfreien Medium, wenn kein Serum vorhanden ist.
Vitamine
Zahlreiche Vitamine sind für die Entwicklung und Vermehrung von Zellen notwendig. Vitamine können von den Zellen nicht in ausreichender Menge produziert werden und sind daher in der Gewebekultur als Nahrungsergänzungsmittel unerlässlich.
In der Zellkultur ist das Serum die Hauptquelle für Vitamine; Medien werden jedoch auch mit verschiedenen Vitaminen behandelt, um sie für einen bestimmten Zelltyp geeignet zu machen. In der Regel werden die Vitamine der B-Gruppe zur Wachstumsstimulation verwendet.
Spurenelemente
Chemische Elemente wie Kupfer, Zink, Selen und Tricarbonsäure-Zwischenprodukte werden als Spurenelemente bezeichnet. Spurenelemente werden häufig Medien zugesetzt, die kein Serum enthalten, um diejenigen zu ersetzen, die normalerweise im Serum vorhanden sind. Diese Elemente sind wichtige chemische Bestandteile, die für eine gesunde Zellentwicklung erforderlich sind. Viele biochemische Reaktionen hängen von bestimmten Mikronährstoffen ab, z. B. die Aktivität von Enzymen.
Ergänzungen zum Medium
Das für bestimmte Zelllinien empfohlene Vollwachstumsmedium benötigt zusätzliche Komponenten, die in den Basismedien und im Serum nicht enthalten sind. Diese Nahrungsergänzungsmittel unterstützen das Zellwachstum und eine angemessene Stoffwechselfunktion.
Obwohl Hormone, Wachstumsfaktoren und Signalmoleküle für die angemessene Vermehrung bestimmter Zelllinien unerlässlich sind, sollten die folgenden Vorsichtsmaßnahmen stets beachtet werden: Da die Zugabe von Ergänzungsmitteln die Osmolalität des gesamten Wachstumsmediums verändern kann, was die Zellentwicklung hemmen kann, ist es immer ratsam, die Osmolalität nach der Zugabe von Ergänzungsmitteln zu überprüfen. Für die meisten Zelllinien liegt die optimale Osmolalität zwischen 260 und 320 mOSM/kg.
Antibiotika
Antibiotika werden häufig eingesetzt, um die Entwicklung von bakteriellen und pilzlichen Verunreinigungen zu hemmen [16], obwohl sie für das Zellwachstum nicht unbedingt erforderlich sind. Da Antibiotika eine Kontamination durch Mykoplasmen und resistente Bakterien verschleiern können, wird ihr routinemäßiger Einsatz in der Zellkultur nicht empfohlen [17, 18].
Außerdem können Antibiotika den Stoffwechsel von überempfindlichen Zellen stören. Die Penicillin-Streptomycin-Kombinationen von MilliporeSigma und Life Technologies werden häufig verwendet. Plasmocin wurde bei der Kultivierung der Gliomzelllinien TS603, TS516 und BT260 eingesetzt [19] und hat sich bei der Entfernung von Mykoplasmenkontaminationen als wirksam erwiesen (20).
Serum
Albumine, Wachstumsfaktoren und Wachstumsinhibitoren sind alle im Serum vorhanden. Serum ist einer der wichtigsten Bestandteile des Zellkulturmediums, da es Aminosäuren, Proteine, Vitamine (insbesondere fettlösliche Vitamine wie A, D, E und K), Kohlenhydrate, Lipide, Hormone, Wachstumsfaktoren, Mineralien und Spurenelemente enthält.
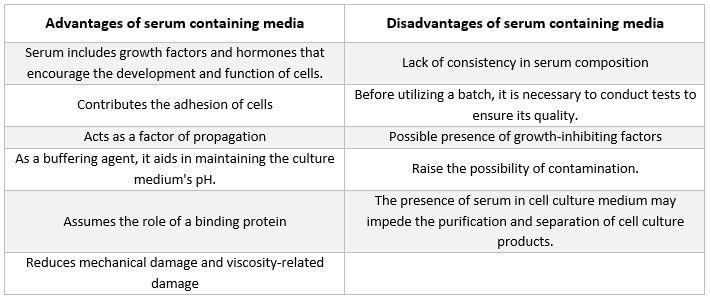
Zur Förderung der Entwicklung kultivierter Zellen wird häufig fötales Serum oder Rinderserum verwendet. Fötalserum ist ein reichhaltiger Lieferant von Wachstumsfaktoren und eignet sich für das Klonen von Zellen und die Entwicklung empfindlicher Zellen. Aufgrund seiner geringeren wachstumsfördernden Eigenschaften wird Kälberserum bei Experimenten zur Kontakthemmung verwendet. Normale Wachstumsmedien enthalten häufig 2 bis 10 % Serum. Die Zugabe von Serum zum Nährmedium dient folgenden Zwecken [21]:
-
Das Serum liefert die wesentlichen Nährstoffe für die Zellen (sowohl in Lösung als auch an Proteine gebunden).
-
Das Serum enthält mehrere Wachstumsfaktoren und Hormone, die an der Wachstumsförderung und der spezialisierten Zellaktivität beteiligt sind.
-
Es bietet viele Bindungsproteine, wie Albumin und Transferrin, die andere Chemikalien in die Zelle transportieren. Albumin liefert zum Beispiel Fette, Vitamine, Hormone usw. in die Zellen.
-
Außerdem liefert es Proteine wie Fibronektin, die die Zellhaftung am Substrat erhöhen. Außerdem produziert es Spreizungselemente, die die Ausdehnung der Zellen vor der Teilung unterstützen.
-
Es liefert Proteaseinhibitoren, die die Proteolyse in den Zellen verhindern.
-
Außerdem enthält es Mineralien wie Na+, K+, Zn2+ und Fe2+.
-
Es erhöht die Viskosität des Mediums und schützt so die Zellen vor mechanischen Verletzungen beim Rühren der Suspensionskultur.
-
Es ist auch ein Puffer.
Referenzen
[1] Morgan J, Morton H, Parker R. Nutrition of animal cells in tissue culture; initial studies on a synthetic medium. Proc Soc Exp Biol Med. 1950;73:1-8
[2] Kerbel R, Blakeslee D. Rapid adsorption of a foetal calf serum component by mammalian cells in culture. Eine mögliche Quelle von Artefakten bei Untersuchungen von Antiseren gegen zellspezifische Antigene. Immunology. 1976;31:881-91
[3] Sula K, Draber P, Nouza K. Zusatz von Serum zum Medium, das für die Zubereitung von Zellsuspensionen verwendet wird, als mögliche Quelle von Artefakten bei zellvermittelten Reaktionen, die mit Hilfe des Popliteal-Lymphknoten-Tests untersucht werden. J Immunogenet. 1980;7:483-9
[4] Mariani E, Mariani A, Monaco M, Lalli E, Vitale M, Facchini A. Kommerzielle serumfreie Medien: Hybridomawachstum und Produktion monoklonaler Antikörper. J Immunol Methods. 1991;145:175-83
[5] Barnes D, Sato G. Methods for growth of cultured cells in serum-free medium. Anal Biochem. 1980;102:255-70
[6] Yu H, Lu S, Gasior K, Singh D, Vazquez Sanchez S, Tapia O,et al. HSP70 chaperones RNA-free TDP-43 into anisotropic intranuclear liquid spherical shells. Wissenschaft. 2021;371:
[7] Meharena H, Marco A, Dileep V, Lockshin E, Akatsu G, Mullahoo J,et al. Down-Syndrome-induced senescence disrupt the nuclear architecture of neural progenitors. Cell Stem Cell. 2022;29:116-130.e7
[8] Iscove N, Melchers F. Vollständiger Ersatz von Serum durch Albumin, Transferrin und Sojalipid in Kulturen von Lipopolysaccharid-reaktiven B-Lymphozyten. J Exp Med. 1978;147:923-33
[9] Stoll T, Muhlethaler K, von Stockar U, Marison I. Systematic improvement of a chemically-defined protein-free medium for hybridoma growth and monoclonal antibody production. J Biotechnol. 1996;45:111-23
[10] Darfler F. A protein-free medium for the growth of hybridomas and other cells of the immune system. In Vitro Cell Dev Biol. 1990;26:769-78
[11] Barnes D, Sato G. Serumfreie Zellkultur: ein vereinheitlichender Ansatz. Cell. 1980;22:649-55
[12] Hamilton W, Ham R. Clonal growth of chinese hamster cell lines in protein-free media. In Vitro. 1977;13:537-47
[13] Zigler J, Lepe Zuniga J, Vistica B, Gery I. Analysis of the cytotoxic effects of light-exposed HEPES-containing culture medium. In Vitro Cell Dev Biol. 1985;21:282-7
[14] Berthois Y, Katzenellenbogen J, Katzenellenbogen B. Phenolrot in Gewebekulturmedien ist ein schwaches Östrogen: Implikationen für die Untersuchung von östrogenempfindlichen Zellen in Kultur. Proc Natl Acad Sci U S A. 1986;83:2496-500
[15] Karmiol S. Entwicklung von serumfreien Medien. In: Master JRW, editor. Animal Cell culture, 3rd ed. Oxford:Oxford University Press; 2000.
[16] Perlman D. Verwendung von Antibiotika in Zellkulturmedien. Methods Enzymol. 1979;58:110-6
[17] McGarrity G. Spread and control of mycoplasmal infection of cell cultures. In Vitro. 1976;12:643-8
[18] Masters J, Stacey G. Changing medium and passaging cell lines. Nat Protoc. 2007;2:2276-84
[19] Chakraborty A, Laukka T, Myllykoski M, Ringel A, Booker M, Tolstorukov M,et al. Histon-Demethylase KDM6A erkennt direkt Sauerstoff, um Chromatin und Zellschicksal zu kontrollieren. Science. 2019;363:1217-1222
[20] Molla Kazemiha V, Azari S, Amanzadeh A, Bonakdar S, Shojaei Moghadam M, Habibi Anbouhi M,et al. Efficiency of Plasmocin™ on various mollicutes infected mammalian cell lines in comparison with commonly used antibiotics in cell culture: a local experience. Cytotechnology. 2011;63:609-20
[21] Kragh Hansen U. Molecular aspects of ligand binding to serum albumin. Pharmacol Rev. 1981;33:17-53