Humane mesenkymale stamceller - knoglemarv (HMSC-BM)

























Generel information
| Beskrivelse | Humane mesenkymale stamceller fra knoglemarv (HMSC-BM) er et robust og alsidigt redskab til in vitro-forskning. Disse multipotente mesenkymale stromaceller (MSC'er) har den unikke evne til at forny sig selv og differentiere sig til et bredt spektrum af celletyper, herunder adipocytter, osteoblaster og chondrocytter. HMSC-BM's potentiale til at differentiere sig til disse tre vigtige cellelinjer er veldokumenteret, hvilket gør dem uvurderlige for studier med fokus på regenerativ medicin, vævsingeniørvidenskab og cellulære differentieringsveje. Disse MSC'er dyrkes under strenge betingelser, hvilket sikrer deres multipotens og høje levedygtighed efter optøning. Et af de kendetegnende træk ved HMSC-BM sammenlignet med MSC'er fra andre kilder, såsom fedtvæv eller navlestreng, er deres overlegne evne til osteogen differentiering. Dette gør dem særligt nyttige inden for knoglebiologi og ortopædisk forskning, hvor det er afgørende at forstå de molekylære mekanismer, der styrer knogledannelse og -reparation. Derudover udviser HMSC-BM et robust immunmodulerende profil, hvilket gør dem til en fremragende model til at studere immuninteraktioner og inflammatoriske reaktioner. Disse unikke egenskaber gør også HMSC-BM til et foretrukket valg til prækliniske studier, der undersøger knoglemarvsmikromiljøet, hæmatopoiese og patofysiologien af knoglemarvsrelaterede sygdomme. Hvert kryorør med HMSC-BM indeholder mindst 1 x 106 celler med en levedygtighed på mellem 92 % og 95 %, som bestemt ved Trypan Blue-farvestofeksklusionstesten. Disse celler stammer fra knoglemarv indsamlet fra raske voksne donorer, som alle har givet deres informerede samtykke. For at sikre de højeste standarder gennemgår hver batch en streng kvalitetskontrol for at vurdere celleidentifikation, renhed, styrke og levedygtighed. Denne grundige test garanterer, at MSC'erne opfylder strenge kriterier, hvilket gør dem egnede til en bred vifte af forskningsformål, herunder cellebiologistudier, lægemiddeludvikling og undersøgelse af cellulære reaktioner på forskellige stimuli. Disse celler er ikke beregnet til terapeutiske eller in vivo-formål, og deres anvendelse er begrænset til forskningsformål i et kontrolleret laboratoriemiljø. |
|---|---|
| Organisme | Menneske |
| Væv | Knoglemarv |
| Anvendelser | Test af lægemidler, regenerativ medicin, sygdomsforskning |
Karakteristika
| Alder | Spørg venligst |
|---|---|
| Køn | Spørg venligst |
| Etnicitet | Kaukasisk |
| Morfologi | Veludbredt spindelformet, fibroblastlignende morfologi i mindst 5 passager. Færre end 2 % af cellerne udviser spontan myofibroblast-lignende morfologi inden for hver passage. |
| Celletype | Stamcelle |
| Vækstegenskaber | Vedhæftende |
Regulatoriske data
| Citat | Humane mesenkymale stamceller, knoglemarv (HMSC-BM) (Cytion katalognummer 300665) |
|---|---|
| Biosikkerhedsniveau | 1 |
| NCBI_TaxID | 9606 |
Biomolekylære data
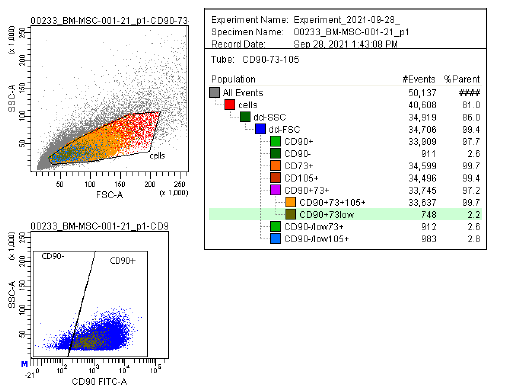
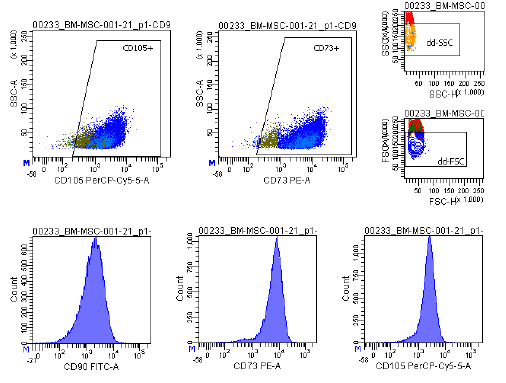
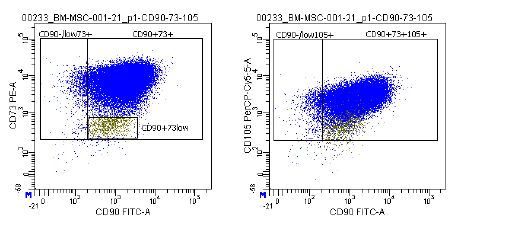
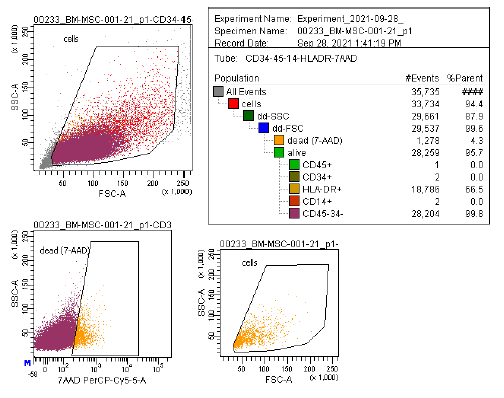
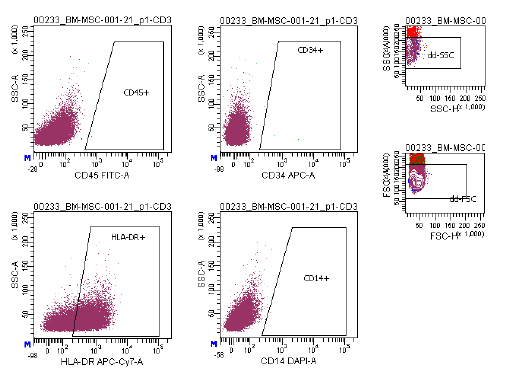
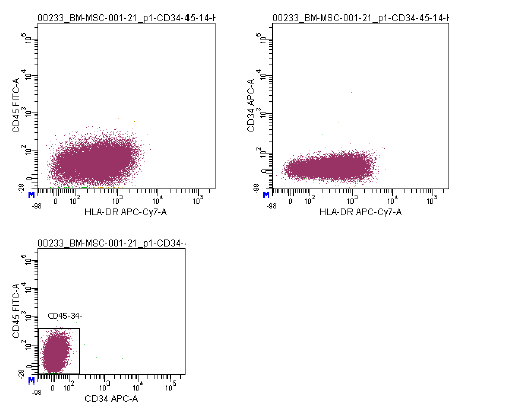
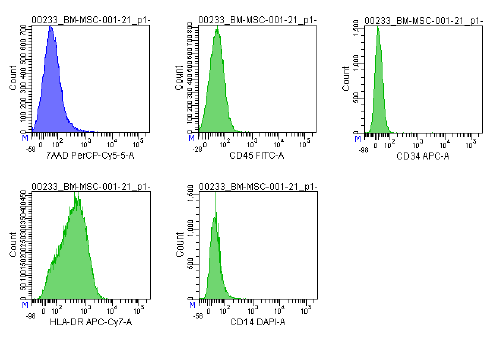
| Antigen-ekspression | Et omfattende panel af markører, herunder CD73/CD90/CD105 (positive) og CD14/CD34/CD45/HLA-DR (negative), anvendes i flowcytometrianalyse til at identificere dyrkede MSC'er (P2-P3) før kryopræservering. Disse markører anbefales af ISCT's MSC-udvalg. |
|---|---|
| Virus | Donor er negativ for HBV (PCR), Treponema pallidum (PCR) og HIV-1/2 (IFA). Cellerne er negative for HBV, HCV, HSV1, HSV2, CMV, EBV, HHV6, Toxoplasma gondii, Treponema pallidum, Chlamydia trachomatis, Ureaplasma urealyticum og Ureaplasma parvum. |
Håndtering
| Kulturmedium | Alpha MEM, m: 2,0 mM stabil glutamin, uden: Ribonukleosider, w/o: Deoxyribonukleosider, w: 1,0 mM Natriumpyruvat, w: 2,2g/L NaHCO3 |
|---|---|
| Kosttilskud | Suppler mediet med 10% FBS, 2 ng/mL bFGF |
| Dissociationsreagens | Trypsin-EDTA |
| Subkulturer | Til rutinemæssig adhærent cellekultur: Aspirer det gamle dyrkningsmedium fra de adhærente celler, og vask dem med PBS for at fjerne eventuelt resterende medium. Efter opsugning af PBS tilsættes den passende mængde Trypsin/EDTA-opløsning baseret på kulturbeholderens størrelse (f.eks. 1 ml til en T25-kolbe, 3 ml til en T75-kolbe), og der inkuberes ved stuetemperatur eller 37 °C, indtil cellerne løsner sig (5-10 minutter). Overvåg løsrivelsen under et mikroskop, og bank forsigtigt på beholderen, hvis det er nødvendigt for at frigøre cellerne. Når cellerne er løsnet, tilsættes komplet medium for at inaktivere trypsin/EDTA, cellerne resuspenderes forsigtigt, og en alikvot del af cellesuspensionen overføres til en ny kulturbeholder, der indeholder frisk medium. Anbring beholderen i en inkubator, der er indstillet til 37 °C med 5 %CO2, og skift mediet hver 2.-3. dag. |
| Såtæthed | 1 til 3 x 104 celler/cm2 |
| Fornyelse af væske | Første væskefornyelse efter 24 timer, derefter hver 2. til 3. dag. |
| Frys medium | Som kryopræserveringsmedium bruger vi 80 % FBS + 10 % basalmedium + 10 % DMSO for at opretholde levedygtigheden eller CM-1 (Cytion katalognummer 800100) for at opnå en bedre kryobeskyttelse, der forhindrer uønsket differentiering og samtidig bevarer pluripotensen. |
| Optøning og dyrkning af celler |
|
| Inkubationsatmosfære | 37°C, 5%CO2, befugtet atmosfære. |
| Overfladebehandling af flasker | For at opnå optimal vedhæftning og levedygtighed efter optøning anbefaler vi at bruge kollagenbelagte kolber eller plader. |
| Fryseprocedure | Kryopræserverede cellelinjer sendes på tøris i valideret, isoleret emballage med tilstrækkeligt kølemiddel til at opretholde ca. -78 °C under hele transporten. Ved modtagelse skal beholderen straks inspiceres, og hætteglassene skal straks overføres til passende opbevaring. |
| Forsendelsesbetingelser | Kryopræserverede cellelinjer sendes på tøris i valideret, isoleret emballage med tilstrækkeligt kølemiddel til at opretholde ca. -78 °C under hele transporten. Ved modtagelse skal beholderen straks inspiceres, og hætteglassene skal straks overføres til passende opbevaring. |
| Opbevaringsforhold | For langtidsopbevaring anbringes hætteglas i flydende nitrogen i dampfase ved ca. -150 til -196 °C. Opbevaring ved -80 °C er kun acceptabelt som et kort mellemtrin før overførsel til flydende nitrogen. |
Kvalitetskontrol / Genetisk profil / HLA
| Sterilitet | Mycoplasma-kontaminering udelukkes ved hjælp af både PCR-baserede assays og luminescensbaserede mycoplasma-detektionsmetoder. For at sikre, at der ikke er nogen bakterie-, svampe- eller gærforurening, underkastes cellekulturerne daglige visuelle inspektioner. |
|---|
Analysecertifikat (COA)
| Partiets nummer | Certifikatets type | Dato | Katalognummer |
|---|---|---|---|
| 300665-240423P1 | Certifikat for analyse | 26. Mar. 2026 | 300665 |
Aftale om overførsel af materiale
Hvis du kun vil bruge Cytion-cellelinjer til intern forskning på et enkelt forskningssted, skal du udfylde og underskrive vores materialeoverførselsaftale (MTA) og sende den sammen med din ordre.
Ved kommerciel anvendelse – herunder, men ikke begrænset til, arbejde mod betaling, kvalitetskontrol, produktfrigivelse, diagnostisk brug eller regulatoriske undersøgelser – bedes du udfylde formularen til tilsigtet brug, så vi kan udarbejde en aftale, der er skræddersyet til dit projekt.
Bemærk: MTA gælder kun for visse cellelinjer. Hvis denne meddelelse og MTA-dokumentet vises på en produktside, er aftalen gældende. For cellelinjer, der ikke er omfattet af MTA, vises der ingen henvisning til aftalen. MTA er ikke gyldig for kunder i Amerika, Kina eller Taiwan. Kontakt vores amerikanske afdeling for at modtage den relevante aftale.
